舒肝丸由川楝子、姜厚朴、木香、醋延胡索等13味药组成,各药味经粉碎后,加入不同的辅料精制成大蜜丸、小蜜丸、水蜜丸或水丸。临床上主要用于舒肝和胃、理气止痛等。收载于中国药典2015年版一部[1],且仅收载了芍药苷的含量测定。厚朴、木香具有和胃、止呕的作用,目前对这2味药材已进行了较为深入的研究,明确了其功效成分。厚朴药材中的主要成分和厚朴酚与厚朴酚常被用作厚朴的质量评价标准[2-5];木香挥发油中的活性木香烃内酯和去氢木香内酯,具有松弛平滑肌和解痉作用,其含量可作为木香质量优劣的评价指标之一[6-8]。因此为了更好地控制产品的内在质量,保证临床用药的安全有效,在相关多成分含量测定方法报道的基础上[9-10],本研究以厚朴、木香为研究对象,采用反相高效液相色谱法同时测定舒肝丸中和厚朴酚、木香烃内酯、去氢木香内酯及厚朴酚4个成分的含量,方法准确,操作简便,为本品提供了更加全面有效的定量分析依据。
1 仪器与试药 1.1 仪器LC-20AT高效液相色谱仪(日本岛津公司);Thermo Acclaim C18色谱柱(250 mm×4.6 mm,5 μm;填料:十八硅基硅烷键合硅胶;Thermo公司);AE240型电子天平(上海梅特勒仪器有限公司)。
1.2 试药对照品:和厚朴酚(批号110730-201313,含量99.1%)、厚朴酚(批号110729-200412)、去氢木香内酯(批号111525-201209,含量99.8%)、木香羟内酯(批号111524-201208,含量99.5%)购自中国食品药品检定研究院。
样品10批,购自市场,大蜜丸来自4个生产企业(批号分别为4015087、15030921、395034、1506141),水蜜丸来自3个生产企业(批号分别为2035292、3035527、20150501、20130701),小蜜丸来自1生产企业(批号分别为150201、150401),编号1~10。
甲醇、乙腈为色谱纯,水为去离子水,其他试剂均为分析纯。
2 方法与结果 2.1 溶液的制备 2.1.1 混合对照品溶液精密称取和厚朴酚、木香羟内酯、去氢木香内酯、厚朴酚的对照品分别约0.012、0.010、0.012、0.012 g,分别置25 mL量瓶中,加甲醇适量使溶解并稀释至刻度,摇匀,即得单一成分对照品储备液;分别精密量取上述的和厚朴酚、木香羟内酯、去氢木香内酯、厚朴酚的对照品储备液依次为2、3、5、4 mL,置同一100 mL量瓶中,加甲醇稀释至刻度,摇匀,即得和厚朴酚、木香羟内酯、去氢木香内酯、厚朴酚浓度分别为10、12、25、20 μg的混合对照品溶液。
2.1.2 供试品溶液取重量差异项下的本品,剪碎,取约0.8 g,精密称定,置具塞锥形瓶中,精密加入甲醇25 mL,密塞,称量,加热回流90 min,取出,放冷,再称量,用甲醇补足减失的量,摇匀,滤过,即得。
2.1.3 阴性样品溶液按处方比例及处方工艺制备缺木香、缺厚朴的阴性样品,并按“2.1.2”项下方法制备溶液,即得。
2.2 色谱条件与系统适用性试验色谱柱:Thermo Acclaim C18(250 mm×4.6 mm,5 μm);流动相:乙腈-0.05%磷酸(47:53);检测波长:230 nm;流速:1.0 mL·min-1;进样量:20 μL。理论板数按和厚朴酚峰计算应不低于3 000;各峰与相邻峰的分离度均大于1.5。
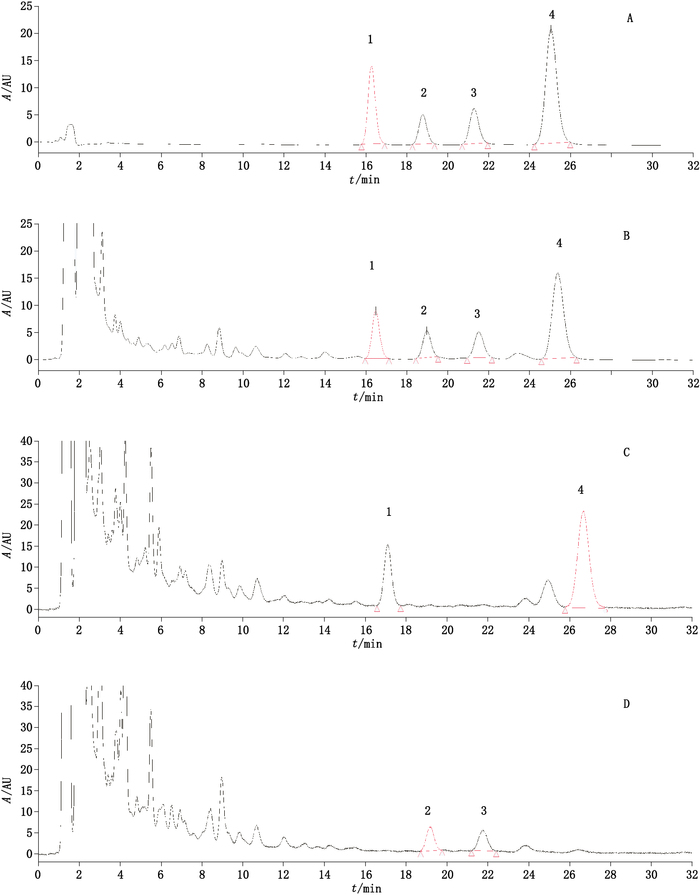
2.3 专属性考察分别取混合对照品溶液、供试品溶液及阴性样品溶液,按“2.2”项下色谱条件进样分析;结果样品色谱中,与对照品色谱相同保留时间处有色谱峰,而阴性样品色谱的相应位置无相应峰,不干扰测定。待测成分杂质分离度良好,结果见图 1。
|
1.和厚朴酚(honokiol)2.木香羟内酯(costunolide)3.去氢木香内酯(dehydrocostuslactone)4.厚朴酚(magnolol) 图 1 对照品(A)、样品(B)、厚朴阴性样品(C)及木香阴性样品(D)色谱图 Figure 1 Chromatograms of reference substances(A), sample(B), negative sample without Aucklandiae Radix(C)and negative sample without Magnoliae Officinalis Cortex(D) |
精密量取混合对照品溶液2 mL置10 mL量瓶中,加甲醇稀释至刻度,摇匀,得混合对照品溶液Ⅱ。精密吸取混合对照品溶液Ⅱ 5、10 μL及混合对照品溶液5、10、20 μL,分别注入液相色谱仪,按拟定的色谱条件测定,记录峰面积。以对照品进样量(μg)为横坐标,峰面积积分值为纵坐标,进行线性回归。结果和厚朴酚、木香羟内酯、去氢木香内酯、厚朴酚线性方程分别为
Y=3.724×106X-5.70×104
Y=1.650×106X-1.55×104
Y=1.131×106X-2.16×104
Y=5.315×106X-3.98×104
线性范围分别为0.020~0.401、0.025~0.499、0.051~ 1.029、0.040~0.796 μg;相关系数均为0.999 9,表明各待测成分线性关系良好。
2.5 重复性试验取同一大蜜丸样品(编号1)约0.64、0.8、0.96 g各3份,精密称定,按“2.1.2”项下方法制备9份供试品溶液,分别测定含量,结果样品中和厚朴酚、木香羟内酯、去氢木香内酯、厚朴酚的含量分别为0.106、0.175、0.292、0.232 mg·g-1,RSD分别为1.2%、1.3%、1.4%、1.1%,结果表明方法重复性良好。
2.6 稳定性试验取同一供试品溶液(编号1),分别在0、1、4、10、20和24 h进样测定,记录峰面积。结果RSD分别为1.2%、1.5%、1.2%、0.7%,表明供试品溶液中4个待测成分在室温放置24 h内基本稳定。
2.7 回收率试验取“2.5”项下已知含量的样品0.4 g,共9份,精密称定,分别置具塞锥形瓶中,精密加入不同浓度的对照品溶液各25 mL分别精密称取和厚朴酚、木香烃内酯、去氢木香内酯、厚朴酚对照品适量,以甲醇配制低浓度(含和厚朴酚1.203 μg·mL-1,木香羟内酯2.493 μg·mL-1,去氢木香内酯4.117 μg·mL-1,厚朴酚3.182 μg·mL-1)、中等浓度(含和厚朴酚1.503 μg·mL-1,木香羟内酯3.116 μg·mL-1,去氢木香内酯5.146 μg·mL-1,厚朴酚3.978 μg·mL-1)、高浓度(含和厚朴酚1.804 μg·mL-1,木香羟内酯3.740 μg·mL-1,去氢木香内酯6.175 μg·mL-1,厚朴酚4.773 μg·mL-1)对照品溶液适量,按“2.1.2”项下方法制备供试溶液,按“2.2”项下色谱条件进行分析,计算回收率,结果见表 1~4。和厚朴酚、木香羟内酯、去氢木香内酯、厚朴酚的平均回收率(n=9)分别为99.1%、100.4%、98.4%、101.4%,RSD分别为1.4%、1.7%、1.7%、2.0%,结果表明方法回收率良好,方法可行。
|
|
表 1 和厚朴酚回收率试验结果 Table 1 The results of the recovery tests of honokiol |
|
|
表 2 木香羟内酯回收率试验结果 Table 2 The results of the recovery tests of costunolide |
|
|
表 3 去氢木香内酯回收率试验结果 Table 3 The results of the recovery tests of dehydrocostuslactone |
|
|
表 4 厚朴酚回收率试验结果 Table 4 The result of the recovery test of Magnolol |
取10批舒肝丸样品(大蜜丸、小蜜丸、水蜜丸),分别按“2.1.2”项下方法制备供试品溶液,按“2.2”项下色谱条件进行测定,记录峰面积,再用外标法分别计算各成分的含量,结果见表 5。
|
|
表 5 样品测定结果(mg·g-1,n=2) Table 5 Contents of samples |
样品处方中药味多,成分复杂,杂质多,性质相近的成分多,流动相以甲醇作为有机相时,未能得到良好分离,结合提取方法考察及色谱条件的考察,最终选择乙腈作为有机相,将流动相比例设定为乙腈-0.05%磷酸溶液(47:53),各成分分离良好。
3.2 检测波长的选择称取和厚朴酚、木香羟内酯、去氢木香内酯、厚朴酚的对照品适量,分别用甲醇配制成适宜浓度的对照品溶液,在200~400 nm进行光谱扫描。结果表明,厚朴酚与和厚朴酚在210 nm波长附近未端最大吸收,去氢木香内酯与木香羟内酯仅在230 nm以下有末端吸收。在200~220 nm波长下,对样品进行测定,结果待测成分与杂质峰分离较差,因此选用待测成分响应较强且无杂质峰干扰的230 nm作为测定波长,此波长下各待测成分与杂质峰分离良好,阴性无干扰。
3.3 小结近年来,对中成药制剂的质量控制中仅控制单一指标不足以代表处方的整体作用。因此,制定多成分、多指标的含量测定方法[11-14],可从多方面控制中药制剂的产品质量,使其疗效可靠、稳定。
| [1] |
中国药典2015年版. 一部[S]. 2015: 1600. ChP 2015. Vol Ⅰ[S]. 2015:1600 |
| [2] |
陈斯, 李佩, 沈雨, 等. 厚朴饮片有效成分含量测定与分级标准研究[J]. 时珍国医国药, 2014, 25(8): 1964. CHEN S, LI P, SHEN Y, et al. Determination of effective components in Cortex Magnoliae Officinalis standard of classification[J]. Lishizhen Med Mater Med Res, 2014, 25(8): 1964. |
| [3] |
薛珍珍, 晏仁义, 余盛贤, 等. HPLC-DAD测定厚朴中6种活性成分的含量[J]. 中国实验方剂学杂志, 2014, 20(22): 45. XUE ZZ, YAN RY, YU SX, et al. Determination of six active compounds in commercial samples of Magnoliae Officinalis Cortex by HPLC-DAD[J]. Chin J Exp Tradit Med Form, 2014, 20(22): 45. |
| [4] |
张怡辰. 厚朴药材中厚朴酚与和厚朴酚的含量测定及化学模式识别[J]. 亚太传统医药, 2012, 8(3): 20. ZHANG YC. Measuring of magnolol and honokiol of Magnoliae and studies of chemical pattern recognition[J]. Asia-Pacific Tradit Med, 2012, 8(3): 20. |
| [5] |
杨红兵, 石磊, 李明明, 等. 湖北恩施产厚朴叶中厚朴酚与和厚朴酚定量分析[J]. 湖北中医药大学学报, 2012, 14(1): 43. YANG HB, SHI L, LI MM, et al. Quantitative analysis of the content of magnolol and honokiol in the leaf of Magnolia Officinalis produced in Hubei Enshi[J]. Hubei Univ Chin Med, 2012, 14(1): 43. |
| [6] |
李晓花, 马小军, 张忠廉, 等. 不同干燥条件下云木香中木香烃内酯和去氢木香内酯含量的高效液相色谱法测定[J]. 时珍国医国药, 2016, 27(3): 594. LI XH, MA XJ, ZHANG ZL, et al. Contents of costunolide and dehydrocostuslactone in Saussurea costus (Falc.) Lipech. with different drying temperature by HPLC[J]. Lishizhen Med Mater Med Res, 2016, 27(3): 594. |
| [7] |
胡益杰, 刘爽, 邓丽娜, 等. 川木香药材HPLC指纹图谱及含量测定方法研究[J]. 药物分析杂志, 2015, 35(11): 1946. HU YJ, LIU S, DENG LN, et al. HPLC fingerprint and determination method of herbal Vladimiria souliei (Franch.) Ling[J]. Chin J Pharm Anal, 2015, 35(11): 1946. |
| [8] |
易跃能. 不同产地和采收时间木香药材中木香烃内酯和去氢木香内酯的测定[J]. 长沙医学院学报, 2016, 14(3): 16. YI YN. Determination of costunolide and dehydrocostuslactone in Aucklandiae Radix produced in different areas and time by HPLC[J]. J Changsha Med Univ, 2016, 14(3): 16. |
| [9] |
蒋秋香, 黄昊, 蓝凤良. HPLC法测定香砂养胃片中4种有效成分的含量[J]. 药物分析杂志, 2015, 35(9): 1669. JIANG QX, HUANG H, LAN FL. Simultaneous determination of four effective components in the Xiangsha Yangwei tablets by HPLC[J]. Chin J Pharm Anal, 2015, 35(9): 1669. |
| [10] |
黄澜, 黄丽. RP-HPLC法同时测定保济丸中厚朴酚、和厚朴酚、木香烃内酯及去氢木香内酯的含量[J]. 药物分析杂志, 2012, 32(3): 396. HUANG L, HUANG L. RP-HPLC simultaneous determination of magnolol, honokiol, costunolide and dehydrocostuslactone in Baoji pills[J]. Chin J Pharm Anal, 2012, 32(3): 396. |
| [11] |
王姿媛, 胡惠兰. HPLC法同时测定厚朴温中滴丸中5个有效成分的含量[J]. 药物分析杂志, 2010, 30(9): 1717. WANG ZY, HU HL. HPLC simultaneous determination of five bioactive-components in Houpu Wenzhong drop-pills[J]. Chin J Pharm Anal, 2010, 30(9): 1717. |
| [12] |
刘楚阳, 刘韵. HPLC法同时测定沉香舒郁丸中四种成分的含量[J]. 实用药物与临床, 2017(5): 569. LIU CY, LIU Y. Simultaneous determination of the content of four constituents in Chenxiang Shuyu pill by HPLC[J]. Pract Pharm Clin Rem, 2017(5): 569. |
| [13] |
汪芳, 林吉, 邓丽红, 等. HPLC法同时测定加味穿心莲散中6种成分[J]. 中成药, 2014, 36(12): 2521. WANG F, LIN J, DENG LH, et al. Simultaneous determination of six constituents in Jiawei Chuanxinlian powder by HPLC[J]. Chin Tradit Pat Med, 2014, 36(12): 2521. DOI:10.3969/j.issn.1001-1528.2014.12.017 |
| [14] |
丁晓菊, 赵云丽, 高晓霞, 等. 高效液相色谱法同时测定厚朴温中胶囊中的7种有效成分[J]. 色谱, 2009, 27(1): 107. DING XJ, ZHAO YL, GAO XX, et al. Simultaneous determination of seven effective components in Houpu Wenzhong capsules using high performance liquid chromatography[J]. Chin J Chromatogr, 2009, 27(1): 107. |
 2017, Vol. 37
2017, Vol. 37 
