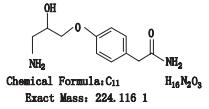
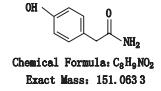
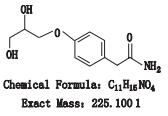
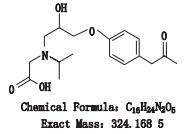
阿替洛尔为选择性β1肾上腺素受体阻滞剂,主要用于治疗高血压、心绞痛、急性心肌梗死,也可用于心肌病和心律失常等[1-7]。目前全国共有阿替洛尔片剂生产企业70个,涉及批准文号105个。经国内文献和外标准查询,英国药典2015年版、欧洲药典8.0版收载了阿替洛尔的8个杂质[8-9](图 1),但国内少有针对阿替洛尔片有关物质的系统研究与结构鉴定报道。
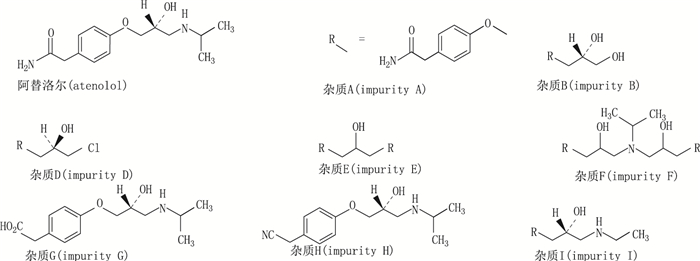
|
图 1 阿替洛尔及其杂质(A-I)的结构式 Figure 1 Structural formula of atenolol and the impurities(A-I) |
本研究以2015年国家药品计划抽验为契机,建立了适用于阿替洛尔片剂的LC-MS/MS分析方法,并结合稳定性研究对片剂中产生的有关物质进行结构鉴定和溯源,旨在完善质量标准,加强药品质量控制。
1 仪器与试药 1.1 仪器安捷伦公司Agilent 1260高效液相色谱仪及工作站;安捷伦公司Agilent 6530精确质量数四极杆-飞行时间质谱仪及工作站;沃特世公司Waters X-Bridge C18色谱柱(4.6 mm×250 mm,5 μm;填料:十八烷基硅烷键合硅胶)。
1.2 药品与试剂阿替洛尔原料(浙江亚太药业股份有限公司提供,批号3561A2RⅡ)及片剂(浙江亚太药业股份有限公司,批号8140510,规格50 mg);阿替洛尔对照品(中国食品药品检定研究院,批号100117-201105,100%);甲醇、三氟乙酸均为色谱纯,水为超纯水。
2 方法与结果 2.1 LC条件采用Waters X-Bridge C18色谱柱(4.6 mm×250 mm,5 μm),以0.1%三氟乙酸溶液-甲醇(90:10)为流动相,流速1.0 mL·min-1,柱温30 ℃,检测波长:225 nm及272 nm。
2.2 MS条件采用电喷雾离子源(ESI),正离子扫描模式,正离子化喷雾电压4.0 kV,雾化气压力31.03 kPa,干燥器温度350 ℃,干燥器流速12 mL·min-1,碎片电压150 V,碰撞能量15、25 eV。
2.3 供试品溶液配制取阿替洛尔片,精密称定,研细,精密称取适量(相当于阿替洛尔25 mg),置100 mL量瓶中,加流动相30 mL,超声使溶解,加流动相稀释至刻度,摇匀,滤过,取续滤液即得。
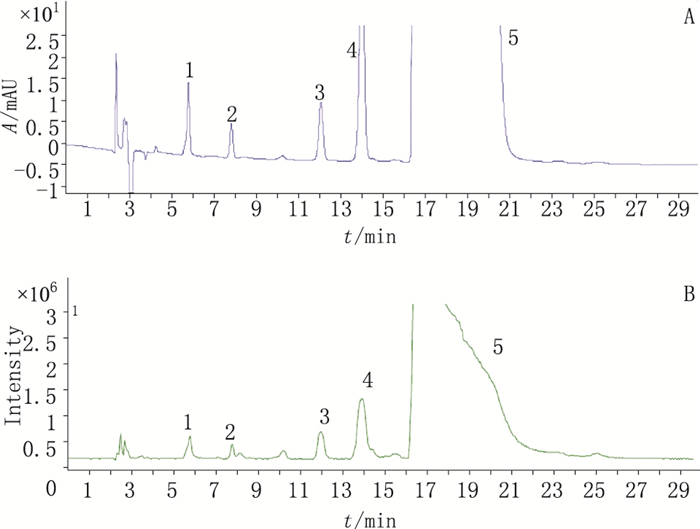
3 结果 3.1 阿替洛尔片有关物质检查按“2.1”和“2.2”项下的色谱和质谱条件,进样测定阿替洛尔片的供试品溶液。结果(图 2)表明,可检测到4个有关物质峰,采用外标法计算各有关物质,含量见表 1。
|
1.杂质1(impurity 1)2.杂质2(impurity 2)3.杂质3(impurity 3)4.杂质4(impurity 4)5.阿替洛尔(atenolol) 图 2 阿替洛尔片的色谱图(A)和总离子流图(B) Figure 2 PDA(A)and total ion(B)chromatograms of atenolol tablets |
|
|
表 1 阿替洛尔片有关物质含量 Table 1 Determination of the related substances in atenolol tablets |
对上述检出的4个有关物质进行质谱解析,并鉴定其可能结构。首选根据一级质谱测得各有关物质的精确相对分子质量和元素信息,再根据二级质谱获得的碎片信息,结合化合物的一般裂解规律,推测其可能的化学结构。阿替洛尔片有关物质的质谱信息见表 2。
|
|
表 2 阿替洛尔片中有关物质的LC-MS/MS信息 Table 2 Information of the related substances in atenolol tablets by LC-MS/MS |
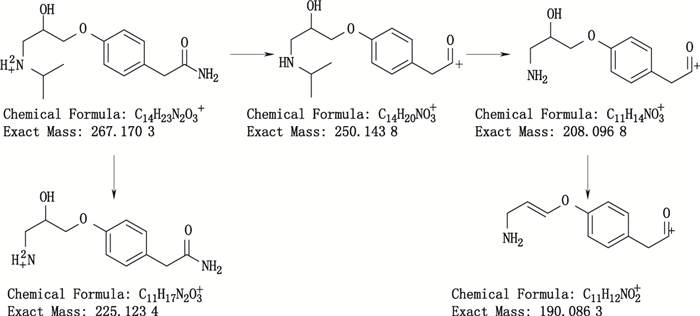
LC-MS/MS测得主化合物阿替洛尔的[M+H]+离子为m/z 267.170 3,其中子离子m/z 250.143 8为主化合物的[M+H]+离子丢失一分子氨基后形成的碎片离子;子离子m/z 225.123 4为主化合物的[M+H]+离子中性丢失异丙基后形成的碎片离子;子离子m/z 208.096 8为m/z 250.123 4脱去异丙基后形成的碎片离子;子离子m/z 190.086 3为m/z 208.096 8脱去一分子H2O后形成的碎片离子。其[M+H]+的MS2可能的裂解途径如图 3所示。
|
图 3 阿替洛尔可能的裂解途径 Figure 3 Proposed fragmentation pathways of atenolol |
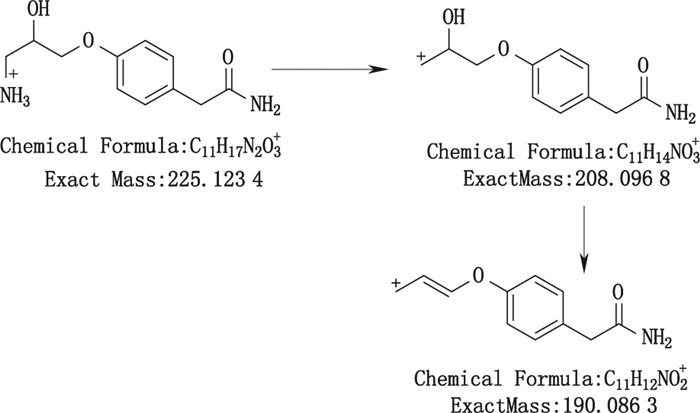
杂质1的[M+H]+离子为m/z 225.123 4,与[C11H17N2O3]+离子式相对应。其中子离子m/z 208.096 8为杂质1的[M+H]+离子脱去一分子氨基后形成的碎片离子,说明该杂质含有裸露的氨基;子离子m/z 190.086 3为m/z 208.095 7脱去一分子H2O后形成的碎片离子,该杂质未见丢失异丙基的碎片信息,说明该杂质不含异丙基。综上所述,杂质1所推测的结构及其[M+H]+离子MS2裂解途径见图 4。
|
图 4 杂质1可能的裂解途径 Figure 4 Proposed fragmentation pathways of impurity 1 |
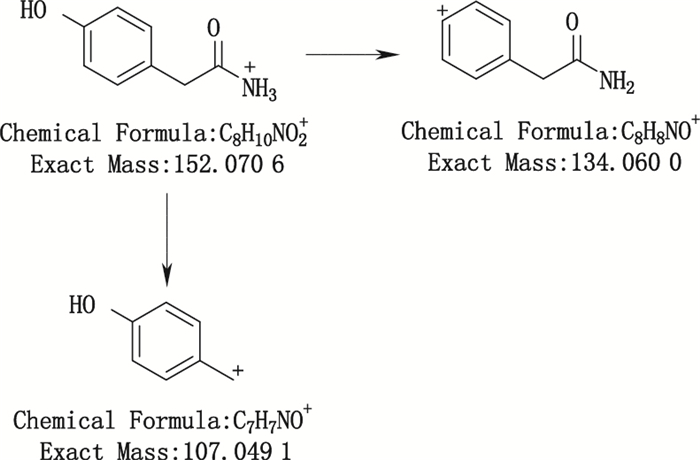
杂质2的[M+H]+离子为m/z 152.070 6,与[C8H10NO2]+离子式相对应。子离子m/z 134.060 0为杂质2的[M+H]+离子脱去一分子H2O后形成的碎片离子,说明该杂质含有裸露的羟基;子离子m/z 107.0491为杂质2的[M+H]+离子脱去乙酰基后形成的碎片离子。综上所述,杂质2所推测的结构及其[M+H]+离子MS2裂解途径见图 5。
|
图 5 杂质2可能的裂解途径 Figure 5 Proposed fragmentation pathways of impurity 2 |
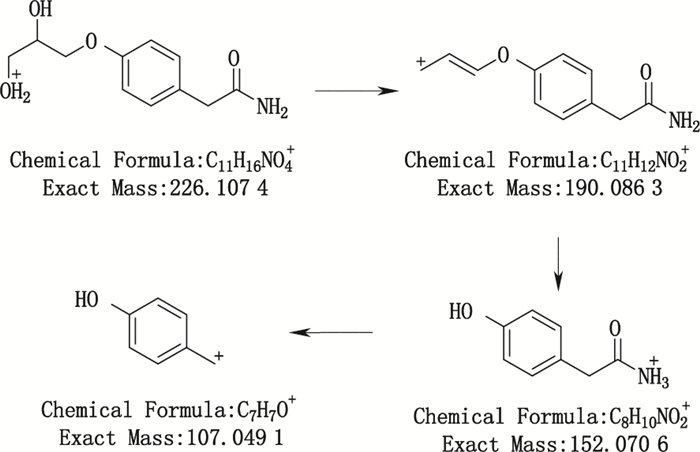
杂质3的[M+H]+离子位m/z 226.107 4,与[C11H16NO4]+离子式相对应。子离子m/z 190.086 3为杂质3的[M+H]+离子脱去两分子H2O后形成的碎片离子,判断该杂质可能含有2个裸露的羟基;子离子m/z 152.070 6为m/z 190.086 3脱去分子式为C3H2的片段后形成的碎片离子;子离子m/z 107.049 1为m/z 152.070 6脱去一分子乙酰基后形成的碎片离子,该杂质未见丢失异丙基的碎片信息,说明该杂质不含异丙基。综上所述,杂质3所推测的结构及其[M+H]+离子MS2裂解途径见图 6。
|
图 6 杂质3可能的裂解途径 Figure 6 Proposed fragmentation pathways of impurity 3 |
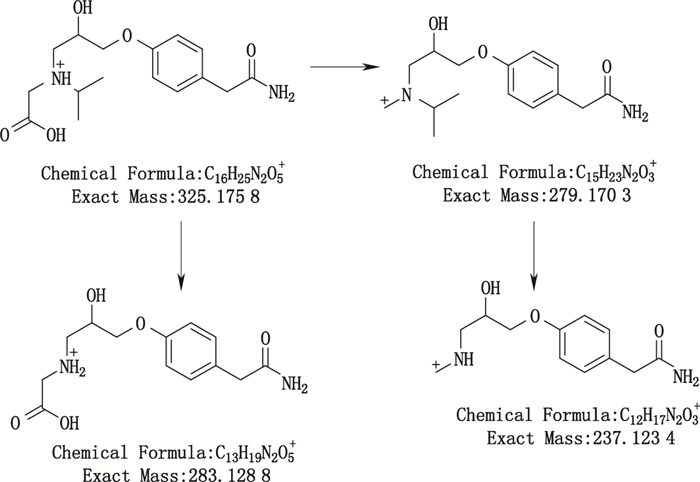
杂质4的[M+H]+离子为m/z 325.175 8,与[C16H25N2O5]+离子式相对应。子离子m/z 283.128 8为杂质4的[M+H]+离子中性丢失异丙基后形成的碎片离子,说明该杂质保留着主化合物的异丙基;子离子m/z 279.170 3为杂质4的[M+H]+离子脱去CH2O2的片段后形成的碎片离子,说明该杂质可能还有羧基;子离子m/z 237.123 4为m/z 279.170 3脱去异丙基后形成的碎片离子。综上所述,杂质4所推测的结构及其[M+H]+离子MS2裂解途径见图 7。
|
图 7 杂质4可能的裂解途径 Figure 7 Proposed fragmentation pathways of impurity 4 |
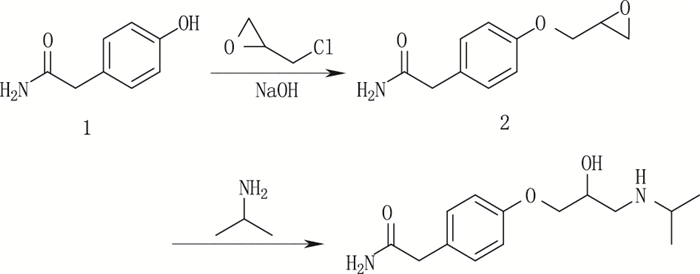
从生产企业提供的阿替洛尔合成路线:由对羟基苯乙酰胺与环氧氯丙烷在氢氧化钠碱液条件下反应得到环氧化物(缩合物),再与异丙胺反应得到阿替洛尔。见图 8。
|
1.对羟基苯乙酰胺(4-hydroxybenzeneacetamide)2.缩合物(condensation)3.阿替洛尔(atenolol) 图 8 阿替洛尔的合成工艺 Figure 8 Process for the synthesis of atenolol |
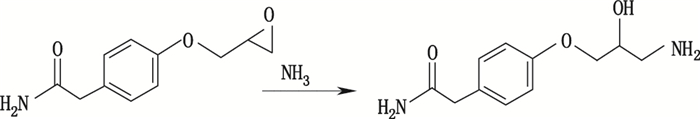
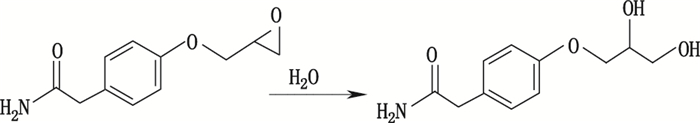
根据质谱解析结果及英国药典2015年版收载的阿替洛尔8个已知杂质结构(图 1),结合阿替洛尔合成路线,最终确定上述4个杂质的结构和化学名,见表 3,其中:杂质1为未知杂质,可能为缩合物被氨水开环得到,氨水可能来源于异丙胺,其可能的生成途径见图 9;杂质2即英国药典2015年版收载的杂质A,为未反应完全而残留的对羟基苯乙酰胺;杂质3即英国药典2015年版收载的杂质B,可能为缩合物被水开环得到,水可能来源于氢氧化钠碱液,其可能的生成途径见图 10;杂质4为未知杂质,来源有待进一步考察。
|
|
表 3 阿替洛尔片中的有关物质信息列表 Table 3 Information of the related substances in atenolol tablets |
|
图 9 杂质1可能的生成途径 Figure 9 Proposed production pathways of impurity 1 |
|
图 10 杂质3可能的生成途径 Figure 10 Proposed production pathways of impurity 3 |
中国药典2015年版等国内外药典[8-12]及相关文献[13-15]中收载的阿替洛尔有关物质检查方法,流动相中大多采用离子对试剂,无法用于质谱分析。本文建立了适合阿替洛尔LC-MS/MS分析的色谱条件,并对其进行了优化。在该色谱条件下,阿替洛尔及其有关物质均能有效分离且峰形较好。
4.2 阿替洛尔有关物质本文采用LC-MS/MS分析法,检测出阿替洛尔片的4个杂质,其中包含英国药典2015年版收载的2个已知杂质,其余2个杂质的结构未见报道。利用二级质谱对2个未知杂质进行结构解析,推测出其可能的结构,但结构的精准鉴定还有待借助多种手段进一步确证。
| [1] |
刘玉真, 聂新永, 谢英花, 等. RP-HPLC二极管阵列检测器对阿替洛尔注射液质量的研究[J]. 药物分析杂志, 2006, 26(3): 387. LIU YZ, NIE XY, XIE YH, et al. RP-HPLC diode array detector for determinating of related substances of atenolol and its injection[J]. Chin J Pharm Anal, 2006, 26(3): 387. |
| [2] |
李冰, 胡德福, 刘斐. HPLC法测定复方阿替洛尔片中阿替洛尔与硝苯地平的含量[J]. 药物分析杂志, 2004, 24(5): 485. LI B, HU DF, LIU F. HPLC determination of atenolol and nifedipine in compound atenolol tablets[J]. Chin J Pharm Anal, 2004, 24(5): 485. |
| [3] |
于丽丽, 刘佳川, 李华侃. 氯冉酸荷移分光光度法测定阿替洛尔片的含量[J]. 药物分析杂志, 2010, 30(3): 538. LIU LL, LIU JC, LI HK. Spectrophotometry determination of atenolol in tablets based on charge transfer complex of atenolol with chloranilic acid[J]. Chin J Pharm Anal, 2010, 30(3): 538. |
| [4] |
孙晶, 王艳杰, 李桂香. 阿替洛尔对映体的制备、活性以及手性分析方法简述[J]. 中医临床研究, 2010, 2(5): 104. SUN J, WANG YJ, LI GX. Description of atenolol to the preparation, activity and chiral analysis method of enantiomer[J]. Clin J Chin Med, 2010, 2(5): 104. |
| [5] |
董丽丽, 王春平. 拟反相液相色谱法测定阿替洛尔[J]. 分析试验室, 2013, 32(1): 114. DONG LL, WANG CP. Analysis of atenolol by pseudo reversedphase high performance liquid chromatography[J]. Chin J Anal Lab, 2013, 32(1): 114. |
| [6] |
郭小兰, 赵娟, 王兰, 等. 高效液相色法测定阿替洛尔片中阿替洛尔的含量[J]. 中南药学, 2007, 5(2): 117. GUO XL, ZHAO J, WANG L, et al. Dertermination of atenolol in atenolol tablets[J]. Cent South Pharm, 2007, 5(2): 117. |
| [7] |
陈静, 涂莉, 肖佩玉. 阿替洛尔片溶出度测定方法的改进[J]. 华西药学杂志, 2006, 21(6): 613. CHEN J, TU L, XIAO PY. Improvement of the dissolution test method of atenolol tablets[J]. West China J Pharm Sci, 2006, 21(6): 613. |
| [8] |
BP 2015. Vol Ⅲ[S]. 2015:157
|
| [9] |
EP 8.0. Vol Ⅲ[S]. 2012:1595
|
| [10] |
USP 38-NF33. Vol Ⅲ[S]. 2015:2309
|
| [11] |
中国药典2015年版. 二部[S]. 2015: 572 ChP 2015. Vol Ⅱ[S]. 2015:572 |
| [12] |
IP 2010. Vol Ⅱ[S]. 2010:848
|
| [13] |
刘红莉, 曹凤习, 赫晓军, 等. 阿替洛尔及其片剂有关物质检查法的改进[J]. 中国药品标准, 2009, 10(5): 380. LIU HL, CAO FX, HE XJ, et al. Improvement of related substances test method for atenolol and tablets[J]. Drugs Stand China, 2009, 10(5): 380. |
| [14] |
沈娟, 武向峰, 孔爱英, 等. 高效液相色谱法测定阿替洛尔片中阿替洛尔含量及其有关物质[J]. 中国医院药学杂志, 2004, 24(12): 744. SHEN J, WU XF, KONG AY, et al. Determination of atenolol and the relevant impurities in atenolol tablets by HPLC[J]. Chin Hosp Pharm J, 2004, 24(12): 744. DOI:10.3321/j.issn:1001-5213.2004.12.013 |
| [15] |
刘红莉, 姜建国, 宋更申, 等. 两个波长处测定阿替洛尔有关物质的比较[J]. 中国药业, 2010, 19(12): 50. LIU HL, JIANG JG, SONG GS, et al. Comparsion of detecting related substances of atenolol by two wavelengths[J]. China Pharm, 2010, 19(12): 50. DOI:10.3969/j.issn.1006-4931.2010.12.035 |
 2017, Vol. 37
2017, Vol. 37