2. 南京工业大学江苏省药物研究所, 南京 210009
2. Jiangsu Provincial Institute of Material Medica, Nanjing Tech University, Nanjing 210009, China
聚四氟乙烯(polytetrafluoroethene,PTFE),俗称”塑料王”,商标名Teflon。作为一种特种工程塑料,近年来聚四氟乙烯一直是用量最大的氟塑料,由于其抗酸抗碱、高度的化学稳定性、极强的耐高低温性能[1]等具有广泛的应用。
药品与药品包装材料之间可能会发生渗透、溶出、吸附等问题,所以包装材料尽量采用化学惰性的材料,聚四氟乙烯包装材料因其耐酸碱、不易与药品发生反应,同时具有良好的阻隔性而广泛的用于药品包装领域。在聚四氟乙烯聚合过程中加入全氟辛酸(pentadecafluorooctanoic acid,PFOA)和全氟辛基磺酸类物质,可以起到均分散的作用[2]。然而随着人们对全氟辛酸和全氟辛基磺酸类物质的毒理学[3]、环境行为[4]和迁移检验[5]的研究的不断深入,全氟类化合物已造成严重的环境累积和污染,成为继有机氯农药、二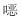
PFOA的结构式见图 1,十五氟辛酸,化学式为C8HF15O2,相对分子质量为414.07,呈强酸性,在水中能完全解离与强氧化剂及还原剂不起反应。有较高界面活性,与纯碱反应生成盐;与伯醇、仲醇反应生成酯。
|
图 1 全氟辛酸结构式 Figure 1 Structure of PFOA |
PFOS的结构式见图 2,十七氟辛烷磺酸,分子式为C8H4F17NO3S,分子量为500.13,它是完全氟化的阴离子,以盐的形式广泛使用或渗入较大的聚合物。

|
图 2 全氟辛基磺酸结构式 Figure 2 Structure of PFOS |
本文所研究的是QT脂质体注射液用镀膜胶塞中的PFOA及PFOS的迁移,其胶塞是镀聚四氟乙烯膜(Polytetrafluoroethene,Teflon)胶塞,目前国内的研究多集中于PFOA和PFOS在生物体内含量的检测[15-16],而鲜有对药用镀聚四氟乙烯膜中的全氟辛酸及全氟辛基磺酸的迁移同时检测的报道。由于本实验中的检测灵敏度较高,全氟辛酸及全氟辛基磺酸的灵敏度均为10 ng·mL-1,故采用高灵敏度、高选择性的高效液相色谱-质谱/质谱(LC-MS/MS)的方法同时检测QT脂质体注射液用镀膜胶塞中的PFOA及PFOS,对建立药品包装材料中PFOA和PFOS的迁移研究具有一定的参考借鉴意义。
1 仪器与试药Waters Quattro Micro三重四极杆质谱仪,Waters 2695液相色谱仪(沃特斯中国有限公司),含在线真空脱气机、四元梯度泵、恒温自动进样器、柱温箱、电喷雾离子源(ESI);Masslynx4.0数据分析系统。Waters Symmetry C18色谱柱(填料:十八烷基硅烷键合硅胶;150 mm×3.0 mm,5 μm;沃特斯中国有限公司)。
QT脂质体注射液(规格20 mL:40 mg,批号:20160225);药用镀聚四氟乙烯膜氯化丁基橡胶/聚异戊二烯橡胶塞(规格:抗生素瓶塞;批号:3128010603,新加坡西氏医药服务公司);PFOS对照品(100 μg·mL-1甲醇溶液,SIGMA-ALDRICH公司,批号SZBE008XV);PFOA对照品(SIGMA-ALDRICH公司,纯度96%,批号MKBT7500V);甲醇溶液(Honeywell公司,HPLC Grade,AH230-4HC);乙腈溶液(Honeywell公司,HPLC Grade,AH015-4HC);乙酸铵(Aladdin公司,纯度99.99%,Lot#k1516011)。
2 方法与结果 2.1 LC-MS条件 2.1.1 色谱条件色谱柱:Waters Symmetry C18柱(150 mm×3.0 mm,5μm);流动相:0.01 mol·mL-1乙酸铵-乙腈(55:45);流速:0.4 mL·min-1,分流进样;进样量:20μL;柱温:40 ℃。
2.1.2 质谱条件电喷雾离子(ESI)源,负离子模式检测;毛细管电压:3.0 kV;锥孔电压:30 V;源温:120 ℃;脱溶剂区温度:350 ℃碰撞气(氩气);压力:1.0×10-4 mbar;脱溶剂气流速:400 L·h-1;气帘气流速:50 L·h-1。
2.2 溶液配制PFOA储备液:取PFOA对照品10 mg至100 mL量瓶中,用甲醇溶解、稀释、定容,制成100 μg·mL-1的储备液;
PFOA与PFOS混合对照品溶液:精密量取PFOA100 μg·mL-1的储备液、PFOS100 μg·mL-1的储备液各1 mL至100 mL量瓶中,加甲醇溶解定容,制成1 μg·mL-1的PFOA与PFOS的混合溶液;再精密量取1 μg·mL-1的PFOA与PFOS的混合溶液1 mL至100 mL量瓶中,制成10 ng·mL-1PFOA与PFOS的混合溶液,摇匀,作为混合对照品溶液;
空白溶液:精密量取QT脂质体注射液1 mL,置10 mL量瓶中,加甲醇稀释、定容,摇匀,作为空白溶液。
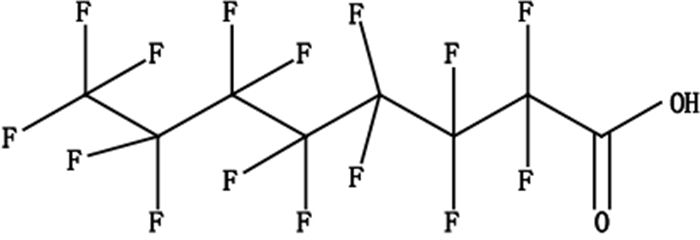
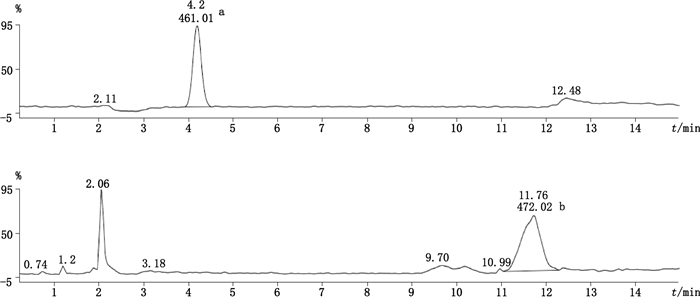
2.3 专属性试验精密量取“2.2”中PFOA与PFOS混合对照品溶液、空白溶液各20μL,注入液相色谱仪,进样测定,结果无干扰,见图 3~4。
|
a.PFOA碎片离子峰(fragment ion peak of PFOA)b.PFOA碎片离子峰(fragment ion peak of PFOS); 图 3 PFOA与PFOS混合对照品溶液二级质谱图 Figure 3 The MS/MS spectra of PFOS、PFOA mixed reference solution |
|
图 4 空白溶液二级质谱图 Figure 4 The MS/MS spectra of blank solution |
精密量取“2.2”中PFOA储备液,加甲醇稀释、定容制成2 μg·mL-1的PFOA储备液,再分别移取不同体积的上述储备液加甲醇稀释、定容制成浓度约为8.0、10.0、25.0、50.0、100.0、200.0 ng·mL-1的标准曲线溶液,分别进样,记录离子流图。以浓度C(ng·mL-1)为横坐标,母离子峰面积A为纵坐标,进行线性回归,得回归方程为:
A=42.52C-19.25 r=0.999 9
结果表明PFOA在8.296~207.4 ng·mL-1范围内线性良好。
精密量取PFOS储备溶液,加甲醇稀释、定容制成2 μg·mL-1的PFOS储备液,再分别移取不同体积的上述储备液加甲醇稀释、定容制成浓度约为8.0、10.0、25.0、50.0、100.0、200.0 ng·mL-1的标准曲线溶液,分别进样,记录离子流图。以浓度C(ng·mL-1)为横坐标,母离子峰面积A为纵坐标,进行线性回归,得回归方程为:
A=44.10C-2.872 r=0.999 8
结果表明PFOA在8.000~200.0 ng·mL-1范围内线性良好。
以信噪比S/N=3为最低检出限,信噪比为S/N=10为定量限。结果表明PFOA、PFOS在本色谱条件下检出限分别为2.074 ng·mL-1、2.000 ng·mL-1,定量限分别为8.296 ng·mL-1、8.000 ng·mL-1。
2.5 回收率试验及进样精密度试验分别精密量取QT脂质体注射液1.0 mL,置10 mL量瓶中,再分别精密加入不同浓度的PFOA对照品储备液0.05 mL,加入甲醇稀释、定容,摇匀,制成浓度分别约含PFOA为10.0、50.0、200.0 ng·mL-1的溶液。进样测定,结果平均回收率为105.9%,RSD为7.5%。
分别精密量取QT脂质体注射液1.0 mL,置10 mL量瓶中,再分别精密加入不同浓度的PFOS对照品储备液0.05 mL,加入甲醇稀释、定容,摇匀,使制成浓度分别约含PFOS为10.0、50.0、200.0 ng·mL-1的溶液。进样测定,结果平均回收率为103.7%,RSD为7.2%。
取工作曲线中间浓度的混合对照品溶液,连续进样5针,结果表明,该液质条件下PFOA与PFOS的日内进样精密度良好,RSD分别为2.5%、3.0%。
取工作曲线中间浓度的混合对照品溶液,于不同天重复进样,结果表明,该液质条件下PFOA与PFOS的日间进样精密度良好,RSD分别为2.4%、3.1%。
2.6 重复性试验与中间精密度试验取QT脂质体注射液,按回收率试验方法,精密量取PFOA对照品储备液适量,加入甲醇稀释定容,制成浓度含PFOA 51.85 ng·mL-1的供试品溶液(n=6);再精密量取PFOS对照品储备液适量,加入甲醇稀释定容,制成浓度含PFOS 50 ng·mL-1的供试品溶液(n=6)进样测定,结果供试品溶液中检测出的PFOA与PFOS平均含量分别为51.19、49.25 ng.mL-1
于不同天不同操作人员,按上述方法制成供试品溶液(n=3),进样测定,结果供试品溶液中检出的PFOA与PFOS的RSD分别为1.5%、1.1%。
2.7 样品测定及结果分别按“2.2”中PFOA与PFOS混合对照溶液的方法,制得对照品溶液;精密量取QT脂质体注射液1 mL,置10 mL量瓶中,加甲醇稀释、定容,摇匀,作为供试品溶液;分别精密量取混合对照品溶液和供试品溶液各20μL,分别注入LC-MS/MS,记录离子流图,按外标法以母离子峰面积计算。结果见表 1。
|
|
表 1 PFOA与PFOS迁移测定结果 Table 1 Migration assay results of PFOA and PFOS |
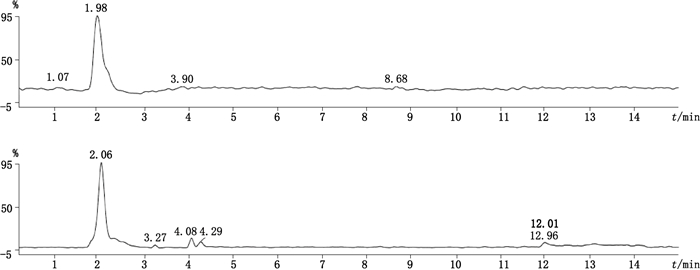
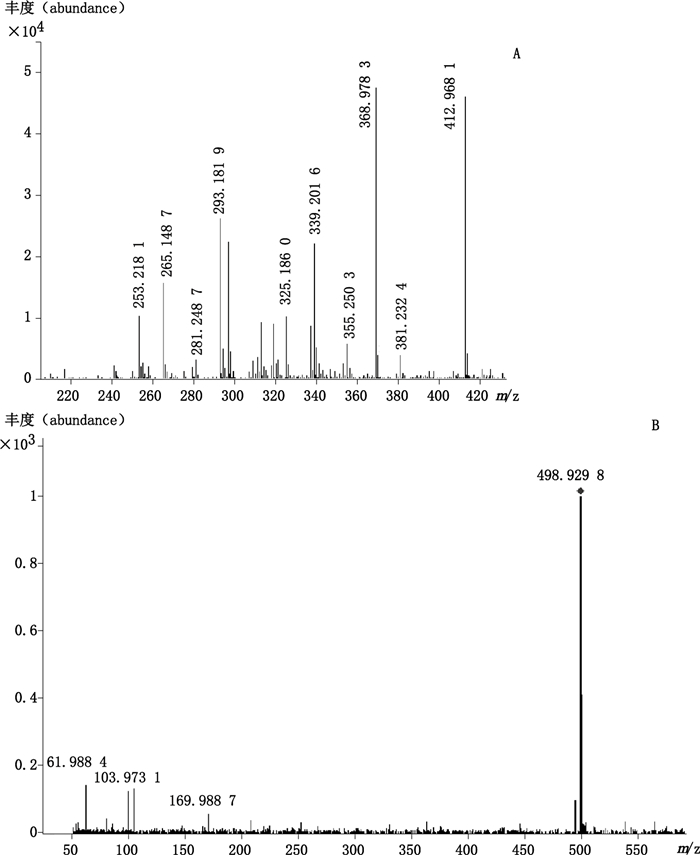
PFOA(A)和PFOS(B)的二级质谱图见图 5,从图中可以看出PFOA母离子[M-H]- m/z 412.968 1的主要碎片峰有m/z368.978 3、339.201 6、293.181 9、265.148 7、253.218 1,由于m/z368.978 3的灵敏度最高,故选用m/z 368.978 3作为PFOA的检测离子;同理PFOS母离子[M-H]- m/z 498.929 8的主要碎片峰有m/z 169.988 7、103.973 1、61.988 4,故选用m/z 498.929 8作为PFOS的检测离子。
|
图 5 PFOA(A)和PFOS(B)的二级质谱图 Figure 5 The MS/MS spectra of PFOA(A)and PFOS(B) |
本实验中PFOA与PFOS限度为10 ng·mL-1,检测浓度极低,且二者结构中均无共轭双键,无紫外吸收,因此采用LC-MS/MS方法测定QT脂质体注射液胶塞中PFOA、PFOS的迁移。另本实验所用样品为脂质体注射液,其中含有氢化卵磷脂、双硬脂酰磷脂酰胆碱、胆固醇等强脂溶性辅料,这些辅料很难从色谱柱上洗脱下来,基线持续上扬,使得PFOA及PFOS响应降低,故本实验采用三通阀切换将油性基质分流,不进质谱仪。
| [1] |
夏俊, 王学军, 王维东. 聚四氟乙烯材料相关标准现状与趋势[J]. 塑料工业, 2014, 42(4): 124. XIA J, WANG XJ, WANG WD. The standards situation and trends of PTFE[J]. China Plast Ind, 2014, 42(4): 124. |
| [2] |
吕刚. 药品包装材料中全氟辛基磺酸类物质检测与安全评价技术[D], 2009-8 LV G. Study on Determination and Safety Assessment of Perfluorooctane Sulfonate(PFOS) in drug packaging materials. [D], 2009-8 |
| [3] |
孙丽莎, 陆光华, 叶秋霞. 全氟化合物的分布、累积及生态毒理学效应[J]. 四川环境, 2012, 31(2): 119. SUN LS, LU GH, YE QX. The distribution、cumulative and ecotoxicology effects of perfluorinated compounds[J]. Sichuan Envir, 2012, 31(2): 119. |
| [4] |
史亚利, 蔡亚岐. 全氟和多氟化合物环境问题研究[J]. 化学进展, 2014, 4(26): 665. SHI YL, CAI YQ. Research of perfluorinated and polyfluorinated compound environmental problems[J]. Progr Chem, 2014, 4(26): 665. |
| [5] |
冯盘, 施佳慧, 朱加进. 不粘锅涂层和爆米花袋残留全氟化合物的提取方法[J]. 食品与机械, 2010, 26(3): 167. FENG P, SHI JH, ZHU JJ. Research progress on the extraction of perfluorinated compounds residues from the surface of non-stick cookware and microwave popcorn packaging bags[J]. Food Machin, 2010, 26(3): 167. |
| [6] |
张倩, 张超杰, 周琪. SPE-HPLC/MS联用法测定地表水中的PFOA及PFOS含量[J]. 四川环境, 2006, 25(4): 10. ZHANG J, ZHANG CJ, ZHOU Q. Determination of PFOA and PFOS in the surface water by SPE-HPLC/MS[J]. Sichuan Envir, 2006, 25(4): 10. |
| [7] |
王传现, 郭德华, 李波, 等. 固相萃取富集净化-高效液相色谱串联质谱法测定饮用水中全氟化合物[J]. 卫生研究, 2007, 36(6): 727. WANG CX, GUO DH, LI B, et al. Determination of perfluorinated compounds in drinking water by high performance liquid chromatography-tandem mass spectrometry with solid phase extraction and preconcentration[J]. J Hygin Res, 2007, 36(6): 727. |
| [8] |
蒋海宁, 孙明星, 陈宗宏. Teflon材料及不粘锅涂层中的微量全氟辛酸(PFOA)的GC-MS测定研究[J]. 复旦学报(自然科学版), 2007, 46(3): 291. JIANG HL, SUN MX, CHEN ZH. Determination of PFOA in Teflon non-stick coatings and materials by GC-MS[J]. J Fudan Univ(Nat Sci), 2007, 46(3): 291. |
| [9] |
周庆, 张满成, 卢宇飞, 等. 全氟类化合物的检测与治理研究进展[J]. 环境科学与技术, 2008, 31(7): 44. ZHOU Q, ZHANG MC, LU YF, et al. Advances in detection and treatment of perfluorinated compounds[J]. Envir Sci Technol, 2008, 31(7): 44. |
| [10] |
关于限制全氟辛基磺酸销售及使用的指令[S]. 2016-12-27 Directive on the restriction of PFOS sales and use(2006122EC) [S]. 2016-12-27 |
| [11] |
于文佳, 卫碧文, 杨荣静. 液相色谱-串联质谱法快速测定电子电气产品中全氟辛酸和全氟辛基磺酸[J]. 中国分析试验室, 2010, 29(9): 35. YU WJ, WEI BW, YANG RJ. Rapid determination of PFOA and PFOS in electrical and electronic products by LC-MS/MS[J]. Chin J Anal Lab, 2010, 29(9): 35. |
| [12] |
于徊萍, 卢利军, 张代辉, 等. 液相色谱串联质谱法测定纺织品中PFOS和PFOA[J]. 纺织学报, 2008, 29(5): 80. YU HP, LU LJ, ZHANG DH, et al. Determination of PFOS and PFOA in textiles by LC-MS-MS[J]. J Textile Res, 2008, 29(5): 80. |
| [13] |
联邦食品、药品和化妆品法案[S]. 2016-1-4 Federal food, drug and Cosmetic Act[S]. 2016-1-4 |
| [14] |
陈剑君, 方凯, 胡鸣韵. PFOA和PFOS检测方法研究进展[J]. 化工生产与技术, 2011, 18(3): 9. CHEN JJ, FANG K, HU MY. Research Progress on detection methods of PFOA[J]. Chem Prod Technol, 2011, 18(3): 9. |
| [15] |
王雨昕, 李敬光, 赵云峰. 生物基质中全氟辛酸与全氟辛基磺酸及其前体化合物的超高效液相色谱-串联质谱法研究[J]. 分析化学研究报告, 2011, 39(8): 1134. WANG YX, LI JG, ZHAO YF. Research of PFOA、PFOS and precursor compound in the biological substrate by UPLC-MS/MS[J]. Chin J Anal Chem, 2011, 39(8): 1134. |
| [16] |
王贤亲, 吴建章, 李艳霞. LC-MS/MS测定人血浆中阿米替林的含量[J]. 药物分析杂志, 2009, 11(29): 1846. WANG XQ, WU JZ, LI YX. Determination of amitriptyline in human plasma by LC-MS/MS[J]. Chin J Pharm Anal, 2009, 11(29): 1846. |
 2017, Vol. 37
2017, Vol. 37 
