补中益气丸由黄芪、白术、陈皮、升麻、柴胡、人参、甘草和当归组成,黄芪为君药,该复方主治脾虚气陷证,具有抗溃疡、调节免疫、抗肿瘤及抗胃黏膜损伤等功效[1-2]。中药的药理药效是多种有效组分协同作用的结果,制剂的质量评定应是多种组分的考察。现代研究表明,补中益气丸中有效成分很多,如陈皮和甘草中的黄酮类,具有抗炎症、抗氧化、心血管保护等生物活性[3-4];人参和柴胡中的皂苷类具有神经保护、抗肿瘤等功效[5-6]。这些化合物含量的同时分析在相关文献报道[2, 7-10]中并未涉及,现行标准只采用HPLC法对黄芪甲苷进行定量测定,亦不能有效地控制药品的内在质量[11]。近年来LC-MS法已成为一种多成分微量分析的重要方法,尤其是超高效色谱(UPLC)分离技术的应用,使得高通量分析成为可能[12-13]。鉴于补中益气丸中多指标成分精确定量测定方法的研究尚未见报道,本文采用UPLC-MS法同时检测补中益气丸复方中15种指标成分,为该制剂的质量控制提供参考。
1 仪器与材料Agilent 1290 Infinity-6460 QqQ LC-MS/MS联用仪(色谱工作站:MassHunter B.04.00,美国Agilent公司),十万分之一电子分析天平(Mettler Toledo AB135-S型),万能粉碎机(北京中兴伟业仪器有限公司)。Zorbax Eclipse Plus C18色谱柱(填料:十八烷基硅烷键合硅胶;100 mm×2.1 mm,1.8 μm;Agilent公司)。
甘草苷(批号20151031)、柚皮苷(批号20150512)、橙皮苷(批号20150622)、新橙皮苷(批号20150622)、甘草素(批号20150730)、橙皮素(批号20150510)、柚皮素(批号20150512)、升麻素(批号20150129)、黄芪甲苷(批号20151122)、人参皂苷Rb1(批号20150821)、人参皂苷Rb2(批号20150811)、人参皂苷Rd(批号20150427)、人参皂苷Rg1(批号20150427)、甘草酸(批号20151031)、柴胡皂苷a(批号20150923)和内标(IS)黄芩苷(批号20150905)对照品均由南京泽朗生物科技有限公司提供,对照品经HPLC峰面积归一化法检测纯度均在98%以上。甲醇、乙腈为色谱纯(Merk公司),甲酸为色谱纯(Tedia公司),超纯水经过Milli-Q系统纯化制备,其余试剂均为分析纯,购自国药集团。黄芪、白术、陈皮、升麻、柴胡、人参、甘草和当归购买自亳州中药材公司,6批补中益气丸由江苏省连云港中医药高等职业技术学校中药饮片厂制作,批号分别为20151208、20151214、20151220、20151224、20151229、20160107。8味药材等量制丸,丸重(180± 20)mg,每丸共含生药3.206 mg。
2 方法与结果 2.1 仪器条件色谱柱为Agilent Zorbax Eclipse Plus C18(100 mm×2.1 mm,1.8 μm);体积流量0.4 mL·min-1;进样量5 μL;柱温35 ℃;流动相为0.1%甲酸乙腈溶液(A)-0.1%甲酸溶液(B),梯度洗脱程序:0~4 min,15%→25%A;6~10 min,45%→55%A;12~15 min,70%→85%A。平衡时间为5 min。
电离方式为负离子模式(ESI-);多反应离子检测模式(MRM)。毛细管电压4.5 kV;离子源温度120 ℃;脱溶剂温度320 ℃;脱溶剂气体(N2)体积流量600 L·h-1。各成分的检测离子的质荷比,锥孔能量见表 1。
|
|
表 1 十五种化合物的MRM质谱参数,线性范围,r2和定量下限 Table 1 MRM parameters, linear ranges, coefficient of determinations(r2)and LLOQ for 15 analytes |
分别精密称取各对照品10 mg,单独以纯甲醇溶解并定容,制成质量浓度分别为1.0 mg·mL-1对照品储备液;分别精密量取适量储备液混合置容量瓶中,以甲醇稀释,制得系列混合对照品溶液,避光4 ℃保存。内标黄岑苷对照品溶液,加甲醇稀释至质量浓度为500 ng·mL-1。
2.2.2 供试品溶液取补中益气丸10粒,精密称定质量,按1︰10比例加入纯水,水浴回流1 h,称定质量,用纯水填补损失的质量,重复两次提取。避光保存,临用前12 000 r·min-1离心10 min,取上清液作为供试品溶液。
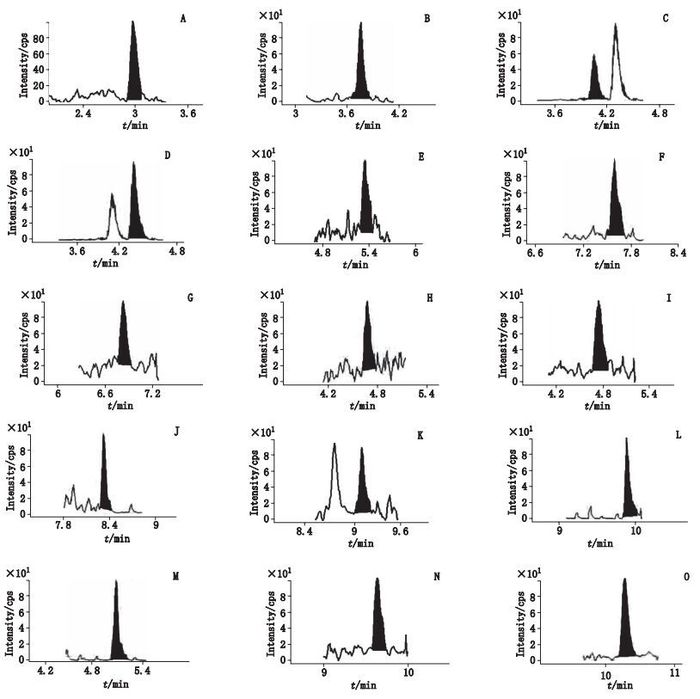
2.3 线性关系考察所测成分的定量下限(LLOQs)要求信噪比S/N>10,6次进样的峰面积精密度的RSD≤15%。根据预实验的样品含量范围考察,选择7个浓度的混合对照品溶液在3 d内每天重复进样(n=3),分别计算各成分的平均峰面积与相应内标的平均峰面积的比值Y,以比值Y对进样质量浓度X(ng·mL-1)进行线性回归,得回归方程。15种主要成分回归方程线性范围、相关系数(r2)、LLOQs见表 1,批号20151229样品的MRM离子图见图 1。结果表明,各化合物在相应质量浓度范围内呈良好的线性关系(r2为0.992~0.998)。
|
A.甘草苷(liquiritin)B.柚皮苷(naringin)C.橙皮苷(hesperidin)D.新橙皮苷(neohesperidin)E.甘草素(liquiritigenin)F.橙皮素(hesperetin)G.柚皮素(naringenin)H.升麻素(cimifugin)I.黄芪甲苷(astragaloside Ⅳ)J.人参皂苷Rb1(ginsenoside Rb1)K.人参皂苷Rb2(ginsenoside Rb2)L.人参皂苷Rd(ginsenoside Rd)M.人参皂苷Rg1(ginsenoside Rg1)N.甘草酸(glycyrrhizic acid)O.柴胡皂苷a(saikosaponin a) 图 1 15种化合物的样品MRM质谱图 Figure 1 Typical MRM chromatograms of the 15 compounds from a real sample |
取质量浓度为20 ng·mL-1(低浓度)和1 000 ng·mL-1(高浓度)混合对照品溶液,连续进样6次,测定各化合物的峰面积与内标峰面积比值Y,计算得15种化合物低高浓度下的Y的RSD分别在1.2%~4.6%和1.6%~7.4%之间。
2.5 重复性试验按“2.2.2”项供试品溶液制备方法平行制备6份供试品溶液,分别测定,样品中甘草苷、柚皮苷、橙皮苷、新橙皮苷、甘草素、橙皮素、柚皮素、升麻素、黄芪甲苷、人参皂苷Rb1、Rb2、Rd、Rg1、甘草酸和柴胡皂苷a含量的RSD分别为1.4%、1.2%、1.2%、0.96%、1.5%、1.5%、1.7%、1.6%、0.74%、2.3%、2.1%、1.5%、2.2%、0.53%和1.4%,结果表明该方法重复性良好。
2.6 稳定性试验取精密度试验项下的混合对照品溶液,自配制后第0、2、4、8、12、24、48 h依次进样,分别测定,结果低浓度下甘草苷,柚皮苷,橙皮苷,新橙皮苷,甘草素,橙皮素,柚皮素,升麻素,黄芪甲苷,人参皂苷Rb1、Rb2、Rd、Rg1,甘草酸和柴胡皂苷a的RSD分别为2.8%、1.6%、2.2%、1.0%、2.2%、3.0%、0.81%、1.7%、2.0%、3.3%、3.1%、4.9%、2.5%、2.0%、3.8%,高浓度下的RSD在0.96%~4.5%间,结果表明供试品溶液在24 h内稳定。
2.7 加样回收率试验取已测定的补中益气丸(批号20160107)10粒,精密加入高、低2种质量浓度的各成分混合对照品适量,每组平行3份,按供试品溶液配制方法操作,测定各成分的量,计算回收率。结果甘草苷,柚皮苷,橙皮苷,新橙皮苷,甘草素,橙皮素,柚皮素,升麻素,黄芪甲苷,人参皂苷Rb1、Rb2、Rd、Rg1,甘草酸和柴胡皂苷a的平均回收率分别为96.6%、96.7%、103.5%、104.3%、98.2%、97.2%、98.1%、102.5%、97.3%、95.8%、96.8%、96.7%、97.0%、98.4%和103.8%,对应的RSD在2.4%~8.7%间。
2.8 样品测定6批补中益气丸样品,按照“2.2.2”项方法处理,每个批次制备3份供试品,进行分析,内标法计算。结果每粒补中益气丸含甘草苷,柚皮苷,橙皮苷,新橙皮苷,甘草素,橙皮素,柚皮素,升麻素,黄芪甲苷,人参皂苷Rb1、Rb2、Rd、Rg1,甘草酸和柴胡皂苷a的平均含量分别为2.454、1.066、3.887、0.868、0.472、0.762、0.587、1.892、3.076、1.264、0.642、0.253、0.187、2.806和0.374 μg·丸-1,见表 2。
|
|
表 2 不同批次补中益气丸中15种主要成分的量(n=3) Table 2 Contents of 15 main components in BZYQ pills of different batches |
近几年对中药多成分同时定量检测的质量控制显得尤为重要。本实验采用UPLC-MS所建立的方法,可同时测定补中益气丸中的15种生物活性物质,该方法操作简单、快速,1次测定就能较全面地反映所含8种药材的质量。
根据化合物的理化性质和色谱行为,比较了以甲醇、乙腈与水、甲酸水、磷酸水构成的洗脱系统。结果表明,以甲醇-水或酸水为系统各成分的分离效果不理想,乙腈-磷酸水系统色谱峰的对称性不好,经优化后的乙腈-甲酸-水系统各成分的分离效果较好,各色谱峰的分离度和理论塔板数均符合要求。超高效色谱柱Zorbax SB-C18、Zorbax Eclipse Plus C18和Zorbax Eclipse XDB进行分析,以比较色谱峰形和分离度,结果显示Zorbax Eclipse Plus C18分离效果最好,分析时间最短。根据各化合物直接进样质谱仪后的全离子质谱图,15种分析物和内标在负源模式都有很高的响应,虽然柚皮苷、橙皮苷、新橙皮苷和甘草酸在质谱正离子源响应较负源强,但一次分析过程中质谱正负源转化或同时使用的扫描模式会影响定量灵敏度,所以综合考虑选择质谱负离子源模式。
本实验对补中益气丸中15种主要生物活性成分进行定量分析,建立的UPLC-MS方法简单快速,灵敏度高,为补中益气丸的制剂质量控制提供了参考,同时,也为临床检测富含15种化合物的中药制剂提供了良好的检测手段。
| [1] |
高璟春, 张金超, 陈瑶, 等. 补中益气汤的LC-MS分析及其对免疫抑制小鼠的调节作用[J]. 中草药, 2006, 37(8): 1134. GAO JC, ZHANG JC, CHEN Y, et al. LC-MS analysis of Buzhongyiqi Tang and its regulating effect on immune-depressed mice[J]. Chin Tradit Herbal Drugs, 2006, 37(8): 1134. |
| [2] |
薛薇, 毛菊华, 王志芳. HPLC法同时测定补中益气丸中3种活性成分的含量[J]. 中国药房, 2014, 25(16): 1524. XUE W, MAO JH, WANG ZF. Simultaneous determination of 3 active constituents in Buzhong Yiqi pills by HPLC[J]. China Pharm, 2014, 25(16): 1524. DOI:10.6039/j.issn.1001-0408.2014.16.30 |
| [3] |
GARCIA OB, CASTILLO J. Update on uses and properties of Citrus flavonoids: New findings in anti-cancer, cardiovascular, and anti-inflammatory activity[J]. J Agric Food Chem, 2008, 56(15): 6185. DOI:10.1021/jf8006568 |
| [4] |
LIU RT, TANG JT, ZOU LB, et al. Liquiritigenin attenuates the learning and memory deficits in an amyloid protein precursor transgenic mouse model and the underlying mechanisms[J]. Europ J Pharm, 2011, 669(1): 76. |
| [5] |
DANG HX, CHEN Y, LIU XM, et al. Antidepressant effects of ginseng total saponins in the forced swimming test and chronic mild stress models of depression[J]. Progr Neuro-Psychopharm Bio Psychiatry, 2009, 33(8): 1417. DOI:10.1016/j.pnpbp.2009.07.020 |
| [6] |
WU WS. ERK signaling pathway is involved in p15INK4b/p16INK4a expression and HepG2 growth inhibition triggered by TPA and Saikosaponin a[J]. Oncogene, 2003, 22(7): 955. DOI:10.1038/sj.onc.1206237 |
| [7] |
陈晓虎. HPLC-ELSD测定补中益气颗粒中黄芪甲苷含量[J]. 中国现代中药, 2014, 16(3): 229. CHNE XH. Determination of astragaloside Ⅳ in Buzhong Yiqi granules by HPLC-ELSD[J]. Modern Chin Med, 2014, 16(3): 229. |
| [8] |
董秀丽, 李洪娟. HPLC法测定补中益气丸中芒柄花黄素的含量[J]. 中国药房, 2012, 36(23): 3440. DONG XL, LI HJ. Content determination of formononetin in Buzhong Yiqi pills by HPLC[J]. China Pharm, 2012, 36(23): 3440. |
| [9] |
徐小利, 陈晓虎, 谢静. 高效液相色谱蒸发光散射检测法测定补中益气丸(浓缩丸)中黄芪甲苷含量[J]. 中国药业, 2008, 19(17): 34. XU XL, CHEN XH, XIE J. HPLC-ELSD determination of astragaloside Ⅳ in Buzhong Yiqi granules[J]. China Pharm, 2008, 19(17): 34. |
| [10] |
孙国祥, 蔡新凤, 丁楠. 平行五波长高效液相色谱指纹图谱全息整合法定量鉴定补中益气丸整体质量[J]. 中南药学, 2010, 8(6): 473. SUN GX, CAI XF, DING N. Quantitative identification of Buzhong Yiqi Wan by integrating all information from paralleled five wavelength HPLC fingerprints[J]. Central South Pharm, 2010, 8(6): 473. |
| [11] |
中国药典2015年版. 一部[S]. 2015: 283 ChP 2015. Vol Ⅰ[S]. 2015: 283 |
| [12] |
YAN ZX, CHEN C, XIE XB, et al. Rapid screening and quantification of sulfonate derivatives in white peony root by UHPLC-MS-MS[J]. Anal Bioanal Chem, 2012, 402(6): 2173. DOI:10.1007/s00216-011-5643-6 |
| [13] |
LI TX, HU L, ZHANG MM, et al. A sensitive UPLC-MS/MS method for simultaneous determination of eleven bioactive components of Tong-Xie-Yao-Fang decoction in rat biological matrices[J]. J Chromatogr B, 2014, 944: 90. DOI:10.1016/j.jchromb.2013.11.015 |
 2017, Vol. 37
2017, Vol. 37 
