2. 北京万生药业有限责任公司, 北京 101113
2. Beijing Winsunny Pharmaceutical Co., Ltd, Beijing, 101113, China
罗氟司特是一种新型的选择性磷酸二酯酶-4(PDE-4)抑制剂,适用于慢性阻塞性肺病(COPD)的治疗。奈科明公司(Nycomed)的罗氟司特片商品名为Daxas[1-4],是批准用于慢性阻塞性肺疾病治疗的新型选择性磷酸二酯酶-4抑制剂,对肺部系统具有高效的抗炎活性。可抑制磷酸二酯酶-4,减少炎症介质的释放,进而抑制如慢性阻塞性肺病和哮喘等呼吸道疾病对肺组织造成的损伤[5-7]。
目前国内对罗氟司特有关物质的测定方法报道[8-13]较少,且国内报道方法对罗氟司特特定杂质的分析较少。国外文献[14-15]使用粒径为1.8μm色谱柱对罗氟司特的有关物质进行测定,但是由于色谱柱粒径较小,色谱柱使用寿命短,且难以分离所有杂质。本文采用普通C18柱对罗氟司特杂质3-环丙基甲氧基-4-二氟甲氧基苯甲酸(杂质A)、4-氨基-3,5-二氯吡啶(杂质B)、3-(环丙基甲氧基)-N-(3,5-二氯吡啶-4-基)-4-羟基苯甲酰胺(杂质C)、3-羟基-N-(3,5-二氯吡啶-4-基)-4-(二氟甲氧基)苯甲酰胺(杂质D)、3,4-二羟基-N-(3,5-二氯吡啶-4-基)苯甲酰胺(杂质E)、3-(环丙基甲氧基)-N-(吡啶-4-基)-4-(二氟甲氧基)苯甲酰胺(杂质F)、3-(环丙基甲氧基)-N-(3-氯吡啶-4-基)-4-(二氟甲氧基)苯甲酰胺(杂质G)、3-(二氟甲氧基)-N-(3,5-二氯吡啶-4-基)-4-(环丙基甲氧基)苯甲酰胺(杂质H)、3,4-二(环丙基甲氧基)-N-(3,5-二氯吡啶-4-基)苯甲酰胺(杂质I)、3,4-二(二氟甲氧基)-N-(3,5-二氯吡啶-4-基)苯甲酰胺(杂质J)和罗氟司特氮氧化物(杂质K)进行分离测定,克服了小粒径色谱柱使用的局限性,而且增加了对目前罗氟司特所有潜在杂质的分离度,进而有效地控制罗氟司特原料药的质量,同时也为制剂的质量控制提供参考。罗氟司特和杂质的结构见图 1。

|
图 1 罗氟司特及其各杂质成分的化学结构式 Figure 1 Structures of roflumilast and its known impurities |
Waters e2695高效液相色谱仪(2998二极管阵列检测器,四元泵;Waters公司),Aglient ZORBAX SB-C18色谱柱(4.6 mm×150 mm,5 μm;填料:十八烷基硅烷键合硅胶;Aglient公司),BP211D十万分之一天平(Sartorius公司)。
1.2 试药罗氟司特原料药(北京万生药业有限责任公司,批号20120201、20120401、20120501、20120502、20120601)、罗氟司特对照品(由原料药精制而得,经紫外、红外、质谱和核磁共振分析确证,批号D20120201,含量99.74%)以及各杂质对照品(杂质C:批号L002-20120401,纯度98.47%;杂质D:批号L003-20120402,纯度97.09%;杂质E:批号L004-20120405,纯度99.85;杂质F:批号L011-20120201,纯度97.63%;杂质G:批号L012-20120206,纯度98.71%;杂质H:批号L021-20120213,纯度96.55%;杂质I:批号L023-20120301,纯度96.20%;杂质J:批号L024-20120312,纯度99.91和杂质K:批号L031-20120214,纯度99.81%)均由北京万生药业有限责任公司制备;杂质A由天津法莫西医药科技有限公司提供,批号20120114,纯度99.09%;杂质B由南京康满林化工实业有限公司提供,批号20120113,纯度99.76%。乙腈为色谱纯;其他均为分析纯,水为超纯水。
2 方法与结果 2.1 色谱条件色谱柱:Aglient ZORBAX SB-C18(4.6 mm×150 mm,5 μm);流动相:以0.01 mol·L-1磷酸二氢钾溶液(磷酸调节pH至3.5±0.1)为流动相A,乙腈为流动相B,梯度洗脱(表 1),流速0.5 mL·min-1,柱温25 ℃,检测波长215 nm,进样量10 μL。
|
|
表 1 梯度洗脱程序 Table 1 Gradient elution program |
定位溶液:取杂质A、杂质B、杂质C、杂质D、杂质E、杂质F、杂质G、杂质H、杂质I、杂质J和杂质K的对照品各约10 mg,精密称定,分别置100 mL量瓶中,加乙腈溶解并稀释至刻度,摇匀,分别作为以上各杂质的定位溶液。
供试品溶液:取罗氟司特原料药约10 mg,精密称定,置50 mL量瓶中,加乙腈溶解并稀释至刻度,摇匀,作为供试品溶液。
对照品溶液:分别取杂质A、杂质B、杂质C、杂质D、杂质E、杂质F、杂质G、杂质H、杂质I、杂质J、杂质K和罗氟司特对照品各适量,精密称定,加乙腈溶解并稀释制成每1 mL中含各0.1 mg的溶液,作为储备溶液,精密量取储备溶液1 mL置50 mL量瓶中,加乙腈稀释至刻度,摇匀,精密量取1 mL置10 mL量瓶中,加乙腈稀释至刻度,摇匀,作为对照品溶液。
系统适用性溶液:取罗氟司特对照品10 mg,精密称定,置50 mL量瓶中,分别精密加入杂质A、杂质B、杂质C、杂质D、杂质E、杂质F、杂质G、杂质H、杂质I、杂质J和杂质K的定位溶液各1 mL,加乙腈溶解并稀释至刻度,摇匀,作为系统适用性溶液。
精密量取系统适用性溶液10 μL,注入液相色谱仪,记录色谱图。各杂质与主峰的分离度以及各杂质峰之间的分离度均大于2.0,系统适用性良好。见表 2和图 2。
|
|
表 2 系统适用性试验结果 Table 2 Results of specificity and system applicability test |
2.3 破坏性试验
未破坏样品溶液:取本品约10 mg,精密称定,置50 mL量瓶中,加乙腈溶解并稀释至刻度,摇匀,滤过,取续滤液作为未破坏样品溶液。
酸破坏样品溶液:取本品约10 mg,精密称定,置50 mL量瓶中,加0.1 mol·L-1盐酸溶液5 mL,在80 ℃水浴中放置24 h,取出,放冷,加0.1 mol·L-1氢氧化钠溶液5 mL,加乙腈溶定容至刻度,摇匀,滤过,取续滤液作为酸破坏样品溶液。
碱破坏样品溶液:取本品约10 mg,精密称定,置50 mL量瓶中,加0.1 mol·L-1氢氧化钠溶液5 mL,在80 ℃水浴中放置24 h,取出,放冷,加0.1 mol·L-1盐酸溶液5 mL,加乙腈定容至刻度,摇匀,滤过,取续滤液作为碱破坏样品溶液。
氧化破坏样品溶液:取本品约10 mg,精密称定,置50 mL量瓶中,加30%过氧化氢溶液5 mL,于80 ℃水浴放置24 h,取出,放冷,加乙腈定容至刻度,摇匀,滤过,取续滤液作为氧化破坏样品溶液。
高温破坏样品溶液:取本品细粉适量,置称量瓶中,在105 ℃烘箱中放置24 h,取出,放冷,取约10 mg,精密称定,置50 mL量瓶中,加乙腈溶解并稀释至刻度,摇匀,滤过,取续滤液,作为高温破坏样品溶液。
光照破坏样品溶液:取本品约10 mg,精密称定,置50 mL量瓶中,于4 500 lx下放置24 h,取出,加乙腈溶解并稀释至刻度,摇匀,滤过,取续滤液,作为强光破坏样品溶液。
精密量取上述溶液各10 μL,注入液相色谱仪,记录色谱图见图 3。经强酸强制降解后,降解杂质主要为B、D、E;经强碱强制降解后,降解杂质主要为A、B、C;经氧化强制降解后,降解杂质主要为A、B、D、K;在高温和光照条件下相对稳定。降解试验后各杂质与主成分的分离度均符合规定。

|
a.高温降解(high temperature degradation)b.光照降解(light degradation)c.酸降解(acid degradation)d.碱降解(base degradation)e.氧化降解(oxidation degradation) 图 3 降解试验色谱图 Figure 3 Chromatograms of degradation tests |
分别取罗氟司特对照品及杂质A、杂质B、杂质C、杂质D、杂质E、杂质F、杂质G、杂质H、杂质I、杂质J和杂质K的对照品约10 mg,精密称定,置同一100 mL量瓶中,加乙腈溶解并稀释至刻度,摇匀,作为储备溶液。取储备溶液适量,用乙腈逐级稀释,制得罗氟司特质量浓度依次为0.04、0.08、0.20、0.80和1.20 μg·mL-1的溶液。分别取上述溶液10 μL,注入液相色谱仪,记录色谱图。以质量浓度C(μg·mL-1)为横坐标,峰面积A为纵坐标进行线性回归,并按照斜率法计算各已知杂质的相对校正因子。罗氟司特和各杂质的线性方程以及各杂质的相对校正因子结果见表 3。结果表明:在各自浓度范围内,各组分与峰面积呈良好的线性关系,除杂质B、杂质D和杂质G外,各已知杂质的相对校正因子均在0.90~1.10之间,为了保证检验结果的准确性,采用外标对照法计算各已知杂质的含量,其他未知杂质采用不加校正因子的主成分对照法计算。
|
|
表 3 回归方程、线性范围及校正因子 Table 3 Regression equations, linear ranges and correction factors |
取“2.4”项下0.20 μg·mL-1的溶液适量,用乙腈逐步稀释成不同浓度,在上述色谱条件下,分别进样10 μL。按信噪比S/N=3测定其检出限,按信噪比S/N=10测定其定量限。罗氟司特、杂质A、杂质B、杂质C、杂质D、杂质E、杂质F、杂质G、杂质H、杂质I、杂质J和杂质K的检出限分别为0.03、0.1、0.03、0.1、0.1、0.1、0.03、0.1、0.1、0.1、0.1和0.1 ng,定量限分别为0.1、0.3、0.1、0.3、0.2、0.2、0.1、0.2、0.2、0.2、0.3和0.3 ng,检出能力高,能够满足测定要求。
2.6 仪器精密度试验取“2.4”项下0.20 μg·mL-1的溶液,分别精密量取10 μL,注入液相色谱仪,连续进样6次,记录色谱图,罗氟司特、杂质A、杂质B、杂质C、杂质D、杂质E、杂质F、杂质G、杂质H、杂质I、杂质J和杂质K峰面积的RSD依次为1.4%、1.8%、1.8%、1.6%、1.8%、1.5%、2.0%、1.6%、1.7%、1.2%、1.3%和2.0%。说明仪器精密度良好。
2.7 重复性试验取罗氟司特原料药6份,每份约10 mg,照“2.2”项下方法制备供试品溶液。分别精密量取10 μL,注入液相色谱仪,按外标法计算有关物质的含量,杂质C、杂质D和杂质H的平均含量分别为0.008%、0.006%和0.006%,RSD分别为6.4%、7.8%和7.0%,结果表明重复性良好,见表 4。
|
|
表 4 重复性试验结果(n=6) Table 4 Results of repeatability |
取“2.4”项下0.20 μg·mL-1的溶液,于室温条件下放置24 h,分别在0、2、4、8、12、24 h,精密量取10 µL注入液相色谱仪,记录色谱图。罗氟司特、杂质A、杂质B、杂质C、杂质D、杂质E、杂质F、杂质G、杂质H、杂质I、杂质J和杂质K峰面积的RSD依次为1.8%、1.8%、1.5%、1.3%、1.2%、1.4%、1.6%、2.1%、1.2%、1.4%、0.9%和1.3%。说明各组分在室温条件下放置24 h性质稳定。
2.8.2 供试品溶液的稳定性取罗氟司特原料约10 mg,精密称定,置10 mL量瓶中,加乙腈溶解并稀释至刻度,摇匀,即得供试品溶液;于室温条件下放置,分别在0、2、4、8、12、24 h,精密量取10 µL注入液相色谱仪,记录色谱图。罗氟司特峰面积的RSD为0.15%,杂质C、杂质D、杂质H峰面积的RSD为分别为2.0%、1.6%和0.73%,其他杂质均未检出,说明供试品溶液在室温条件下放置24 h性质稳定。
2.9 回收率试验取罗氟司特9份,平均分为3组,每组3份,每份约10 mg,精密称定,置50 mL量瓶中,分别加入杂质储备溶液(质量浓度为10 μg·mL-1)0.5、1.0和1.5 mL,加乙腈溶解并稀释至刻度,摇匀,即得回收率供试溶液;精密量取10 µL注入液相色谱仪,记录色谱图,计算回收率,结果见表 5,表明各已知杂质在3个不同浓度水平(0.05%水平、0.1%水平、0.15%水平)的回收率均在80%~120%之间,符合规定。
|
|
表 5 回收率试验结果(n=9) Table 5 Results of recovery |
取上述系统适用性溶液和供试品溶液,考察本色谱条件对流动相的pH、柱温、流速和色谱柱粒径的耐用性,结果表明,本方法对流速、色谱柱粒径耐用性较好,对流动相pH和柱温耐用性较差,需严格控制。耐用性试验结果见表 6。
|
|
表 6 耐用性试验结果 Table 6 Results of durability test |
分别取5批原料药,按照“2.2”项下方法,分别制备供试品溶液和对照品溶液,进样测定,各已知杂质按外标法计算,未知杂质按照主成分外标法计算有关物质的含量,结果见表 7。
|
|
表 7 样品检验结果 Table 7 Results of sample tests |
国外文献[14-15]采用0.005 mol·L-1甲酸铵溶液(pH 3.5)-乙腈体系测定罗氟司特的有关物质,经试验发现,该条件下梯度漂移较大,以至于在漂移的基线上杂质很难检测出来。将甲酸铵换成0.010 mol·L-1磷酸二氢钾溶液,并对梯度洗脱程序进行调整,结果表明,采用0.010 mol·L-1磷酸二氢钾溶液可明显降低基线漂移,且各杂质均能有效分离。
3.2 pH耐用性试验随着磷酸盐缓冲液pH的增加,杂质F的保留时间增加,当pH为3.7时,杂质F的保留时间大于杂质D的保留时间,因此,须严格控制缓冲盐的pH范围为3.3~3.6。
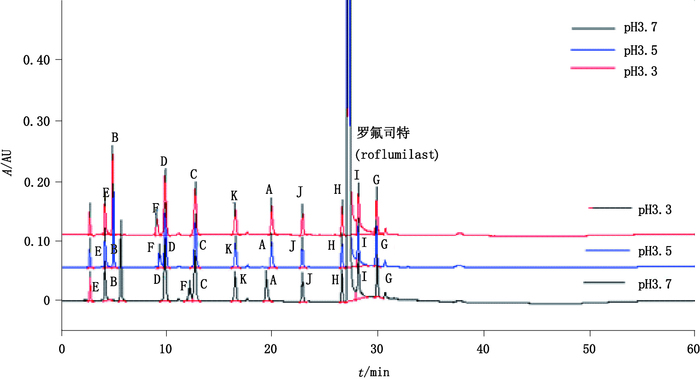
|
图 8 pH耐用性色谱图谱 Figure 8 Chromatograms of pH durability test |
取“2.2”项下供试品溶液、以及各已知杂质的溶液,采用PDA检测器进行检测,罗氟司特在215 nm和250 nm波长附近有特征最大吸收,各杂质在215 nm均有较大吸收,而个别杂质在250 nm吸收较弱,因此,选用215 nm作为检测波长。
| [1] |
BOLAND S, ALEN J, BOURIN A, et al. Novel roflumilastanalogsas soft PDE4 inhibitors[J]. Bioorg Med Chem Lett, 2014, 24(18): 4594. DOI:10.1016/j.bmcl.2014.07.016 |
| [2] |
闫文娜, 陈艳明, 倪成亮, 等. 罗氟司特中有关物质的鉴定和含量测定[J]. 药物分析杂志, 2013, 33(10): 1726. YAN WN, CHEN YM, NI CL, et al. Identification and quantitative analysis of related substances in roflumilast[J]. Chin J Pharm Anal, 2013, 33(10): 1726. |
| [3] |
MILARA J, MORELL A, BALLESTER B, et al. Roflumilast improves corticosteroid resistance COPD bronchial epithelial cells stimulated with toll like receptor 3 agonist[J]. Respir Res, 2015, 16(1): 12. DOI:10.1186/s12931-015-0179-5 |
| [4] |
马培奇. 慢性阻塞性肺病治疗新药罗氟司特[J]. 上海医药, 2011, 32(4): 201. MA PQ. Roflumilast:a novel approach to treating COPD[J]. Shanghai Med Pharm J, 2011, 32(4): 201. |
| [5] |
封宇飞. 磷酸二酯酶-4抑制剂罗氟司特的药理与临床研究新进展[J]. 中国新药杂志, 2011, 20(14): 1257. FENG YF. Progress in pharmacological and clinical studies of the phosphodiesterase-4 inhibitor roflumilast[J]. Chin J New Drugs, 2011, 20(14): 1257. |
| [6] |
祝巍, 陈萍. 磷酸二酯酶抑制药-罗氟司特在慢性阻塞性肺疾病治疗中的应用[J]. 中国新药与临床杂志, 2011, 30(11): 819. ZHU W, CHEN P. Application of phosphodiesterase inhibitor-roflumilastin chronic obstructive pulmonary disease[J]. Chin J New Drugs Clin Rem, 2011, 30(11): 819. |
| [7] |
韩伟, 周新. 慢性阻塞性肺疾病的治疗新选择-罗氟司特[J]. 世界临床药物, 2011, 32(7): 396. HAN W, ZHOU X. Roflumilast, a highly selective PDE-4 inhibitor in the treatment of chronic obstructive pulmonary disease[J]. World Clin Drugs, 2011, 32(7): 396. |
| [8] |
王江玲, 梁建华. HPLC法测定罗氟司特有关物质[J]. 河南大学学报(医学版), 2014, 33(4): 253. WANG JL, LIANG JH. Determination of related substances in roflumilast by HPLC[J]. J Henan Univ(Med Sci), 2014, 33(4): 253. |
| [9] |
郑曦孜. HPLC法测定罗氟司特的有关物质[J]. 光谱实验室, 2013, 30(6): 3122. ZHENG XM. Determination of related substances in roflumilast by HPLC[J]. Chin J Spectrosc Lab, 2013, 30(6): 3122. |
| [10] |
张莉, 黎其荣, 杨伟涵, 等. HPLC法测定罗氟司特有关物质方法研究[J]. 今日药学, 2014, 24(2): 114. ZHANG L, LI QR, YANG WH, et al. HPLC determination of roflumilast related substances[J]. Pharm Today, 2014, 24(2): 114. |
| [11] |
赵永娟, 付建, 赵海桥. HPLC法测定罗氟司特片有关物质[J]. 中国化工贸易, 2013, 12(12): 321. ZHAO YJ, FU J, ZHAO HQ. Determination of related substances in roflumilast tablets by HPLC[J]. China Chem Trade, 2013, 12(12): 321. DOI:10.3969/j.issn.1674-5167.2013.12.303 |
| [12] |
杨丽霞, 闫建军, 冯彩婷. 高效液相色谱法测定罗氟司特药品中罗氟司特和4种杂质[J]. 理化检测(化学分册), 2015, 51(5): 594. YANG LX, YAN JJ, FENG CT. HPLC determination of roflumilast and 4 impurities in roflumilast drug[J]. Phys Test Chem Anal Part B(Chem Anal), 2015, 51(5): 594. |
| [13] |
何凤琴, 周磊, 秦妮, 等. 罗氟司特主药和有关物质的HPLC法测定[J]. 医学美学美容, 2013(3): 155. HE FQ, ZHOU L, QIN N, et al. Determination of roflumilast and related substances by HPLC[J]. Med Aesthet Cosmetol, 2013(3): 155. |
| [14] |
BARHATE VD, DEOSTHALEE PC. Validation of rapid liquid chromatographic method for the determination of roflumilast[J]. J Chem Pharm Res, 2011, 3(2): 770. |
| [15] |
BARHATE VD, DEOSTHALEE P. Rapid liquid chromatographic method for the determination of roflumilast in the presence of degradation products[J]. Indian J Pharm Sci, 2010, 72(3): 401253. |
 2017, Vol. 37
2017, Vol. 37 

