风险控制是对人类健康、动植物或环境可能产生不良影响的危害进行评价,并在此基础上采取的规避或降低危害影响的措施。国际食品法典委员会将风险分析定义为由风险评估、风险管理和风险交流组成的一个过程[1-2]。风险评估是基于科学的事实,是客观的,实事求是的,也是带有不确定性的。风险管理则主要是由政府按照风险评估的结果,权衡政策,选择和实施适当控制;主要依靠社会及各项制度进行管理的过程,包括制定标准,法律法规的完善,政府的监管行为等。风险交流则是各个利益相关方之间交换信息和建议,包括对风险评估结果的解释和风险管理决定的基础等[3]。
在2015年银杏叶药品质量专项治理中,补充检验方法的建立就是风险评估的过程,而法定标准制定、政府的监管行为则属于风险管理,风险交流是贯穿于风险控制的整个过程中,包括在标准制定过程中广泛听取社会团体及骨干企业的意见,补充检验方法及时向社会公开,检验结果向社会公布等。本文就风险控制体系在银杏叶药品专项治理技术支撑工作中的作用作论述。
1 风险评估 1.1 风险识别风险识别是风险评估工作的起点,其任务是通过一定的方法和手段,识别、确认并分类风险及其来源,找出形成显著风险的关键因素。风险识别的准确程度,对风险评估起着相当重要的作用。风险识别为风险评估提供对象和基础,从而也为风险管理提供工作方向。
指纹图谱可以全面反映样品的整体信息,发现样品可能存在的问题。本文采用指纹图谱技术方法,以查明可疑样品与正常样品的差别,为飞行检查提供技术支持。
1.1.1 仪器与试药UltiMate 3000型高效液相色谱仪(赛默飞世尔科技公司),Eclipse Plus C18(4.6 mm×250 mm,5 μm;填料:十八烷基硅烷键合硅胶;Agilent公司),METTLER XS105DU电子天平(梅特勒-托利多公司),Milli-Q超纯水处理系统(默克密理博公司),KQ-500E型超声波清洗器(昆山超声仪器有限公司)。
槲皮素(批号100081-201408)、山柰素(山柰酚,批号110861-201310)、异鼠李素(批号110860-201410)、槐角苷(批号111695-200501)、银杏叶对照提取物(批号110886-201204)、槐角对照药材(批号121214-0101)均由中国食品药品检定研究院提供。甲醇及乙腈为色谱纯,水为高纯水。
银杏叶提取物、银杏叶片、银杏叶胶囊样品分别购于北京市场。
1.1.2 方法与结果 1.1.2.1 色谱条件与系统适用性试验采用Agilent Eclipse Plus C18(4.6 mm×250 mm,5 μm)色谱柱,以乙腈(A)-0.4%磷酸溶液(B)为流动相,进行梯度洗脱,梯度洗脱程序见表 1,检测波长为360 nm和260 nm,柱温为40 ℃。
|
|
表 1 梯度洗脱程序 Table 1 Gradient elution program |
分别取槲皮素、山柰素、异鼠李素、槐角苷的对照品适量,精密称定,加甲醇制成每1 mL分别含30、30、20、20 μg的溶液,作为混合对照品溶液。另取银杏叶对照提取物40 mg,加入80%甲醇溶液20 mL超声(功率250 W,频率33 kHz)处理10 min,滤过,取续滤液,即得银杏叶对照提取物溶液;再取槐角对照药材40 mg,同法制成槐角对照药材溶液。取银杏叶提取物约40 mg;或取银杏叶片10片,糖衣片除去包衣,精密称定,研细,取约相当于总黄酮醇苷9.6 mg的粉末;或取银杏叶胶囊装量差异项下的内容物,混匀,研细,取约相当于总黄酮醇苷9.6 mg的粉末。精密称定,置具塞锥形瓶中,精密加入80%甲醇溶液20 mL,密塞,称量,超声处理(功率250 W,频率33 kHz)20 min,取出,放冷,再称量,用80%甲醇溶液补足减失的量,摇匀,滤过,取续滤液,即得供试品溶液。
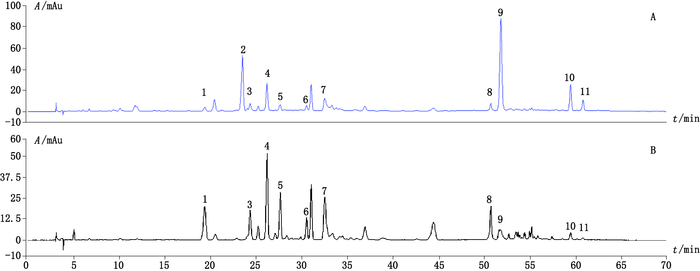
1.1.2.3 结果60 nm下银杏叶提取物的异常样品与正常样品的指纹图谱见图 1。从图 1中可以看出,异常样品与正常样品的指纹图谱存在明显差异,异常样品一些色谱峰峰强度明显增高,还有一些色谱峰峰强度明显降低。其中,1、3、4、5、6、7、8号峰,异常样品与正常样品指纹图谱比较,峰强度均明显下降;2号峰,在异常样品中存在,而在正常样品中不存在该色谱峰;9、10、11号峰分别为槲皮素、山柰素和异鼠李素,异常样品与正常样品指纹图谱比较,峰强度均明显增强。
|
9.槲皮素(quercetin)10.山柰素(kaempferol)11.异鼠李素(isorhamnetin) 图 1 360 nm下异常样品(A)与正常样品(B)指纹图谱 Figure 1 HPLC chromatograms of abnormal sample(A)and normal sample(B)at 360 nm |
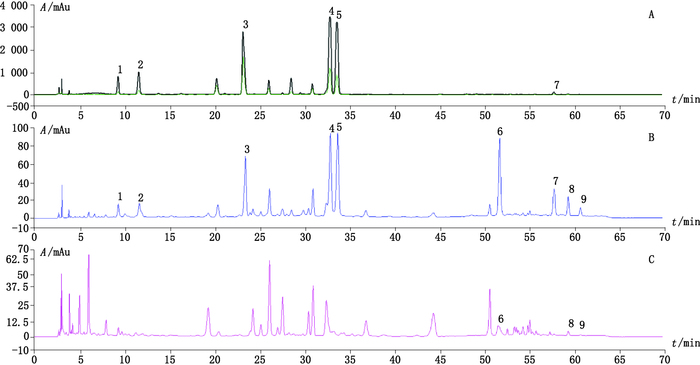
260 nm下槐角对照药材、异常样品与正常样品的指纹图谱见图 2。从图 2可以看出,在异常样品中可检出一些在银杏叶对照提取物中不存在的一些色谱峰。其中,6、8、9号峰分别为槲皮素、山柰素和异鼠李素,异常样品与正常样品指纹图谱比较,峰强度均明显增强;1、2、3、4、5、7号峰(4号峰为槐角苷,7号峰为染料木素)为异常样品中存在,而正常样品中不存在的色谱峰,而这些色谱峰恰与槐角对照药材的色谱峰吻合,提示样品中可能存在非法添加槐角的情况。
|
4.槐角苷(sophoricoside)6.槲皮素(quercetin)7.染料木素(genistein)8.山柰素(kaempferol)9.异鼠李素(isorhamnetin) 图 2 260 nm下槐角对照药材(A)、异常样品(B)与正常样品(C)指纹图谱 Figure 2 HPLC chromatograms of reference crude drug of Sophorae Fructus(A), abnormal sample(B)and normal sample(C)at 260 nm |
风险识别从指纹图谱入手,发现银杏叶提取物及其制剂中可能存在的问题如下:(1)可能改变生产工艺,使得游离黄酮含量异常增高,究其根本原因是:中国药典2010年版一部[4]334银杏叶提取物“总黄酮醇苷”项是以酸水解以后测定游离的槲皮素、山柰素及异鼠李素,而测定的并非黄酮醇苷的原型。研究表明[5-6],黄酮类化合物是银杏叶提取物中主要有效成分,可发挥抗氧化和清除氧自由基的作用,稀盐酸提取造成黄酮醇苷的水解,可能会减弱或者改变银杏叶提取物的功效;(2)可能存在非法添加槐角的情况。槐角中的黄酮类化合物种类很多,主要的苷元形式只有4种,即槲皮素、染料木素、山柰酚和异鼠李素,文献[7]比较了槐角皮和槐角种子中水解后染料木素、槲皮素和山柰素的含量,结果显示槐角水解后主要的黄酮苷元中染料木苷和山柰素的含量较高,其中槐角皮中水解山柰素可达3%,由此可见,添加少量的槐角就可以显著提高山柰素的含量。
1.2 风险分析针对风险识别发现的问题建立补充检验方法。药品补充检验方法来源于《药品管理法实施条例》第五十八条规定:“对有掺杂、掺假嫌疑的药品,在国家药品标准规定的检验方法和检验项目不能检验时,药品检验机构可以补充检验方法和检验项目进行药品检验;经国务院药品监督管理部门批准后,使用补充检验方法和检验项目所得出的检验结果,可以作为药品监督管理部门认定药品质量的依据”。
补充检验方法是用于监管的法定标准,补充检验方法的研究制定并不是简单的科研工作,而是需要以风险评估的科学理论为指导,建立严谨的补充检验方法。笔者之前已详述了银杏叶提取物及其制剂补充检验的建立[8],在此文中仅就补充检验方法建立过程中的风险分析进行论述。补充检验方法制定过程中主要面临三类风险:技术风险、标准风险、监管风险。
1.2.1 技术风险技术风险强调检验方法的准确性、可操作性、可重复性。
游离槲皮素、山柰素、异鼠李素的测定方法,并没有采用复杂的检测技术,而是依照监督检查获得的证据,以及对可能非法添加情况进行分析,以现有药典方法的成熟技术为依托,检测游离槲皮素、山柰素、异鼠李素。色谱条件参照中国药典2010年版一部银杏叶提取物[4]334总黄酮醇苷项下色谱条件,样品经80%甲醇溶液超声处理后进行测定。与药典标准比较,仅在供试品溶液制备上有所不同(不需水解),有效保证了方法可靠、简便、易行,可以有效识别假劣药品,并可迅速用于飞行检查的现场试验。
槐角苷的检测采用高效液相色谱法。为了有效地避免复杂基质的干扰,首创了色谱系统专属性试验要求,同时采用槐角苷对照品、槐角对照药材、银杏叶对照提取物作为对照,进行系统的方法验证,有效排除色谱分离不好造成的假阳性干扰。同时,结果判断时,对于阳性检出样品,需先与槐角苷对照品进行光谱比对,进行定性鉴别后再进行定量计算,并固定了色谱柱,极大程度地保证了结果的可靠性。
建立补充检验方法时,进行方法验证、复核,充分保证方法的可靠性。在药检系统内部加强技术培训,避免产生技术误判,极大提高了检验效率,保证了监管的权威性。
1.2.2 标准风险标准风险强调标准的科学性、合理性。通过风险识别,发现银杏叶提取物及其制剂存在的系统性问题。针对擅自改变提取工艺或者非法添加其他使得游离黄酮增加的物质,建立了游离黄酮检查法;针对可能存在的非法添加槐角的情况,建立了槐角苷检查项。为保证专项治理的快速推进,补充检验方法使用的对照物质为已发放的法定对照物质。通过制订合理的限度标准,把监管风险最小化。
1.2.3 监管风险监管风险强调打击违法潜规则,为行业发展引导正确方向,同时要兼顾国情和行业发展历史与现状。游离黄酮和槐角苷两类不同的补充检验方法可以满足打劣打假的不同要求,可针对违法事实进行有区别的监管、处罚。
天然的银杏叶中,游离黄酮的含量是非常低的,但不同产地、不同采收季节、不同树龄的银杏叶药材中游离槲皮素含量有一定差异[9-11],生产设备和工艺参数的细微差异也会造成游离槲皮素含量有所波动,所以为保护正规企业的合法利益,有效控制监管风险,现阶段将限度适当放宽。
槐角苷补充检验方法限度标准的制定宽严有据。槐角苷为槐角中的主要化学成分,目前尚未见有报道在银杏叶中有槐角苷存在,按照中国药典法定工艺生产的银杏叶提取物理论上不应存在槐角苷。但中国药典2010年版一部银杏叶项[4]316下规定银杏叶药材中可以存在少量杂质,其限度为2%。补充检验方法应能有效区别少量槐叶、槐角作为杂质混入与人为添加。
2 风险管理风险管理是指如何在一个肯定有风险的环境里把风险减至最低的管理过程。风险管理就是通过风险的识别、预测和衡量、选择有效的手段,以尽可能降低成本,有计划地处理风险。风险管理的核心目的是管住各个可能出现风险的环节,并提前采取措施予以防范。
在银杏叶提取物专项治理工作之初,中检院短时间内在北京市场收集了不同剂型银杏叶制剂34批次,建立了HPLC指纹图谱测定方法,发现了可疑产品的特征鉴别点,初步锁定了一批涉嫌企业及样品批号,并拟定了飞行检查现场快速检测方法。并对北京市场收集到的34批次样品筛查,并对假劣药品产生原因、主要制假方法、整体市场不合格率、涉及的监管范围等风险作出初步评估,显示异常样品接近一半,将此风险提前上报国家总局。国家总局根据市场情况,首次实施了企业大规模主动召回政策,快速净化市场,减小监管压力;执行对违法生产销售银杏叶提取物及制剂行为分类处罚的原则,成功的降低了行业风险。
在“银杏叶事件”发生仅半个月后,2015年6月4日,国家总局发布了银杏叶药品的补充检验方法。作为监管执法的重要手段,某种成分的补充检验方法一般不公开发布。此次公开发布补充检验方法,是总局为在最短时间内有效控制药品风险,给企业自查和监管部门专项治理提供技术支持。
3 风险交流所谓风险交流,是指风险评估人员、风险管理人员、消费者、企业、学术界和其他利益相关方就某项风险所涉及的因素和风险认知相互交换信息和意见的过程。换言之,风险交流是一个公开的、双向的信息和观点的交流,其目的是风险能够得到更好的理解,并做出更好的风险管理决定。
在银杏叶提取物及其制剂的补充检验方法研究过程中,组织召开银杏叶提取物及其制剂质量咨询座谈,邀请主要生产企业以及相关行业协会参加,对行业的现状、指标的选择、限度的设置等方面进行沟通,广泛征求意见,同时明确政策、明确监管决心。补充检验方法的审批高度尊重技术意见,程序完备但快速推进。
4 结语此次银杏叶提取物及其制剂的专项治理工作,无论是检测方法研究、限量标准与补充检验方法制订,还是样品筛查等,都是基于风险控制的科学理论指导下进行,使技术上、过程上的复杂性能够以一种高效的、可操作的方式纳入统一的风险管理框架。目前,风险分析已经成为国际上应对和处理食品药品安全问题、防范食品药品安全风险所公认的科学原则和手段[12-15]。中国也已经成立了相关机构并在新食品安全法中做出了明确规定[16-18],须尽快建立健全药品风险分析体系,以更好的应对和处理频发的药品安全事件。
| [1] |
FAO and WHO. Food safety risk analysis. A guide for national food safety authorities[J]. FAO Food Nutr Pap, 2006, 87:ix-xii, 1-102
|
| [2] |
Food and Agriculture Organization of the United Nations. The Procedural Manual of the Codex Alimentarius Commission, 12 th Ed. 2002:43[EB/OL].[2016-05-05]. http://www.fao.org/docrep/005/y2200e/y2200e00.htm#Contents
|
| [3] |
马双成, 金红宇, 刘丽娜, 等. 中药中外源性有害物质残留风险控制初探[J]. 中国药学杂志, 2015, 50(2): 99. MA SC, JIN HY, LIU LN, et al. Risk control of exogenous harmful residues in traditional Chinese medicines[J]. Chin Pharm J, 2015, 50(2): 99. |
| [4] |
中国药典2010年版. 一部[S]. 2010: 334, 316 ChP 2010. Vol Ⅰ[S]. 2010: 334, 316 |
| [5] |
BRIDI R, CROSSETTI FP, STEFFEN VM, et al. Phytother Res, The antioxidant activity of standardized extract of Ginkgo biloba(EGb 761) in rats[J]. 2001, 15(5):449
|
| [6] |
DU G, WILLET K, MOUITHYS-MICKALAD A, et al. EGb 761 protects liver mitochondria against injury induced by in vitro anoxia/reoxygenation[J]. Free Radic Biol Med, 1999, 27(5/6): 596. |
| [7] |
王志玲, 勾凌燕, 刘景东, 等. 槐角不同部位中主要黄酮苷元成分的比较[J]. 时珍国医国药, 2012, 23(3): 594. WANG ZL, GOU LY, LIU JD, et al. Comparative study on three flavonoid aglycone equivalents in the pericarps and the seeds of Sophora japonica L[J]. Lishizhen Med Mater Med Res, 2012, 23(3): 594. |
| [8] |
刘丽娜, 何轶, 李耀磊, 等. 银杏叶提取物及其制剂补充检验方法的建立[J]. 药物分析杂志, 2016, 36(5): 856. LIU LN, HE Y, LI YL, et al. Study on the supplemental testing methods for Ginkgo biloba extract and its preparations[J]. Chin J Pharm Anal, 2016, 36(5): 856. |
| [9] |
刘叔倩, 郑俊华, 王弘. 不同气候区银杏叶中黄酮和萜内酯含量的变化[J]. 中草药, 2000, 31(6): 424. LIU SQ, ZHENG JH, WANG H. Variation of flavonoids and terpenlactones in Ginkgo(Ginkgo biloba)leaves from regions with different climatic conditions[J]. Chin Tradit Herb Drugs, 2000, 31(6): 424. |
| [10] |
ZHAO YY, WANG JH, FU XT, et al. Simultaneous determination of eleven flavonoid glycosides in Ginkgo biloba leaves collected in different seasons by UPLC PDA method[J]. Acta Pharm Sin, 2013, 48(1): 98. |
| [11] |
钱大玮, 鞠建明, 朱玲英. 不同树龄银杏叶在不同季节中总黄酮和总内酯的含量变化[J]. 中草药, 2012, 33(11): 1025. QIAN DW, JU JM, ZHU LY. Study on changing rules for total flavonoids and total terpene lactones in Ginkgo biloba leaves at different ages of trees and collecting seasons[J]. Chin Tradit Herb Drugs, 2012, 33(11): 1025. |
| [12] |
CALDWELL DJ, MASTROCCO F, NOWAK E, et al. An assessment of potential exposure and risk from estrogens in drinking water[J]. Environ Health Perspect, 2010, 118(3): 338. |
| [13] |
LACHENMEIER DW, LIMA MC, NÓBREGA, I C, et al. Cancer risk assessment of ethyl carbamate in alcoholic beverages from Brazil with special consideration to the spirits cachaca and tiquira[J]. BMC Cancer, 2010, 10: 266. DOI:10.1186/1471-2407-10-266 |
| [14] |
SINGER AC, HOWARD BM, JOHNSON AC, et al. Meeting report:risk assessment of tamiflu use under pandemic conditions[J]. Environ Health Perspect, 2008, 116(11): 1563. DOI:10.1289/ehp.11310 |
| [15] |
JUHASZ AL, SMITH E, WEBER J, et al. In vivo assessment of arsenic bioavailability in rice and its significance for human healthrisk assessment[J]. Environ Health Perspect, 2006, 114(12): 1826. |
| [16] |
陶宏, 风险分析在食品安全国家标准制定中的应用研究[D]. 北京: 清华大学, 2012 TAO H. Study on Risk Analysis Application in National Food Safety Standard Development[D]. Beijing:Tsinghua University, 2012 http://cdmd.cnki.com.cn/Article/CDMD-10003-1013016718.htm |
| [17] |
慕静. 食品安全监管模式创新与食品供应链安全风险控制的研究[J]. 食品工业科技, 2012, 33(10): 49. MU J. Research of supervising model innovation of food safety and safety venture control of food supply chain[J]. Sci Technol Food Ind, 2012, 33(10): 49. |
| [18] |
李淑华. 从美国的食品安全监管看我国的食品安全风险控制[J]. 华北科技学院学报, 2012, 9(4): 60. LI SH. On risk control of China's food safety from the perspective of US food safety administration[J]. J North China Inst Sci Technol, 2012, 9(4): 60. |
 2017, Vol. 37
2017, Vol. 37 
