2. 桐乡市第一人民医院药剂科, 桐乡 314500
2. Department of Pharmacy, The First People's Hospital of Tongxiang, Tongxiang 314500, China
厚朴排气合剂收载于国家药品标准《新药转正标准第82册》[1],其处方组成为厚朴、木香、枳实和大黄,具有行气消胀、宽中除满的功效,临床常用于腹部非胃肠吻合术后早期肠麻痹,症见腹部胀满,胀痛不适,腹部膨隆,无排气排便,舌质淡红,舌苔薄白或薄腻[2, 3]。厚朴排气合剂的标准目前仅为薄层鉴别和大黄的含量测定项,对君药厚朴没有进行相关规定[4]。国家食品药品监督管理局于2009年向生产企业下发的药品标准颁布件中,仅对厚朴的和厚朴酚与厚朴酚进行了含量规定,未对其他成分有要求,在厚朴排气合剂的质量控制上存在一定的缺陷,而2015年中国药典也未收载该品种,因此建立厚朴排气合剂主要成分检测方法对控制成药质量势在必行。厚朴主含和厚朴酚与厚朴酚,是厚朴排气合剂理气作用的主要有效成分[5],大黄中的大黄素和大黄酚是排气排便的主要成分[6-7],本文拟采用HPLC法同时检测厚朴排气合剂中的上述4种成分,为厚朴排气合剂的质量控制提供参考。
1 仪器与试药 1.1 仪器Agilent 1100高效液相色谱仪,安捷伦科技公司;OV-2001柱温箱,赛默飞世尔科技公司;Syncronis C18(250 mm×4.6 mm,5 μm;填料:十八烷基硅烷基键合硅胶)色谱柱,Thermo公司;XS-205电子分析天平,梅特勒-托利多公司;AS3120A型超声提取器,天津奥特赛恩斯仪器有限公司;3K15离心机,Sigma公司。
1.2 试药对照品和厚朴酚(批号110730-20020)、厚朴酚(批号110729-20020)、大黄素(批号110756-200110)和大黄酚(批号110796-201017)均由中国食品药品检定研究院提供。厚朴排气合剂,规格为每瓶50 mL,国药准字Z20050563,瑞阳制药有限公司生产,批号15011501、15012301、15060801、15080301和15101601。甲醇为色谱纯、磷酸和乙酸乙酯均为分析纯,重蒸馏水。
2 方法与结果 2.1 色谱条件色谱柱:Syncronis C18(250 mm×4.6 mm,5 μm);流动相:甲醇(A)-0.1%磷酸水(B),梯度洗脱(0~15 min,80%A→85%A;15~40 min,85%A→95% A);流速:1.0 mL·min-1;检测波长:254nm;柱温:30 ℃;进样量:20 μL。
2.2 溶液的制备 2.2.1 混合对照品溶液精密称取由五氧化二磷减压干燥至恒重的和厚朴酚、厚朴酚、大黄素与大黄酚的对照品适量,置于50 mL棕色量瓶中,加甲醇制成每1 mL含和厚朴酚194.67 mg,厚朴酚282.00 mg,大黄素23.07 ng和大黄酚、77.33 mg,即得混合对照品储备液。精密量取储备液3 mL,置于20 mL量瓶中,加甲醇制成每1 mL含和厚朴酚29.20 mg,厚朴酚42.31 mg,大黄素3.46 mg和大黄酚11.61 mg的混合对照品溶液。对照品储备液及混合对照品溶液均置于4 ℃冰箱密闭保存。
2.2.2 供试品溶液取厚朴排气合剂5 mL,用乙酸乙酯振摇提取3次,每次10 min,每次用乙酸乙酯20 mL,合并乙酸乙酯液,蒸干,残渣加甲醇溶解并转移至20 mL量瓶中,加甲醇至刻度,摇匀,用0.22 μm微孔滤膜滤过,取续滤液,即得。
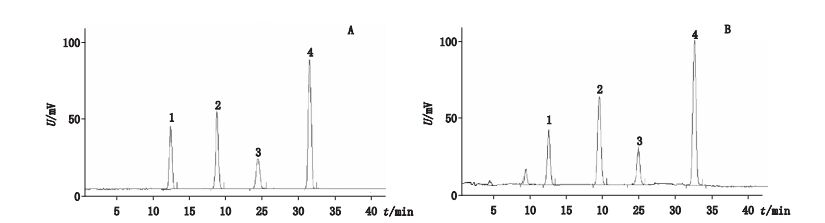
2.3 专属性取混合对照品溶液和供试品溶液各20 μL,按上述色谱条件,进行HPLC分析,和厚朴酚、厚朴酚、大黄素和大黄酚的保留时间分别为13.1、19.0、24.1和32.1 min,见图 1。
|
1.和厚朴酚(honokiol)2.厚朴酚(magnolol)3.大黄素(emodin)4.大黄酚(chrysophanol) 图 1 混合对照品(A)及厚朴排气合剂(B)的HPLC色谱图 Figure 1 Chromatograms of mixed reference substances(A)and Houpopaiqi mixture(B) |
精密量取混合对照品储备液0.5、1.0、2.0、3.0、4.0、5.0和6.0 mL,分别置于20 mL量瓶中,加流动相至刻度,摇匀,记录色谱图,以质量浓度(X)为横坐标,峰面积(Y)为纵坐标作图,进行线性回归,结果见表 1。
|
|
表 1 回归方程、相关系数(r)及线性范围 Table 1 The regression equations, correlation coefficients(r)and linear ranges |
将混合对照品溶液连续进样5次,记录色谱图,记录和厚朴酚、厚朴酚、大黄素和大黄酚的峰面积并计算RSD,结果分别为3.2%、3.1%、3.2%和2.8%,表明精密度较好。
2.6 稳定性试验取批号为15011501的厚朴排气合剂制成供试品溶液,每隔1 h进样1次,获得6次进样的和厚朴酚、厚朴酚、大黄素和大黄酚峰面积,计算RSD分别为3.2%、3.1%、3.4%和2.9%,表明供试品溶液中稳定性较好。
2.7 重复性试验取批号为15011501的厚朴排气合剂5份,按“2.2.2”项下方法操作,进样测定和厚朴酚、厚朴酚、大黄素和大黄酚峰面积,计算平均含量分别为17.26、25.41、2.01和1.81 mg·mL-1,RSD分别为3.1%、3.0%、3.2%和2.6%,表明本法的重复性较好。
2.8 加样回收率试验分别精密量取批号为15011501的厚朴排气合剂4份各1 mL,分别置于10 mL量瓶中,分别精密加入和厚朴酚、厚朴酚、大黄素和大黄酚的混合对照品溶液(和厚朴酚、厚朴酚、大黄素和大黄酚的浓度分别为1.46、2.12、0.17和0.87 mg·mL-1)1.0、3.0和5.0 mL,各2份,用溶剂稀释至刻度,混匀,每个溶液连续进3次,测定和厚朴酚、厚朴酚、大黄素和大黄酚加样回收率,结果见表 2。
|
|
表 2 和厚朴酚、厚朴酚、大黄素和大黄酚回收率 Table 2 The recovery of honokiol, magnolol, emodin and chrysophanol |
取5个批号的厚朴排气合剂,分别按“2.2.2”项方法制备供试品溶液,进样测定,以回归方程计算含量,结果见表 3。
|
|
表 3 5批样品含量测定结果(mg·mL-1) Table 3 Determination results of 5 samples |
等度洗脱很难将和厚朴酚、厚朴酚、大黄素和大黄酚4种极性有差别的成分同时分离,因此采用梯度洗脱。依据大黄和厚朴中有效成分的分离文献[8-12],分别考察了甲醇-水、乙腈-水、甲醇-0.1%磷酸水、甲醇-0.1%醋酸、乙腈-1%醋酸及乙腈-0.2%磷酸梯度洗脱法,结果显示采用甲醇-0.1%磷酸水的梯度洗脱法,各个峰的分离效果较好,分离度均>1.5。
3.2 检测波长的选择参考文献[13-15]并结合和厚朴酚、厚朴酚、大黄素和大黄酚4个化合物的全波长扫描,分析在324、262和254 nm波长处各色谱峰的强度,结果显示4个化合物的色谱峰在254 nm处均有较大吸收,因此选择254 nm为检测波长。
3.3 提取溶剂的选择分别考察以甲醇、乙醇、含水甲醇、含水乙醇及乙酸乙酯为提取溶剂的提取效果,结果采用乙酸乙酯提取的杂质峰较少,有效去除干扰成分,且不影响4个待测物的测定,因此选择乙酸乙酯为厚朴排气合剂的提取溶剂。
3.4 小结目前公开的厚朴排气合剂的质量控制仅见于厚朴的和厚朴酚与厚朴酚含量测定,2015年版中国药典也未对厚朴排气合剂进行相关的质量规定,而本品在消化外科应用较广,因此有必要提高该制剂的质量标准,从有效成分的含量切入常常是质量标准提高的重要研究部分。本课题检测了上市品种的5批厚朴排气合剂中和厚朴酚、厚朴酚、大黄素和大黄酚含量,结果显示各批次的上述4个成分均可检测到,方法回收率高,重复性好,可见HPLC同时检测厚朴排气合剂中的和厚朴酚、厚朴酚、大黄素和大黄酚成分是可行性的,本法可为厚朴排气合剂、原材料或中间品的质量控制标准的建立提供参考。
| [1] |
国家食品药品监督管理局. YBZ20442005-2009Z厚朴排气合剂标准. 新药转正标准第82册[S]. 2009: 84. State Food and Drug Administration. YBZ20442005-2009Z Standard of Houpopaiqi mixture. Standardization for New Drugs. No. 82[S]. 2009:84 |
| [2] |
马士存, 李云云, 杜明芬. 厚朴排气合剂的临床应用[J]. 现代中药研究与实践, 2014, 28(5): 84. MA SC, LI YY, DU MF. The clinical application of Houpopaiqi mixture[J]. Res Pract Chin Med, 2014, 28(5): 84. |
| [3] |
KIM BM, LEE SB, KIM JY, et al. A multivariate receptor modeling study of air-borne particulate PAHs:Regional contributions in a roadside environment[J]. Chemosphere, 2016, 144(2): 1270. |
| [4] |
田金苗. 厚朴排气合剂HPLC指纹图谱的建立[J]. 中国药师, 2014, 16(3): 389. TIAN JM. Establishment of HPLC fingerprint of Houpopaiqi mixture[J]. China Pharm, 2014, 16(3): 389. |
| [5] |
李健. 中药材厚朴治疗肠麻痹的疗效观察及药理分析[J]. 世界最新医学信息文摘, 2016, 16(1): 185. LI J. Study on houpo in treatment of intestinal paralysis and pharmacological effect[J]. World Latest Med Inf, 2016, 16(1): 185. |
| [6] |
于建玉, 廖欣, 丁厚伟, 等. 中药大黄药理作用研究进展及其临床应用[J]. 中国现代药物应用, 2016, 10(11): 286. YU JY, LIAO X, DING HW, et al. The pharmacological effects of traditional Chinese medicine rhubarb research progress and its clinical application[J]. Chin J Mod Drug Appl, 2016, 10(11): 286. |
| [7] |
ARVINDEKAR A, MORE T, PAYGHAN PV, et al. Evaluation of anti-diabetic and alpha glucosidase inhibitory action of anthraquinones from Rheumemodi[J]. Food Funct, 2015, 6(8): 2693. DOI:10.1039/C5FO00519A |
| [8] |
弓晓东, 谈瑄忠, 毛春芹, 等. RP-HPLC法同时测定大黄厚朴颗粒中7种成分[J]. 中成药, 2012, 35(3): 479. GONG XD, TAN XZ, MAO CQ, et al. Simultaneous determination of 7 components in Dahuang Houpu granules by RP-HPLC[J]. Chin Tradit Pat Med, 2012, 35(3): 479. |
| [9] |
杨跃华, 胡春丽, 张洪霞, 等. RP-HPLC法同时测定利胆排石片中5种有效成分的含量[J]. 沈阳药科大学学报, 2012, 29(5): 373. YANG YH, HU CL, ZHANG HX, et al. Simultaneous determination of 5 effective components in Lidan Paishi tablets by RP-HPLC[J]. J Shenyang Pharm Univ, 2012, 29(5): 373. |
| [10] |
经雅昆, 宋潇, 柴欣, 等. UPLC-UV-MS法应用于胃肠安丸中11个活性成分的定性与定量分析[J]. 药物分析杂志, 2012, 32(7): 1165. JING YK, SONG X, CHAI X, et al. Qualitative and quantitative analysis of 11 active ingredients in gastrointestinal pill by UPLCUV-MS[J]. Chin J Pharm Anal, 2012, 32(7): 1165. |
| [11] |
翁德会, 刘先琼, 许腊英, 等. 不同等级厚朴饮片质量评价指标的系统聚类分析[J]. 中国实验方剂学杂志, 2016, 22(23): 6. WENG DH, LIU XQ, XU LY, et al. Systematic cluster analysis on quality evaluation index of different grades of Magnolia officinalis[J]. Chin J Exp Tradit Med Form, 2016, 22(23): 6. |
| [12] |
谢剑琳, 张振秋, 梁朔, 等. HPLC波长切换法同时测定大黄、牡丹皮药对提取物中11个成分的含量[J]. 药物分析杂志, 2013, 33(1): 103. XIE JL, ZHANG ZQ, LIANG S, et al. Simultaneous determination of the 11 components in the combination extracts of Rhei Radix et Rhizoma and Moutan Cortex by HPLC wavelength switching method[J]. Chin J Pharm Anal, 2013, 33(1): 103. |
| [13] |
历淑芬, 杜伟锋, 赵耀东, 等. 大承气汤的质量控制研究[J]. 中国新药杂志, 2012, 21(22): 2674. LI SF, DU WF, ZHAO YD, et al. Quality control of Dachengqi decoction[J]. Chin J New Drugs, 2012, 21(22): 2674. |
| [14] |
王婧宁, 王梦瑶, 张振秋, 等. HPLC法同时测定大黄、厚朴药对提取物中7个成分的含量[J]. 辽宁中医杂志, 2014, 41(4): 763. WANG JN, WANG MY, ZHANG ZQ, et al. Simultaneous determination of 7 components in combination extracts of Rhei Radix et Rhizoma and Magnoliae Officinalis Cortex by HPLC[J]. Liaoning J Tradit Chin Med, 2014, 41(4): 763. |
| [15] |
申峰云, 魏惠珍, 孙勇兵, 等. UPLC-MS/MS同时测定大承气汤大鼠血浆中9种活性成分的含量[J]. 中国中药杂志, 2014, 39(12): 2345. SHEN FY, WEI HZ, SUN YB, et al. Simultaneous determination of 9 active components of Dachengqi decoction in rat plasma by UPLCMS/MS[J]. China J Chin Mater Med, 2014, 39(12): 2345. |
 2017, Vol. 37
2017, Vol. 37 