牛黄清感胶囊是由黄芩、金银花、连翘、人工牛黄、珍珠母共5味药材组成的,具疏风解表、清热解毒之功效[1],并且有研究发现其对甲型H3N2流感病毒抑制和预防的作用[2]。牛黄清感胶囊为2015年版中国药典新收录的中药制剂,2015年版中国药典通过测定黄芩苷的含量对其进行质量控制,其中黄芩苷、黄芩素、汉黄芩素是黄芩中起主要作用的成分,绿原酸和连翘苷分别是是金银花和连翘中起主要作用的成分,有关牛黄清感胶囊的含量测定和质量控制文献较少,都是测定其中1种药物成分[3-4],目前未见同时测定此药多种组分含量的报道。为了更好地控制制剂质量,本文建立了高效液相色谱法同时测定绿原酸、黄芩苷、汉黄芩苷、黄芩素、汉黄芩素、连翘苷6个成分的含量,这对于牛黄清感胶囊的质量控制具有重要意义。
1 材料岛津公司LC-20AT高效液相色谱仪,包括SPD-M20A二极管阵列检测器、SIL-20A自动进样器、岛津LC-solution工作站;迪马科技有限公司DIKMA Platisil ODS色谱柱(250 mm×4.6 mm,5 μm;填料:十八烷基硅烷键合硅胶);Millipore公司Synergy 185超纯水仪,昆山市超声仪器有限公司KQ-250DE型数控超声波清洗器。
对照品绿原酸(批号110753-201415)、黄芩苷(批号110715-200514),汉黄芩苷(批号112002-201501),黄芩素(批号111595-201306),汉黄芩素(批号111514-201304),连翘苷(批号0812-200104) 均购自中国食品药品检定研究院;牛黄清感胶囊(黑龙江澳利达奈德制药有限公司,批号14070305、14050702、14090408)。乙腈为色谱纯,水为超纯化水,其他试剂均为分析纯。
2 方法与结果 2.1 对照品溶液的制备精密称取汉黄芩苷对照品4.2 mg,置10 mL量瓶中,以甲醇定容,即得汉黄芩苷储备液;精密称取绿原酸、黄芩苷、黄芩素、汉黄芩素、连翘苷的对照品适量及汉黄芩苷储备液1 mL,置于同一10 mL量瓶中,用甲醇定容,制成含绿原酸0.164 mg·mL-1、黄芩苷0.106 mg·mL-1、汉黄芩苷0.042 mg·mL-1、黄芩素0.026 25 mg·mL-1、汉黄芩素0.015 mg·mL-1、连翘苷0.033 3 mg·mL-1的混合对照品溶液。
2.2 供试品溶液的制备取牛黄清感胶囊内容物1.0 g,精密称定,置具塞锥形瓶中,精密加50%甲醇50 mL,密塞,称量,超声(250 W,40 kHz)处理30 min,放冷,再称量,用50%甲醇补足减失的量,摇匀,经0.45 μm微孔滤膜过滤,即得供试品溶液[1]。
2.3 阴性样品溶液的制备按处方分别制备缺少金银花、黄芩、连翘的阴性样品,按“2.2”项方法操作,即得阴性样品溶液。
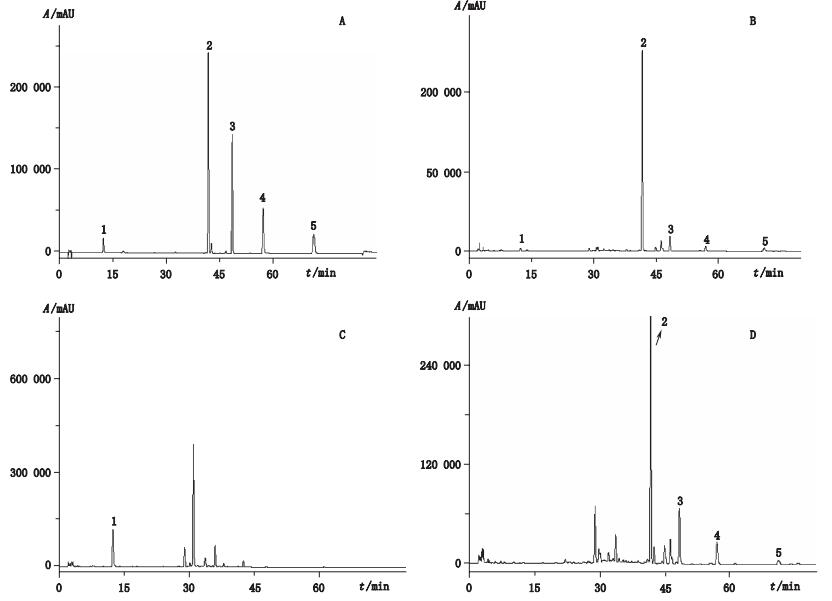
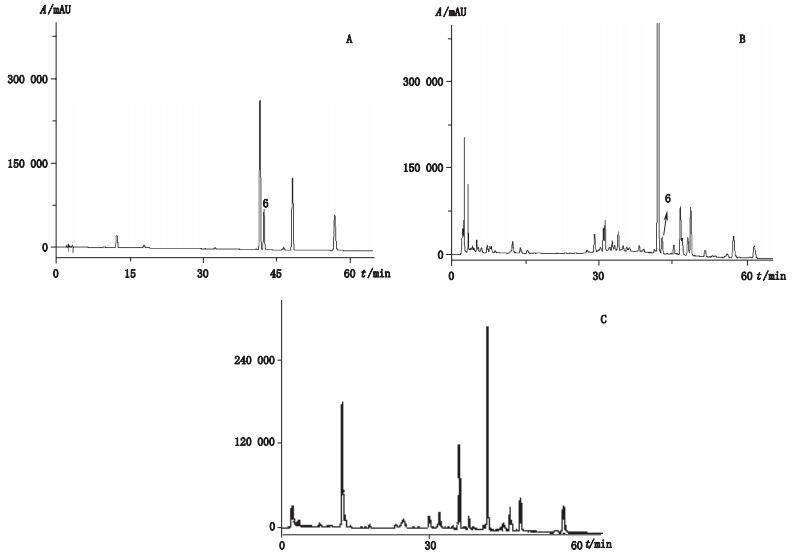
2.4 色谱条件色谱柱:DIKMA Platisil ODS(250 mm×4.6 mm,5 μm);流动相:乙腈(A)-0.1%磷酸水溶液(B),梯度洗脱(0~20 min,10%A→16%A;20~40 min,16%→30%A;40~60 min,30%→40%A;60~80 min,40%A);流速:1 mL·min-1;柱温:30 ℃;检测波长:278 nm(绿原酸、黄芩苷、汉黄芩苷、黄芩素、汉黄芩素)、210 nm(连翘苷);进样量:10 μL。在上述色谱条件下,各待测组分分离度均大于1.5、理论塔板数均大于5 000。混合对照品溶液、样品溶液及各阴性样品溶液色谱图见图 1、2。
|
1.绿原酸(chlorogenic acid) 2.黄芩苷(baicalin) 3.汉黄芩苷(wogonoside) 4.黄芩素(baicalein) 5.汉黄芩素(wogonin) 图 1 混合对照品(A)、样品(B)、不含黄芩的阴性样品(C)、不含金银花的阴性样品(D)在278 nm处色谱图 Figure 1 HPLC chromatograms of mixed reference substances (A), sample (B), negative sample without Scutellariae Radix (C) and negative sample without Lonicerae Japonicae Flos (D) at 278 nm |
|
6.连翘苷(phillyrin) 图 2 混合对照品(A)、样品(B)、不含连翘的阴性样品(C)在210 nm处色谱图 Figure 2 HPLC chromatograms of mixed reference substances(A), sample(B), and negative sample without Forsythiae Fructus(C)at 210 nm |
精密吸取混合对照品溶液1、5、8、10、15、20 μL进样测定;以峰面积(Y)为纵坐标,进样量(X)为横坐标进行线性回归,得绿原酸、黄芩苷、汉黄芩苷、黄芩素、汉黄芩素、连翘苷的线性回归方程见表 1。
|
|
表 1 绿原酸、黄芩苷、汉黄芩苷、黄芩素、汉黄芩素、连翘苷线性的回归方程 Table 1 Linear regression equations of chlorogenic acid, baicalin, wogonoside, baicalein, wogonin and phillyrin |
取混合对照品溶液,按“2.4”项下色谱条件连续进样6次,测得混合对照品中绿原酸、黄芩苷、汉黄芩苷、黄芩素、汉黄芩素、连翘苷峰面积的RSD(n=6) 分别为0.44%、0.36%、0.34%、0.29%、0.71%、0.58%。
2.7 稳定性试验取同一供试品溶液,室温放置,分别于0、2、4、6、12、24 h进行测定,测得绿原酸、黄芩苷、汉黄芩苷、黄芩素、汉黄芩素、连翘苷峰面积的RSD(n=6) 分别为0.85%、0.81%、0.68%、0.42%、0.74%、0.79%,表明供试品溶液在常温下24 h内稳定。
2.8 重复性试验取牛黄清感胶囊样品,按“2.2”项下方法平行制备6份供试品溶液,以“2.4”项下色谱条件进行测定,得绿原酸、黄芩苷、汉黄芩苷、黄芩素、汉黄芩素、连翘苷的平均含量(n=6) 分别为0.759、34.223、1.401、0.782、0.519、0.735 mg·g-1,RSD分别为0.96%、1.06%、0.88%、0.93%、1.1%、0.78%。
2.9 加样回收率试验精密称取“2.8”项已测知含量样品约0.5 g,共9份,平均分为3组,按低、中、高浓度(0.8倍、1倍、1.2倍)分别加入一定量的绿原酸、黄芩苷、汉黄芩苷、黄芩素、汉黄芩素、连翘苷对照品,按照“2.2”项下方法制备供试溶液,进样10 μL进行测定,结果绿原酸、黄芩苷、汉黄芩苷、黄芩素、汉黄芩素、连翘苷的平均回收率(n=9) 分别为99.6%、99.3%、100.7%、99.6%、100.2%、99.6%,RSD分别为1.2%、1.1%、1.4%、1.2%、1.5%、1.8%。
2.10 样品含量测定取3批样品各1.0 g,按“2.2”项下方法制备供试品溶液,按“2.4”项下色谱条件进样测定,以外标法计算待测成分含量,结果见表 2。
|
|
表 2 牛黄清感胶囊中6个成分的测定(mg·g-1,n=3) Table 2 Determination of six components in Niuhuang Qingan Capsules |
由于牛黄清感胶囊是2015年版中国药典中新收录的中成药,所以相关文献较少,在流动相的选择上,笔者考察了乙腈-磷酸水、甲醇-磷酸水2个溶剂系统[5-13],结果发现甲醇-磷酸水为流动相时,黄芩里的几个待测组分出峰时间较晚。采用乙腈-磷酸水时,汉黄芩素在有机相比例较高时分离度不好,所以前期有机相比例较低,导致整个分析时间较长。
3.2 波长的选择波长扫描得到绿原酸最大吸收波长为327 nm,黄芩苷、汉黄芩苷、黄芩素、汉黄芩素为278 nm,连翘苷为210 nm。278 nm虽然不是绿原酸的最大吸收波长,但是由于其在制剂中含量相对较高,采用278 nm作为测定波长能够达到方法学考察的要求,得到合格的色谱峰,考虑到同一波长下测定使得方法更加简单,增加了普适性,所以绿原酸、黄芩苷、汉黄芩苷、黄芩素、汉黄芩素选择278 nm作为检测波长。
3.3 样品处理本研究在样品的处理上,参考了中国药典中的处理方法[1],但是浓度提高了几倍,因为在测定的过程中发现此药中黄芩苷含量特别高,完全按药典中的处理方法,其余几种成分含量相对较少,测定较困难,因此提高了供试品溶液的浓度。
3.4 总结牛黄清感胶囊对甲型H1N1、H3N2流感病毒及其他病毒都具有治疗及预防的作用[2, 14-15],市场发展空间很大,需要提高质量要求。本药由由黄芩、金银花、连翘、人工牛黄、珍珠母5种药物组成,本实验测定了含量最高也是起主要作用的前3种药物,对提高此种药物质量控制具有重要的意义。
| [1] |
中国药典2015年版. 一部[S]. 2015: 659. ChP 2015. Vol Ⅰ[S]. 2015:659 |
| [2] |
常洋, 周有财, 段书敏, 等. 牛黄清感胶囊对甲型H3N2流感病毒抑制和预防作用的实验研究[J]. 中国医药科学, 2013, 3(16): 27. CHANG Y, ZHOU YC, DUAN SM, et al. Experimental study of inhibition and prevention effect of Niuhuang Qinggan capsules for H3N5 influenza virus A[J]. China Med Pharm, 2013, 3(16): 27. |
| [3] |
韩家忠, 贾善学. 高效液相色谱法测定牛黄清感胶囊中连翘苷的含量[J]. 医药导报, 2009, 28(10): 1358. HAN JZ, JIA SX. Simultaneous determination of phillyrin in Niuhuang Qingan capsules by HPLC[J]. Her Med, 2009, 28(10): 1358. DOI:10.3870/yydb.2009.10.050 |
| [4] |
于鑫. 牛黄清感胶囊质量标准研究[J]. 黑龙江中医药, 2015, 44(1): 65. YU X. Studies on the quality standards of Niuhuang Qinggan capsules[J]. Heilongjiang J Tradit Chin Med, 2015, 44(1): 65. |
| [5] |
谢清萍, 彭文明, 刘萍绿. RP-HPLC法同时测定小儿咽扁颗粒中5个成分的含量[J]. 药物分析杂志, 2013, 35(12): 2163. XIE QP, PENG WM, LIU PL. Simultaneous determination of five active components in Xiao'er Yanbian granules by RP-HPLC[J]. Chin J Pharm Anal, 2013, 35(12): 2163. |
| [6] |
何元松, 刘勇, 石晋丽, 等. HPLC法同时测定复方抗焦虑胶囊中4种活性成分的含量[J]. 药物分析杂志, 2015, 35(10): 1806. HE YS, LIU Y, SHI JL, et al. Simultaneous determination of the contets of active components in anti-anxiety compound capsules by HPLC[J]. Chin J Pharm Anal, 2015, 35(10): 1806. |
| [7] |
白月明, 刘雅敏, 胡春月, 等. HPLC法同时测定小儿清热宁颗粒中5种成分含量[J]. 中药材, 2015, 38(8): 1741. BAI YM, LIU YM, HU CY, et al. Simultaneous determination of five components in Xiaoer Qingrening granules by HPLC[J]. J Chin Med Mater, 2015, 38(8): 1741. |
| [8] |
孟姝, 林玉莲, 都述虎. HPLC同时测定利胆片中绿原酸和黄芩苷的含量[J]. 中国实验方剂学杂志, 2015, 21(10): 77. MENG Z, LIN YL, DU SH. Simultaneous determination of baicalin and chlorogenic acid in Lidan tablets by HPLC[J]. Chinese Journal of Experimental Traditional Medical Formulae, 2015, 21(10): 77. |
| [9] |
郝乘仪, 冯波, 郭淑英, 等. 黄连上清片中9种成分的HPLC波长切换法测定[J]. 中国医药工业杂志, 2015, 46(9): 995. HAO CY, FENG B, GUO SY, et al. Determination of nine compounds in Huanglian Shangqing tablets by HPLC combined with wavelength switching method[J]. Chin J Pharm, 2015, 46(9): 995. |
| [10] |
郭东晓, 林林, 汪冰, 等. HPLC波长切换法同时测定抗感颗粒中7个成分的含量[J]. 药物分析杂志, 2015, 35(10): 1796. GUO DX, LIN L, WANG B, et al. Simultaneous determnation of the content of seven components in Kanggan granules by HPLC wavelength switching technology[J]. Chin J Pharm Anal, 2015, 35(10): 1796. |
| [11] |
邓茂芳, 程维明. HPLC同时测定鱼腥草芩蓝合剂中3种活性成分的含量[J]. 中国现代应用药学, 2015, 32(5): 589. DENG MF, CHENG WM. Simultaneous determination of three ingredients in Yuxingcao Qinlan mixtures by HPLC[J]. Chin J Mod Appl Pharm, 2015, 32(5): 589. |
| [12] |
李想, 卢静华. HPLC法同时测定加味香连丸中芍药苷、柚皮苷、橙皮苷和黄芩苷[J]. 中成药, 2015, 37(9): 1955. LI X, LU JH. Simultaneous determination of paeoniflorin, naringin, hesperidin and baicalin in Jiawei Xianglian pills by HPLC[J]. Chin Tradit Pat Med, 2015, 37(9): 1955. |
| [13] |
崔生飞, 齐广才, 谢凡凡, 等. 双波长HPLC同时测定羚羊清肺散中4种有效成分的含量[J]. 中国实验方剂学杂志, 2016, 22(13): 77. CUI SF, QI GC, XIE FF, et al. Simultaneous determination of four effective components in Lingyang Qingfei powder by double wavelength HPLC[J]. Chin J Exp Tradit Med Form, 2016, 22(13): 77. |
| [14] |
周有财, 常洋, 王玉莹. 牛黄清感胶囊对呼吸道合胞病毒体外预防作用的实验研究[J]. 中国医药指南, 2014, 12(29): 68. ZHOU YC, CHANG Y, WANG YY. Experimental study of inhibition and prevention effect of Niuhuang Qinggan capsules for respiratory syncytial virus[J]. Guide China Med, 2014, 12(29): 68. |
| [15] |
周有财, 宫君相, 段书敏, 等. 牛黄清感胶囊对高致病甲型H1N1流感病毒的预防作用的实验研究[J]. 中国保健营养, 2013(6): 101. ZHOU YC, GONG JX, DUAN SM, et al. Experimental study of inhibition and prevention effect of Niuhuang Qinggan capsules for H1N1 influenza virus A[J]. China Health Care Nutr, 2013(6): 101. |
 2017, Vol. 37
2017, Vol. 37 
