榄香烯(elemene)系我国首先从姜科植物温莪术中提取的具有抗癌活性的倍半萜烯天然抗癌药物。以β-榄香烯为主要成分的榄香烯乳注射液是我国自主研发成功的二类抗肿瘤新药,目前在临床上广泛用于恶性浆膜腔积液、肺癌、消化道肿瘤、脑瘤以及其他浅表性肿瘤的治疗[1-3]。榄香烯的含量测定主要以GC法和GC-MS联用的方法为主[4-8],也有报道采用LC法[9-14]。但是,榄香烯有关物质的检查方法文献报道较少,主要为RP-HPLC法[13],国外药典和中国药典均未收载本品,国家药品标准WS1-(X-094)-2000Z收载了榄香烯[15]原料药的有关物质检查,方法与含量测定方法一致,为填充柱法。据厂家研究资料,榄香烯是以莪术油为原料,通过精馏分离得到,终产品必定为沸点和极性十分相近的化合物的混合物,除β-、γ-、δ-榄香烯(分子式同为C15H24)确定为有效成分外,其他为未知杂质,大多又为β-榄香烯的同分异构体。应用原方法测定时,β-榄香烯与其他2个组分及其他挥发性组分不能得以较好分离,影响有关物质检测的准确性。采用毛细管气相色谱法(CGC法)则能较大地提高各组分之间的分离度,提高有关物质检测的准确性。在所查阅的研究文献中,尚未有人确证其中的未知杂质,作者采用GC-MS的方法确证了其中一个含量最大(约为8%)的杂质为β-石竹烯(分子式为C15H24)。本文采用CGC法并辅以GC-MS的方法,对榄香烯原料的有关物质进行了检测,方法简便,准确度高,适合于榄香烯有关物质的检测。
1 仪器与试药Agilent 7890A气相色谱仪,GC-MS2010气相色谱-质谱联用仪,METTLER TOLEDO MT5百万分之一天平。
对照品β-榄香烯(中国食品药品检定研究院,批号100268-200401,含量99.2%);γ-榄香烯(大连远大制药有限公司提供,批号20081009,含量70.39%);δ-榄香烯(大连远大制药有限公司提供,批号20081009,含量77.79%);β-石竹烯[TCI(上海)化成工业发展有限公司,批号C0796,含量 > 90.0%(GC)]。丙酮为色谱纯。榄香烯原料药,大连华立德泽药业有限公司提供,批号分别为1011211、1012031、1012121。
2 方法与结果 2.1 色谱条件采用安捷伦DB-WAXetr毛细管柱(60 m×0.32 mm× 0.25 μm),PEG-20M为固定液,柱温为程序升温(起始柱温为80 ℃,维持5 min,以3 ℃·min-1的速率升温至185 ℃,再以20 ℃·min-1的速率升温至230 ℃,维持60 min),进样口温度230 ℃,检测器温度230 ℃,分流比10:1,柱前恒压124.11 kPa,进样量1.0 μL。
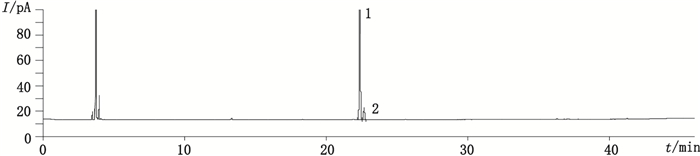
2.2 色谱系统适用性试验取β-榄香烯对照品和β-石竹烯各适量,用丙酮制成每1 mL中含β-榄香烯1 mg和β-石竹烯0.08 mg的混合溶液,作为系统适用性试验溶液。按上述色谱条件试验,β-榄香烯峰与β-石竹烯峰之间的分离度应符合规定,理论板数按β-榄香烯峰计算应不低于200 000。实测结果显示,两峰之间的分离度为2.0,β-榄香烯峰的理论板数为391 145。系统适用性色谱图见图 1。
|
1.β-榄香烯(β-elemene)2.β-石竹烯(β-caryophyllene) 图 1 系统适用性试验色谱图 Figure 1 Chromatogram of system suitability test |
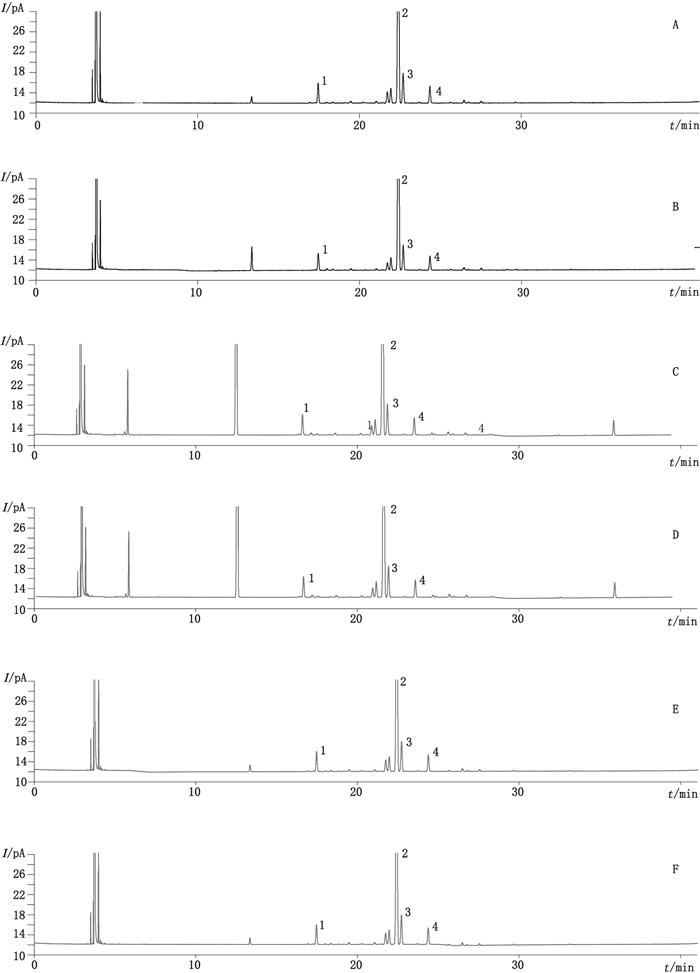
取本品约10 mg,置10 mL刻度试管中,加丙酮定容至刻度,摇匀,进样,记录色谱图,见图 2-A。
|
A.未破坏(not destroyed)B.酸破坏(destroyed by acidification)C.碱破坏(destroyed by basification)D.氧化破坏(destroyed by oxidation)E.加热破坏(destroyed by heating)F.光照破坏(destroyed by illumination) 1.δ-榄香烯(δ-elemene)2.β-榄香烯(β-elemene)3.β-石竹烯(β-caryophyllene)4.γ-榄香烯(γ-elemene) 图 2 榄香烯有关物质检查方法专属性试验色谱图 Figure 2 Chromatograms of method specificity tests for determination of related substances in elemene |
称取本品约10 mg,置10 mL刻度试管中,加0.5 mL丙酮,再加入1 mol·L-1盐酸溶液0.5 mL,混匀,放置1 h,加入0.5 mL的1 mol·L-1氢氧化钠溶液中和,振摇,再加丙酮至刻度,摇匀,以4 000 r·min-1离心10 min,取上清液进样,记录色谱图,见图 2-B。
2.3.3 碱破坏试验称取本品约10 mg,置10 mL刻度试管中,加丙酮0.5 mL,再加入1 mol·L-1氢氧化钠溶液0.5 mL,混匀,放置1 h,加入1 mol·L-1盐酸溶液0.5 mL中和,振摇,再加丙酮至刻度,摇匀,以4 000 r·min-1离心10 min,取上清液进样,记录色谱图,见图 2-C。
2.3.4 氧化破坏试验称取本品约10 mg,置10 mL刻度试管中,加0.5 mL丙酮,再加入30%过氧化氢溶液0.5 mL,混匀,放置1 h,再加丙酮至刻度,摇匀,进样,记录色谱图,见图 2-D。
2.3.5 加热破坏试验称取本品约10 mg,置10 mL刻度试管中,密塞,在60 ℃水浴中加热1 h,取出放冷,加丙酮定容至刻度,摇匀,进样,记录色谱图,见图 2-E。
2.3.6 光照破坏试验取本品适量,置石英比色杯中,密塞,先在紫外灯(254 nm)下照射1 h,再在紫外灯(366 nm)下照射1 h,称取照射后的样品约10 mg,置10 mL刻度试管中,加丙酮定容至刻度,摇匀,进样,记录色谱图,见图 2-F。
比对空白溶剂和未破坏的样品色谱图可以发现,榄香烯原料药仅在碱破坏试验条件下降解或转化较多,其他试验条件下均显示较好的稳定性,所确定的色谱系统对所产生的杂质均能较好地分离。
2.4 线性试验精密称取β-榄香烯对照品50.440 mg,置250 mL量瓶中,用丙酮定容至刻度,摇匀,即得对照品储备液;精密量取储备液各适量,分别置适宜的量瓶中,用丙酮制成每1 mL中含β-榄香烯5.003 6、10.007、20.015、40.029、80.058、120.09与160.12 μg的溶液,作为系列线性试验用对照品溶液,依法检测,记录色谱图,以峰面积A为纵坐标,质量浓度C为横坐标,得线性方程:
A=0.522 3C-0.090 13 r=1.000(n=7)
β-榄香烯质量浓度在5.003 6~160.12 μg·mL-1范围内线性良好。
2.5 进样精密度试验取“2.4”项下质量浓度为40.029 μg·mL-1的线性试验用对照品溶液连续进样6次,记录峰面积,RSD=0.73%,表明进样精密度良好。
2.6 定量限与检出限试验精密量取“2.4”项下质量浓度为20.015 μg·mL-1的线性试验用对照品溶液3 mL,置20 mL量瓶中,加丙酮稀释至刻度,摇匀,即得定量限试验用溶液,进样,记录色谱图;以S/N=10计算,β-榄香烯的定量限为2.68 μg·mL-1。精密量取“2.4”项下质量浓度为20.015 μg·mL-1的线性试验用对照品溶液1 mL,置20 mL量瓶中,加丙酮稀释至刻度,摇匀,即得检出限试验溶液,依法检测,记录色谱图;以S/N=3计算,β-榄香烯的检出限为0.87 μg·mL-1。
2.7 溶液稳定性供试品溶液在室温下放置,于0、33、58 h进样,记录峰面积,计算RSD,结果见表 1。结果表明,供试品溶液在58 h内稳定,杂质无明显变化。
|
|
表 1 溶液稳定性试验结果 Table 1 Results for solution stability test |
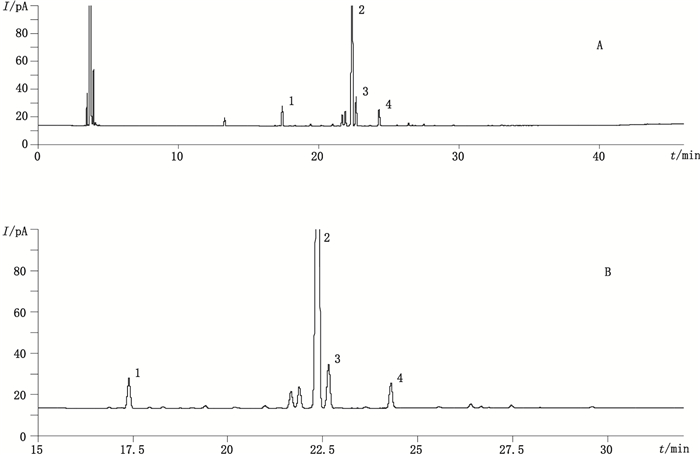
精密称取本品适量,加丙酮制成每1 mL中约含1 mg的溶液,作为供试品溶液;取β-榄香烯对照品适量,精密称定,加丙酮制成每1 mL中含0.15 mg的溶液,作为对照品溶液。精密量取对照品溶液1.0 μL,注入气相色谱仪,调节检测灵敏度,使对照品溶液主峰的峰高约为满量程的20%;再精密量取供试品溶液、对照品溶液各1.0 μL,分别注入气相色谱仪,记录色谱图。在供试品溶液的色谱图中,除空白溶剂峰和β-榄香烯峰、δ-榄香烯峰(相对保留时间约0.75)、γ-榄香烯峰(相对保留时间约1.10)外,如有杂质峰,按外标法以各杂质峰面积的和计算,不得过15.0%。批号分别为1011211、1012031、1012121的3批样品中有关物质总量依次为15.4%、15.5%、14.7%;供试品溶液的色谱图及其局部放大图见图 3。
|
1.δ-榄香烯(δ-elemene)2.β-榄香烯(β-elemene)3.β-石竹烯(β-caryophyllene)4.γ-榄香烯(γ-elemene) 图 3 榄香烯有关物质检查供试品溶液(批号1011211)色谱图(A)及其局部放大图(B) Figure 3 Chromatogram of related substances in elemene(lot No.1011211)(A)and the partially enlarged view(B) |
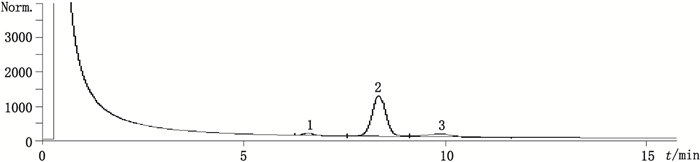
榄香烯原料药标准WS1-(X-094)-2000Z收载的有关物质检查与含量测定方法一致,为填充柱法,按照填充柱法进行检测,除了检测到β-榄香烯之外,还可以检测到γ-榄香烯和δ-榄香烯,检测到其他杂质峰较少(见图 4)。受柱效的影响,分离出的杂质量非常有限,杂质限度订为不超过8.0%很容易达到,但是无法反映产品的真实质量。采用CGC毛细管柱法,对杂质的分离远优于填充柱法,测得样品的杂质量均大大超出原标准的限度(8.0%)。在含量限度(85.0%)不变的情况下,考虑质量守恒的要求,杂质限度修订为杂质总量不超过15.0%。
|
1.δ-榄香烯(δ-elemene)2.β-榄香烯(β-elemene)3.γ-榄香烯(γ-elemene) 图 4 填充柱法得到的供试品色谱图 Figure 4 Sample chromatogram obtained by packed-column gas chromatography |
试验时选取了4根不同的色谱柱[DB-WAXetr(60 m×0.32 mm×0.25 μm)、DB-WAXetr(30 m×0.32 mm×1.0 μm)、DB-WAXetr(30 m×0.25 mm×0.5 μm)、HP-5(30 m×0.32 mm×0.25 μm)]进行试验,并调整GC的程序升温条件。除HP-5色谱柱基本不能将β-石竹烯与β-榄香烯分离以及DB-WAXetr(30 m×0.32 mm×1.0 μm)的分离度不能达到要求外,其他2条色谱柱均适用,尤其以DB-WAXetr(60 m×0.32 mm×0.25 μm)色谱柱分离效果最好,各色谱柱的分离效果见表 2。
|
|
表 2 色谱柱柱效比较 Table 2 Comparison of column efficiency |
在试验的过程中,采用优化后的色谱系统对本品进行分离,发现在β-榄香烯峰之后有1个较大的未知色谱峰与β-榄香烯峰较难分离,通过检索质谱库并采用对照品比较分析的方法确认,该杂质峰应为β-石竹烯峰,且其峰面积约为β-榄香烯峰面积的8%左右。故配制β-榄香烯和β-石竹烯的混合对照品溶液作为系统适用性试验溶液,规定两者之间的分离度应符合规定,β-榄香烯的理论板数应不低于200 000。
3.4 有关物质计算方法榄香烯以莪术油为原料,通过精馏分离得到。据厂家研究资料和GC-MS数据显示,除β-、γ-、δ-榄香烯(分子式同为C15H24)确定为有效成分外,能够确证的杂质为β-石竹烯(分子式为C15H24),其他为未知杂质,大多又为β-榄香烯的同分异构体,在FID检测器中的响应基本相同。本品中β-、γ-、δ-榄香烯的含量之和约为85%,不宜采用主成分自身对照法计算,故采用β-榄香烯对照品用外标法计算有关物质的含量。
3.5 其他探索性研究由供试品溶液的色谱图(图 3)可知,在β-榄香烯峰之前有2个大小差不多的较大未知杂质峰,本文曾采用GC-MS的方法试图搞清楚其为何化合物,经检索质谱库发现,保留时间为21.659 min的未知杂质的相对分子质量为204,参考物质为(1α,4aα,8aα)-1,2,3,4,4a,5,6,8a-octahydro-7-methyl-4-methylene-1-(1-methylethyl)-naphthalene,相似度为88%。保留时间为21.880 min的未知杂质的相对分子质量为204,参考物质为β-榄香烯,相似度为94%。显然,它们均为β-榄香烯的同分异构体,要进一步确证其结构信息,必须获得一定量高纯度的单体,在目前的实验条件下,实现的难度较大,留待今后实验条件具备的时候做进一步研究。
| [1] |
花文峰, 蔡绍晖. β-榄香烯抗肿瘤作用的基础与临床研究[J]. 中药材, 2006, 29(1): 93. HUA WF, CAI SH. Basic and clinical study on antitumor effect of β-elemene[J]. J Chin Med Mater, 2006, 29(1): 93. |
| [2] |
Pajean M, Herbage D. Effect of collagen on liposome permeability[J]. Int J Pharm, 1993, 91(4): 209. |
| [3] |
周洪语, 侯菊生, 罗其中. 榄香烯抗肿瘤作用机制的研究进展[J]. 中国肿瘤临床, 2000, 27(5): 392. ZHOU HY, HOU JS, LUO QZ. Research progress in the anticancer mechanism of elemene[J]. Chin J Clin Oncol, 2000, 27(5): 392. |
| [4] |
苏佳妍, 于大海, 李庆民. 毛细管柱气相色谱法测定榄香烯及榄香烯注射液的含量[J]. 山西医药杂志, 2012, 41(11): 1120. SU JY, YU DH, LI QM. Determination of elemene and elemene injection by capillary gas chromatography[J]. Shanxi Med J, 2012, 41(11): 1120. DOI:10.3969/j.issn.0253-9926.2012.11.028 |
| [5] |
谢守德, 李希, 冯建安, 等. 超滤法-气相色谱法测定β-榄香烯脂质体药物含量及包封率[J]. 中国药业, 2009, 18(18): 27. XIE SD, LI X, FENG JA, et al. Content determination and entrapment efficiency of β-elemene liposomes by ultrafiltration-GC[J]. Chin Pharm, 2009, 18(18): 27. DOI:10.3969/j.issn.1006-4931.2009.18.020 |
| [6] |
王艳芝, 覃春菀, 郑甲信, 等. 固体脂质纳米粒中β-榄香烯含量的气相色谱法测定[J]. J郑州大学学报(医学版), 2008, 43(1): 160. WANG YZ, QIN CW, ZHENG JX, et al. Determination of β-elemene in β-elemene solid lipid nanoparticles by gas chromatography[J]. J Zhengzhou Univ(Med Sci), 2008, 43(1): 160. |
| [7] |
杜霞, 吴琳华, 赵红光. 气相色谱-质谱联用测定莪术油中β-榄香烯的含量[J]. 药物分析杂志, 2007, 27(2): 216. DU X, WU LH, ZHAO HG. GC-MS determination of β-elemene in Zedoary turmeric oil[J]. Chin J Pharm Anal, 2007, 27(2): 216. |
| [8] |
魏福祥, 邓小丽, 陈晓, 等. 气相色谱法测定莪术挥发油中榄香烯含量[J]. 河北科技大学学报, 2005, 26(3): 219. WEI FX, DENG XL, CHEN X, et al. Determination of element in essential oil from curcuma by GC[J]. J Hebei Univ Sci Tech, 2005, 26(3): 219. DOI:10.7535/hbkd.2005yx03014 |
| [9] |
袁子民, 赵琳, 王静, 等. HPLC测定β-榄香烯冻干针剂中主药的含量[J]. 中国实验方剂学杂志, 2012, 18(20): 64. YUAN ZM, ZHAO L, WANG J, et al. Determination of β-elemene in lyophilized powder for injection of β-elemene-polybutylcyanoacrylate nanoparticles by HPLC[J]. Chin J Exp Tradit Med Form, 2012, 18(20): 64. |
| [10] |
韦会平, 赵牧, 阎妍, 等. HPLC法测定紫茎泽兰和五色梅中β-榄香烯的含量[J]. 中国药房, 2012, 23(39): 3709. WEI HP, ZHAO M, YAN Y, et al. Content Determination of β-elemene in Eupatorium adenophorum and Lantana camara by HPLC[J]. China Pharm, 2012, 23(39): 3709. DOI:10.6039/j.issn.1001-0408.2012.39.22 |
| [11] |
田金苗, 张满来, 胡海洋, 等. HPLC法测定榄香烯亚微乳注射液中β-榄香烯的含量[J]. 中国药事, 2011, 25(8): 802. TIAN JM, ZHANG ML, HU HY, et al. Determination of β-elemene in elemene microemulsion injection by HPLC[J]. Chin Pharm Aff, 2011, 25(8): 802. |
| [12] |
李兆明, 孙杰, 张曼红, 等. HPLC法测定β-榄香烯自微乳浓缩液中的药物含量[J]. 齐鲁药事, 2010, 29(12): 718. LI ZM, SUN J, ZHANG MH, et al. Determination of the β-elemene content in the self-microemulsifying system concentrate by HPLC[J]. Qilu Pharm Aff, 2010, 29(12): 718. |
| [13] |
乔丽, 王静, 袁子民. RP-HPLC法测定β-榄香烯的含量及有关物质[J]. 中国现代药物应用, 2010, 4(5): 1. QIAO L, WANG J, YUAN ZM. RP-HPLC determination of β-elemene and its related substances[J]. Chin J Mod Drug Appl, 2010, 4(5): 1. |
| [14] |
宋笑丹, 王学军, 杜霞, 等. HPLC法测定β-榄香烯脂质体药物含量及包封率[J]. 药物分析杂志, 2007, 27(8): 1222. SONG XD, WANG XJ, DU X, et al. HPLC determination of the content and entrapment efficiency of β-elemene liposome[J]. Chin J Pharm Anal, 2007, 27(8): 1222. |
| [15] |
WS1-(X-094)-2000Z国家药品标准新药转正标准. 第22册[S]. 2002: 677 WS1-(X-094)-2000Z Drug Standards Promulgated by the SFDA. Vol 22[S]. 2002: 677 |
 2017, Vol. 37
2017, Vol. 37 