糖尿病合并缺血性心脏疾病患者,在经皮冠状动脉介入治疗、冠状动脉旁路移植术治疗时可导致心肌缺血再灌注(ischemia/reperfusion, I/R)损伤。研究表明,糖尿病患者心肌缺血再灌注损伤的发病率不仅高于非糖尿病患者,且心肌受损程度更为严重、预后更差、死亡率更高[1]。糖尿病合并心肌缺血再灌注时,心肌细胞坏死和凋亡是其损伤加重和敏感性增加的重要原因[2]。细胞焦亡是近年发现的一种新的促炎程序性细胞死亡方式,最主要的生物学特征是依赖于半胱天冬酶-1(caspase-1)并伴随炎症级联反应,在内源性和外源性刺激作用下,凋亡相关斑点样蛋白(apoptosis-associated speck-like protein containing, ASC)作用于pro-caspase-1形成炎性小体并激活pro-caspase-1,活化的caspase-1诱导下游细胞因子白细胞介素(interleukin, IL)-1β、IL-18活化,细胞释放乳酸脱氢酶(LDH)等胞内物质,介导组织细胞损伤[3]。研究表明,大鼠糖尿病心肌中caspase-1的mRNA水平和蛋白质的表达显著增加[4],进一步研究发现NLRP3炎性小体激活caspase-1介导的细胞焦亡在糖尿病性心肌病(diabetic cardiomyopathy, DCM)发生发展中起重要作用[5]。研究发现,肾小管上皮细胞缺血再灌注时,caspase-1和IL-1β表达增加,证实细胞焦亡是肾小管上皮细胞I/R损伤的重要机制[6]。然而caspase-1依赖的细胞焦亡是否参与糖尿病心肌缺血再灌注损伤,caspase-1依赖的细胞焦亡是否介导增加糖尿病心肌缺血再灌注损伤的敏感性和易损性尚未见报道。本研究拟探究caspase-1依赖的细胞焦亡在糖尿病大鼠心肌缺血再灌注损伤中的作用及可能机制。
1 材料与方法 1.1 动物及分组SPF级健康成年雄性SD大鼠,体重210-230 g,由北京华阜康生物科技股份有限公司提供。适应性观察1周,禁食12 h后经腹腔注射l%链脲佐菌素-柠檬酸盐缓冲液(Sigma公司,美国)60 mg/kg,3 d后禁食6 h,断尾取血测空腹血糖,若血糖值>16.7 mmol/L,并出现多饮、多食、多尿即糖尿病大鼠模型制备成功。此后每周测定一次空腹血糖和体重,普食饲养8周。非糖尿病大鼠腹腔注射等量柠檬酸盐缓冲液。取非糖尿病和糖尿病大鼠各40只,采用随机数字表法,分别将其分为两个亚组(n=20):正常假手术组(NS组)、正常心肌缺血再灌注组(NIR组)、糖尿病假手术组(DS组)、糖尿病心肌缺血再灌注组(DIR组)。
1.2 心肌I/R模型大鼠术前禁食12 h,采用腹腔注射1%戊巴比妥钠60 mg/kg麻醉固定大鼠。大鼠气管插管后接动物呼吸机行机械通气,皮下电极监测Ⅱ导联心电图。于左锁骨中线第四肋间打开胸腔暴露心脏,在左心耳下缘与肺动脉圆锥间左冠状动脉前降支(LAD)起始部下3 mm处以6-0尼龙线结扎,缺血30 min,松开结扎线再灌注120 min,假手术组只穿线不接扎。判断缺血成功的标准:心尖部及左心室前壁变白,心电图示QRS波增宽,ST段抬高,T波高尖,心室壁运动减弱;再灌注成功的标准:心尖部位及左心室前壁恢复红色,心电图示ST段回落。
1.3 心肌梗死面积测定每组分别在再灌注结束后随机取6只大鼠,再次结扎LAD,股静脉穿刺注射3%伊文斯蓝1 ml,至大部分心脏蓝染后取出心脏,置于-20 ℃保存2 h,于心脏垂直于长轴方向将心脏切成2 mm厚的薄片,用PBS配制的1%TTC溶液(sigma公司,美国)37 ℃避光孵育15 min,4%多聚甲醛固定20 min,用扫描仪拍片。采用Image-ProPlus 6.0图像分析软件分析,正常心肌呈蓝色,缺血心肌呈砖红色,梗死心肌呈灰白色,分析测定心肌缺血面积和梗死面积。
1.4 CK-MB和LDH检测再灌注120 min后,采集动脉血样,离心后取血清,按照CK-MB、LDH活性检测试剂盒说明测定CK-MB含量和LDH活性。
1.5 HE染色于再灌注120 min结束后,取缺血区心尖部心肌组织,用4%多聚甲醛溶液固定,石蜡包埋后于切片机上切片,HE染色,显微镜下观察病理结果。
1.6 Western Blot法检测心肌组织NLRP3、caspase-1、ASC、IL-1β的表达于再灌注120 min结束时,每组取8只大鼠,处死后取左室心肌缺血区心肌组织100 mg,用冰PBS灌洗干净后,加入1 000 μl RIPA裂解液,冰上静置30 min,再冰浴电动匀浆,4 ℃下12 000 g离心15 min,取上清,用BCA法测定蛋白浓度。加5×上样缓冲液混匀煮沸10 min。Western Blot进行蛋白定量检测,分别用10%分离胶和5%浓缩胶、15%分离胶和5%浓缩胶进行电泳,于PVDF膜上进行转膜,5%脱脂奶粉室温封闭1 h,分别用NLRP3多克隆抗体(1:200,Novus公司,美国)、caspase-1多克隆抗体(稀释度1:200,Santa公司,美国)、ASC多克隆抗体(稀释度1:200,Santa公司,美国)和IL-1β多克隆抗体(稀释度1:1 000,Abcam公司,美国)进行4 ℃过夜孵育。TBST洗涤3次,每次10 min,用山羊抗兔多克隆荧光二抗(稀释度1:10 000,Li-Cor公司,美国)室温孵育1 h,TBST洗涤3次,每次10 min。用Odyssey双色红外激光扫描显影仪(Li-Cor公司,美国)扫描荧光蛋白条带,用Odyssey系统软件进行结果分析,通过目的蛋白条带灰度值与内参GAPDH条带灰度值的比值表示目的蛋白的表达水平。
1.7 统计学处理采用SPSS 19.0统计学软件进行分析,计量资料以均数±标准差(x±s)表示,两组比较采用t检验,组间比较采用单因素方差分析,P < 0.05为差异有统计学意义。
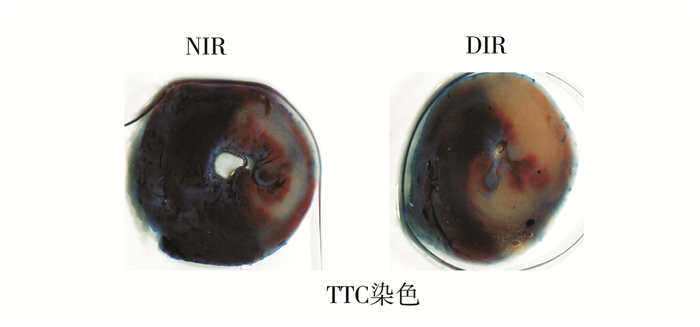
2 结果 2.1 心肌梗死面积与假手术组比较,缺血再灌注组心肌梗死面积百分比明显增大(P < 0.05);与正常心肌缺血再灌注组相比,糖尿病心肌缺血再灌注组心肌梗死面积百分比增加(P < 0.05),见图 1、表 1。
|
图 1 NIR组和DIR组大鼠心脏TTC染色 伊文斯蓝和TTC染色,正常心肌呈蓝色,缺血心肌呈砖红色,梗死心肌呈灰白色 |
| 表 1 各组大鼠心肌缺血面积百分比和心肌梗死面积百分比的比较(%,n=6,x±s) |
与假手术组比较,缺血再灌注组血清CK-MB和LDH的活性升高(P < 0.05);与正常心肌缺血再灌注组相比,糖尿病心肌缺血再灌注组血清CK-MB和LDH的活性升高(P < 0.05),见表 2。
| 表 2 各组大鼠血清CK-MB和LDH活性的比较(U/L, n=6,x±s) |
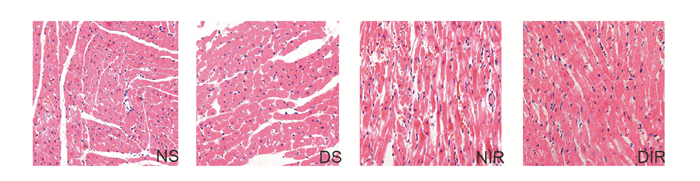
显微镜下HE病理结果,NS组心肌纤维排列整齐,心肌细胞无肿胀,横纹清楚;DS组心肌纤维排列稍紊乱,有部分溶解断裂,间质纤维化;NIR组心肌纤维增生、水肿,灶状坏死、断裂,心肌间质充血水肿伴大量炎性细胞浸润;DIR组心损伤较NIR更加严重,见图 2。
|
图 2 光镜下大鼠心脏组织病理改变(HE×200) NS:正常假手术组;DS:糖尿病假手术组;NIR:正常缺血再灌注组;DIR:糖尿病缺血再灌注组 |
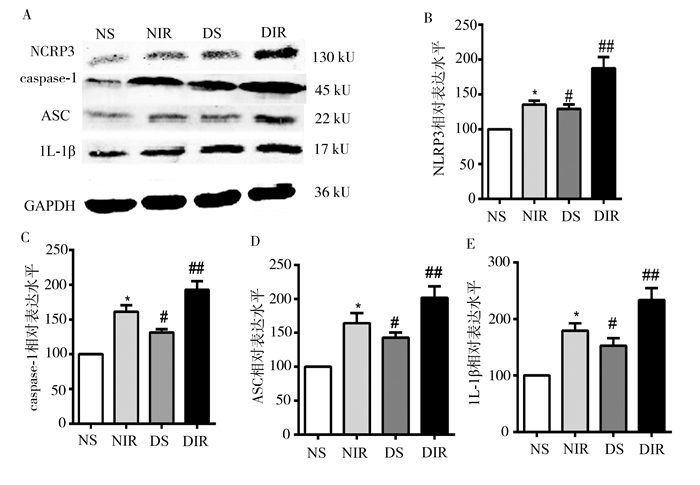
与正常大鼠相比,糖尿病大鼠心肌组织NLRP3、caspase-1、ASC和IL-1β蛋白表达增加(P < 0.05);相比于假手术组,心肌缺血再灌注大鼠心肌组织NLRP3、caspase-1、ASC和IL-1β蛋白表达增加(P < 0.05);且糖尿病大鼠心肌缺血再灌注时,心肌组织NLRP3、caspase-1、ASC和IL-1β蛋白表达比非糖尿病大鼠缺血再灌注时增加(P < 0.05);结果见图 3。
|
图 3 各组大鼠心肌组织NLRP3、caspase-1、ASC和IL-1β蛋白表达水平的比较(n=8,x±s) 与NS组比较,*P < 0.05,#P < 0.05;与DS组比较,##P < 0.05;与NIR组比较,##P < 0.05 |
本研究采用腹腔注射链脲佐菌素制备大鼠糖尿病模型,成功制备大鼠糖尿病模型后,普饲8周,确保糖尿病心肌病变形成,此阶段糖尿病心肌病变明显,对心肌缺血再灌注更加敏感[7]。采用结扎LAD法制备心肌I/R损伤模型。结果表明,与假手术组比较,非糖尿病大鼠和糖尿病大鼠心肌I/R后缺血和梗死面积明显增加,血清CK-MB和LDH的活性升高;光镜下心肌纤维增生水肿,灶状坏死,断裂,间质充血水肿伴大量炎性细胞浸润,证明成功制备了大鼠心肌缺血再灌注损伤模型。
研究证明,细胞焦亡主要的特点是由caspase-1受胞内多蛋白复合物炎性小体的调控而活化介导的。炎性小体通常是含NACHT (nucleotide binding oligomerization domain)、LRR (leucine rich repeat)和PYD (pyrin domain)结构域的蛋白、凋亡相关斑点样蛋白(ASC)和caspase-1前体所构成的多蛋白复合物。细胞在外源性相关病原体分子模式(PAMP)和内源性危险相关的分子模式(DAMPS)作用下,通过不同信号途径作用于炎性小体,NLRs暴露出效应结构域,通过CARD-CARD或PYD-PYD同型相互作用,间接或直接通过ASC募集、激活caspase-1,作用于下游因子IL-1β、IL-18前体裂解及释放,介导细胞渗透性肿胀破裂,形成细胞膜小孔,胞内物质(如乳酸脱氢酶LDH等)流出,并诱导其他炎性因子、黏附分子等的合成和释放,放大局部和全身炎症反应,导致细胞促炎程序性死亡-细胞焦亡[8]。NOD样受体(NLRP1,NLRP3,NLRC4,NLRC5),PYRIN和AIM2是炎性小体家族的主要成员,在炎症反应发生和维持中起重要作用。NLRP3炎性小体是目前研究最广泛的NOD样受体,NLRP3炎性识别非微生物危险信号,非生物危险信号如过量的ATP、葡萄糖、活性氧(ROS)、胆固醇和结晶可以激活NLRP3,NLRP3在各种疾病条件下识别非微生物危险信号并导致的非细菌性炎性反应。研究证实,NLRP3在糖尿病心肌病、心肌梗死和心肌缺血再灌注损伤中起重要作用[9, 10]。
本研究结果表明,糖尿病大鼠相比于非糖尿病大鼠,心肌发生病理改变,且NLRP3、caspase-1、ASC、IL-1β蛋白表达增加,提示糖尿病状态下,NLRP3活性增加,通过与ASC形成炎性小体激活caspase-1,caspase-1作用于下游细胞因子IL-1β诱导炎症反应,诱导心肌细胞焦亡发生,导致糖尿病心肌病理损伤。本研究结果显示,I/R显著增加了糖尿病和非糖尿病心肌缺血和梗死面积,并增加CK-MB、LDH活性,提示心肌缺血再灌注损伤;NLRP3、caspase-1、ASC和IL-1β蛋白表达都明显增加,提示在心肌缺血再灌注时,氧化应激等刺激因素激活NLRP3炎性体,通过作用于caspase-1,介导心肌细胞焦亡,诱发并加重心肌缺血再灌注损伤。与NIR组比较,DIR组心肌梗死面积增加、CK-MB和LDH活性增加,表明糖尿病相比于非糖尿病大鼠心肌缺血再灌注损伤加重;DIR组的NLRP3、caspase-1、ASC和IL-1β蛋白增加显著,提示糖尿病状态下心肌缺血再灌注时,内源性和外源性损伤刺激通过激活NLRP3炎性小体相关通路作用于caspase-1,介导心肌细胞焦亡,诱发和加重心肌细胞再灌注损伤。
综上所述,本研究结果说明细胞焦亡与糖尿病大鼠心肌病有重要关系,在糖尿病心肌缺血再灌注时,氧化应激等刺激通过NLRP3和ASC炎性小体激活caspase-1信号通路诱导细胞焦亡,使糖尿病心肌对缺血再灌注更加敏感、心肌缺血再灌注损伤加重,在缺血再灌注损伤中起重要作用。通过进一步对糖尿病心肌缺血再灌注损伤的细胞焦亡信号通路的研究,探究细胞焦亡的具体作用机制可以为防治糖尿病心肌缺血再灌注损伤提供新方向和领域。
| [1] | Keller PF, Carballo D, Roffi M. Diabetes and acute coronary syndrome[J]. Minerva Med, 2010, 101(2): 81-104. |
| [2] | Liu Y, Yang H, Liu LX, et al. NOD2 contributes to myocardial ischemia/reperfusion injury by regulating cardiomyocyte apoptosis and inflammation[J]. Life Sci, 2016, 149: 10-17. DOI: 10.1016/j.lfs.2016.02.039. |
| [3] | Doitsh G, Galloway NL, Geng X, et al. Cell death by pyroptosis drives CD4 T-cell depletion in HIV-1 infection[J]. Nature, 2014, 505(7484): 509-514. |
| [4] | Li X, Du N, Zhang Q, et al. MicroRNA-30d regulates cardiomyocyte pyroptosis by directly targeting foxo3a in diabetic cardiomyopathy[J]. Cell Death Dis, 2014, 5: e1479. DOI: 10.1038/cddis.2014.430. |
| [5] | Luo B, Li B, Wang W, et al. NLRP3 Gene Silencing Ameliorates Diabetic Cardiomyopathy in a Type 2 Diabetes Rat Model[J]. PLoS One, 2014, 9(8): e104771. DOI: 10.1371/journal.pone.0104771. |
| [6] | Yang JR, Yao FH, Zhang JG, et al. Ischemia-reperfusion induces renal tubule pyroptosis via the CHOP-caspase-11 pathway[J]. Am J Physiol Renal Physiol, 2014, 306(1): F75-F84. DOI: 10.1152/ajprenal.00117.2013. |
| [7] | Li H, Liu Z, Wang J, et al. Susceptibility to myocardial ischemia reperfusion injury at early stage of type 1 diabetes in rats[J]. Cardiovasc Diabetol, 2013, 12: 133. DOI: 10.1186/1475-2840-12-133. |
| [8] | Byrne BG, Dubuisson JF, Joshi AD, et al. Inflammasome components coordinate autophagy and pyroptosis as macrophage responses to infection[J]. M Bio, 2013, 4(1): e00620. |
| [9] | Sandanger ∅, Ranheim T, Vinge LE, et al. The NLRP3 inflammasome is up-regulated in cardiac fibroblasts and mediates myocardial ischaemia-reperfusion injury[J]. Cardiovasc Res, 2013, 99(1): 164-174. DOI: 10.1093/cvr/cvt091. |
| [10] | Takahashi M. NLRP3 inflammasome as a novel player in myocardial infarction[J]. Int Heart J, 2014, 55(2): 101-105. DOI: 10.1536/ihj.13-388. |
 2017, Vol. 38
2017, Vol. 38

 ,
,