文章信息
- 刘威, 张艳, 朱剑军
- Liu Wei, Zhang Yan, Zhu Jianjun
- STYK1激活Akt信号通路促进肺癌细胞增殖
- STYK1 promotes proliferation of lung carcinoma cells via activating Akt signal
- 实用肿瘤杂志, 2020, 35(2): 134-139
- Journal of Practical Oncology, 2020, 35(2): 134-139
基金项目
- 山西医科大学校级博士基金项目(XD1808);山西医科大学省级博士基金项目(SD1808)
-
作者简介
- 刘威(1986-), 男, 河南驻马店人, 主治医师, 从事胸部肿瘤的基础和临床研究.
-
通信作者
- 朱剑军, E-mail: scdx007@163.com
-
文章历史
- 收稿日期:2019-04-24
2. 郑州大学附属洛阳中心医院病理科, 河南 洛阳 471009;
3. 山西医科大学基础医学院, 山西 太原 030001
2. Department of Pathology, Luoyang Central Hospital Affiliated to Zhengzhou University, Luoyang 471009, China;
3. Basic Medical College, Shanxi Medical University, Taiyuan 030001, China
肺癌是发病率和病死率最高的恶性肿瘤。2018年,全世界新增肺癌病例约210万例,死亡病例约176万例[1-2]。因此,鉴定与肺癌发生和进展相关的癌基因或抑癌基因并研究其主要作用能够为全面阐明肺癌发生与进展的病理机制提供线索与帮助[1-2]。酪氨酸蛋白激酶1 (tyrosine-protein kinase 1, STYK1)的GeneBank登录号为NM- 018423,定位于12q13.2,基因全长3 022 bp, 编码422个氨基酸。属于受体型酪氨酸蛋白激酶家族(receptor protein tyrosine kinase, RPTK)[3-4]。RPTK在肿瘤细胞的恶性增殖、凋亡抵抗、转移侵袭及分化等过程中发挥着重要作用[4]。STYK1在前列腺癌、卵巢癌和结直肠癌等多种恶性肿瘤中呈高表达[5-8]。本研究收集肺癌组织和对照癌旁组织检测STYK1在肺癌中的表达情况,分析其表达水平与肺癌患者临床病理特征间的关系;检测STYK1对肺癌细胞的影响,初步探讨STYK1促进肺癌发生和发展的分子机制,从而为肺癌的早期诊断及预后评估提供理论基础。
1 资料与方法 1.1 一般资料收集2015年1月至2016年10月在郑州大学附属洛阳中心医院收治的35例肺癌患者。35例患者均经病理诊断为肺癌,无其他第二原发肿瘤。患者年龄33 ~ 67岁,中位年龄51岁;其中男性26例,女性9例;TNM分期,Ⅰ期4例,Ⅱ期13例,Ⅲ期15例,Ⅳ期3例;高分化5例,中分化18例,低分化12例。癌组织和癌旁组织保存于液氮中。所有标本均取得患者及家属同意并签署知情同意书。
1.2 试剂及细胞株肺癌细胞A549和HCC827来自中国科学院细胞库。Trizol试剂和转染试剂购自美国Invitrogen公司。cDNA合成试剂盒及定量PCR试剂盒购自日本Takara公司。CCK-8试剂购自上海碧云天公司。AnnexinV-FITC/PI双染细胞凋亡试剂盒购自上海贝博公司。STYK-1、Akt、p-Akt、Bcl-2和Bcl-xL抗体购自英国Abcam公司。β-actin和二抗购自武汉三鹰公司。
1.3 实验方法 1.3.1 细胞培养用含10%胎牛血清的F12K培养液于37℃ 5% CO2细胞培养箱中培养肺癌细胞A549和HCC827。
1.3.2 siRNA片段转染取适量细胞接种于6孔板,24 h后弃培养液,加入1.5 mL无血清培养液。取5 μL转染试剂加入250 μL无血清培养液,混匀,静置5 min;取5 μL siRNA片段加入250 μL无血清培养液,混匀;将上述2种液体混匀,静置20 min后加入细胞培养液中。转染6 h后,弃转染液,加入2 mL含血清的培养液。siRNA序列由上海吉玛制药技术有限公司合成。siRNA-1:正义链5’-UCCUGGAAUGCAGUCUCAGdTdT-3’;反义链3’-dTdTAGGACCUUACGUCAGAGUC-5’。siRNA-2:正义链5’-GGAAAACUUUCUGGGAGCUdTdT-3’;反义链3’-dTdTCCUUUUGAAAGACCCUCGA-5’。siRNA-3:正义链5’-UGGUGCAGCUGGAAGGCUGdTdT-3’;反义链3’-dTdTACCACGUCGACCUUCCGAC-5’。阴性对照序列由上海吉玛制药技术有限公司提供。
1.3.3 定量PCR实验按照Trizol试剂说明书步骤提取细胞总RNA。按照cDNA合成试剂盒说明书步骤对总RNA进行反转录得cDNA。运用SYBR Green染料扩增目的基因。引物由上海生工合成,引物序列见表 1。β-actin为内参照基因。采用2-△△Ct方法计算目的基因相对表达量。
| 基因 | 正向引物 | 方向引物 |
| STYK1 | 5’-CCGTATCCTGAAGTCCCTCC-3’ | 5’-GCCTCGTCATCTGCAGTTTT-3’ |
| Bcl-2 | 5’-GCCTTCTTTGAGTTCGGTGG-3’ | 5’-GAAATCAAACAGAGGCCGCA-3 |
| Bcl-xL | 5’-AAGAGAACAGGACTGAGGCC-3 | 5’-TTGCTTTACTGCTGCCATGG-3’ |
| β-actin | 5’-ACTCTTCCAGCCTTCCTTCC-3’ | 5’-TCTCCTTCTGCATCCTGTCG-3’ |
| 注 STYK1:酪氨酸蛋白激酶1 (tyrosine-protein kinase 1) | ||
用细胞裂解液裂解细胞,获细胞总蛋白,加入适量5×SDS-PAGE还原型缓冲液,煮沸,变性。经SDS-PAGE垂直电泳分离总蛋白,转膜,封闭,一抗孵育(4℃过夜),HBSS冲洗,二抗常温孵育2 h。HBSS冲洗后,将PVDF膜置于收集器内,发光,拍照。β-actin为内参照。用Quantity One软件对条带进行灰度值分析。
1.3.5 CCK-8法检测细胞增殖取适量肺癌细胞接种于96孔板。后续根据实验需要,分别在转染后1、2、3和4 d时加入CCK-8试剂。避光孵育1 h后,采用酶标仪在450 nm处检测吸光度(absorbance, A)值。每组设6个复孔。
1.3.6 Annexin V-FITC/PI法检测细胞凋亡取适量肺癌细胞接种于6孔板。经转染后,常规收集细胞。用预冷的PBS缓冲液冲洗细胞2次,加入400 μL结合缓冲液,重悬细胞。于避光条件下,加入10 μL Annexin V-FITC染料,4℃孵育10 min。加入5 μL PI染料,4℃避光孵育10 min,上机检测。每组设3个复孔。
1.4 统计学分析采用SPSS 16.0软件分析。计量资料采用均数±标准差(x±s)表示。多组数据分析采用单因素方差检验,两组间比较采用t检验。以P < 0.05为差异具有统计学意义。
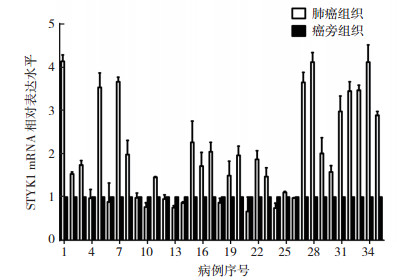
2 结果 2.1 STYK1在肺癌组织中呈高表达定量PCR结果显示,STYK1在肺癌组织中的表达水平高于癌旁组织(P < 0.01,图 1)。STYK1在晚期肺癌(Ⅲ期和Ⅳ期)组织中的表达水平高于早期肺癌(I期和Ⅱ期)组织(P < 0.01,表 2)。STYK1基因表达水平在肺癌患者年龄、性别和肺癌分化程度方面比较,差异均无统计学意义(均P>0.05)。
|
| 图 1 肺癌及癌旁组织中STYK1 mRNA水平检测 Fig.1 The mRNA level of STYK1 in lung cancer and paracancer tissues |
| 临床病理特征 | 例数(%) | STYK1 mRNA相对表达水平(x±s) | P值 |
| 性别 | 0.981 | ||
| 男性 | 26(74.3) | 1.598 ±0.313 | |
| 女性 | 9(25.7) | 1.589 ±0.207 | |
| 年龄 | 0.283 | ||
| < 60岁 | 24(68.6) | 1.753±0.276 | |
| ≥60岁 | 11(31.4) | 1.339±0.169 | |
| TNM分期 | 0.002 | ||
| Ⅰ期+ Ⅱ期 | 17(48.6) | 1.111 ± 0.174 | |
| Ⅲ期+ Ⅳ期 | 18(51.4) | 2.344 ± 0.226 | |
| 分化程度 | 0.404 | ||
| 高分化 | 5(14.3) | 1.142 ± 0.206 | |
| 中分化 | 18(51.4) | 1.687 ± 0.296 | |
| 低分化 | 12(34.3) | 1.808 ± 0.355 | |
| 注 STYK1:酪氨酸蛋白激酶1 (tyrosine-protein kinase 1) | |||
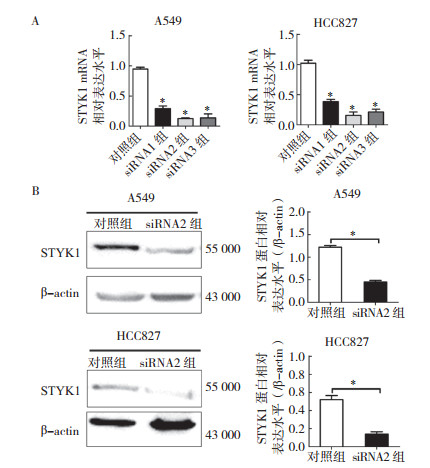
为研究STYK1在肺癌发展过程中的作用,合成3对靶向沉默STYK1基因的siRNA片段。结果发现,siRNA2对STYK1 mRNA的沉默效果最佳。在A549细胞中,其沉默效率高达(87.2±8.1)%;在HCC827细胞中,其沉默效率达(84.2±10.2)%(图 2A)。通过Western blot检测siRNA2对STYK1蛋白的沉默效果发现,siRNA2能够有效沉默STYK1蛋白表达水平。在A549细胞中,其沉默效率高达(73.0±2.6)%;在HCC827细胞中,其沉默效率高达(72.5±12.1)%(图 2B)。因此,后续实验采用siRNA2片段。
|
| 注 A:定量PCR检测STYK1基因表达水平;B:Western blot检测STYK1蛋白表达水平;STYK1:酪氨酸蛋白激酶1 (tyrosineprotein kinase 1);*P < 0.01 图 2 肺癌A549和HCC827细胞转染siRNA沉默STYK1表达 Fig.2 Knockdown of STYK1 by siRNA in lung cancer A549 and HCC827 cells |
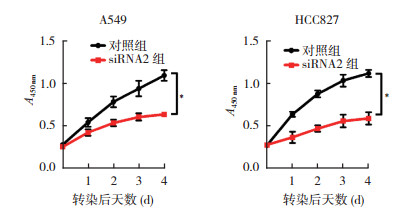
采用CCK-8法检测沉默STYK1对肺癌细胞增殖的影响。结果发现,沉默STYK1能够抑制肺癌细胞的增殖。在A549细胞中,siRNA片段转染4 d后,siRNA2组与对照组比较,增殖抑制率高达(41.6±2.5)%,差异具有统计学意义(P < 0.01,图 3)。在HCC827细胞中,siRNA2组细胞与对照组比较,增殖抑制率高达(46.7±3.7)%,差异具有统计学意义(P < 0.01,图 3)。
|
| 注 *P < 0.01 图 3 沉默STYK1抑制肺癌A549和HCC827细胞增殖 Fig.3 Knockdown of STYK1 inhibits the proliferation of lung cancer A549 and HCC827 cells |
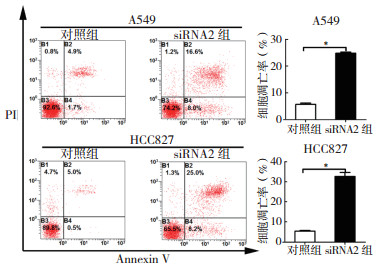
采用流式细胞术检测沉默STYK1对肺癌细胞凋亡的影响。结果发现,沉默STYK1基因能够促进肺癌细胞凋亡。在A549细胞中,与对照组比较,沉默STYK1后细胞凋亡率升高[(5.7±0.9)% vs(24.8±0.8)%, P < 0.01;图 4)]。在HCC827细胞中,与对照组比较,沉默STYK1后细胞凋亡率升高[(5.5±0.6)% vs(32.8±3.5)%, P < 0.01; 图 4)]。
|
| 注 *P < 0.01 图 4 沉默STYK1促进肺癌A549和HCC827细胞凋亡 Fig.4 Knockdown of SYTK1 promotes the apoptosis of lung cancer A549 and HCC827 cells |
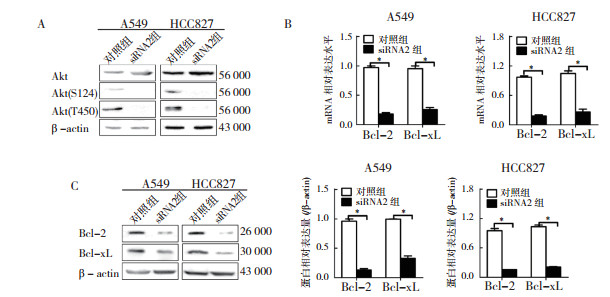
初步研究STYK1促进肺癌细胞增殖的作用机制发现,沉默STYK1后,Akt(S120)和Akt(T450)的磷酸化水平均降低,Bcl-2和Bcl-xL mRNA表达水平降低(图 5A~5B)。在A549细胞中,沉默STYK1后Bcl-2和Bcl-xL mRNA表达水平下降(81.4±2.5)%和(72.8±7.2)%。在HCC827细胞中,沉默STYK1后Bcl-2和Bcl-xL mRNA表达水平下降(81.3±2.9)%和(74.7±9.6)%。沉默STYK1后,Bcl-2和Bcl-xL蛋白水平均下调(图 5C)。在A549细胞中,沉默STYK1后,Bcl-2和Bcl-xL蛋白水平下降(86.5±4.4)%和(66.8±6.1)%。在HCC827细胞中,沉默STYK1后,Bcl-2和Bcl-xL蛋白水平下降(83.3±1.3)%和(79.4±2.1)%。
|
| 注A:沉默STYK1抑制Akt磷酸化;B:沉默STYK1抑制Bcl-2和Bcl-xL mRNA表达;C:沉默STYK1抑制Bcl-2和Bcl-xL蛋白表达;STYK1:酪氨酸蛋白激酶1 (tyrosine-protein kinase 1);*P < 0.01 图 5 STYK1激活Akt信号通路并促进Bcl-2和Bcl-xL基因表达 Fig.5 STYK1 upregulates the expression of Bcl-2 and Bcl-xL via activating Akt signal pathway |
肺癌是发病率和病死率最高的恶性肿瘤[1]。近年来,肺癌的诊断与治疗取得很大的进步,但是肺癌患者5年生存率仍较低,究其原因可能与患者首次就诊时肺癌已发展为中晚期有关[1, 9-11]。因此,筛选与肺癌早期发病相关的癌基因或抑癌基因,对于肺癌临床早期发现、早期诊断与早期治疗有着至关重要的作用[1]。STYK1编码产物为酪氨酸激酶受体蛋白,归属于酪氨酸激酶受体复合物家族。本研究表明,STYK1在肺癌组织中的表达水平高于癌旁组织,在晚期肺癌组织中的表达水平高于早期肺癌组织,提示STYK1表达水平与肺癌的恶性进展有关。研究显示,STYK1在肺癌组织中的阳性表达率为75.4%,高于癌旁组织的14.1%[12]。以上通过不同的检测方法均发现,STYK1在肺癌中呈高表达,STYK1是一个潜在的肺癌诊断标志物。
本研究表明,沉默STYK1基因抑制肺癌细胞的增殖,促进肺癌细胞凋亡。研究表明,沉默STYK1基因抑制胰腺癌细胞增殖,促进胰腺癌细胞凋亡,促进胰腺癌细胞转移[13]。在肝癌细胞中,降低STYK1表达水平后,肝癌细胞增殖、肝癌细胞迁移和侵袭活性减弱[14]。敲除STYK1抑制胆管癌的发生和发展[15]。敲除STYK1抑制鼻咽癌细胞增殖、迁移和侵袭活性[16]。以上研究均表明,STYK1可能通过促进细胞增殖和抑制细胞凋亡促进恶性肿瘤的发生和发展。
在乳腺癌细胞中STYK1能够促进Akt磷酸化,进而导致糖基合成酶激酶3β (glycoge synthase kinase 3β, GSK-3β)发生磷酸化[17]。STYK1通过抑制E-cadherin表达,促进上皮间质转换,促进p38磷酸化,促进胰腺癌的发生和发展[13]。在胆囊癌和鼻咽癌细胞中,STYK1通过激活PI3K/Akt信号通路促进肿瘤细胞增殖和恶性转化[16, 18]。以上研究均表明,STYK1促进恶性肿瘤的发生和发展可能与激活Akt信号通路有关。本研究发现,STYK1通过促进Akt磷酸化、激活Akt信号通路及诱导抗凋亡蛋白Bcl-2和Bcl-xL转录激活,导致肺癌细胞产生凋亡抵抗。
总之,本研究发现,STYK1在肺癌组织中表达水平升高。沉默STYK1基因能够抑制肺癌细胞增殖,促进细胞凋亡。其机制可能是通过激活Akt信号通路,导致肺癌细胞对凋亡产生抵抗,最终促进肺癌的恶性进展。
| [1] |
Bray F, Ferlay J, Soerjomataram I, et al. Global cancer statistics 2018:GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J]. CA Cancer J Clin, 2018, 68(6): 394-424. |
| [2] |
毕良文, 张丽珍, 赵滑峰, 等. 转移性Ⅳ期非小细胞肺癌患者的生存状况及预后分析[J]. 实用肿瘤杂志, 2018, 33(5): 36-40. |
| [3] |
Ye X, Ji C, Huang Q, et al. Isolation and characterization of a human putative receptor protein kinase cDNA STYK1[J]. Mol Biol Rep, 2003, 30(2): 91-96. |
| [4] |
García Echeverría C, Fabbro D. Therapeutically targeted anticancer agents:inhibitors of receptor tyrosine kinases[J]. Mini Rev Med Chem, 2004, 4(3): 273-283. |
| [5] |
Chung S, Tamura K, Furihata M, et al. Overexpression of the potential kinase serine/threonine/tyrosine kinase 1(STYK 1) in castration-resistant prostate cancer[J]. Cancer Sci, 2010, 100(11): 2109-2114. |
| [6] |
Jackson KA, Oprea G, Handy J, et al. Aberrant STYK1 expression in ovarian cancer tissues and cell lines[J]. J Ovarian Res, 2009, 2(1): 15. |
| [7] |
Orang AV, Safaralizadeh R, Hosseinpour Feizi MA, et al. Diagnostic relevance of overexpressed serine threonine tyrosine kinase/novel oncogene with kinase domain (STYK1/NOK) mRNA in colorectal cancer[J]. Asian Pac J Cancer Prev, 2014, 15(16): 6685-6689. |
| [8] |
Hu L, Chen HY, Cai J, et al. Serine threonine tyrosine kinase 1 is a potential prognostic marker in colorectal cancer[J]. BMC Cancer, 2015, 15(1): 246. |
| [9] |
曹强, 杨扬, 许瑞彬, 等. WT1基因在NSCLC中的表达及其临床意义[J]. 实用肿瘤杂志, 2019, 34(1): 23-26. |
| [10] |
张海华, 张涛. 早期非小细胞肺癌亚肺叶切除临床研究进展[J]. 实用肿瘤杂志, 2019, 34(3): 198-201. |
| [11] |
凌发昱, 喻东亮. 局部晚期肺癌扩大切除的外科治疗现状[J]. 实用肿瘤杂志, 2018, 33(5): 476-479. |
| [12] |
Chen P, Li WM, Lu Q, et al. Clinicopathologic features and prognostic implications:of NOK/STYK1 protein expression in non-small cell lung cancer[J]. BMC Cancer, 2014, 14(1): 1-7. |
| [13] |
Chen L, Ma C, Bian Y, et al. Aberrant expression of STYK1 and E-cadherin confer a poor prognosis for pancreatic cancer patients[J]. Oncotarget, 2017, 8(67): 111333-111345. |
| [14] |
Wang Z, Qu L, Deng B, et al. STYK1 promotes epithelial-mesenchymal transition and tumor metastasis in human hepatocellular carcinoma through MEK/ERK and PI3K/AKT signaling[J]. Sci Rep, 2016, 2016(6): 33205. |
| [15] |
Chen MY, Zhang H, Jiang JX, et al. Depletion of STYK1 inhibits intrahepatic cholangiocarcinoma development both in vitro and in vivo[J]. Tumour Biol, 2016, 37(10): 1-9. |
| [16] |
Zhao Y, Yang L, He J, et al. STYK1 promotes Warburg effect through PI3K/AKT signaling and predicts a poor prognosis in nasopharyngeal carcinoma[J]. Tumour Biol, 2017, 39(7): 1010428317711644. |
| [17] |
Li J, Wu F, Sheng F, et al. NOK/STYK1 interacts with GSK-3β and mediates Ser9 phosphorylation through activated Akt[J]. FEBS Lett, 2012, 586(21): 3787-3792. |
| [18] |
Hu YP, Wu ZB, Jiang L, et al. STYK1 promotes cancer cell proliferation and malignant transformation by activating PI3K-AKT pathway in gallbladder carcinoma[J]. Int J Biochem Cell Biol, 2018, 97: 16-27. |
 2020, Vol. 35
2020, Vol. 35


