文章信息
- 杨清, 杨海松, 张世泳, 张萌萌, 朱文龙, 邸广升, 杨森果, 张苗
- Yang Qing, Yang Haisong, Zhang Shiyong, Zhang Mengmeng, Zhu Wenlong, Di Guangsheng, Yang Senguo, Zhang Miao
- miRNA-27a在人乳腺癌MCF-7/ADR细胞株中的表达及其对细胞耐药的影响
- Expression of miRNA-27a in human breast cancer MCF-7/ADR cell line and its effect on cell resistance
- 实用肿瘤杂志, 2021, 36(1): 28-32
- Journal of Practical Oncology, 2021, 36(1): 28-32
基金项目
- 贵州省科技厅联合基金资助项目[黔科合LH字(2017)7182号];贵阳市科技局基金资助项目[筑科合同(2018)1-89]
-
通信作者
- 杨海松,E-mail: yanghaisong609@sina.com
-
文章历史
- 收稿日期:2020-09-16
2. 黔东南州人民医院甲乳外科,贵州 凯里 556000
2. Thyroid and Breast Surgery, Qiandongnan People's Hospital, Kaili 556000, China
中国女性恶性肿瘤中乳腺癌发病率居前列。由于乳腺癌在发病早期即可发生转移,乳腺癌已发展成导致许多女性早期死亡的恶性肿瘤[1]。尽管乳腺癌的综合治疗已经有了很大的进步,但乳腺癌的化疗耐药仍然是很多早期治疗失败的原因之一[2]。其中肿瘤药物的多药耐药(multidrug resistance,MDR)机制是导致肿瘤耐药的主要原因[3]。
microRNAs(miRNAs)是内源性非编码RNA(non-coding RNA,ncRNA),含有20~23个核苷酸,介导基因转录后调节,参与几乎所有的生物学过程,包括细胞增殖、凋亡、分化、应激反应和细胞周期调控等[4-6]。miRNA-27a可以调节肿瘤细胞的生长、增殖、迁移、侵袭和血管生成[7-8]。调控miRNA-27a的表达可以影响三阴性乳腺癌中多药耐药蛋白转运体P-glycoprotein(P-gp)的表达[9]。P-gp是一种ATP性依赖细胞膜蛋白,主要作用是泵出细胞内的药物。该蛋白的高表达导致细胞外排药物的能力增强,药物作用浓度降低,最终降低药物对细胞的杀伤作用[10]。在已耐药的乳腺癌细胞MCF-7/Adriamycin(MCF-7/ADR)中miRNA-27a和P-gp的联系尚未有研究。本研究主要探究miRNA-27a在人类乳腺癌耐药和非耐药细胞中的表达水平及上调miRNA-27a后P-gp蛋白和mRNA表达水平的变化,为乳腺癌临床诊疗提供理论基础及潜在的分子靶点。
1 材料与方法 1.1 材料人乳腺癌多柔比星耐药细胞株MCF7/ADR购自上海美轩生物科技有限公司;人乳腺癌细胞株MCF-7受赠于贵州医科大学附属医院临床研究中心周定安博士;miRNA-27a模拟物(mimics)购自中国上海吉玛制药技术有限公司;miRNA-27a和P-gp引物购自上海吉玛制药技术有限公司;RPMI 1640和DMEM培养液以及澳洲胎牛血清购自美国GIBCO公司;RNA提取试剂盒购自南京诺唯赞生物科技有限公司;反转录试剂盒和Real-time PCR(RT-PCR)试剂盒购自日本TaKaRa公司,P-gp抗体购自美国Abcam公司;内参抗体购自杭州贤至生物科技有限公司;山羊抗兔二抗购自北京普美生物;细胞/组织快速裂解液购自北京索莱宝科技有限公司;SDS-PAGE蛋白上样缓冲液、一抗稀释液、二抗稀释液和封闭液购自上海碧云天生物技术公司;彩虹245广谱蛋白marker购自北京索莱宝科技有限公司;lipofectamine 3000购自美国赛默飞公司。
1.2 实验方法 1.2.1 细胞培养人乳腺癌细胞株MCF-7用含10%胎牛血清和1%双抗的DMEM培养液培养;耐药细胞株MCF-7/ADR用含10%胎牛血清、1%双抗和1 000 ng/mL多柔比星的PRMI 1640培养液,置于37℃5%CO2培养箱中培养,根据细胞生长情况,隔天换液,3~4 d传代。
1.2.2 RT-PCR检测细胞中miRNA-27a和P-gp mRNA表达水平分别收集MCF-7细胞和MCF-7/ADR细胞,用MiPure Cell/Tissue miRNA Kit提取细胞总RNA,测量RNA浓度,去除DNA,反转录成cDNA(操作按TaKaRa试剂盒说明书进行,miRNA-27a cDNA合成过程中采用miRNA-27a RT特异性颈环引物构建反转录体系),反应条件为:37℃ 15 min,85℃ 5 s,4℃无限循环。以cDNA为模板,利用P-gp和miRNA-27a特异性引物分别进行PCR扩增。PCR反应条件为:95℃30 s,95℃5 s,60℃34 s,共40个循环。P-gp和miRNA-27a相对表达量采用2-ΔΔct方法进行计算。
1.2.3 Western blot检测细胞中P-gp蛋白表达水平收集MCF-7细胞和MCF-7/ADR细胞,加入RIPA裂解液(含蛋白酶抑制剂),待细胞在冰上充分裂解(约3~5 min)后,将裂解液移至1.5 mL离心管中,10 000 r/min 4℃离心5 min。吸取上清液装于1.5 mL离心管中,BCA试剂盒检测其蛋白浓度。备8%SDS-PAGE,SDS-PAGE电泳:80 V跑浓缩胶60 min;120 V跑分离胶120 min,转膜:120V 150 min,封闭60 min,敷一抗4℃过夜,二抗室温孵育1 h,ECL发光显影;ImageJ软件分析条带灰度值。
1.2.4 细胞转染接种MCF-7/ADR细胞于6孔板内,密度为10×104个/孔,培养液不加抗生素,待细胞生长至70%融合度时,按照lipofectamine 3000说明书转染miRNA-27a模拟物和阴性对照,48 h后提取RNA进行RT-PCR实验,72 h收集蛋白进行Western blot实验。
1.2.5 细胞划痕实验接种MCF-7/ADR细胞于6孔板,密度为60×104个/孔,置于37℃ 5%CO2培养箱中。次日用200 μL型的枪头紧贴直尺板垂直于背后的1条横线划痕。PBS轻柔洗涤细胞3次,洗去所有悬浮细胞,转染miRNA-27a模拟物和阴性对照,加入无血清且无双抗的培养液2 mL。置于37℃5%CO2培养箱培养。0、24、48和72 h拍照观察,ImageJ软件分析划痕距离。
1.3 统计学分析所有实验重复3次,应用GraphPad Prism 7.0进行数据分析。组间比较采用t检验。以P < 0.05为差异具有统计学意义。
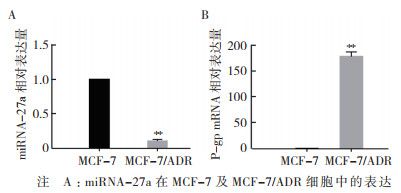
2 结果 2.1 在MCF-7和MCF-7/ADR细胞中miRNA-27a和P-gp mRNA的差异表达RT-PCR结果显示,MCF-7细胞中miRNA-27a表达量高于MCF-7/ADR细胞,而P-gp mRNA表达量低于MCF-7/ADR细胞,差异均具有统计学意义(均P < 0.05,图 1)
|
| 注 A:miRNA-27a在MCF-7及MCF-7/ADR细胞中的表达情况;B:P-gp mRNA在MCF-7及MCF-7/ADR细胞中的表达情况;** 与MCF-7细胞比较,P < 0.01 图 1 miRNA-27a及P-gp mRNA在MCF-7及MCF-7/ADR细胞中的表达情况 Fig.1 The mRNA expression levels of miRNA-27a and P-gp in MCF-7 and MCF-7 /ADR cells |
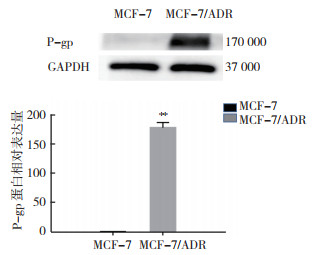
Western blot结果显示,与MCF-7细胞比较,P-gp在多柔比星耐药细胞株MCF-7/ADR中的表达量增加,差异具有统计学意义(P < 0.05,图 2)。
|
| 注 ** 与MCF-7细胞比较,P < 0.01 图 2 P-gp蛋白在MCF-7和MCF-7/ADR细胞中的表达 Fig.2 The expression of P-gp protein in MCF-7 and MCF-7/ADR cells |
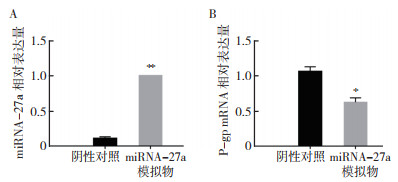
转染miRNA-27a模拟物至MCF-7/ADR细胞中,RT-PCR检测显示,与阴性对照组比较,转染miRNA-27a模拟物后miRNA-27a的表达增高(P < 0.05),而P-gp mRNA的表达降低(P < 0.05,图 3)
|
| 注 A:miRNA-27a在转染阴性对照和miRNA-27a模拟物的MCF-7/ADR细胞株中的表达情况;B:P-gp mRNA在转染阴性对照和miRNA-27a模拟物的MCF-7/ADR细胞株中的表达情况;*与阴性对照比较,P < 0.05;** 与阴性对照比较,P < 0.01 图 3 miRNA-27a及P-gp mRNA在转染miRNA-27a模拟物的MCF-7/ADR细胞株中的表达情况 Fig.3 miRNA-27a and P-gp mRNA expression levels in MCF-7/ADR cells transfected with miRNA-27a mimics |
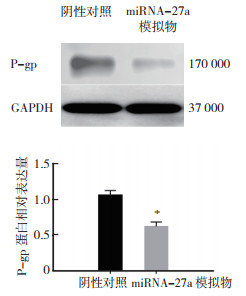
向MCF-7/ADR细胞转染miRNA-27a模拟物,RT-PCR检测转染成功,Western blot法检测转染后P-gp蛋白的表达显示,与阴性对照组比较,转染miRNA-27a模拟物后,P-gp蛋白的表达降低,差异具有统计学意义(P < 0.05,图 4)
|
| 注 *与阴性对照比较,P < 0.05 图 4 Western blot法检测MCF-7/ADR细胞转染miRNA-27a模拟物后P-gp蛋白的表达情况 Fig.4 Western blot detection of P-gp protein expression in MCF-7/ADR cells after transfection with miRNA-27a mimics |
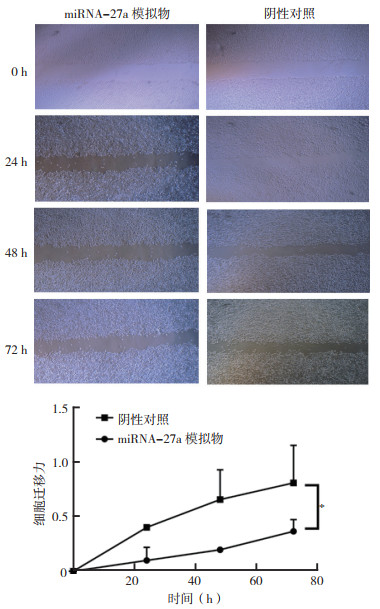
划痕实验显示,转染miRNA-27a模拟物后MCF-7/ADR细胞的迁移能力减弱(P < 0.05,图 5)
|
| 注 *P < 0.05 图 5 细胞划痕实验检测转染miRNA-27a模拟物后MCF-7/ADR细胞的迁移能力 Fig.5 Cell scratch detection of migration ability of MCF-7/ADR cells after transfection with miRNA-27a mimics |
乳腺癌若早发现、早诊断和早治疗,5年生存率可达90%以上。乳腺癌的治疗从最初的手术治疗发展到现在的全身化疗、局部放疗、内分泌治疗和靶向治疗等的精准治疗,但仍面临着复发、转移和化疗耐药的难题。目前,在MCF-7/ADR细胞中对miRNA-27a的研究尚少,其对耐药的具体作用及其机制尚不明确。miRNA-27a是miRNA-27家族的组成部分之一,有报道称miRNA-27a位于19号染色体上,在肿瘤发生和发展中发挥重要作用。在乳腺癌中,上调miRNA-27a促进乳腺癌细胞的增殖、迁移和侵袭,其机制可能是通过负调控SFRP 1来激活Wnt/β-catenin信号通路[11]。研究发现,上调miRNA-27a能够提高MCF-7细胞的增殖、侵袭和迁移能力,其机制可能与促进PCNA、MMP-2和MMP-9蛋白表达有关[12]。而在子宫颈癌中的研究发现,上调miRNA-27a能够抑制子宫颈癌细胞体外迁移和侵袭能力,其机制可能与抑制MMP-2和MMP-9表达有关[13]。因此miRNA-27a在肿瘤细胞中是起促进还是抑制作用仍无定论。同时,越来越多的证据支持miRNA-27a在调节多态性、肿瘤发生、增殖、凋亡、侵袭、迁移和血管生成中发挥重要作用[14]。
P-gp是ATP结合盒家族转运体(ATP-binding cassette transporters,ABC)家族的一员,与肿瘤的耐药密切相关[15-16]。当P-gp过表达时,肿瘤细胞将会对大量的结构与功能不同的抗肿瘤药物产生耐药[17]。抗肿瘤药物可通过诱导凋亡来杀伤肿瘤细胞,P-gp还具有抑制肿瘤细胞凋亡的作用,这说明肿瘤耐药与细胞凋亡之间存在联系[18]。
本研究显示,上调miRNA-27a后,MCF-7/ADR细胞中的P-gp的相对表达量减少,且抑制细胞的迁徙能力,证明miRNA-27a对P-gp的表达起抑制作用。这与李济馨等[13]在子宫颈癌中的研究结果一致。但本研究为体外细胞实验,后期本课题组将从动物实验方面探究上调miRNA-27a对体内乳腺癌细胞迁移和侵袭的影响及其相关的分子机制,从而为乳腺癌的靶向治疗提供科学依据。
综上所述,与MCF-7细胞比较,miRNA-27a在MCF-7/ADR细胞中呈低表达,上调miRNA-27a的表达抑制MCF-7/ADR细胞的迁移能力,提示miRNA-27a通过抑制P-gp的表达水平逆转MCF-7/ADR细胞对多柔比星的耐药性。miRNA-27a在乳腺肿瘤中是潜在的生物标志物和治疗靶点。
| [1] |
洪欢, 吴军, 阿力比亚提·艾尼. 乳腺癌新辅助化疗的疗效及影响因素分析[J]. 实用肿瘤杂志, 2020, 35(1): 42-47. |
| [2] |
Luigi S, Luca S, Michela I, et al. Inorganic phosphate prevents erk1/2 and stat3 activation and improves sensitivity to doxorubicin of MDA-MB-231 breast cancer cells[J]. Molecules, 2015, 20(9): 15910-15928. DOI:10.3390/molecules200915910 |
| [3] |
Gottesman MM, Fojo T, Bates SE. Multidrug resistance in cancer: role of ATP-dependent transporters[J]. Nat Rev Cancer, 2002, 2(1): 48-58. DOI:10.1038/nrc706 |
| [4] |
Fang Z, Du R, Edwards A, et al. The sequence structures of human microRNA molecules and their implications[J]. PLoS One, 2013, 8(1): e54275. DOI:10.1371/journal.pone.0054275 |
| [5] |
Peng H, Wang X, Zhang P, et al. miR-27a promotes cell proliferation and metastasis in renal cell carcinoma[J]. Int J Clin Exp Pathol, 2015, 8(2): 2259-2266. |
| [6] |
Zhu ED, Li N, Li BS, et al. miR-30b, down-regulated in gastric cancer, promotes apoptosis and suppresses tumor growth by targeting plasminogen activator inhibitor-1[J]. PLoS One, 2014, 9(8): e106049. DOI:10.1371/journal.pone.0106049 |
| [7] |
刘卫民, 柳学芳, 龚文端. miRNA-27a靶向SPRY2调控Wnt/β-catenin信号通路对人卵巢癌细胞增殖和侵袭能力的影响[J]. 癌症进展, 2018, 16(3): 282-285. |
| [8] |
Zhu H, Wu H, Liu X, et al. Role of microRNA miR-27a and miR-451 in the regulation of MDR1/P-glycoprotein expression in human cancer cells[J]. Biochem Pharmacol, 2008, 76(5): 582-588. DOI:10.1016/j.bcp.2008.06.007 |
| [9] |
杨海松, 张萌萌, 陈腾祥, 等. miR-27a在三阴性乳腺癌中的表达及其对细胞耐药的影响[J]. 现代肿瘤医学, 2018, 26(19): 3049-3054. DOI:10.3969/j.issn.1672-4992.2018.19.013 |
| [10] |
王作鹏, 李凯. miRNA与肿瘤耐药性及逆转耐药策略[J]. 中华小儿外科杂志, 2013, 34(2): 140-143. DOI:10.3760/cma.j.issn.0253-3006.2013.02.016 |
| [11] |
Kong LY, Xue M, Zhang QC, et al. In vivo and in vitro effects of microRNA-27a on proliferation, migration and invasion of breast cancer cells through targeting of SFRP1 gene via Wnt/β-catenin signaling pathway[J]. Oncotarget, 2017, 8(9): 15507-15519. DOI:10.18632/oncotarget.14662 |
| [12] |
蒋雪梅, 权毅. 上调miRNA-27a-3p对乳腺癌MCF-7细胞增殖、侵袭和迁移能力的影响[J]. 郑州大学学报: 医学版, 2019, 54(2): 279-282. |
| [13] |
李济馨, 谭文华. miRNA27a对子宫颈癌细胞迁移和侵袭的影响[J]. 实用肿瘤杂志, 2020, 35(3): 223-227. |
| [14] |
Li X, Xu M, Ding L, et al. MiR-27a: A novel biomarker and potential therapeutic target in tumors[J]. J Cancer, 2019, 10(12): 2836-2848. DOI:10.7150/jca.31361 |
| [15] |
Toscano-Garibay JD, Aquino-Jarquin G. Regulation exerted by miRNAs in the promoter and UTR sequences: MDR1/P-gp expression as a particular case[J]. DNA Cell Biol, 2012, 31(8): 1358-1364. DOI:10.1089/dna.2012.1703 |
| [16] |
Altenberg GA. Structure of multidrug-resistance proteins of the ATP-binding cassette (ABC) superfamily[J]. Curr Med Chem-Anti-Cancer Agents, 2004, 4(1): 53-62. DOI:10.2174/1568011043482160 |
| [17] |
Zhang X, Yashiro M, Qiu H, et al. Establishment and characterization of multidrug-resistant gastric cancer cell lines[J]. Anticancer Res, 2010, 30(3): 915-921. |
| [18] |
Zu Y, Yang Z, Tang S, et al. Effects of P-glycoprotein and its inhibitors on apoptosis in K562 cells[J]. Molecules, 2014, 19(9): 13061-13075. DOI:10.3390/molecules190913061 |
 2021, Vol. 36
2021, Vol. 36


