文章信息
- 门慧, 谈顺
- Men Hui, Tan Shun
- MARCH2在胃癌侵袭转移中的作用
- Role of MARCH2 in invasion and metastasis of gastric cancer
- 实用肿瘤杂志, 2021, 36(5): 423-428
- Journal of Practical Oncology, 2021, 36(5): 423-428
-
通信作者
- 门慧,E-mail:18987057@qq.com
-
文章历史
- 收稿日期:2021-02-04
胃癌是全世界常见的恶性肿瘤之一,发病率约11.1/10万,位居恶性肿瘤第4位,死亡率位居第3位,在东南亚国家更为常见,而在我国位居消化道恶性肿瘤死亡率之首,多数早期胃癌无明显症状,发现时多为进展期胃癌,严重影响患者生存预后[1-4]。
研究发现,泛素E3连接酶膜相关锌指蛋白2(membrane-associated RING CH 2,MARCH2)属于MARCH家族,主要定位于内质网,约含有246个氨基酸,包含1个RING结构域,可参与免疫调节、膜运输、细胞运输、DNA修复和信号转导等多种细胞活动[5-8]。MARCH2与人类免疫缺陷病毒1型(human immunodeficiency virus type 1,HIV-1)感染相关[9-10],MARCH2在肿瘤方面的研究较少,与卵巢癌[11-12]、结直肠癌[13]和胰腺癌[14]密切相关。本研究探讨MARCH2在胃癌侵袭转移中的作用[15],为胃癌临床治疗提供分子靶点依据[16]。
1 资料与方法 1.1 材料胃癌细胞株BGC823、人胚肾细胞293T和胃癌组织来自中南大学湘雅医学院附属海口医院。RPMI 1640培养液和胎牛血清来自以色列BI生物公司。0.25%胰酶来自美国Life公司。MARCH2多克隆抗体来自美国Abcam公司。β-actin单克隆抗体来自广州中杉金桥公司。SDS-PAGE凝胶配制试剂盒及蛋白浓度测定试剂盒来自美国Bioword公司。5×SDS蛋白上样缓冲液、ECL化学发光液和全蛋白提取试剂盒来自江苏凯基生物科技有限公司。Matrigel基质胶及Boyden小室来自美国BD公司。CCK-8试剂来自日本同仁公司。TRIzol试剂、反转录试剂盒和荧光定量试剂均来自北京TaKaRa公司。4~6周雄性裸鼠来自南方医科大学实验动物中心。低温离心机和分光光度计来自美国Thermo公司。酶标仪来自美国BIO-BRAD公司。电泳仪来自北京AYGENE公司。MARCH2干扰质粒及慢病毒包装试剂盒来自广州复能公司。
1.2 胃癌组织相关资料收集中南大学湘雅医学院附属海口医院病理科2013年1月至2015年12月40例胃癌患者手术标本,所有标本均包括胃癌组织与正常组织(距癌组织5 cm的正常组织),其中男性26例,女性14例,年龄37~58岁,中位年龄47.5岁;中、高分化28例,低分化12例;肿瘤直径≤5 cm 9例,> 5 cm 31例;淋巴结有转移27例,无转移13例;浸润深度:黏膜下层10例,浆膜层30例。
1.3 随访电话随访所有胃癌患者术后生存情况。随访时间7~60个月,中位随访时间27.5个月。失访0例。
1.4 细胞培养人胃癌细胞株BGC823和人胚肾细胞293T采用含10%胎牛血清RPMI 1640培养液培养,置于37℃ 5%CO2培养箱,选择状态佳细胞株用于实验。
1.5 MARCH2干扰稳定株构建提前2 d铺293T细胞于75 cm2培养瓶中,融合度达到70%左右后,把细胞培养液换成空培(无血清的RPMI 1640培养液)。BGC823/shMARCH2组吸取2.5 μg MARCH2干扰质粒和5 μL HIV包装质粒混合物置于1.5 mL无菌EP管。BGC823/NC组吸取2.5 μg空载质粒载体和5 μL HIV包装质粒混合物置于1.5 mL无菌EP管。两组分别吸取Opti-Mem液至总体积200 μL,混匀,吸取15 μL EndoFection转染试剂于无菌1.5 mL EP管,用Opti-Mem补充体积至200 μL,混匀,将这200 μL混合液全部对应加入前1支1.5 mL EP管,混匀,静置10~25 min。再把上述两组混合液各自加入已经铺好293T细胞培养瓶中,各加入总体积1/500的TiterBoostTM增强剂。置于细胞培养箱内培养8~14 h后,用5%血清RPMI 1640培养液换液(内含有双抗1∶100配制),继续置于细胞培养箱,48 h后收集病毒上清,900 r/min离心4 min,留取上清液,并将上清液置于0.45 μm滤过膜进行过滤,收集滤液,于-80℃保存备用。前1 d铺BGC823细胞于6孔板中,细胞密度约为70%,第2天弃掉6孔板里BGC823细胞培养液,改为已收集好的两组病毒上清,加入1~2 mL/孔,置于细胞培养箱内培养36 h,然后用含5%血清RPMI 1640培养液(内含有双抗1∶100配置)换液,继续培养至细胞铺满,然后用含有嘌呤霉素的培养液进行药筛,直至对照组的细胞全部死掉,最后将实验组存活下来的细胞进行扩大培养。
1.6 荧光定量PCR细胞总RNA提取:细胞长满瓶底,加入TRIzol试剂冰上裂解,4℃ 12 000 r/min离心15 min,上层水相转移至去酶1.5 mL离心管,沉淀RNA中加入等体积异丙醇,室温静置10 min,4℃ 12 000 r/min离心10 min,收沉淀,75%乙醇洗涤,离心,室温至干燥,适量DEPC水溶解RNA,测RNA浓度。组织总RNA提取:研钵置180℃烤箱烘烤5 h,冷却备用,研钵中加入适量的液氮,绿豆大小组织研磨成粉状,加1 mL TRIzol裂解,余步骤同前。反转录反应:按照TaKaRa反转录试剂盒说明书配制反应体系,于PCR仪中37℃反应15 min,85℃灭活5 min,取反转录产物,用DEPC水稀释至4倍,-20℃保存。荧光定量PCR反应:MARCH2荧光定量PCR引物序列上游引物为5’CCGGAATTCATGACGACGGGTGACTGC3’,下游引物为5’CGCGGATCCCGTACTGGTGTCTCCTCTGCCA3’。按照TaKaRa RT-PCR试剂盒说明书配制反应体系,实时荧光定量PCR(quantitative real-time PCR,qPCR)仪中95℃预变性10 min,95℃15 s,60℃约30 s,72℃34 s,共40个循环。取各模板Ct值,用Folds=2-ΔΔCt值代表实验组及对照组基因表达。
1.7 Western blotBCA法测蛋白浓度测定,利用酶标仪器测570 nm处吸光度值(absorbance,A值),计算蛋白浓度。配制10% SDS-PAGE分离胶和5% SDS-PAGE浓缩胶,每个泳道上样量40 μg,跑胶,根据Marker位置切目的条带,冰上转膜,目的条带封闭1 h,一抗4℃孵育过夜。第2天目的条带复温,加入HRP标记抗兔二抗,室温孵育约1 h,PBST洗膜。化学发光仪发光。
1.8 CCK8细胞增殖实验选用状态良好癌细胞进行实验,消化细胞株进行铺板,每孔1×103个细胞接种至96孔板,每孔体积100 μL,每组5个目的复孔,1个空白对照孔,37℃ 5%CO2培养箱培养7 d。铺板24 h后开始测A值,检测450 nm处各孔A值,A值比值代表细胞增殖能力,每组取5个复孔平均值,连测7 d,绘制增殖曲线。
1.9 Boyden小室细胞侵袭实验选取状态良好的癌细胞进行实验,小室预处理:滤膜铺胶,用RPMI 1640培养液稀释的Matrigel基质胶(1∶5混合),50 μL/小室,置于超净台紫外照射2 h杀菌,消化细胞并计数,上室中加入200 μL细胞悬液(细胞数200×103个),下室中加入600 μL约10%胎牛血清RPMI 1640培养液。37℃5%CO2培养箱培养48~72 h,取出小室,清洗、固定并染色。显微镜下计数穿过膜细胞数,200倍光学显微镜下随机选取上、下、左、右和中心5个视野,拍图,取5个视野细胞数均值。
1.10 裸鼠体内肺转移实验取4~6周雄性裸鼠随机分两组,每组5只,消化细胞并计数,每只裸鼠经尾静脉注射约5×106个细胞,约1个月左右观察肺脏肿瘤转移情况,肺脏标本常规固定、取材、包埋并制作石蜡切片,镜下观察肿瘤细胞肺转移情况。
1.11 统计学分析采用Graphpad Prism 6统计软件分析数据。两组均数间比较采用配对样本t检验,多组均数间比较采用析因方差分析。采用Kaplan-Meier曲线分析生存情况。以P < 0.05为差异具有统计学意义。
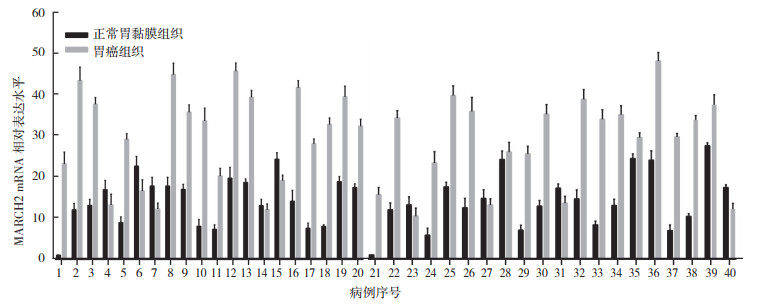
2 结果 2.1 胃癌组织中MARCH2 mRNA表达上调RT-PCR检测40例配对新鲜胃癌组织中MARCH2的mRNA表达。与周围正常胃黏膜组织比较,胃癌组织中MARCH2 mRNA高表达28例(高表达组),低表达12例(低表达组)。与周围正常胃黏膜组织比较,胃癌组织中MARCH2的mRNA表达水平上调(P < 0.05,图 1)。
|
| 图 1 RT-PCR检测40例胃癌组织及癌旁组织中MARCH2 mRNA表达水平 Fig.1 The mRNA expression of MARCH2 in 40 fresh paired gastric cancer tissues detected by RT-PCR |
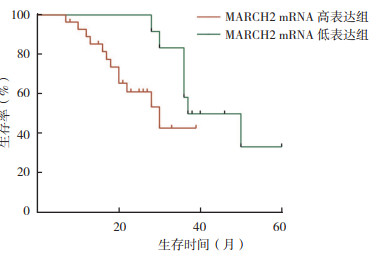
利用Graphpad Prism 6统计软件进行Kaplan-Meier生存曲线分析MARCH2表达水平与胃癌患者生存时间的关系。40例胃癌患者中,MARCH2 mRNA高表达组和低表达组中位生存时间分别为30个月和43.5个月,差异具有统计学意义(P < 0.05,图 2)。
|
| 图 2 MARCH2 mRNA高表达组与低表达组总生存曲线 Fig.2 Survival curves of gastric cancer patients with high and low expression of MARCH2 mRNA |
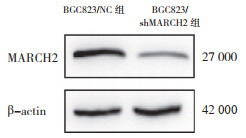
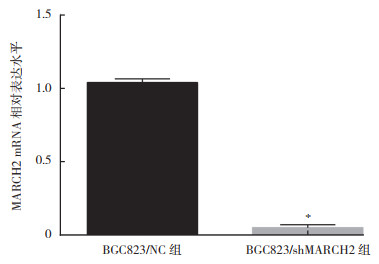
Western blot及RT-PCR检测MARCH2慢病毒载体转染BGC823细胞后MARCH2水平,结果显示,与BGC823/NC组比较,BGC823/shMARCH2组的MARCH2蛋白及mRNA水平均下降(均P < 0.05,图 3~4)。
|
| 图 3 Western blot检测BGC823/shMARCH2稳定细胞株构建效率 Fig.3 The construction efficiency of BGC823/shMARCH2 cell line detected by Western blot |
|
| 注 *与BGC823/NC组比较,P<0.01 图 4 RT-PCR检测BGC823/shMARCH2稳定细胞株构建效率 Fig.4 The construction efficiency of BGC823/shMARCH2 cell line detected by RT-PCR |
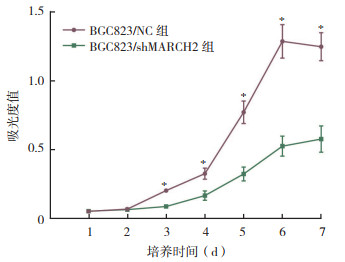
利用CCK8细胞增殖实验检测MARCH2沉默后胃癌细胞BGC823培养7 d的增殖能力显示,与BGC823/NC组比较,BGC823/shMARCH2组细胞株细胞增殖能力在第3、4、5、6和7天均下降,差异均具有统计学意义(均P < 0.01,图 5)。
|
| 注 *与BGC823/shMARCH2组比较,P<0.01 图 5 CCK8检测MARCH2沉默后BGC823细胞株体外增殖情况 Fig.5 The proliferation of BGC823 cell line after silencing MARCH2 detected by CCK8 |
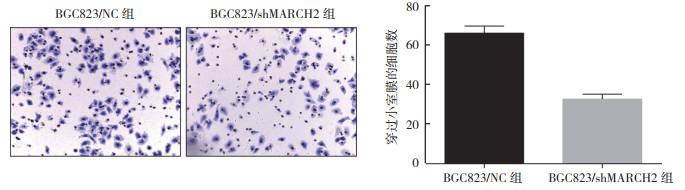
与BGC823/NC组比较,BGC823/shMARCH2组穿过小室膜细胞数目减少(t=13.13,P < 0.01),胃癌细胞侵袭能力减弱(图 6)。
|
| 注 *与BGC823/NC组比较,P<0.01 图 6 Boyden小室侵袭实验检测MARCH2沉默后BGC823细胞侵袭情况 Fig.6 The invasion of BGC823 cell line after silencing MARCH2 detected by Boyden chamber invasion assay |
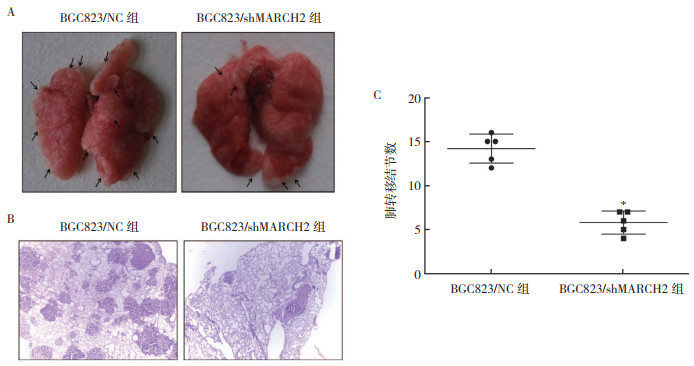
与BGC823/NC组比较,BGC823/shMARCH2组肺脏转移灶的数目减少(t=8.954,P < 0.01),胃癌细胞体内肺转移能力减弱(图 7)。
|
| 注 A:肉眼所见肺转移结节(箭头示);B:肺转移灶病理检查结果(HE×20);C:肺转移结节数统计图;*与BGC823/NC组比较,P<0.01 图 7 裸鼠尾静脉实验检测沉默MARCH2后BGC823细胞体内肺转移情况 Fig.7 The effect of MARCH2 silencing on lung metastasis in nude mice detected by tail vein pulmonary metastasis tumors |
胃癌发病年龄趋于年轻化,多数早期胃癌无明显症状,发现时多为进展期胃癌,严重影响患者生存预后。MARCH家族是一个结构上相关联的蛋白家族。MARCH家族11个成员,结构特点为由N端的环指蛋白(RING-CH)结构域和紧连的C端2个或多个跨膜区组成[17]。这种跨膜RING-CH指蛋白具有多种生物学功能,如免疫调节、蛋白质控和膜运输等。MARCH2与HIV-1感染相关,在肿瘤方面,MARCH2与卵巢癌、结直肠癌和胰腺癌等密切相关。MARCH2在胃癌中的生物学作用至今未报道。
本研究通过荧光定量PCR检测发现,MARCH2在胃癌组织中mRNA高表达,Kaplan-Meier生存曲线显示,MARCH2高表达胃癌患者预后较差。构建沉默MARCH2胃癌细胞株BGC823/shMARCH2发现,沉默MARCH2能够抑制胃癌细胞BGC823体外增殖、侵袭及体内肺转移能力,说明MARCH2表达与胃癌的增殖、侵袭及转移密切相关。
沉默MARCH2通过ATF4-CHOP-TRIB3-AKT-MTOR轴调控结肠癌细胞自噬[18],通过诱导内质网应急从而抑制结直肠癌生长[19]。MARCH2通过促进CFTR泛素化和降解以及PIK3CA-AKT-MTOR信号传导调节自噬[20],说明MARCH2在一些肿瘤进展过程中与自噬密切相关。自噬是一个相对保守的过程,广泛存在于真核细胞并通过溶酶体或液泡被水解酶降解,在细胞增殖、分化和衰老中具有重要作用,细胞自噬基因突变会导致疾病及肿瘤发生[21-22]。
本研究发现,自噬调节因子MARCH2在胃癌组织中高表达,并与患者预后有关,MARCH2促进胃癌细胞株BGC823的体外增殖、侵袭及体内肺转移能力,但MARCH2作用的相关机制及相关信号通路还有待进一步研究。MARCH2有望成为临床胃癌诊治及新药研究靶点依据。
| [1] |
Chan WL, Lam KO, So TH, et al. Third-line systemic treatment in advanced/metastatic gastric cancer: a comprehensive review[J]. Ther Adv Med Oncol, 2019, 11(6): 1-11. |
| [2] |
Liu H, Kinoshita T, Tonouchi A, et al. What are the reasons for a longer operation time in robotic gastrectomythan in laparoscopic gastrectomy for stomach cancer?[J]. Surg Endosc, 2019, 33(1): 192-198. DOI:10.1007/s00464-018-6294-x |
| [3] |
Reddavid R, Sofia S, Chiaro P, et al. Neoadjuvant chemotherapy for gastric cancer. Is it a must or a fake?[J]. World J Gastroenterol, 2018, 24(2): 274-289. DOI:10.3748/wjg.v24.i2.274 |
| [4] |
Jia F, Teer JK, Knepper TC, et al. Discordance of somatic mutations between asian and caucasian patient populations with gastric cancer[J]. Mol Diagn Ther, 2017, 21(2): 179-185. DOI:10.1007/s40291-016-0250-z |
| [5] |
Bartee E, Mansouri M, Hovey NB, et al. Downregulation of major histocompatibility complex class Ⅰ by human ubiquitin ligases related to viral immune evasion proteins[J]. J Virol, 2004, 78(3): 1109-1120. DOI:10.1128/JVI.78.3.1109-1120.2004 |
| [6] |
Boutell C, Sadis S, Everett RD. Herpes simplex virus type 1 immediate-early protein ICP0 and is isolated RING finger domain act as ubiquitin E3 ligases in vitro[J]. J Virol, 2002, 76(2): 841-850. DOI:10.1128/JVI.76.2.841-850.2002 |
| [7] |
Cheng J, Guggino W. Ubiquitination and degradation of CFTR by the E3 ubiquitin ligase MARCH2 through its association with adaptor proteins CAL and STX6[J]. PLoS One, 2013, 8(6): e68001. DOI:10.1371/journal.pone.0068001 |
| [8] |
Nakamura N, Fukuda H, Kato A, et al. MARCH-Ⅱ is a syntaxin-6-binding protein involved in endosomal trafficking[J]. Mol Biol Cell, 2005, 16(4): 1696-1710. DOI:10.1091/mbc.e04-03-0216 |
| [9] |
Zhang Y, Lu J, Liu X. MARCH2 is upregulated in HIV-1 infection and inhibits HIV-1 production through envelope protein translocation or degradation[J]. Virology, 2018, 518: 293-300. DOI:10.1016/j.virol.2018.02.003 |
| [10] |
Zhang Y, Tada T, Ozono S, et al. Membrane-associated RING-CH (MARCH) 1 and 2 are MARCH family members that inhibit HIV-1 infection[J]. J Biol Chem, 2019, 294(10): 3397-3405. DOI:10.1074/jbc.AC118.005907 |
| [11] |
Xia D, Qu L, Li G, et al. MARCH2 regulates autophagy by promoting CFTR ubiquitination and degradation and PIK3CA-AKT-MTOR signaling[J]. Autophagy, 2016, 12(9): 1614-1630. DOI:10.1080/15548627.2016.1192752 |
| [12] |
Yoo W, Cho EB, Kim S, et al. The E3 ubiquitin ligase MARCH2 regulates ERGIC3-dependent trafficking of secretory proteins[J]. J Biol Chem, 2019, 294(28): 10900-10912. DOI:10.1074/jbc.RA119.007435 |
| [13] |
Xia D, Ji W, Xu C, et al. Knockout of MARCH2 inhibits the growth of HCT116 colon cancer cells by inducing endoplasmic reticulum stress[J]. Cell Death Dis, 2017, 8(7): e2957. DOI:10.1038/cddis.2017.347 |
| [14] |
Yu S, Li Y, Liao Z, et al. Plasma extracellular vesicle long RNA profiling identifies a diagnostic signature for the detection of pancreatic ductal adenocarcinoma[J]. Gut, 2020, 69(3): 540-550. DOI:10.1136/gutjnl-2019-318860 |
| [15] |
许晓明, 董学妍, 陈岳明, 等. 富含脯氨酸小蛋白2A对胃癌细胞增殖和迁移能力的影响[J]. 实用肿瘤杂志, 2020, 35(6): 511-517. |
| [16] |
李丹妮, 刘静, 刘云鹏. 胃癌靶向治疗的现状与思考[J]. 实用肿瘤杂志, 2019, 34(2): 106-110. |
| [17] |
Wang X, Herr RA, Hansen T. Viral and cellular MARCH ubiquitin ligases and cancer[J]. Semin Cancer Biol, 2008, 18(6): 441-450. DOI:10.1016/j.semcancer.2008.09.002 |
| [18] |
夏丹, 孟琴. 沉默MARCH2通过ATF4-CHOPTRIB3-AKT-MTOR轴调控结肠癌细胞自噬[J]. 临床与实验病理学杂志, 2020, 36(4): 406-410. |
| [19] |
Xia D, Ji W, Xu C, et al. Knockout of MARCH2 inhibits the growth of HCT116 colon cancer cells by inducing endoplasmic reticulum stress[J]. Cell Death Dis, 2017, 8(7): e2957. DOI:10.1038/cddis.2017.347 |
| [20] |
Xia D, Qu L, Li G, et al. MARCH2 regulates autophagy by promoting CFTR ubiquitination and degradation and PIK3CA-AKT-MTOR signaling[J]. Autophagy, 2016, 12(9): 1614-1630. DOI:10.1080/15548627.2016.1192752 |
| [21] |
蒋琦炜, 张德宇, 石烟祝, 等. 细胞自噬与肿瘤发生发展[J]. 军事医学, 2021, 45(3): 314-320. |
| [22] |
刘兴哲, 车楠. 自噬调控肿瘤发生与发展的研究进展[J]. 医学研究生学报, 2021, 34(4): 414-417. |
 2021, Vol. 36
2021, Vol. 36


