文章信息
- 向鹏程, 屈少华, 韩俊毅
- 精氨酸剥夺疗法在结直肠癌治疗中的研究进展
- 实用肿瘤杂志, 2022, 37(2): 186-190
基金项目
- 国家自然科学基金(82160515);浦东新区卫生和计划生育委员会重点专科项目基金(PWZzk2017-26);浦东新区科技发展基金项目(PKJ2017-Y17)
-
通信作者
- 韩俊毅,E-mail:doctortonyhjy@tongji.edu.cn
-
文章历史
- 收稿日期:2021-03-25
精氨酸是一种人体半必需氨基酸,在正常生理状态下,有内源性和外源性2种获得途径:(1)通过鸟氨酸循环自身合成;(2)通过膜蛋白转运受体将胞外精氨酸转移至胞内。精氨酸可以直接或者间接参与细胞代谢关键酶调节和神经及免疫的系统调节,并在细胞信号通路中起重要作用[1]。
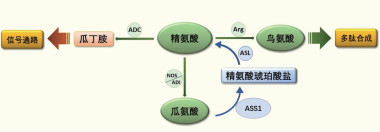
精氨酸在细胞内的代谢通路有3条常见途径(图 1):(1)精氨酸可以通过精氨酸酶-1(arginase-1,Arg-1)作用生成鸟氨酸,鸟氨酸又参与到多胺合成;(2)精氨酸也可以通过精氨酸脱羧酶(arginine decarboxylase,ADC)的作用,生成胍丁胺,进而参与到细胞信号通路中;(3)在精氨酸脱氨酶(arginine deiminase,ADI)或者一氧化氮合成酶(nitric oxide synthase,NOS)的作用下,可以生成瓜氨酸,瓜氨酸在细胞内可以通过精氨酸琥珀酸盐合成酶-1(argininosuccinate synthetase-1,ASS1)及精氨酸琥珀酸盐裂解酶(argininosuccinate lyase,ASL)的先后作用,通过中间产物精氨酸琥珀酸盐,再次合成精氨酸[2]。
|
| 注 ADC:精氨酸脱羧酶(arginine decarboxylase);Arg:精氨酸酶(arginase);NOS:一氧化氮合成酶(nitric oxide synthase);ADI:精氨酸脱氨酶(arginine deiminase);ASL:精氨酸琥珀酸盐裂解酶(argininosuccinate lyase);ASS1:精氨酸琥珀酸盐合成酶-1(argininosuccinate synthetase-1) 图 1 基于精氨酸代谢的常见途径的代谢流程图 |
在肿瘤的发生和发展过程中,氨基酸的代谢异常是不容忽视的一部分,在此之中,精氨酸的代谢异常越发得到重视,精氨酸分解代谢异常可能是肿瘤细胞代谢异常的特点,特别是与结直肠癌的发生和发展关系密切[3]。通过精氨酸降解酶将循环精氨酸降解,营造精氨酸缺乏环境来抑制肿瘤细胞生长,被称之为精氨酸剥夺疗法,现已被用于多种恶性肿瘤治疗中[4]。本文拟对结直肠癌(colorectal cancer,CRC)中的精氨酸剥夺疗法的最新进展作一综述。
1 精氨酸剥夺疗法在恶性肿瘤治疗中的应用在部分恶性肿瘤发展的进程中,为满足肿瘤细胞快速生长的能量需要,通过代谢重编程的作用,鸟氨酸循环关键酶的表达出现异常,主要是ASS1的表达缺失,致使肿瘤细胞自身合成精氨酸减少,必须通过增加外源性精氨酸的摄入,进而更加依赖于外源性的精氨酸补给,这种现象被称为精氨酸营养缺陷[5-6]。早期研究发现,多数肝细胞癌、恶性黑色素瘤以及前列腺癌ASS1表达持续阴性,而结直肠癌和肺癌中ASS则表达持续阳性,肉瘤、浸润性乳腺癌以及肾细胞癌ASS表达并不稳定[6]。后续研究中又发现胰腺癌、间皮瘤以及淋巴瘤也呈现为精氨酸营养缺陷型[7]。
由此,减少外源性精氨酸补给以达到抑制肿瘤的作用成为治疗新思路。但是通过饮食调整仅能达到血清精氨酸浓度下降30%的作用,因此通过相关精氨酸降解酶来减少血清精氨酸浓度以达到抑制肿瘤的作用则成为主要手段。目前精氨酸降解酶应用最为广泛的就是聚乙二醇化精氨酸脱氨酶(pegylated arginine deaminase,ADI-PEG)和聚乙二醇化人重组Arg-1(pegylated human recombinant Arg-1,rhArg1-PEG)。ADI可以将胞外精氨酸代谢为瓜氨酸,以降低血清精氨酸浓度,但胞外瓜氨酸被摄取入进细胞内后,在ASS与ASL的作用下,瓜氨酸可以直接在胞内合成精氨酸,因此ADI治疗的有效性必须建立在ASL或ASS表达缺失基础上;Arg在胞外将精氨酸代谢为鸟氨酸,其治疗的有效性也依赖于鸟氨酸氨甲酰基转移酶(ornithine transcarbamylase,OTC)、ASL或ASS的表达缺失[8]。目前大多以ASS和ASL的表达量作为对精氨酸剥夺疗法是否敏感的检测要素[9-10]。在过去一直认为CRC中ASS1的表达是高于癌旁正常组织[6, 11],因而在以往的研究中一直认为精氨酸剥夺疗法并不适用于CRC的治疗,相关研究也因此停滞不前。
CRC细胞是否真的属于非精氨酸营养缺陷型这个问题是目前精氨酸剥夺疗法能否用于CRC治疗的关键。近期研究表明,通过在无精氨酸的培养液与对照组培养液中培养CRC细胞发现,所有的CRC细胞株均不能在无精氨酸的培养液中生长,并且伴随着DNA复制的停滞和细胞周期蛋白Cyclin D1的表达下调,通过外源性补给精氨酸,所观察的现象大多可以逆转[12]。动物实验也表明,接种了CRC细胞的免疫缺陷性老鼠在接受无精氨酸的饮食后,肿瘤体积和重量都降低且不伴随小鼠体质量的下降[12]。这部分结果也证实,部分CRC细胞事实上应该是精氨酸营养缺陷性的,这就为精氨酸代谢通路作为CRC治疗的可能靶点提供了依据。
2 精氨酸剥夺在CRC治疗中的进展目前在其他精氨酸营养缺陷型的肿瘤中,已经广泛研究并投入使用的主要是ADI-PEG和rhArg1-PEG。通过聚乙醇化的降解酶在血液中更为稳定,并且很少引起过敏等反应。
2.1 精氨酸饥饿对CRC细胞的影响在无精氨酸环境中,即精氨酸饥饿状态下,CRC细胞HT116呈现明显抵抗型,而CRC细胞HT29则是敏感型[13]。但这两种CRC细胞在无精氨酸情况下培养,无论2D与3D培养,其胞内精氨酸浓度均会快速下降,表明胞内精氨酸基础浓度对精氨酸剥夺的影响并不深刻[14]。CRC细胞经精氨酸饥饿,能下调哺乳动物雷帕霉素靶蛋白(mammalian target of rapamycin,mTOR)通路下游关键蛋白的磷酸化水平,不同点在于敏感性HT29细胞是持续性的,但在抵抗性的HT116细胞中则表现为短暂下调,仅能维持2~8 h。进一步研究也发现,在CRC细胞中,精氨酸剥夺的效应部分依赖于Tp53的表型,精氨酸剥夺可激活Tp53基因,并促使野生型细胞周期停滞在G1/G0期,这有助于Tp53野生型细胞在无精氨酸存在的条件下生存[14]。这表明CRC细胞在精氨酸缺乏状态下,可以通过激活多种细胞通路来耐受精氨酸的缺乏状态,不同的CRC细胞株所产生的应答是存在差异的,这也说明精氨酸剥夺在CRC的治疗中并不能一概而论。
2.2 rhArg1-PEG对CRC细胞的影响使用rhArg1-PEG诱导精氨酸降解后发现,无论ASS1表达与否,CRC细胞均呈现与药物剂量相关的生长受限。其原因可能与DNA合成减少导致的细胞增殖减慢有关[12]。CRC细胞株HT29、Caco-2以及SW837对rhArg1-PEG处理是极其敏感的,胞内精氨酸浓度下降,细胞增殖受限,Skco-1以及SW1116细胞则不然,Skco-1细胞表现低度敏感,而SW1116细胞则不敏感,但rhArg1-PEG的这种细胞毒性作用可以被外源性的瓜氨酸的加入所逆转[15]。并且,在经过rhArg1-PEG处理后,ASS1的表达在CRC细胞株中增加,可能与c-Myc的表达增强有关[12],这一点与c-Myc在恶性黑色素瘤接受精氨酸剥夺后介导ASS1的再表达的结果是一致的[16]。在动物实验中,rhArg1-PEG仍能抑制肿瘤的生长,但动物实验中未发现精氨酸剥夺治疗后肿瘤细胞通过ASS1或OTC的再表达而获得耐药性[12]。经rhArg1-PEG处理后进行细胞划痕实验,Caco-2细胞的伤口修复能力减弱,但在加入外源性的瓜氨酸后,该作用几乎被完全逆转,与未经rhArg1-PEG处理的细胞几乎一致,这表明rhArg1-PEG介导的精氨酸剥夺能降低Caco-2细胞的运动能力。SW837细胞在细胞划痕实验中对精氨酸剥夺并不十分敏感,而rhArg1-PEG对HT29细胞的运动能力的影响又无法被外源性瓜氨酸补给所逆转。对Caco-2细胞的进一步研究发现,其ASS1的基础水平就高,在经rhArg1-PEG处理后下降,后又在外源性瓜氨酸补给后回升[15]。研究还表明,rhArg1-PEG处理会降低Caco-2细胞的黏附能力, 考虑到细胞的黏附能力受RhoA的调节,所以进一步研究也发现,rhArg1-PEG对细胞黏附能力的影响是间接通过影响RhoA活化水平来实现的;在3D培养的细胞模型中也发现,rhArg1-PEG处理的Caco-2细胞侵袭性也降低,这种影响是间接通过下调基质金属蛋白酶-9(matrix metalloprotein-9,MMP-9)的表达水平来实现的。rhArg1-PEG对Caco-2细胞侵袭性和黏附能力的影响均可以被外源性的瓜氨酸补给所逆转[15]。考虑到瓜氨酸对多种CRC细胞在精氨酸缺乏状态下的黏附和迁移能力的影响,研究发现,即使在精氨酸缺乏的情况下,ASS1表达仍上调,有能力将外源性摄入的瓜氨酸转化为精氨酸,以满足肿瘤的生长需求,但细胞实验也表明,在2D和3D培养的状态下,生理浓度的瓜氨酸都不能使CRC细胞在无精氨酸的培养液中正常生长,仅远高于生理浓度的瓜氨酸才能部分扭转精氨酸缺乏带来的抑制作用[17]。
2.3 ADI-PEG对CRC细胞的影响研究显示,ASS1缺陷性是ADI介导精氨酸剥夺疗法的敏感要素之一,这与经ADI-PEG处理后RKO以及HT29细胞生长受限而SW480细胞由于对ASS1的高表达而呈现对ADI-PEG的不敏感是一致的[12]。但值得注意的是,HCT116细胞尽管可检测到少量ASS1的表达,却是对ADI-PEG最为敏感的CRC细胞株。类似的结果在之前的研究中也有阐述,这可能与在HCT116细胞中ADI-PEG抑制mTORC1和激活未折叠蛋白反应,导致对ASS1及低氧诱导因子-1(hypoxia inducible factor-1,HIF-1)的抑制有关[18]。在动物实验中ADI-PEG同样可以抑制肿瘤的增长,但与rhArg1-PEG不同的是,经过ADI-PEG处理后的小鼠模型中可检测到ASS1的表达上调[12]。
2.4 精氨酸剥夺的联合治疗在单药方案的精氨酸剥夺治疗中,ASS1以及ASL的表达上调与对ADI-PEG的耐药密切相关,而对rhArg1-PEG的耐药除与ASS1和ASL相关外,还与OTC相关[19]。另外肿瘤细胞自噬导致自身内源性精氨酸利用增加也会导致部分耐药[20]。因此对于精氨酸剥夺在CRC中的应用,为避免耐药性增加,联合用药仍是有希望的选择。
刀豆氨酸(canavanine,Cav)是植物来源的一种精氨酸类似物,已经被广泛研究,具有很强的细胞毒性和抗肿瘤活性。研究表明,Cav可以增加精氨酸剥夺诱导的多种肿瘤细胞的凋亡作用[21]。类似的协调作用在CRC细胞中也有发现,考虑CRC细胞中ASS1的表达与瓜氨酸可能存在的补偿作用,研究也发现,无论瓜氨酸存在与否,Cav联合精氨酸剥夺均可以诱导CRC细胞凋亡,联合rhArg1-PEG与低剂量的Cav可以发挥选择性的抗肿瘤作用,对正常的上皮细胞无影响[17]。
穗花木兰氨酸(indospicine,Isp)也同样是精氨酸的结构类似物,但与Cav不同的是,Isp不仅不会抑制Arg活性,并且不作为Arg的代谢底物参与代谢反应。研究表明,通过精氨酸剥夺,能增强Isp对CRC的细胞毒性;通过对细胞凋亡相关通路的关键基因及蛋白进行分析发现,在精氨酸缺乏环境下,Isp可能通过CRC细胞错误识别、参与蛋白合成进一步激活内质网应激和部分抗增殖与促凋亡的信号通路从而发挥其细胞毒性[22]。
当精氨酸剥夺疗法联合传统化疗药物奥沙利铂以及5-氟尿嘧啶(5-fluorouracil,5-FU)时发现,rhArg1-PEG与奥沙利铂和5-FU均存在拮抗作用;而ADI-PEG则与奥沙利铂在ASS1阴性的RKO及HT29细胞株中有协调作用,在HT29细胞株中与5-FU存在拮抗[12]。
3 小结与展望CRC是目前世界范围内癌症死亡的主要原因之一,我国相关发病率也呈逐步上升趋势,约1/3的晚期患者无根治手术的可能,只能接受姑息治疗[23]。尽管靶向治疗和免疫治疗的进展十分迅速,但对于缺少免疫治疗或靶向治疗靶点的患者,开发新的治疗途径也尤为重要[24]。
精氨酸剥夺疗法以往认为不适用于CRC的治疗,主要考虑的是CRC细胞中,精氨酸代谢的关键酶ASS1、ASL以及OTC等异常表达,导致其对于外源性精氨酸并不是十分依赖。事实上,对于CRC的进一步研究已经发现,精氨酸对于CRC的发生和发展是必须的,几乎所有的CRC细胞均不能在无精氨酸的条件下生长。精氨酸缺失会导致细胞产生多种应答机制,一方面为细胞耐受精氨酸缺乏状态做准备,另一方面也会激活凋亡通路,促进细胞凋亡。
但是值得注意的是,在CRC细胞株中,各个细胞株间存在差异,不仅在精氨酸代谢关键酶如ASS1和ASL等的表达上有不同,也在精氨酸缺乏状态下所激活的细胞通路有不同。另外,CRC细胞株在精氨酸缺乏的状态下,有部分会再次上调ASS1的表达,这可能也是之前的研究中认为CRC不适用精氨酸剥夺的一个原因。但并不是所有CRC细胞均高表达ASS1,不/低表达ASS1的细胞株也存在应激状态下,ASS1诱发表达的情况,这可能是CRC细胞对其耐药的关键原因之一。两种常用的精氨酸剥夺疗法的药物ADI-PEG和rhArg1-PEG均被证明可以抑制细胞生长,但药物诱导的精氨酸缺乏状态与无精氨酸培养即精氨酸饥饿状态是存在差异的,药物诱导的精氨酸剥夺存在其他细胞通路的激活,会导致精氨酸缺乏以外的细胞反应,这也是部分CRC细胞尽管低表达精氨酸代谢关键酶,但却对精氨酸降解酶异常敏感的原因。
另外,精氨酸对免疫系统的影响也是不容忽视的。如何在使得精氨酸剥夺促进肿瘤细胞凋亡的同时又降低对肿瘤免疫抑制的影响是接下来相关研究不可忽视的挑战。目前很多研究都已经表明,精氨酸剥夺的单药治疗效果并不十分理想,ASS1的继发再表达可能与耐药相关[19]。进一步的研究也表明,精氨酸的结构类似物Cav及Isp都对CRC细胞有细胞毒性和抗肿瘤活性,与精氨酸剥夺的联合治疗对多种CRC细胞株均有抑制作用[17, 21-22]。精氨酸剥夺与传统的化疗药物的联合用药,也是一项新的治疗思路,近期研究也表明有效[12]。
综上所述,目前CRC的精氨酸剥夺疗法是值得深入研究的,并在后续的研究中,一部分主要研究方向在于CRC精氨酸代谢关键酶的表达调控,这不仅可以改变CRC的精氨酸营养状态,也对精氨酸耐药机制有更深入的了解;另一部分则应更注重精氨酸剥夺疗法与其他药物的联合作用及其机制,不仅考虑精氨酸的营养状态,也要将精氨酸剥夺的药物所引发的相关细胞反应纳入,这样既可以避免耐药,又可以通过协调作用增加疗效。
致谢: 本文得到上海市东方医院胃肠外科各医师的指导和支持
| [1] |
Matsumoto S, Haberle J, Kido J, et al. Urea cycle disorders-update[J]. J Hum Genet, 2019, 64(9): 833-847. DOI:10.1038/s10038-019-0614-4 |
| [2] |
Gambardella J, Khondkar W, Morelli MB, et al. Arginine and endothelial function[J]. Biomedicines, 2020, 8(8): 277. DOI:10.3390/biomedicines8080277 |
| [3] |
Du T, Han J. Arginine metabolism and its potential in treatment of colorectal cancer[J]. Front Cell Dev Biol, 2021, 9: 658861. DOI:10.3389/fcell.2021.658861 |
| [4] |
Al-Koussa H, El Mais N, Maalouf H, et al. Arginine deprivation: a potential therapeutic for cancer cell metastasis? A review[J]. Cancer Cell Int, 2020, 20: 150. DOI:10.1186/s12935-020-01232-9 |
| [5] |
Fultang L, Vardon A, De Santo C, et al. Molecular basis and current strategies of therapeutic arginine depletion for cancer[J]. Int J Cancer, 2016, 139(3): 501-509. DOI:10.1002/ijc.30051 |
| [6] |
Dillon BJ, Prieto VG, Curley SA, et al. Incidence and distribution of argininosuccinate synthetase deficiency in human cancers: a method for identifying cancers sensitive to arginine deprivation[J]. Cancer, 2004, 100(4): 826-833. DOI:10.1002/cncr.20057 |
| [7] |
Kumari N, Bansal S. Arginine depriving enzymes: applications as emerging therapeutics in cancer treatment[J]. Cancer Chemother Pharmacol, 2021, 88(4): 565-594. DOI:10.1007/s00280-021-04335-w |
| [8] |
Qiu F, Huang J, Sui M. Targeting arginine metabolism pathway to treat arginine-dependent cancers[J]. Cancer Lett, 2015, 364(1): 1-7. DOI:10.1016/j.canlet.2015.04.020 |
| [9] |
Phillips MM, Sheaff MT, Szlosarek PW. Targeting arginine-dependent cancers with arginine-degrading enzymes: opportunities and challenges[J]. Cancer Res Treat, 2013, 45(4): 251-262. DOI:10.4143/crt.2013.45.4.251 |
| [10] |
Long Y, Tsai WB, Wangpaichitr M, et al. Arginine deiminase resistance in melanoma cells is associated with metabolic reprogramming, glucose dependence, and glutamine addiction[J]. Mol Cancer Ther, 2013, 12(11): 2581-2590. DOI:10.1158/1535-7163.MCT-13-0302 |
| [11] |
Delage B, Fennell DA, Nicholson L, et al. Arginine deprivation and argininosuccinate synthetase expression in the treatment of cancer[J]. Int J Cancer, 2010, 126(12): 2762-2772. |
| [12] |
Alexandrou C, Al-Aqbi SS, Higgins JA, et al. Sensitivity of colorectal cancer to arginine deprivation therapy is shaped by differential expression of urea cycle enzymes[J]. Sci Rep, 2018, 8(1): 12096. DOI:10.1038/s41598-018-30591-7 |
| [13] |
Vynnytska-Myronovska B, Bobak Y, Garbe Y, et al. Single amino acid arginine starvation efficiently sensitizes cancer cells to canavanine treatment and irradiation[J]. Int J Cancer, 2012, 130(9): 2164-2175. DOI:10.1002/ijc.26221 |
| [14] |
Vynnytska-Myronovska BO, Kurlishchuk Y, Chen O, et al. Arginine starvation in colorectal carcinoma cells: Sensing, impact on translation control and cell cycle distribution[J]. Exp Cell Res, 2016, 341(1): 67-74. DOI:10.1016/j.yexcr.2016.01.002 |
| [15] |
Al-Koussa H, Al-Haddad M, Abi-Habib R, et al. Human recombinant arginase Ⅰ[HuArgⅠ (Co)-PEG5000]- induced arginine depletion inhibits colorectal cancer cell migration and invasion[J]. Int J Mol Sci, 2019, 20(23): 6018. DOI:10.3390/ijms20236018 |
| [16] |
Tsai WB, Aiba I, Long Y, et al. Activation of Ras/PI3K/ ERK pathway induces c-Myc stabilization to upregulate argininosuccinate synthetase, leading to arginine deiminase resistance in melanoma cells[J]. Cancer Res, 2012, 72(10): 2622-2633. DOI:10.1158/0008-5472.CAN-11-3605 |
| [17] |
Kurlishchuk Y, Vynnytska-Myronovska B, Grosse-Gehling P, et al. Co-application of canavanine and irradiation uncouples anticancer potential of arginine deprivation from citrulline availability[J]. Oncotarget, 2016, 7(45): 73292-73308. DOI:10.18632/oncotarget.12320 |
| [18] |
Burrows N, Cane G, Robson M, et al. Hypoxia-induced nitric oxide production and tumour perfusion is inhibited by pegylated arginine deiminase (ADI-PEG20)[J]. Sci Rep, 2016, 6: 22950. DOI:10.1038/srep22950 |
| [19] |
Wu C, You M, Nguyen D, et al. Enhancing the effect of tumor necrosis factor-related apoptosis-inducing ligand signaling and arginine deprivation in melanoma[J]. Int J Mol Sci, 2021, 22(14): 7628. DOI:10.3390/ijms22147628 |
| [20] |
Szlosarek PW. Arginine deprivation and autophagic cell death in cancer[J]. Proc Natl Acad Sci U S A, 2014, 111(39): 14015-14016. DOI:10.1073/pnas.1416560111 |
| [21] |
Vynnytska BO, Mayevska OM, Kurlishchuk YV, et al. Canavanine augments proapoptotic effects of arginine deprivation in cultured human cancer cells[J]. Anticancer Drugs, 2011, 22(2): 148-157. DOI:10.1097/CAD.0b013e32833e0334 |
| [22] |
Shuvayeva GY, Bobak YP, Vovk OI, et al. Indospicine combined with arginine deprivation triggers cancer cell death via caspase-dependent apoptosis[J]. Cell Biol Int, 2021, 45(3): 518-527. DOI:10.1002/cbin.11321 |
| [23] |
皇甫超男, 徐沭芬, 丁洁, 等. 安罗替尼联合5- 氟尿嘧啶对结直肠癌细胞增殖和凋亡的影响[J]. 实用肿瘤杂志, 2021, 36(1): 507-513. |
| [24] |
米迷, 翁姗姗, 陆德珉, 等. 2021年晚期结直肠癌治疗研究进展[J]. 实用肿瘤杂志, 2022, 37(1): 23-28. |
 2022, Vol. 37
2022, Vol. 37


