文章信息
- 郑清月, 闫春良, 赵秋红
- Zheng Qingyue, Yan Chunliang, Zhao Qiuhong
- 盐酸埃克替尼治疗肺腺癌进展后加量治疗的疗效及安全性分析
- Clinical effi cacy and safety analysis of additional dose of icotinib in treatment of advanced lung adenocarcinoma
- 实用肿瘤杂志, 2020, 35(3): 231-235
- Journal of Practical Oncology, 2020, 35(3): 231-235
-
作者简介
- 郑清月(1986-), 女, 黑龙江佳木斯人, 主治医师, 硕士, 从事呼吸系统肿瘤临床研究.
-
文章历史
- 收稿日期:2019-04-08
世界卫生组织(World Health Organization, WHO)估计全球每年死于肺癌的患者约159万例[1]。目前在中国, 肺癌发病率和死亡率居恶性肿瘤之首, 80%~90%的肺癌患者为非小细胞肺癌(nonsmall-cell lung cancer, NSCLC), 确诊时已多为晚期[2-3]。对于表皮生长因子受体(epidermal growth factor receptor, EGFR)敏感突变(19外显子缺失和21外显子点突变L858R)的晚期NSCLC患者, 一线首选治疗方案为表皮生长因子受体酪氨酸激酶抑制剂(epidermal growth factor receptor-tyrosine kinase inhibitor, EGFR-TKI), 其疗效确切, 不良反应较轻[1, 4]。一代EGFR-TKI治疗后进展者, 如T790M突变阳性推荐使用奥希替尼, 对于T790M突变阴性者可选择的方案包括再次给予相同的EGFR-TKI或者换另一种EGFR-TKI, 以及含铂的联合化疗, 然而标准治疗方案仍未确定[4-5]。需要继续寻找疗效确切和安全性高的治疗方案。本文探讨经标准剂量埃克替尼治疗的晚期肺腺癌患者进展后、基因检测仍存在EGFR敏感突变并且T790M突变阴性的患者, 增加剂量治疗的疗效及安全性。
1 资料与方法 1.1 纳入标准与排除标准纳入标准:(1)经支气管镜或经皮肺活检病理证实为肺腺癌; (2)经一线单药盐酸埃克替尼常规剂量治疗(125 mg口服3次/d), 肿瘤进展后, 给予单药盐酸埃克替尼加量治疗(150~450 mg口服3次/d), 至肿瘤进展、死亡或至最后随访日期(2018年12月31日); (3)常规剂量治疗进展后行组织或血标本基因检测, EGFR敏感突变为阳性, 无T790M突变; (4)具有≥ 1个可评价病灶。
排除标准:(1)无病理诊断结果; (2)无基因检测结果; (3)使用埃克替尼同时联合其他化疗方案或联合其他TKI治疗; (4)使用埃克替尼治疗同时联合手术、放疗或其他肿瘤物理治疗; (5)无可评价的临床病灶。
1.2 一般资料根据纳入和排除标准, 收集2016年1月至2018年6月收治于北京航天总医院的肺腺癌患者22例。其中男性9例, 女性13例; 年龄36~81岁, 中位年龄64岁。收集患者的临床资料, 包括性别、年龄、是否吸烟、肿瘤分期、美国东部肿瘤协作组(Eastern Cooperative Oncology Group, ECOG)评分和EGFR基因检测结果等。
1.3 随访随访内容包括生存情况、可评估病灶的影像学检查结果、血常规、肝肾功能和不良反应等。随访截止时间为患者死亡或最后随访日期(2018年12月31日), 中位随访时间为9个月, 随访方式包括复诊和电话随访。无失访, 截止最后随访日期, 5例生存, 其中4例为无进展生存。
1.4 疗效评价近期疗效评估根据RECIST1.1标准[6]对肺癌可评估病灶进行治疗效果评估, 分为完全缓解(complete response, CR)、部分缓解(partial response, PR)、疾病稳定(stable disease, SD)和疾病进展(progressive disease, PD)。客观缓解率(objective response rate, ORR)是指CR+PR患者占全组患者百分比。疾病控制率(disease control rate, DCR)是指CR+PR+SD患者占全组患者的百分比。远期疗效评估根据无进展生存时间(progression free survival, PFS)和总生存时间(overall survival, OS)。PFS为从开始埃克替尼加量治疗至患者出现肿瘤进展或死亡的时间。OS为从开始埃克替尼加量治疗至无论任何原因导致患者死亡的时间。不良反应分级按常见不良反应事件评价标准(Common Terminology Criteria for Adverse Event, CTCAE)V4.0版本分为1~5级。
1.5 统计学分析使用SPSS19.0软件进行统计学分析。采用Kaplan-Meier法绘制生存曲线, Log-rank检验比较不同临床特征组间PFS和OS。不同临床特征组间ORR和DCR的比较采用χ2检验或Fisher检验。以P < 0.05为差异具有统计学意义。
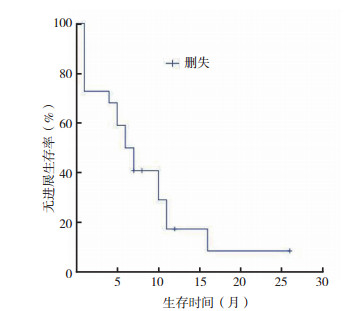
2 结果 2.1 疗效评估22例晚期肺腺癌患者经埃克替尼治疗后, CR 0例(0%), PR 7例(31.8%), SD 9例(40.9%), PD 6例(27.3%), ORR为31.8%, DCR为72.7%。22例中位PFS为6个月(95%CI:3.702~8.298个月), 中位OS为11个月(95%CI:7.260~14.740个月), 见图 1~2。
|
| 图 1 晚期肺腺癌患者经加量埃克替尼治疗后无进展生存曲线 Fig.1 Progression-free survival of patients with advanced lung adenocarcinoma treated with additional dose of icotinib |
|
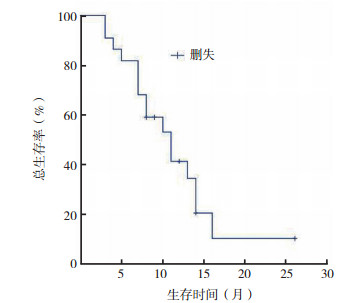
| 图 2 晚期肺腺癌患者经加量埃克替尼治疗后总生存曲线 Fig.2 Overall survival of patients with advanced lung adenocarcinoma treated with additional dose of icotinib |
22例患者根据组织学或细胞学证实为肺腺癌, 年龄36~81岁(中位年龄64岁), 其中 < 65岁11例(50.0%), ≥ 65岁11例(50.0%)。男性9例(40.9%), 女性13例(59.1%)。有吸烟史7例(31.8%), 无吸烟史15例(68.2%)。TNM分期Ⅲ B期10例(45.5%), IV期12例(54.5%)。ECOG评分1~2分12例(54.5%), 3~4分10例(45.5%)。EGFR19外显子缺失15例(68.2%), 21外显子点突变7例(31.8%)。所有患者不同临床特征间短期疗效比较, 差异均无统计学意义(均P>0.05, 表 1)。女性患者比男性患者中位OS长(P=0.040), 无吸烟史患者较有吸烟史患者中位OS长(P=0.011)。
| 临床特征 | 例数 | 客观缓解率 | 疾病控制率 | 无进展生存时间 | 总生存时间 | |||||||
| 例数(%) | P值 | 例数(%) | P值 | 中位值(月) | P值 | 中位值(月) | P值 | |||||
| 年龄 | 1.000 | 0.635 | 0.613 | 0.446 | ||||||||
| < 65岁 | 11 | 3(27.3) | 7(63.6) | 5 | 10 | |||||||
| ≥65岁 | 11 | 4(36.4) | 9(81.8) | 7 | 14 | |||||||
| 性别 | 0.648 | 0.178 | 0.238 | 0.040 | ||||||||
| 男 | 9 | 2(22.2) | 5(55.6) | 6 | 8 | |||||||
| 女 | 13 | 5(38.5) | 11(84.6) | 7 | 14 | |||||||
| 吸烟史 | 1.000 | 0.054 | 0.110 | 0.011 | ||||||||
| 无 | 15 | 5(33.3) | 13(86.7) | 7 | 14 | |||||||
| 有 | 7 | 2(28.6) | 3(42.9) | 1 | 7 | |||||||
| ECOG评分 | 0.381 | 0.348 | 0.275 | 0.774 | ||||||||
| 1~2分 | 12 | 5(41.7) | 10(83.3) | 6 | 11 | |||||||
| 3~4分 | 10 | 2(20.0) | 6(60.0) | 6 | 8 | |||||||
| TNM分期 | 0.172 | 0.162 | 0.146 | 0.050 | ||||||||
| Ⅲ B期 | 10 | 5(50.0) | 9(90.0) | 10 | 14 | |||||||
| Ⅳ期 | 12 | 2(16.7) | 7(58.3) | 4 | 7 | |||||||
| EGFR突变 | 0.350 | 1.000 | 0.874 | 0.955 | ||||||||
| 19del | 15 | 6(40.0) | 11(73.3) | 7 | 11 | |||||||
| 21 L858R | 7 | 1(14.3) | 5(71.4) | 6 | 8 | |||||||
22例使用埃克替尼的患者中, 出现皮疹14例(63.6%), 食欲下降10例(45.4%), 腹泻7例(31.8%), 转氨酶升高3例(13.6%), 白细胞减少2例(9.1%), 口腔溃疡2例(9.1%), 以上不良反应均为1~2级, 无≥ 3级不良反应出现。所有不良反应经对症治疗后可好转, 无患者因不良反应中断治疗。
3 讨论在全世界, 肺癌是恶性肿瘤导致死亡的主要病因, 约20%的恶性肿瘤致死是由于肺癌导致的。NSCLC约占肺癌的85%, 多数患者确诊时已经为不能手术切除的晚期肺癌患者[7]。EGFR-TKI的作用机制为抑制EGFR自身磷酸化, 从而阻断肿瘤细胞生长增殖所需的信号传导通路, 取得抑制肿瘤细胞增殖的效果。盐酸埃克替尼是全球第3个上市的EGFR-TKI药物, 被推荐用于EGFR基因敏感突变的晚期NSCLC的一线治疗、晚期NSCLC的二/三线治疗和晚期NSCLC的维持治疗[8]。尽管具有EGFR敏感突变的NSCLC患者使用EGFR-TKI疗效明显, 但通常9~14个月就会出现疾病进展。一代EGFR-TKI耐药机制包括EGFR二次突变、KRAS突变、NRAS突变、MET基因扩增、BRAF (G469A和V600E)突变和人表皮生长因子受体2(human epidermal growth factor receptor 2, HER2)扩增等旁路途径激活以及病理表型的转换等, 其中>50%的获得性耐药机制为EGFR 20外显子T790M突变[9-11]。目前T790M突变阳性患者指南推荐使用奥希替尼, T790M突变阴性患者治疗方案包括继续给予相同EGFR-TKI或换另一种EGFR-TKI和含铂的联合化疗, 然而标准方案仍没有定论[1, 4]。盐酸埃克替尼的半衰期较短, 治疗窗较宽, 治疗窗为300 mg/d (100 mg, 3次/d)~1 875 mg/d (625 mg, 3次/d), 推荐治疗剂量为125 mg, 3次/d, 最大耐受剂量(maximum tolerated dose, MTD)为500 mg/次。盐酸埃克替尼的生物利用度和药物浓度呈线性相关性, 经大量预处理的晚期NSCLC患者具有良好的抗肿瘤活性和药代动力学特征[12-13]。这为埃克替尼加量治疗提供可能性。
一线埃克替尼治疗耐药后, 二线给予增加剂量埃克替尼治疗的临床研究稀缺。吕丽英等[14]研究为EGFR敏感突变Ⅳ期肺腺癌患者一线常规剂量埃克替尼治疗耐药后, 二线给予埃克替尼加量治疗, CR 0例(0%), PR 5例(11.4%), SD 23例(52.2%), PD 16例(36.4%), ORR为11.4%, DCR为63.6%, 中位PFS及中位OS分为3.5个月和10.2个月, 疗效与培美曲塞化疗组比较差异无统计学意义(ORR比较P=0.059, DCR比较P=0.160, PFS比较P=0.396, OS比较P=0.499)。本研究结果显示, CR 0例(0%), PR 7例(31.8%), SD 9例(40.9%), PD 6例(27.3%), ORR为31.8%, DCR为72.7%, 中位PFS及中位OS分为6个月和11个月。本研究治疗效果优于吕丽英等[14]的研究, 考虑主要原因为研究患者疾病分期不同, 本研究患者包含Ⅲ B和Ⅳ期, 吕丽英等[14]的研究患者均为Ⅳ期。本研究中不同临床特征比较结果显示, 二线增加剂量埃克替尼治疗, 女性比男性中位OS长, 无吸烟史患者较有吸烟史患者中位OS长, 与以往推荐剂量埃克替尼治疗研究结果相符[15], 其余不同临床特征间比较, 差异均无统计学意义(均P>0.05), 不除外样本量较小等因素影响。
大量研究显示, 盐酸埃克替尼安全性较高[12, 15]。CONVINCE研究显示, 埃克替尼(125 mg, 3次/d口服)一线治疗晚期肺腺癌患者常见的不良反应是皮疹(14.9%)、腹泻(7.4%)、白细胞减少(7.4%)、谷草转氨酶升高(8.1%)和谷丙转氨酶升高(6.8%), 其中3或4级不良反应发生率为4.7%, 包括转氨酶升高和白细胞减少[15]。研究显示, 26例增加剂量埃克替尼治疗晚期肺腺癌患者中92.3%发生过≥ 1次不良反应, 皮疹(61.5%)、腹泻(23.1%)和口腔溃疡(11.5%)是最常见的不良反应, 在500 mg 3次/d和625 mg 3次/d两组中共3例(7.7%)发生3级不良反应, 2例为皮疹, 1例为手足综合征[12]。吕丽英等[14]研究盐酸埃克替尼加量组的患者常见的不良反应有皮疹7例(15.9%)、骨髓抑制3例(6.8%)、脱发3例(6.8%)、消化道反应3例(6.8%)和转氨酶升高3例(6.8%)等, 发生≥ 3级不良反应8例(18.2%), 不良反应对症治疗后均可缓解。本研究结果显示, 出现皮疹14例(63.6%)、食欲下降10例(45.4%)、腹泻7例(31.8%)、转氨酶升高3例(13.6%)、白细胞减少2例(9.1%)和口腔溃疡2例(9.1%), 以上不良反应均为1~2级, 无≥ 3级不良反应出现。虽然盐酸埃克替尼加量治疗比常规剂量不良反应发生率增高, 但严重不良反应仍较少, 经治疗后多可逆, 仍有较好的安全性。
综上所述, 本研究显示, 盐酸埃克替尼加量治疗有望成为一线EGFR-TKI治疗耐药的NSCLC患者的选择方案。但本研究存在单中心回顾性研究、样本量较少、缺少对照组资料和因样本量限制未能进行不同剂量组间比较等不足, 仍需多中心大样本前瞻性研究进一步进行疗效及安全性评估。
| [1] |
Planchard D, Popat S, Kerr K, et al. Metastatic nonsmall cell lung cancer:ESMO clinical practice guidelines for diagnosis, treatment and follow-up[J]. Ann Oncol, 2018, 29(4): 192-237. |
| [2] |
Chen W, Zheng R, Baade PD, et al. Cancer statistics in China 2015[J]. CA Cancer J Clin, 2016, 66(2): 115-132. DOI:10.3322/caac.21338 |
| [3] |
张萍, 武晓楠, 聂鑫, 等. 晚期肺腺癌EGFR基因突变及临床特征分析[J]. 实用肿瘤杂志, 2018, 33(2): 150-153. |
| [4] |
National Comprehensive Cancer Network. NCCN clinical practice guidelines in oncology-non-small cell lung cancer(2019 version 2)[EB/OL]. (2018-11-21)[2019-2-10].http://www.nccn.org.
|
| [5] |
Xu JP, Liu XY, Yang S, et al. Apatinib plus icotinib in treating advanced non-small cell lung cancer after icotinib treatment failure:a retrospective study[J]. Oncotargets Ther, 2017(10): 4989-4995. |
| [6] |
Eisenhauer EA, Therasse P, Bogaerts J, et al. New response evaluation criteria in solid tumours:revised RECIST guideline (version 1.1)[J]. Eur J Cancer, 2009, 45(2): 228-247. DOI:10.1016/j.ejca.2008.10.026 |
| [7] |
Zago G, Muller M, van den Heuvel M, et al. New targeted treatments for non-small-cell lung cancer-role of nivolumab[J]. Biologics, 2016, 10: 103-117. |
| [8] |
石远凯, 孙燕, 丁翠敏, 等. 中国埃克替尼治疗非小细胞肺癌专家共识[J]. 中国肺癌杂志, 2016, 19(7): 489-493. |
| [9] |
Deng QF, Xie BX, Wu LL, et al. Competitive evolution of NSCLC tumor clones and the drug resistance mechanism of first-generation EGFR-TKIs in Chinese NSCLC patients[J]. Heliyon, 2018, 4(12): e01031. DOI:10.1016/j.heliyon.2018.e01031 |
| [10] |
Wang HP, Zhang L, Si XY, et al. Re-biopsy status among Chinese non-small-cell lung cancer patients who progressed after icotinib therapy[J]. Oncotargets Ther, 2018, 11: 7513-7519. DOI:10.2147/OTT.S174075 |
| [11] |
郁佳, 吴凤英, 张世佳, 等. EGFR突变晚期NSCLC患者MDT诊治报道[J]. 实用肿瘤杂志, 2017, 32(4): 291-295. |
| [12] |
Liu J, Wu LH, Wu GL, et al. A phaseⅠstudy of the safety and pharmacokinetics of higher-dose icotinib in patients with advanced non-small cell lung cancer[J]. Oncologist, 2016, 21(11): 1294-1295. DOI:10.1634/theoncologist.2016-0256 |
| [13] |
Ni J, Zhang L. Evaluation of three small molecular drugs for targeted therapy to treat non-small cell lung cancer[J]. Chin Med J, 2016, 129(3): 332-340. DOI:10.4103/0366-6999.174484 |
| [14] |
吕丽英, 王留兴.盐酸埃克替尼加量治疗晚期肺腺癌的临床研究[D].郑州: 郑州大学第一附属医院, 2018.
|
| [15] |
Shi YK, Wang L, Han BH, et al. First-line icotinib versus cisplatin/pemetrexed plus pemetrexed maintenance therapy for patients with advanced EGFR mutation-positive lung adenocarcinoma (CONVINCE):a phase 3, open-label, randomized study[J]. Ann Oncol, 2017, 10(28): 2443-2450. |
 2020, Vol. 35
2020, Vol. 35
