文章信息
- 王蕊, 杜芸, 纪晓坤, 吴娟, 吴家宁, 赵银环, 王珩
- Wang Rui, Du Yun, Ji Xiaokun, Wu Juan, Wu Jianing, Zhao Yinhuan, Wang Heng
- EUS-FNA细胞学在诊断胰腺神经内分泌肿瘤中的应用价值
- Application of EUS-FNA cytology in diagnosis of pancreatic neuroendocrine tumors
- 实用肿瘤杂志, 2021, 36(5): 435-439
- Journal of Practical Oncology, 2021, 36(5): 435-439
基金项目
- 河北省卫生厅医学科学研究重点课题计划(20190711)
-
通信作者
- 杜芸,E-mail:aijianzhongxin@163.com
-
文章历史
- 收稿日期:2020-08-03
胰腺神经内分泌肿瘤(pancreatic neuroendocrine tumors,PanNETs)是一种起源于胰腺内多功能胃肠弥散性神经内分泌干细胞的少见肿瘤[1],占胰腺肿瘤的1%~5%[2]。PanNETs常根据是否存在与激素分泌过多相关的特定临床症状而分为功能性或非功能性,非功能的肿瘤占43%~90%[3],且非功能PanNETs的发病率不断上升[4],随着近年来影像学检查技术及介入治疗技术的提高,细胞学诊断的作用越来越受到重视。PanNETs影像学容易误诊,细胞学诊断有一定难度。本文根据组织病理学分级探讨PanNETs的细胞学特点,旨在提高细胞病理学的诊断正确率。
1 资料与方法 1.1 一般资料收集河北医科大学第四医院2017年9月至2020年1月收治的胰腺穿刺患者125例,其中12例术后组织病理诊断为神经内分泌肿瘤。这12例中1例细胞数量过少,无法满足诊断要求,排除在本次观察之外。剩余11例患者的涂片,均褪色后行免疫细胞化学染色。
1.2 标本的采集及处理超声内镜引导下细针穿刺(endoscopic ultrasound guided fine needle aspiration,EUS-FNA)操作方法:超声内镜采用环扫型电子超声内镜(日本奥林巴斯株式会社奥林巴斯GF-UCT240),穿刺针为超声内镜专用穿刺针(日本奥林巴斯株式会社Wilson-COOK 22G)。EUS操作由内镜专家完成。现场Diff-Quik染色观察以确保标本足够。95%乙醇中固定涂片,HE法染色。对患者进行≥24 h的操作后观察。所有患者均签署知情同意书。本次研究得到本院伦理委员会的批准。
1.3 免疫细胞化学染色PanNETs的细胞学涂片的必选抗体为突触素(Synaptophysin,Syn)、嗜铬素A(Chromogranin,CgA)、Ki-67和CD56抗体;可选抗体为β-catenin、白细胞共同抗原(leukocyte common antigen,LCA)、CD56和抗胰蛋白酶(α-1-antichymotrysin,AACT)等,所用抗体及血清均购自福建迈新生物有限公司。本次观察的细胞学涂片,均染色封固后,显微镜下观察后褪色再行免疫细胞化学染色,可以将细胞涂片分成若干区进行不同抗体的染色。主要步骤:移去掉盖玻片(时间久可烤箱加热后去掉盖玻片),放入二甲苯内脱树胶至完全脱胶。梯度乙醇脱水后,1%盐酸乙醇溶液内褪色3 min,蒸馏水水洗3 min晾干备用。免疫细胞化学染色步骤:3%过氧化氢溶液15 min,蒸馏水水洗3 min,枸橼酸盐缓冲液高压修复1.5 min,冷却至室温,磷酸盐缓冲盐溶液(phosphate buffered saline,PBS)冲洗,羊血清封闭抗原37℃孵育15 min,弃掉多余血清后,滴加一抗4℃过夜或37℃室温2 h,PBS冲洗,滴加生物素标记二抗,常温孵育15~20 min,PBS冲洗3 min 3次,滴加二氨基联苯胺(3, 3, -diaminobenzidine,DAB)液显色,显微镜下观察显色适当后放入蒸馏水中终止反应,苏木精对比染色3 min,梯度乙醇脱水,中性树胶封固。
1.4 统计学分析采用SPSS19.0统计学软件进行数据分析。细胞学标本与术后组织标本中Ki-67水平分析采用Pearson积矩相关分析。以P < 0.05为差异具有统计学意义。
2 结果 2.1 临床特征11例患者中,男性4例,女性7例;年龄28~64岁, 中位年龄50岁(表 1)。患者均经CT检查提示胰腺占位,其中胰头占位3例,胰颈2例,体尾6例,大小从直径1.0 cm到6.5 cm×6 cm×3.5 cm,行EUS-FNA细胞学检测后均行手术切除,术后组织病理检查结果根据世界卫生组织(World Health Organization,WHO)分类[4],G1级3例,G2级7例,G3级1例。功能性PanNETs 5例(45.5%),4例胰岛素瘤,1例胰高血糖素瘤。
| 例序 | 性别 | 年龄(岁) | 部位 | 大小 | 细胞标本Ki-67表达(%) | 组织标本Ki-67表达(%) | 肿瘤分级(WHO) | 肿瘤性质 |
| 1 | 男性 | 47 | 头 | 6.5 cm×6 cm×3.5 cm | 4 | 3 | G2 | 非功能性肿瘤 |
| 2 | 男性 | 58 | 体尾 | 4 cm×3 cm×3 cm | 5 | 3 | G2 | 非功能性肿瘤 |
| 3 | 女性 | 50 | 颈 | 3 cm×3 cm×2 cm | 3 | 3 | G2 | 胰岛素瘤 |
| 4 | 女性 | 61 | 头 | 3 cm×2 cm×2 cm | 25 | 20 | G3 | 非功能性肿瘤 |
| 5 | 女性 | 49 | 体 | 直径1.5 cm | 4 | 3 | G2 | 胰岛素瘤 |
| 6 | 女性 | 64 | 头 | 直径1.0 cm | 2 | 2 | G1 | 胰岛素瘤 |
| 7 | 女性 | 28 | 体 | 3.5 cm×3 cm×2.5 cm | 1 | 1 | G1 | 胰岛素瘤 |
| 8 | 男性 | 54 | 体 | 2 cm×1.8 cm×1.8 cm | 8 | 10 | G2 | 非功能性肿瘤 |
| 9 | 女性 | 48 | 体尾 | 5.5 cm×3.8 cm | 3 | 2 | G1 | 非功能性肿瘤 |
| 10 | 女性 | 64 | 颈 | 3 cm×2 cm×2 cm | 12 | 10 | G2 | 非功能性肿瘤 |
| 11 | 男性 | 45 | 体 | 2.2 cm×2 cm×2 cm | 4 | 5 | G2 | 胰高血糖素瘤 |
| 注WHO:世界卫生组织(World Health Organization) | ||||||||
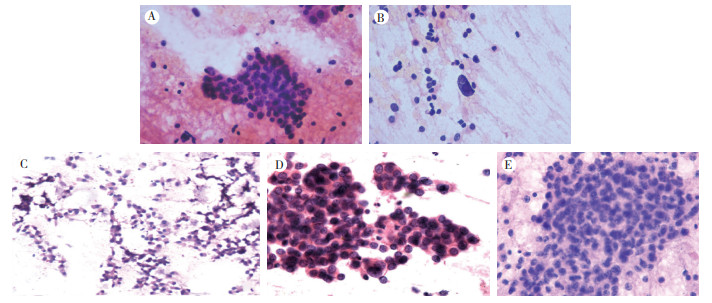
11例细胞学涂片均为血性背景,细胞量丰富,细胞成团或散在分布,以散在细胞为主,细胞形态多样,可呈柱状上皮样、单核细胞样、浆细胞样和淋巴细胞样细胞。细胞核呈圆形或椭圆形,染色质粗颗粒样呈“胡椒盐”样,核膜增厚。胞质中等或偏少,3例G1级的肿瘤细胞学涂片细胞大小较为一致,细胞核大小约为正常导管上皮细胞的2倍,细胞成团排列,或散在排列,偶见增大的裸核细胞。7例G2级肿瘤细胞学涂片,细胞形态可呈单核细胞样、横纹肌细胞样和柱状上皮样,散在细胞明显多于成团细胞,且巨核细胞更为常见,成团细胞常常排列松散,1例可见丰富细胞围绕纤维血管轴心,呈细长乳头状结构。本次仅有1例G3级肿瘤,多数表现为弥散分布的裸核细胞,细胞大小较为一致,染色质粗糙(图 1)。
|
| 注 A:G1级PanNETs细胞学涂片显示细胞成团及散在分布(HE×400);B:G1级PanNETs细胞学涂片可见巨大的裸核细胞图(HE×400);C:G2级PanNETs细胞学涂片可见柱状上皮样细胞(HE×200);D:G2级PanNETs细胞学涂片显示细胞松散排列成团状(HE×400);E:G3级PanNETs细胞学涂片中细胞呈裸核样散在分布(HE×400) 图 1 胰腺神经内分泌肿瘤细胞学涂片 Fig.1 Cytological smears of pancreatic neuroendocrine tumors |
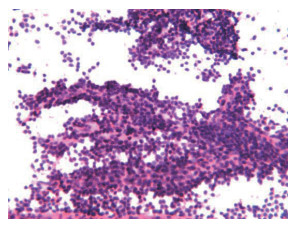
本次11例PanNETs的细胞学诊断中1例诊断为胰腺实性假乳头状瘤,镜下可见大量的纤维血管束,肿瘤细胞围绕纤维血管排列,形成乳头状结构或条索状结构(图 2)。
|
| 注 纤维血管丰富,细胞围绕纤维血管形成细长乳头结构 图 2 1例胰腺神经内分泌肿瘤误诊为实性假乳头状瘤的细胞学涂片(HE× 200) Fig.2 Cytological smear of a pancreatic neuroendocrine tumors misdiagnosed as the pancreatic solid pseudopapilloma |
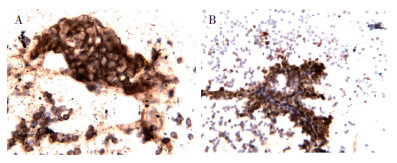
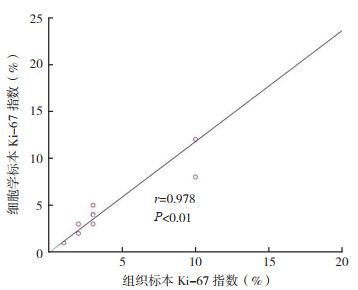
PanNETs细胞学瘤细胞Syn(11/11)、CgA(10/11)及CD56(11/11)均阳性,Ki-67增殖指数1%~25%,其表达与术后组织病理表达相近。11例免疫细胞化学染色只有1例CgA阴性,且此例术后的组织化学染色也是阴性。细胞学误诊为实性假乳头状瘤的1例PanNETs,免疫细胞化学染色β-catenin及Syn等神经内分泌肿瘤标记均表达强阳性(图 3)。此外,细胞学标本与组织学标本的Ki-67指数进行相关分析,两者的Pearson积矩相关系数为0.978(P < 0.01,图 4)。
|
| 注 A:免疫细胞化学染色β-catenin阳性(EliVision×400);B:免疫细胞化学染色Syn阳性(EliVision×200) 图 3 误诊为胰腺实性假乳头状瘤的神经内分泌肿瘤的免疫细胞化学染色 Fig.3 Immunocytochemical staining of a neuroendocrine tumor misdiagnosed as a solid pseudopapilloma of the pancreas |
|
| 图 4 胰腺神经内分泌肿瘤细胞学标本及组织学标本中Ki-67表达的相关性分析 Fig.4 Correlation analysis of Ki-67 expression in cytological and histological specimens of pancreatic neuroendocrine tumors |
WHO在2010年提出根据Ki-67指数和有丝分裂数对PanNETs进行分级分类,同时提出EUS-FNA标本不适合诊断。但是,近年来有研究表明,EUS-FNA获得的标本能很好地预测PanNETs患者的分级分类和预后[5-7]。本研究将细胞学标本与组织学标本Ki-67指数进行比较,表明细胞学标本与组织学标本的Ki-67表达有很好的相关性,细胞学标本的Ki-67对于PanNETs的分级可能有很好的预见性。
通过对不同分级的PanNETs细胞学形态的观察发现,除了分级越高细胞异型性越大以外,分级越高细胞之间越分散是PanNETs细胞学形态的另一个主要特点。PanNETs G1级的细胞学形态相对规则,散在细胞核成团细胞比例相当,细胞核粗颗粒状,胞质适中,裸核细胞可见;G2级细胞学形态差异较大,细胞多分散排列,核染色质粗颗粒状,可见细小核仁,瘤巨细胞及裸核细胞可见。本次观察的1例G3级PanNET,细胞成裸核样分布。PanNETs细胞学诊断主要与胰腺导管腺癌、腺泡细胞癌和胰腺实性假乳头状肿瘤进行鉴别。导管腺癌的细胞异型性更大,常常排列成细胞紧密排列的团状结构,PanNETs的细胞多分散排列,即使成团排列的细胞,细胞之间也较为松散,导管腺癌细胞还会有空泡、核膜增厚和核仁明显等腺癌的特点,易于与PanNETs鉴别。腺泡细胞癌较少见,胞质呈空泡状或细颗粒状,核染色质致密,细胞常常会形成不完整的腺泡样细胞团,这种腺泡结构有助于鉴别。实性假乳头状瘤的细胞学涂片常表现为数层肿瘤细胞黏附于纤维血管结缔组织轴心上。核圆形或卵圆形,淡染,有时有纵向的沟及拉长的细胞质突起。胞质空泡状或颗粒状,可有浆细胞样外观,背景可见多量单个散在的瘤细胞,常呈裸核样[8]。本例G3级PanNETs要与淋巴瘤进行鉴别,本例染色质较淋巴瘤细胞更粗糙,粗颗粒染色质较淋巴瘤更明显。此外,免疫细胞化学染色能进一步进行鉴别诊断。
PanNETs细胞多数较为丰富,因此涂片往往能够满足褪色后免疫细胞化学染色的需要。本研究11例细胞学涂片的免疫细胞化学染色诊断中,Syn与CD56均全部表达,而仅有CgA抗体在1例细胞学标本及组织学标本中均未见表达。因此,当遇到细胞学涂片不典型时,加行免疫细胞化学染色可以对PanNETs作出确定诊断。本次细胞学观察中的诊断为实性假乳头状瘤1例,HE染色镜下呈现典型的细胞围绕纤维血管轴心分布的表现,免疫细胞化学染色β-catenin表达弥漫强阳性,Syn、CD56和CgA均表达强阳性等。β-catenin在胰腺实性假乳头状瘤的肿瘤细胞上表达在胞核及胞质,PanNETs表达在胞膜上。与以往诊断的胰腺实性假乳头状瘤的细胞学涂片比较发现,两者的细胞学涂片存在3个主要区别点:血管纤维轴心外的细胞层的细胞分布上,实性假乳头状瘤在同一轴心上细胞层的分布均匀,而PanNETs细胞层薄厚不均;实性假乳头状瘤散在分布的细胞往往呈现裸核,而PanNETs的散在细胞与附着在血管轴心周围的细胞比较较为一致;胰腺实性假乳头状瘤的细胞核较PanNETs更细腻。
综上所述,常规细胞病理学结合免疫细胞化学染色诊断,可以初步诊断PanNETs。但是,当PanNETs细胞学表现类似实性假乳头状瘤时,细胞学涂片的诊断存在一定局限性。此外,还需要增加PanNETs观察例数(尤其是G3级),进一步探讨PanNETs的细胞学特点,为其术前诊断提供可靠的依据。
| [1] |
Pettersson O, Fröss-Baron K, Crona J, et al. Tumor contrast-enhancement for monitoring of PRRT 177Lu-DOTATATE in pancreatic neuroendocrine tumor patients[J]. Front Oncol, 2020, 10: 193. DOI:10.3389/fonc.2020.00193 |
| [2] |
Fang GM, Shi J. A clinicopathologic and molecular update of pancreatic neuroendocrine neo-plasms with a focus on the new World Health Organization classification[J]. Arch Pathol Lab Med, 2019, 143(11): 1317-1326. DOI:10.5858/arpa.2019-0338-RA |
| [3] |
Ishida H, Lam AK. Pancreatic neuroendocrine neoplasms: the latest surgical and medical treatment strategies based on the current World Health Organization classification[J]. Crit Rev Oncol Hematol, 2020, 145: 102835. DOI:10.1016/j.critrevonc.2019.102835 |
| [4] |
Klimstra DS, Arnold R, Capella C, et al. World Health Organization classification of tumours of the digestive system[M]. Lyon: IARC Press, 2010: 322-326.
|
| [5] |
Hasegawa T, Yamao K, Hijioka S, et al. Evaluation of Ki- 67 index in EUS-FNA specimens for the assessment of malignancy risk in pancreatic neuroendocrine tumors[J]. Endoscopy, 2014, 46(1): 32-38. |
| [6] |
Farrell JM, Pang JC, Kim GE, et al. Pancreatic neuroendocrine tumors: accurate grading with Ki-67 index on fine-needle aspiration specimens using the WHO 2010/ ENETS criteria[J]. Cancer Cytopathol, 2014, 122(10): 770-778. DOI:10.1002/cncy.21457 |
| [7] |
Weynand B, Borbath Ⅰ, Bernard V, et al. Pancreatic neuroendocrine tumour grading on endo-scopic ultrasound-guided fine needle aspiration: high reproducibility and inter-observer agree-ment of the Ki-67 labelling index[J]. Cytopathology, 2014, 25(6): 389-395. |
| [8] |
Jahangir, S, Lo ya, A, Siddiqui, M T, et al. Accuracy of diagnosis of solid pseudopapillary tumor of the pancreas on fine needle aspiration: A multi-institution experience of ten cases[J]. Cytojournal, 2015, 12: 29. DOI:10.4103/1742-6413.171140 |
 2021, Vol. 36
2021, Vol. 36


