文章信息
- 彭小波, 苏晓菊, 王一然, 王斌, 张颖一, 湛先保
- Peng Xiaobo, Su Xiaoju, Wang Yiran, Wang Bin, Zhang Yingyi, Zhan Xianbao
- microRNA-122抑制胰腺癌细胞增殖、迁移和侵袭
- MicroRNA-122 inhibits proliferation, migration and invasion of pancreatic cancer cells
- 实用肿瘤杂志, 2021, 36(1): 23-27
- Journal of Practical Oncology, 2021, 36(1): 23-27
基金项目
- 国家自然科学基金(81672892);上海市抗癌协会“雏鹰”项目(SACA-CY1C12)
-
通信作者
- 湛先保,E-mail: zhanxianbao@126.com
-
文章历史
- 收稿日期:2020-03-06
2. 海军军医大学长海医院消化科,上海 200433
2. Department of Gastroenterology, Changhai Hospital, the Naval Military Medical University, Shanghai 200433, China
胰腺癌是一种高度恶性的肿瘤,全世界每年死亡 > 20万例[1]。2017年美国癌症协会报告胰腺癌位列癌症相关死亡的第4位,新发胰腺癌达到5.36万例,死亡病例4.31万例, 预计2030年胰腺癌死亡将位列癌症相关死亡的第2位[2-3]。中国国家癌症中心的统计数据显示,2000年至2011年胰腺癌发病率与死亡率逐渐上升,2015年全国男性和女性胰腺癌发病例数分别为5.22万和3.79万例,死亡例数则分别为4.56万例和3.38万例[4]。胰腺癌恶性程度高、早期诊断难且生存率低。因此,如何提高胰腺癌早期诊断和治疗效果是目前迫切需要攻克的难题。
MicroRNA (miRNA)是一类分布广泛的小的非编码蛋白质的RNA,通过作用于下游靶基因调控肿瘤细胞生物学功能,在恶性肿瘤的发生和发展过程中发挥重要的作用[5-7]。研究表明,miRNA可以抑制重要的肿瘤相关基因的表达,在癌症的诊断和治疗中起重要作用[8]。
胰腺癌的发生和发展是涉及到miRNA在内多种癌基因和抑癌基因参与的过程[9-11],然而,国内未见microRNA-122(miR-122)在胰腺癌中作用的报道。因此,本研究拟明确miR-122在胰腺癌中的表达情况及对胰腺癌细胞增殖、迁移及侵袭的作用。
1 材料与方法 1.1 资料和细胞收集2017年10月至2018年3月在海军军医大学长海医院普外科治疗的20例胰腺癌患者的手术标本,所有标本均经病理组织学确诊。其中男性13例,女性7例;年龄48~71岁,平均59岁。术前签署同意书,患者术后的病理标本用于医学研究均获得患者同意。患者接受手术切除前无放化疗病史。人源正常胰腺导管上皮细胞株(HPDE)和胰腺癌细胞株(ASPC1、PANC1、MP和SW1990)由上海生命科学院健康营养所詹丽杏研究员课题组保藏和提供。HPDE、PANC1、MP和SW1990细胞培养条件:DMEM(美国Hyclone公司)+10%胎牛血清(fetal bovine serum,FBS;美国BI公司)+1%青-链霉素双抗(美国Gibco公司);ASPC1细胞培养条件:RPMI1640(美国Hyclone公司)+10%FBS+1%青-链霉素双抗。于37℃5% CO2的细胞培养箱中培养。
1.2 miR-122模拟类似物及阴性对照瞬时转染胰腺癌细胞5 nmol的miR-122模拟类似物和阴性对照干粉(上海吉玛制药技术有限公司)先常温10 000 r/min离心1 min,然后用250 μL无酶水稀释成20 μmol/L的储存液,分装储存于-20℃冰箱,避免反复冻融。依据生产商的说明,利用Lipofectamine 2000(美国Life Technologies公司)转染胰腺癌细胞。
1.3 RT-qPCR检测miR-122表达量常规提取胰腺癌组织、癌旁组织和细胞中的RNA,用miRNA反转录试剂盒(日本Takara公司)合成cDNA。用SYBR Premix Ex TaqTM试剂盒(日本Takara公司)进行实时定量PCR。采用U6作为内参照,运用ABI7900实时荧光定量PCR仪自带软件分析,获得扩增产物Ct值,Ct为反应的实时荧光强度达到设定的阈值时所经过的扩增循环数,结果采用2-△△Ct法分析mRNA的相对表达量。miR-122上游引物5’- CGGGCTGGAGTGTGACAATG -3’,下游引物5’- CAGCCACAAAAGAGCACAAT -3’;内参U6上游引物5’-CTCGCTTCGGCAGCACA-3’,下游引物5’-AACGCTTCACGAATTTGCGT-3’。miR-122和内参U6的PCR引物及反转录引物由上海捷瑞生物工程有限公司合成。PCR扩增miRNA反应条件为:95℃预变性5 min;95℃变性10 s,60℃退火30s,40个循环;最后72℃延伸8 min,4℃保存。实验重复3次。
1.4 MTT法检测细胞增殖能力取对数生长期细胞,调整细胞密度为5×104/mL,在96孔板每孔中加入200 μL细胞悬液,每组设5个复孔,铺4块96孔板作为4个时间点(24、48、72和96 h)的检测,细胞接种于96孔板中心。分别在培养24、48、72和96 h后每孔加入10 μL MTT溶液(5 mg/mL,美国Sigma公司), 继续培养4 h, 吸弃96孔板内培养液终止培养,每孔加入100 μL DMSO(美国Sigma公司),37℃培养箱继续孵育30 min,在酶联免疫检测仪490 nm测量各孔吸光度值。
1.5 伤口愈合实验检测细胞迁移能力将预先转染成功的胰腺癌细胞以3×105个细胞/孔的量铺到6孔板中,保证细胞过夜能够生长密度达到90%。用200 μL枪头在每孔中进行垂直与横线划痕。PBS清洗3次去掉划痕后脱落漂浮的细胞,加入3 mL无血清空白培养液,放置于细胞培养箱中培养24 h。取细胞划痕后0 h及24 h进行拍照,计算细胞间距离的均值分析迁移能力。
1.6 Transwell检测细胞侵袭能力Matrigel胶(美国BD Sciences公司)置于4℃过夜预冷。取100 μL Matrigel胶加入BD小室(美国Corning公司)上室,放入37℃培养箱孵育2 h。将BD小室置于24孔板中,小室上部加入200 μL细胞(2×105/mL)。小室下室加入600 μL含有10%FBS的条件培养液。培养24 h后PBS漂洗3遍,4%多聚甲醇(美国Sigma公司)固定30 min,0.1%结晶紫溶液染色30 min,PBS漂净。用棉签拭去小室上室内细胞,小室底部干燥后,显微镜拍照计数。
1.7 统计学分析采用SPSS 21.0软件进行统计学分析,使用GraphPad Prism 5.0进行图片编辑和处理。实验数据先进行正态性检验和方差齐性检验,不符合正态性检验的数据采用非参数方法分析,符合正态性检验的数据;计量资料的两组间比较差异采用非配对t检验,单因素多组比较采用单因素方差分析。以P < 0.05为差异具有统计学意义。
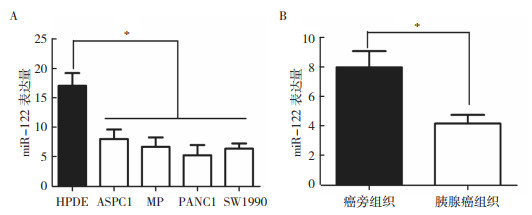
2 结果 2.1 miR-122在胰腺癌细胞和胰腺癌组织中低表达利用RT-qPCR方法检测4种胰腺癌细胞AsPC1、PANC1、MP和SW1990中miR-122表达水平显示,胰腺导管上皮HPDE细胞比较,4种胰腺癌细胞miR-122表达水平均下降(均P < 0.01,图 1A)。同时,在20例胰腺癌临床样本中检测miR-122的表达量,RT-qPCR结果显示与癌旁组织比较,胰腺癌组织中miR-122表达水平降低(P < 0.01,图 1B)。
|
| 注 A:miR-122在胰腺癌细胞中的表达量;B:miR-122在胰腺癌组织中的表达量;*P < 0.01 图 1 miR-122在胰腺癌细胞和组织中的表达量 Fig.1 The expression of miR-122 in the pancreatic cancer cell lines and tissues |
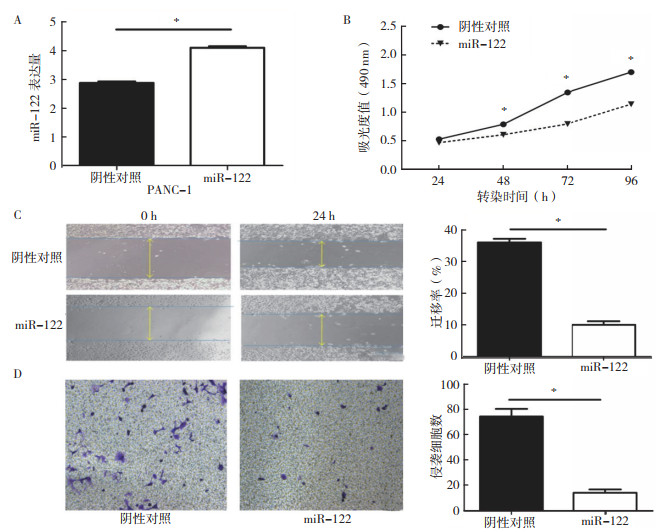
将miR-122模拟类似物和阴性对照瞬转PANC1细胞后48 h,通过RT-qPCR检测两组细胞中miR-122表达量显示,与阴性对照组比较,转染miR-122模拟类似物后miR-122表达量增加(P < 0.01),提示miR-122成功转入PANC1细胞,可用于后续细胞功能研究(图 2A)。PANC1细胞成功瞬转培养24 h后,MTT实验提示过表达miR-122培养48、72和96 h后PANC1细胞增殖能力被抑制(均P < 0.01,图 2B);伤口愈合实验结果显示过表达miR-122培养24 h后PANC1细胞迁移能力被抑制(均P < 0.01,图 2C);transwell侵袭实验结果显示过表达miR-122培养24 h后PANC1细胞侵袭能力被抑制(P < 0.01,图 2D)。
|
| 注 A:RT-qPCR验证miR-122模拟类似物瞬转PANC-1细胞效率;B:MTT实验结果;C:伤口愈合实验结果(×10);D:Transwell侵袭实验结果(×10);*P < 0.01 图 2 miR-122过表达抑制胰腺癌细胞增殖、迁移和侵袭能力 Fig.2 MiR-122 inhibits the proliferation, migration and invasion of pancreatic cancer cells |
肿瘤的发生和发展涉及多基因突变、多阶段和多因素过程。基因改变包括癌基因激活和抑癌基因失活,与癌基因激活比较,抑癌基因的失活在肿瘤发生与发展中起着更重要的作用。非编码RNA(尤其是miRNA)参与肿瘤的发生、发展、侵袭和转移等众多病理过程,因而受到学界越来越多的关注。miRNA是内源性单链小分子非编码RNA,成熟的miRNA具有调节基因表达活性的功能[12]。miRNA作为一种重要的转录后调控因子,广泛参与肿瘤相关基因调控,在肿瘤的诊断和治疗方面扮演重要角色,为肿瘤研究提供新思路。
前期本研究组通过分析癌症基因组图谱(The Cancer Genome Atlas, TCGA)数据库芯片中胰腺癌与正常胰腺组织的差异表达miRNA谱,发现与正常胰腺组织比较,在胰腺癌组织中筛选出多个差异表达miRNA,其中miR-122在癌组织中表达下调并在国内未见相关报道;利用4种胰腺癌细胞和20例胰腺癌组织验证miR-122的表达量变化发现,miR-122在4种胰腺癌细胞中的表达水平较正常胰腺导管上皮细胞降低。同时在20例胰腺导管腺癌临床样本中检测miR-122的表达,亦发现癌组织比癌旁组织中的miR-122表达水平低,提示胰腺癌的发生和发展可能与miR-122的下调相关,提示miR-122在胰腺癌中可能扮演抑癌基因角色。这与之前研究报道的miR-122表达量结果一致[13-15]。
进一步对miR-122在胰腺癌细胞中的生物学功能进行探讨,主要明确miR-122对胰腺癌的增殖、迁移和侵袭能力的作用。体外研究在PANC-1胰腺癌细胞中研究过表达miR-122后是否影响胰腺癌细胞的生物学功能,选择PANC-1细胞的原因在于前期检测胰腺癌细胞中的miR-122表达量时,发现在PANC-1细胞中miR-122表达水平最低。过表达PANC-1细胞中的miR-122表达水平后,能够抑制PANC-1细胞的增殖、迁移和侵袭的能力。这与之前miR-122在膀胱癌和乳腺癌中增殖、迁移和侵袭作用的报道结果一致[16-17]。在胰腺癌中发现反链碘甲状腺素脱碘酶3(iodothyronine deiodinase 3 opposite strand,DIO3OS)可直接与miR-122结合并抑制其表达,而miR-122在胰腺癌细胞中起抑癌作用[18]。miR-122-5p的过表达能够通过下调胰腺导管腺癌(pancreatic ductal adenocarcinoma,PDAC)中细胞周期蛋白G1(cell cyclin G1,CCNG1)的表达,起到抑制细胞的增殖、迁移、侵袭和上皮间充质转化(epithelial mesenchymal transition,EMT)[19]。这些与本研究结果是一致的,提示miR-122-5p可能是PDAC的治疗靶点。
miRNA可通过与靶基因结合,进而对其靶基因表达实现负调控而发挥作用。因此,在miRNA的研究中,对miRNA靶基因的预测及验证在整个miRNA研究中起着非常重要的作用。本研究发现,胰腺癌中miR-122呈现低水平表达,同时过表达miR-122能够抑制胰腺癌细胞的生物学功能,包括增殖、迁移和侵袭能力。本研究组将进一步预测和验证miR-122抑制胰腺癌生物学功能的靶基因,同时体内研究miR-122对胰腺癌增殖和侵袭生物学功能的影响。
| [1] |
Bray F, Ferlay J, Soerjomataram I, et al. Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J]. CA Cancer J Clin, 2018, 68(6): 394-424. DOI:10.3322/caac.21492 |
| [2] |
Smith RA, Andrews KS, Brooks D, et al. Cancer screening in the United States, 2017: a reviewof current American Cancer Society guidelines and current issues in cancer screening[J]. CA Cancer J Clin, 2017, 67(2): 100-121. DOI:10.3322/caac.21392 |
| [3] |
Siegel R, Miller K, Jemal A. Cancer statistics, 2017[J]. CA Cancer J Clin, 2017, 67(1): 7-30. DOI:10.3322/caac.21387 |
| [4] |
Chen W, Zheng R, Baade P, et al. Cancer statistics in China, 2015[J]. CA Cancer J Clin, 2016, 66(2): 115-132. DOI:10.3322/caac.21338 |
| [5] |
胡艳, 黄智平, 周维, 等. miR-605-3p通过靶向ZIK1抑制肝细胞癌迁移和侵袭[J]. 实用肿瘤杂志, 2020, 35(1): 30-36. |
| [6] |
Ma X, Feng J, Lu M, et al. MicroRNA-501-5p promotes cell proliferation and migration in gastric cancer by down-regulating LPAR1[J]. J Cell Biochem, 2020, 121(2): 1911-1922. DOI:10.1002/jcb.29426 |
| [7] |
Ye J, Xie W, Zuo Y, et al. MicroRNA-496 suppresses tumor cell proliferation by targeting BDNF in osteosarcoma[J]. Exp Ther Med, 2020, 19(2): 1425-1431. |
| [8] |
Lu J, Getz G, Miska EA, et al. MicroRNA expression profiles classify human cancers[J]. Nature, 2005, 435(7043): 834-838. DOI:10.1038/nature03702 |
| [9] |
Gurbuz N, Ozpol ATB. MicroRNA-based targeted therapeutics in pancreatic cancer[J]. Anticancer Res, 2019, 39(2): 529-532. DOI:10.21873/anticanres.13144 |
| [10] |
Zhang GF, Zhong JM, Lin L, et al. MiR-19 enhances pancreatic cancer progression by targeting PTEN through PI3K/AKT signaling pathway[J]. Eur Rev Med Pharmacol Sci, 2020, 24(3): 1098-1107. |
| [11] |
Li M, Li T, Ma W, et al. MicroRNA-608 promotes apoptosis via BRD4 downregulation in pancreatic ductal adenocarcinoma[J]. Oncol Lett, 2020, 19(2): 1418-1426. |
| [12] |
Bartel DP. microRNAs: genomics, biogenesis, mechanism and function[J]. Cell, 2004, 116(2): 281-297. DOI:10.1016/S0092-8674(04)00045-5 |
| [13] |
Jin Y, Wang J, Han J, et al. MiR-122 inhibits epithe-lialmesenchymal transition inhepatocellular carcinoma by targeting Snail1 and Snail2 and suppressing WNT/β-cadherin signaling pathway[J]. Exp Cell Res, 2017, 360(2): 210-217. DOI:10.1016/j.yexcr.2017.09.010 |
| [14] |
Qin H, Sha J, Jiang C, et al. miR-122 inhibits metastasis and epithelial mesenchymal transition of non-small-cell lung cancer cells[J]. OncoTargets Ther, 2015, 8(10): 3175-3184. |
| [15] |
Lu W, Zhang Y, Zhou L, et al. miR-122 inhibits cancer cell malignancy by targeting PKM2 in gall bladder carcinoma[J]. Tumor Biol, 2016, 37(11): 15615-15625. |
| [16] |
Wang Y, Xing Q, Liu X, et al. MiR-122 targets VEGFC in bladder cancer to inhibit tumor growth and angiogenesis[J]. Am J Transl Res, 2016, 8(7): 3056-3066. |
| [17] |
Ergun S, Ulasli M, Ziyagci Y, et al. The association of the expression of miR-122-5p and its target ADAM10 with human breast cancer[J]. Mol Biol Rep, 2015, 42(2): 497-505. DOI:10.1007/s11033-014-3793-2 |
| [18] |
Cui K, Jin S, Du Y, et al. Long noncoding RNA DIO3OS interacts with miR-122 to promote proliferation and invasion of pancreatic cancer cells through upregulating ALDOA[J]. Cancer Cell Int, 2019, 19(7): 202. DOI:10.1186/s12935-019-0922-y |
| [19] |
Dai C, Zhang Y, Xu Z, et al. MicroRNA-122-5p inhibits cell proliferation, migration and invasion by targeting CCNG1 in pancreatic ductal adenocarcinoma[J]. Cancer Cell Int, 2020, 20(3): 98. |
 2021, Vol. 36
2021, Vol. 36


