文章信息
- 刘芳欣, 王洲, 李健, 任永凤, 陈飞, 陆静, 许廷兰
- Liu Fangxin, Wang Zhou, Li Jian, Ren Yongfeng, Chen Fei, Lu Jing, Xu Tinglan
- 超声O-RADS分类联合超声造影及血清CA125和HE4检测诊断绝经后卵巢肿物的应用价值
- Application value of ultrasound O-RADS classification combined with contrast-enhanced ultrasound and serum CA125 and HE4 levels in diagnosis of postmenopausal ovarian masses
- 实用肿瘤杂志, 2023, 38(4): 392-397
- Journal of Practical Oncology, 2023, 38(4): 392-397
基金项目
- 安徽理工大学校级资助项目(QN2019137);亳州市人民医院院级科研项目(by2022050)
-
文章历史
- 收稿日期:2022-03-23
随着社会发展、人口老龄化、全民健康意识增强及检测技术的进步,绝经后妇女卵巢肿物检出率日益增多[1]。有报道称,卵巢肿物自40岁年龄组开始增加,并随着年龄增加,卵巢癌的发病率也逐渐增加[2]。据报道我国绝经后妇女卵巢肿物发生率约5%~17%[3]。但因女性绝经后生理特点的特殊性、妇科病史复杂多变以及卵巢肿物声像图表现缺乏特异性,其超声诊断有一定难度[4]。如何运用超声及超声新技术以及联合血清学检查提高卵巢肿物早期确诊率成为当下研究热点。卵巢-附件影像报告和数据系统(Ovarian-Adnexal Reporting and Data System,O-RADS)是2020年由美国放射学会提出的卵巢肿物分类诊断系统,包括卵巢附件肿瘤所有风险类别及对应管理方案,为诊断和管理卵巢附件良恶性肿瘤提供依据[5-6]。本研究旨在探讨超声0-RADS分类联合超声造影及血清糖类抗原125(carbohydrate antigen 125,CA125)、人附睾分泌蛋白4(human epididymis protein 4,HE4)在诊断绝经后卵巢肿物中的应用价值。
1 资料与方法 1.1 一般资料回顾性分析2021年1月至2022年3月在本院收治并经穿刺或手术病理证实的绝经后卵巢肿物患者76例,双侧卵巢肿物者病理性质相同且以O-RADS分类级别高者为研究对象,术前均行超声、超声造影及血清CA125和HE4检查。患者年龄44~86岁,(57.5±9.5)岁;绝经年限1~38年;临床表现: 35例无不适症状,仅在妇科体检时发现卵巢肿物,15例自扪及包块,20例腹痛且腹胀,3例阴道不规则流血,3例阴道分泌物增多。本研究经亳州市人民医院伦理委员会批准,均取得患者知情同意。
1.2 常规超声检查采用迈瑞Resona 6T彩色多普勒超声诊断仪(深圳迈瑞生物医疗电子股份有限公司),腹部凸阵探头(频率1.0~5.0 MHz),腔内探头(频率3.0~10.0 MHz)。采用经腹部及经阴道超声联合检查子宫、卵巢及附件区肿物情况,重点观察并记录卵巢肿物部位、大小、形态、边界、内部回声、有无乳头、囊壁、分隔、实性回声、有无血流及腹腔积液情况等,存储图像并进行O-RADS分类。O-RADS评价方法参照O-RADS超声风险分层与管理指南[5],依据声像图特征分0~5类共计6类:0类,受肠道气体、病变位置和大小等因素影响超声无法全面评估;1类,绝经前正常卵巢,包括≤3 cm的单纯性囊肿或黄体囊肿;2类,几乎可肯定的良性病变(恶性风险<1%),包括单纯性囊肿、囊内壁光滑的非单纯性单房囊肿及最大径<10 cm的典型良性囊肿;3类,恶性低风险病变(恶性风险1%~10%),包括O-RADS 2类中最大径≥10 cm的病变、内壁不规则且壁厚<3 mm的单房囊肿、内壁光滑且彩色血流评分(color score,CS)1~3分的多房囊肿(最大径<10 cm)以及实性或实性部分≥80%的病变(任意大小、外壁光滑且CS 1分);4类,中风险病变(恶性风险10%~50%),包括多房囊肿(最大径≥10 cm且CS 1~3分或任意大小且CS 4分)、有或无不规整分隔/内壁(厚<3 mm)、单房囊实性肿物(任意大小且0~3个乳头样突起)、多房囊实性肿物(任意大小且CS 1~2分)以及实性肿物(光滑、任意大小且CS 2~3分);5类:恶性高风险病变(恶性风险≥50%),包括单房囊肿(任意大小、≥4个乳头状突起且任意血流评分)、多房囊实性肿物(任意大小且CS 3~4分)、不规则的实性肿物以及合并或不合并腹膜结节的腹腔积液。O-RADS分类3~5类纳入彩色血流评分(1~4分):1分,无血流;2分,微量血流;3分,中等量血流;4分,大量血流。诊断标准:以O-RADS 0~3类判为良性,O-RADS 4~5类判为恶性[7]。
1.3 超声造影采用迈瑞Resona 6T彩色多普勒超声诊断仪,腔内探头(频率3.0~10.0 MHz),配有超声造影成像技术;造影切面选取肿瘤实性部分、厚壁囊肿壁和血流丰富区域,并显示部分子宫组织作对照;经左肘静脉团注2.5 mL SonoVue造影剂混悬液,连续观察造影过程并实时存储180 s。记录病灶内造影剂分布特征、病灶增强时间和病灶增强水平等。绘制时间-强度曲线(time-intensity curve,TIC)并计算始增时间、达峰时间和峰值强度等。诊断标准:造影时病灶呈较早增强、增强强度高于子宫肌层灌注强度且消退较快为恶性病变;造影时病灶内无增强或者呈均匀环状增强为良性病变[8]。
1.4 血清CA125和HE4检查采集患者空腹静脉血5 mL,离心,保留血清待检。采用迈瑞化学发光检测系统CL-6000i(深圳迈瑞生物医疗电子股份有限公司),使用化学发光法测定血清CA125和HE4水平,所有检测流程严格按照仪器操作规范及配套试剂盒说明执行。参考试剂说明,诊断标准:CA125≥35 U/mL,HE4测值依据年龄段不同而不同(40~49岁:≥76.33 pmol/L,50~59岁:≥74.31 pmol/L,60~69岁:≥83.26 pmol/L,≥70岁:≥105.69 pmol/L),两者满足一项即为阳性,否则为阴性。
1.5 统计学分析应用SPSS 16.0统计学软件进行数据分析。计数资料采用频数(百分比)表示,组间比较采用χ2检验或校正χ2检验。符合正态分布的计量资料采用均数±标准差(x±s)表示,组间比较采用独立样本t检验;不符合正态分布的计量资料采用中位数(上下四分位数)表示,组间比较采用两独立样本秩和检验。绘制受试者工作特征(receiver operating characteristic,ROC)曲线分析超声O-RADS分类、超声造影及血清CA125和HE4单独诊断及联合应用对绝经后卵巢肿物的诊断效能,以P<0.05为差异具有统计学意义。
2 结果 2.1 病理检查结果76例绝经后患者卵巢肿物以良性居多,良性55例,恶性21例。良性肿物包括成熟性畸胎瘤22例、浆液性囊腺瘤17例、黏液性囊腺瘤11例、卵巢纤维瘤3例和卵泡膜细胞瘤2例。恶性病变包括交界性囊腺瘤3例、浆液性囊腺癌8例、黏液性囊腺癌7例、透明细胞癌2例和转移性癌1例。
2.2 超声O-RADS分类、临床特征与病理检查结果对照分析病理诊断为卵巢良性和恶性肿物的超声O-RADS分类和肿瘤最大径比较,差异均具有统计学意义(均P<0.01,表 1)。良性和恶性肿物在绝经年限及肿物位于单/双侧方面比较,差异均无统计学意义(均P>0.05)。
| 临床特征及O-RADS分类 | 病理结果 | χ2值 | P值 | |
| 良性(n=55) | 恶性(n=21) | |||
| 绝经年限 | 0.045 | 0.997 | ||
| 1~5年 | 22(40.0) | 8(38.1) | ||
| 6~10年 | 16(29.1) | 6(28..6) | ||
| 11~15年 | 5(9.1) | 2(9.5) | ||
| ≥16年 | 12(21.8) | 5(23.8) | ||
| 单双侧 | 0.022 | 0.882 | ||
| 单侧 | 41(74.5) | 16(76.2) | ||
| 双侧 | 14(25.5) | 5(23.8) | ||
| 肿瘤最大径 | 9.792 | 0.003 | ||
| <10 cm | 49(89.1) | 12(57.1) | ||
| ≥10 cm | 6(10.9) | 9(42.9) | ||
| 超声O-RADS分类 | 17.768 | <0.01 | ||
| 2类 | 8(14.5) | 0(0.0) | ||
| 3类 | 34(61.8) | 6(28.6) | ||
| 4类 | 10(18.2) | 8(38.1) | ||
| 5类 | 3(5.5) | 7(33.3) | ||
| 注 O-RADS:卵巢-附件影像报告和数据系统(Ovarian-Adnexal Reporting and Data System) | ||||
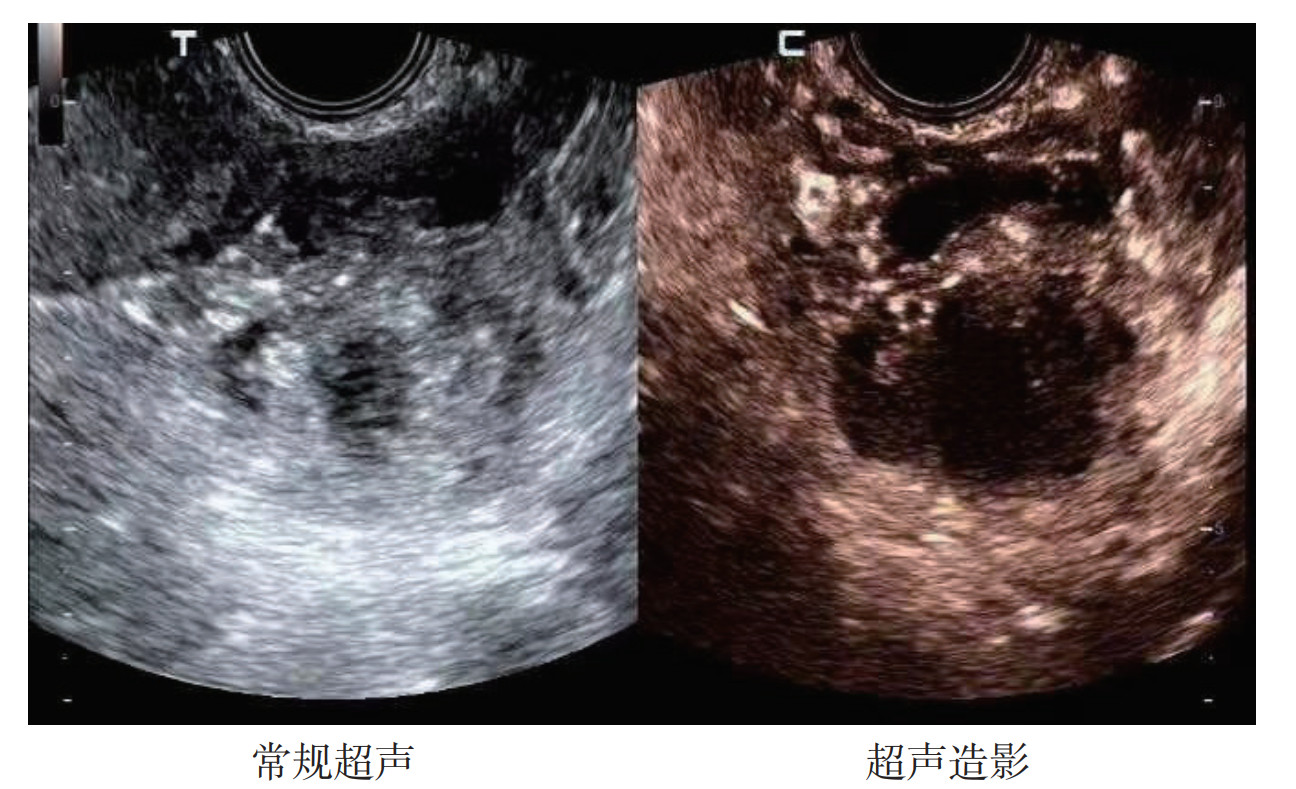
卵巢恶性肿物超声造影多呈快速早期高增强,消退时间早,增强强度高于子宫肌层灌注强度;良性肿物多呈无增强或周边环状增强。TIC曲线显示,卵巢恶性肿物始增时间和达峰时间均低于良性肿物,而恶性肿物峰值强度高于良性肿物,差异均具有统计学意义(均P<0.01,表 2,图 1)。
| 组别 | 例数 | 始增时间(s,x±s) | 达峰时间(s,x±s) | 峰值强度(dB,x±s) | CA125 [U/mL,M(Q1~Q3)] | HE4 [pmol/L,M(Q1~Q3)] |
| 良性组 | 55 | 17.03±3.50 | 27.76±4.32 | 15.35±4.17 | 18.47(12.21~26.81) | 54.21(36.68~65.38) |
| 恶性组 | 21 | 13.53±3.33 | 21.68±4.28 | 22.79±3.69 | 77.53(28.41~312.32) | 136.75(68.37~235.39) |
| Z/t值 | 3.944 | 5.502 | -7.169 | -4.559 | -5.041 | |
| P值 | <0.01 | <0.01 | <0.01 | <0.01 | <0.01 | |
| 注 CA125:糖类抗原125(carbohydrate antigen 125);HE4:人附睾分泌蛋白4(human epididymis protein 4) | ||||||
|
| 注 囊实混合性肿块,边界不清,以实性成分为主,超声O-RADS分类为4类;超声造影示,肿块实性部分早期不均匀性高增强 图 1 1例卵巢透明细胞癌的常规超声及超声造影表现 Fig.1 Routine ultrasound and contrast-enhanced ultrasound results of an ovarian clear cell carcinoma patient |
良性肿物患者血清CA125及HE4水平均低于恶性肿物患者,差异均具有统计学意义(均P<0.01,表 2)。
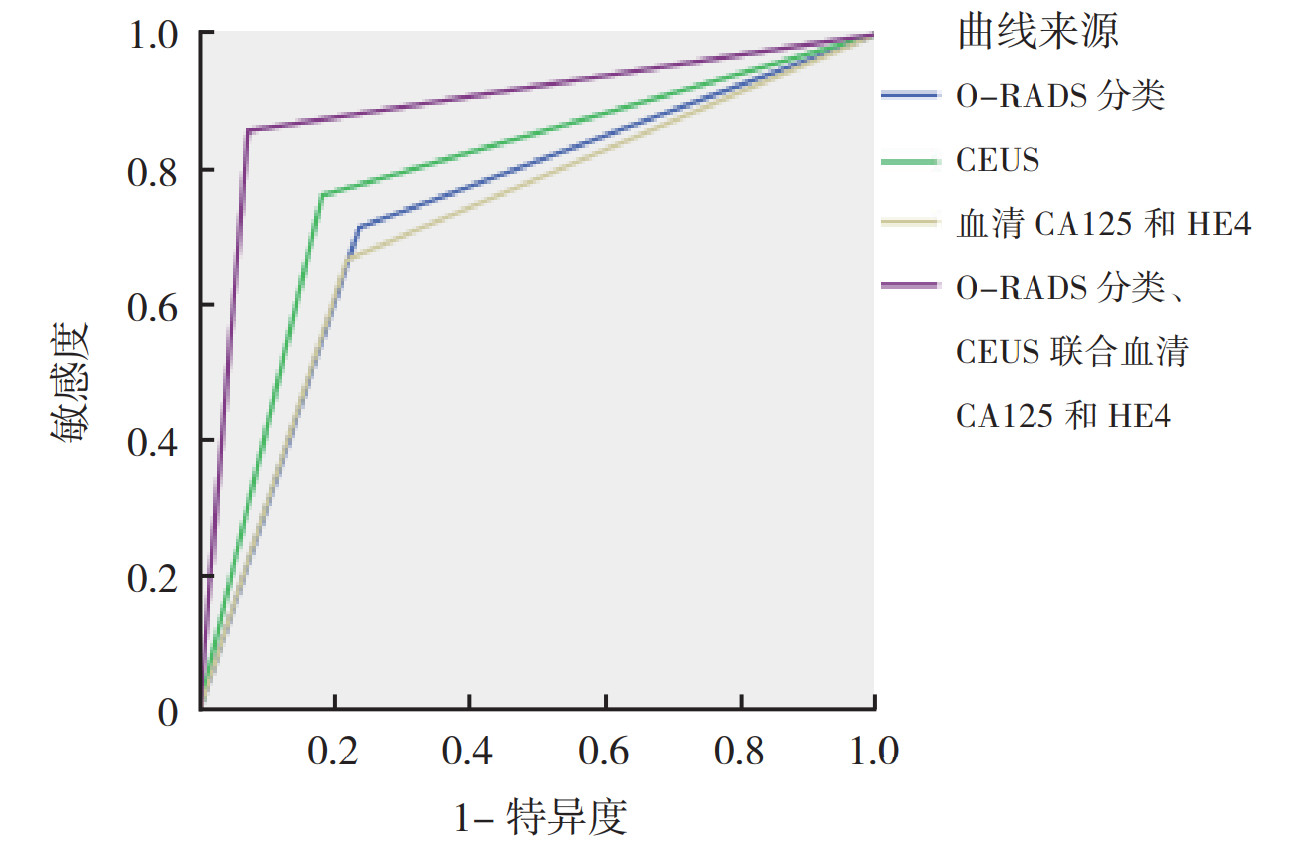
2.5 不同检查方法对绝经后卵巢良恶性肿物的诊断效能ROC曲线分析显示,超声O-RADS分类、超声造影、血清学指标及联合三者诊断卵巢良恶性肿物曲线下面积(area under the curve,AUC)分别为0.739(95% CI:0.609~0.869)、0.790(95% CI:0.668~0.912)、0.724(95% CI:0.590~0.858)和0.892(95% CI:0.796~0.988),见表 3和图 2。联合三者诊断的AUC、敏感度、特异度及准确度均高于单项检查,差异均具有统计学意义(均P<0.05)。
| 检查方式 | 病理结果 | 敏感度(%) | 特异度(%) | 准确度(%) | AUC | |
| 良性(n=55) | 恶性(n=21) | |||||
| O-RADS分类 | ||||||
| 良性 | 42(76.4) | 6(28.6) | 71.4 | 76.4 | 75.0 | 0.739 |
| 恶性 | 13(23.6) | 15(71.4) | ||||
| CEUS | ||||||
| 良性 | 45(81.8) | 5(23.8) | 76.2 | 81.8 | 80.3 | 0.790 |
| 恶性 | 10(18.2) | 16(76.2) | ||||
| 血清CA125和HE4 | ||||||
| 良性 | 43(78.2) | 7(33.3) | 66.7 | 78.2 | 75.0 | 0.724 |
| 恶性 | 12(21.8) | 14(66.7) | ||||
| O-RADS分类、CEUS联合血清CA125和HE4 | ||||||
| 良性 | 51(92.7) | 3(14.3) | 85.7 | 92.7 | 90.8 | 0.892 |
| 恶性 | 4(7.3) | 18(85.7) | ||||
| 注 O-RADS:卵巢-附件影像报告和数据系统(Ovarian-Adnexal Reporting and Data System);CEUS:超声造影(contrast-enhanced ultrasound);CA125:糖类抗原125(carbohydrate antigen 125);HE4:人附睾分泌蛋白4(human epididymis protein 4);AUC: 曲线下面积(area under the curve) | ||||||
|
| 注 O-RADS:卵巢-附件影像报告和数据系统(Ovarian-Adnexal Reporting and Data System);CEUS:超声造影(contrast-enhanced ultrasound);CA125:糖类抗原125(carbohydrate antigen 125);HE4:人附睾分泌蛋白4(human epididymis protein 4) 图 2 O-RADS分类、超声造影、血清CA125和HE4水平及三种方法联合诊断绝经后卵巢肿物的ROC曲线 Fig.2 ROC curves of O-RADS classification, contrast-enhanced ultrasound, serum levels of CA125 and HE4, and the combined method diagnosing postmenopausal ovarian masses |
绝经后卵巢肿物的术前诊断方法有多种,但目前尚无完善的定性诊断方法,尤其对于复杂的卵巢肿物,超声表现缺乏特异性,诊断准确率低,同时单一血清CA125检测敏感度及特异度均较低[9]。然而卵巢恶性肿瘤进展很快,晚期5年生存率低,早期诊断及时治疗可改善预后,提高生存率及生存质量。因此探寻一种有效的联合诊断方法至关重要。本研究旨在探讨联合超声O-RADS分类、超声造影和血清CA125和HE4水平在诊断绝经后卵巢肿物中的应用价值。
超声O-RADS共识指南的推出进一步规范了卵巢-附件肿物的风险评估,有效帮助临床医师为患者选择恰当的治疗方法[5]。已有研究表明,O-RADS分类对卵巢肿瘤具有良好的诊断效能[10-11]。本研究结果显示,O-RADS分类诊断敏感度、特异度、准确度和AUC分别为71.4%、76.4%、75.0%和0.739,诊断效能低于Basha等[10]的研究结果。分析原因,可能是由于研究中纳入样本量的病理类型不同,且研究时把交界性肿瘤归为恶性肿瘤,2例绝经后卵巢交界性肿物仅表现为单房囊性肿瘤,无乳头结构、囊壁光滑,血流评分为1级。此外,本研究通过对比绝经后卵巢良恶性肿物临床资料发现,患者绝经年限及肿瘤位于单侧还是双侧与肿物的良恶性无关。而卵巢肿物最大径与卵巢肿物的良恶性有关,肿瘤最大径≥10 cm者恶性可能性增加,由此表明,绝经后卵巢肿物随着肿瘤最大径增大恶性风险增加,因此,对于卵巢肿物最大径≥10 cm者,应提高警惕,及时手术治疗,排除恶性风险。
近年来,超声造影作为一项新技术,逐步应用于卵巢肿瘤的诊断。与常规超声比较,超声造影不受患者呼吸、运动及声束角度的干扰,能够较为敏感地显示肿瘤微血管灌注情况,通过静脉注射SonoVue微泡造影剂,可显示直径<200 μm的小血管,能够提供病灶周边区域及内部血流灌注信息,同时能清晰显示病灶不同区域灌注强度、灌注及廓清的先后顺序[12]。本研究也显示,卵巢恶性肿物始增时间及达峰时间均低于良性肿物,而恶性肿物的峰值强度高于良性肿物。究其原因,可能是恶性肿物血管密度高,血管较为粗大,走形迂曲,易形成血管网,甚至动静脉分流,并且新生肿瘤血管通常壁薄,通透性好,造影剂注入后,微泡流速快,导致始增时间及达峰时间短,增强强度高[13]。
CA125作为临床上常用的血清肿瘤标志物,具有一定的敏感度,但特异度不高,用于初步分流卵巢可疑恶性肿物。CA125不能用于区分卵巢良恶性肿物,因为子宫肌瘤、炎性反应及子宫内膜异位症等良性病变也可导致CA125水平增高[14]。HE4是一种新型的血清肿瘤标志物,作为一种分泌性的糖蛋白,在良性肿物患者血清中含量低,而在卵巢恶性肿物患者血清中含量升高[15]。近年来,HE4在辅助诊断卵巢肿物方面逐渐受到重视。有学者推荐采用CA125与HE4联合检测可提高卵巢癌诊断的敏感度和特异度[12]。本研究结果显示,卵巢恶性肿瘤血清CA125及HE4水平高于良性肿瘤,采用CA125联合HE4诊断绝经后卵巢肿物的敏感度、特异度和准确度分别为66.7%、78.2%和75.0%。本研究诊断敏感度低于既往研究[12],可能与纳入研究的病理类型不同有关。此外,本研究在血清肿瘤标志物CA125和HE4的基础上进一步联合超声O-RADS分类和超声造影,结果显示,联合技术诊断绝经后卵巢肿物的敏感度、特异度、准确度和AUC达85.7%、92.7%、90.8%和0.892,高于单一检测技术。由此表明,超声影像学检查联合血清肿瘤标志物筛查能够提高绝经后卵巢恶性肿物的诊断效能,降低漏诊及误诊率,联合诊断优势互补,克服单一检查的局限性,不仅能够从肿物的形态学特征、内部结构、微血管灌注及强化差异方面去判断,还能够在形态学及血流动力学改变之前早期筛查卵巢恶性肿物。尽管如此,本研究为单中心研究,纳入样本量较少,且为回顾性分析,仍需进一步扩充样本量、前瞻性、多中心研究进行验证。
综上所述,超声O-RADS分类联合超声造影及血清CA125和HE4检测可提高绝经后卵巢肿物的诊断效能,为早期筛出卵巢恶性肿物提供有效依据,帮助临床制定恰当治疗方案,及时治疗,提高生存率。
| [1] |
Farghaly SA. Current diagnosis and management of ovarian cysts[J]. Clin Exp Obstet Gynecol, 2014, 41(6): 609-612. DOI:10.12891/ceog20322014 |
| [2] |
McBee WC, Escobar PF, Falcone T. Which ovarian masses need intervention?[J]. Cleve Clin J Med, 2007, 74(2): 149-157. DOI:10.3949/ccjm.74.2.149 |
| [3] |
王稳, 王颖梅, 王玉东, 等. 绝经后卵巢肿物诊治的中国专家共识(2021年版)[J]. 中国实用妇科与产科杂志, 2021, 37(10): 1021-1026. DOI:10.19538/j.fk2021100110 |
| [4] |
尹晶, 黄敏丽, 黄品同. 超声诊断卵巢透明细胞癌[J]. 实用肿瘤杂志, 2021, 36(5): 439-443. |
| [5] |
Andreotti RF, Timmerman D, Strachowski LM, et al. O-RADS US risk stratification and management system: a consensus guideline from the ACR ovarian-adnexal reporting and data system committee[J]. Radiology, 2020, 294(1): 168-185. DOI:10.1148/radiol.2019191150 |
| [6] |
Andreotti RF, Timmerman D, Benacerraf BR, et al. Ovarian-adnexal reporting lexicon for ultrasound: A white paper of the ACR ovarian-adnexal reporting and data system committee[J]. J Am Coll Radiol, 2018, 15(10): 1415-1429. DOI:10.1016/j.jacr.2018.07.004 |
| [7] |
杨文敏, 吕国荣, 陈秋月. 卵巢-附件报告及数据系统、妇科影像报告与数据系统和简单法则风险预测模型鉴别诊断卵巢良、恶性肿瘤[J]. 中国医学影像技术, 2021, 37(9): 1368-1372. |
| [8] |
尹晶, 冯玉玲, 向红, 等. 超声造影在附件实性小肿块鉴别诊断中的应用[J]. 中国全科医学, 2014, 17(6): 719-722. DOI:10.3969/j.issn.1007-9572.2014.06.033 |
| [9] |
刘明松, 单华英, 徐月静, 等. 超声联合CA125对卵巢内生性乳头状肿块的诊断价值[J]. 实用肿瘤杂志, 2021, 36(2): 141-144. |
| [10] |
Basha M, Metwally MI, Gamil SA, et al. Comparison of O-RADS, GI-RADS, and IOTA simple rules regarding malignancy rate, validity, and reliability for diagnosis of adnexal masses[J]. Eur Radiol, 2021, 31(2): 674-684. DOI:10.1007/s00330-020-07143-7 |
| [11] |
Pi YL, Wilson MP, Katlariwala P, et al. Diagnostic accuracy and inter-observer reliability of the O-RADS scoring system among staff radiologists in a North American academic clinical setting[J]. Abdom Radiol (NY), 2021, 46(10): 4967-4973. |
| [12] |
郭微群, 朱长玉, 周华玲, 等. 阴道超声造影联合CA125+HE4提高卵巢癌早期诊断的临床价值[J]. 浙江创伤外科, 2021, 26(6): 1089-1091. |
| [13] |
胡毓婷, 黄晓民, 缪恺, 等. 超声造影联合血清学在卵巢癌早期筛查中的应用研究[J]. 中国超声医学杂志, 2022, 38(1): 95-98. |
| [14] |
Timmerman D, Planchamp F, Bourne T, et al. ESGO/ISUOG/IOTA/ESGE consensus statement on pre-operative diagnosis of ovarian tumors[J]. Int J Gynecol Cancer, 2021, 31(7): 961-982. |
| [15] |
郁平, 姬小凡, 王敏, 等. MRI、血清CA125及HE4对卵巢癌的诊断价值分析[J]. 中国CT和MRI杂志, 2019, 17(12): 97-99. |
 2023, Vol. 38
2023, Vol. 38
