文章信息
- 蔡明, 戴维, 冷雪峰, 王奇峰, 韩泳涛, 李骏, 何浪, 石丘玲, 苏义刚, 彭林
- Cai Ming, Dai Wei, Leng Xuefeng, Wang Qifeng, Han Yongtao, Li Jun, He Lang, Shi Qiuling, Su Yigang, Peng Lin
- 局部晚期食管鳞癌术后恢复预期肿瘤治疗的特点及其与预后的关系
- Characteristics of return to intended oncologic therapy and its relationship with prognosis in patients with locally advanced esophageal squamous cancer
- 实用肿瘤杂志, 2022, 37(4): 327-332
- Journal of Practical Oncology, 2022, 37(4): 327-332
-
通信作者
-
苏义刚,E-mail:syg0010084@163.com
彭林,E-mail:penglinms@126.com
-
文章历史
- 收稿日期:2021-05-19
2. 绵阳市肿瘤医院胸外科,四川 绵阳 621000;
3. 四川省肿瘤医院放疗科,四川 成都 610041;
4. 重庆医科大学公共卫生与管理学院,重庆 400016
2. Department of Thoracic Surgery, Mianyang Tumor Hospital, Mianyang 621000, China;
3. Department of Radiation Oncology, Sichuan Cancer Hospital, Chengdu 610041, China;
4. School of Public Health and Management, Chongqing Medical University, Chongqing 400016, China
目前一些新颖的指标可用来评估肿瘤手术的质量,如术后恢复预期肿瘤治疗(return to intended oncologic treatment,RIOT)[1-2]。RIOT的概念由Aloia等[1]于2014年首次提出。在目前的定义中,RIOT至少包括2个方面的内容:(1)应该接受术后抗肿瘤治疗的患者是否接受了预期的治疗;(2)从手术至术后开始肿瘤治疗的时间。成功的RIOT意味着及时且依从性好的术后抗肿瘤治疗,其与良好的临床结局密切相关[3-9],故RIOT被建议作为一个手术质量评价指标。目前已有研究报道RIOT在头颈肿瘤、肝癌、胃癌、结肠癌、胰腺癌和妇科肿瘤中的应用[3-9],但是类似的研究尚未在食管癌中进行。目前尚不清楚食管癌术后延迟化疗是否会影响患者的长期预后。由于伦理原因,回答这个问题的随机对照试验可能不可行。故本研究利用回顾性数据并借用RIOT的概念,分析局部晚期食管鳞癌患者术后RIOT的特点,并调查其与总生存期(overall survival,OS)的关系。
1 资料与方法 1.1 研究对象回顾性分析2015年4月至2017年8月在四川省肿瘤医院行手术治疗的食管癌患者的临床资料,所有资料由电子病案系统导出。纳入标准:(1)病变位于食管胸段,接受三切口(McKeown)或两切口(Ivor-Lewis)手术;(2)术后病理诊断为鳞状细胞癌,病理分期T3~4a或N1~3;(3)只接受了单纯手术或手术加术后化疗。排除标准:(1)有新辅助治疗史;(2)有其他恶性肿瘤史;(3)不完全性切除(R1和R2);(4)远处转移(M1);(5)重要数据缺失。本研究经四川省肿瘤医院伦理委员会批准(伦理批件号:SCCHECC-02-2018-010)。本研究为回顾性研究,患者的知情同意书被四川省肿瘤医院伦理委员会豁免。
患者的术后化疗以铂类(顺铂、卡铂和奈达铂)为基础,联合紫杉类药物(紫杉醇和多西紫杉醇)或氟尿嘧啶类药物(5-氟尿嘧啶、卡培他滨和替吉奥胶囊)。通常为双药联合方案,化疗4个周期。顺铂75~100 mg/m2,d1或者分为3 d;卡铂剂量AUC为5~6;奈达铂80~100 mg/m2,d1。紫杉醇135~175 mg/m2,d1;多西紫杉醇60~75 mg/m2,d1。5-氟尿嘧啶300~500 mg/m2,d1-5;卡培他滨1 250 mg/m2,2次/d,连服14 d,之后停药7 d;替吉奥40~60 mg/次,2次/d,连服14 d,之后停药7 d。
1.2 临床指标定义食管手术方式为两切口(Ivor-Lewis)或三切口(McKeown)食管切除术联合淋巴结清扫术。微创食管切除术包括单纯的胸腔镜、单纯的腹腔镜或者胸腹腔镜联合。开放食管切除术指开胸联合开腹手术。病理分期采用第7版食管癌TNM分期[10]。RIOT定义:RIOT比例为接受预期的术后化疗患者的比例;RIOT时间为手术至术后化疗开始的时间。局部晚期食管癌定义:病理分期为T3~4和(或)N1~3,无远处转移。
1.3 随访随访数据来自临床病历记录和电话随访,时间截至2018年10月15日。OS定义为从诊断到死亡或最后1次随访(删失)的时间。
1.4 统计学分析采用SAS 9.4软件进行数据分析。计量资料以均数±标准差(x±s)或中位数(范围)表示,组间比较采用t检验或Wilcoxon秩和检验。计数资料以频数(百分比)表示,组间比较采用χ2检验。Kaplan-Meier法作生存曲线。采用log-rank检验分析OS。使用Cox回归模型评估是否进行RIOT和开始RIOT周数的预后价值。将可能的混杂因素(如年龄、性别、术后住院时间、手术入路、淋巴结病理状态、病理T分期、肿瘤部位和手术方式等)纳入Cox模型,以控制其对RIOT和OS的潜在影响。以P < 0.05为差异具有统计学意义。
2 结果 2.1 一般资料和随访结果本研究共纳入600例患者,男性494例,女性106例。263例接受单独手术治疗,年龄42~91岁,中位年龄67岁。337例接受手术加术后化疗,年龄43~80岁,中位年龄61岁。术后接受化疗的患者比未接受化疗的患者更年轻(P < 0.01)和具有更多的淋巴结阳性状态(P < 0.01,表 1)。两组间的性别、肿瘤部位、手术入组、手术方式、病理T分期和术后住院时间比较,差异均无统计学意义(均P > 0.05)。中位随访时间为510 d(9~1 053 d)。共有203例死亡,其中100例为单纯手术,103例为手术加术后化疗。
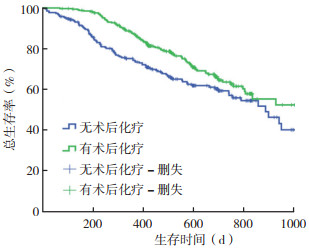
2.2 RIOT比例特点及其与OS的关系RIOT比例为56.2%(337/600)。接受微创和开放手术治疗的患者的RIOT比例分别为57.4%(232/404)和53.6%(105/196),差异无统计学意义(P=0.37,表 1)。术后化疗患者的1年和2年OS率高于术后未化疗患者(87.2% vs 74.4%,P < 0.01;61.9% vs 55.2%,P=0.01,图 1)。Cox回归分析显示,术后未接受化疗、两切口(Ivor-Lewis)手术、病理分期为T4a和淋巴结阳性患者的OS较差(均P < 0.05,表 2)。
| 临床特征 | 术后化疗 | P值 | |
| 是(n=337) | 否(n=263) | ||
| 年龄(岁,x±s) | 60.7±7.6 | 65.8±8.2 | < 0.01 |
| 性别 | 0.16 | ||
| 男性 | 284(84.3) | 210(79.8) | |
| 女性 | 53(15.7) | 53(20.2) | |
| 肿瘤部位 | 0.49 | ||
| 上段 | 58(17.2) | 47(17.9) | |
| 中段 | 200(59.3) | 165(62.7) | |
| 下段 | 79(23.4) | 51(19.4) | |
| 手术入路 | 0.37 | ||
| 微创 | 232(68.8) | 172(65.4) | |
| 开放 | 105(31.2) | 91(34.6) | |
| 手术方式 | 0.69 | ||
| 三切口(McKeown) | 283(84.0) | 224(85.2) | |
| 两切口(Ivor-Lewis) | 54(16.0) | 39(14.8) | |
| 病理T分期 | 0.07 | ||
| T1+T2 | 57(16.9) | 32(12.2) | |
| T3 | 243(72.1) | 188(71.5) | |
| T4a | 37(11.0) | 43(16.3) | |
| 淋巴结病理状态 | < 0.01 | ||
| 阳性(N+) | 247(73.3) | 153(58.2) | |
| 阴性(N-) | 90(26.7) | 110(41.8) | |
| 术后住院时间(d,x±s) | 14.1±6.3 | 16.2±11.0 | 0.06 |
|
| 图 1 有无接受术后化疗的局部晚期食管鳞癌患者的总生存曲线 Fig.1 Overall survival curves of locally advanced esophageal squamous cancer patients with and without postoperative chemotherapy |
| 变量 | B | S.E. | χ2值 | HR | 95%CI | P值 |
| 术后化疗(否vs是) | 0.49 | 0.15 | 10.56 | 1.64 | 1.22~2.21 | < 0.01 |
| 年龄 | 0.00 | 0.01 | 0.16 | 1.00 | 0.98~1.01 | 0.69 |
| 性别(男性vs女性) | -0.20 | 0.20 | 0.98 | 0.82 | 0.55~1.22 | 0.32 |
| 肿瘤部位(胸中段vs胸上下段) | -0.16 | 0.12 | 1.92 | 0.85 | 0.68~1.07 | 0.17 |
| 手术入路(微创vs开放) | 0.01 | 0.18 | 0.00 | 1.01 | 0.71~1.42 | 0.97 |
| 手术方式(三切口vs两切口) | -0.50 | 0.22 | 5.14 | 0.61 | 0.40~0.94 | 0.02 |
| 病理T分期(T3 vs T1+T2) | 0.36 | 0.22 | 2.50 | 1.43 | 0.92~2.22 | 0.11 |
| 病理T分期(T4a vs T1+T2) | 0.93 | 0.27 | 11.93 | 2.54 | 1.50~4.32 | < 0.01 |
| 淋巴结病理状态[阳性(N+)vs阴性(N-)] | 1.00 | 0.18 | 30.18 | 2.72 | 1.90~3.89 | < 0.01 |
| 术后住院时间 | 0.01 | 0.01 | 1.03 | 1.01 | 0.99~1.02 | 0.31 |
228例患者明确了术后化疗开始的日期,且在术后200 d内开始了术后化疗。RIOT时间的中位数为43 d(13~189 d)。食管胸下段患者的RIOT时间比胸上段和胸中段的患者更短(P=0.01,表 3)。患者的RIOT时间在性别、手术入路、手术方式、病理T分期和淋巴结病理状态方面比较,差异均无统计学意义(均P > 0.05)。在228例患者中,171例(75.0%)在术后9周内开始了RIOT。RIOT时间每延迟1周,患者的死亡风险增加9%(HR=1.09,95%CI:1.02~1.15,P=0.01,表 4)。
| 变量 | 术后恢复预期肿瘤治疗时间 | P值* | |||||
| 例数 | 均数(d) | 标准差(d) | 中位数(d) | 最小值(d) | 最大值(d) | ||
| 性别 | 0.79 | ||||||
| 男性 | 192 | 52.7 | 26.3 | 43.0 | 13.0 | 189.0 | |
| 女性 | 36 | 48.6 | 17.6 | 42.0 | 28.0 | 105.0 | |
| 肿瘤部位 | 0.01 | ||||||
| 胸上段 | 38 | 58.0 | 24.0 | 52.5 | 29.0 | 126.0 | |
| 胸中段 | 129 | 52.0 | 23.8 | 43.0 | 16.0 | 162.0 | |
| 胸下段 | 61 | 48.4 | 28.1 | 38.0 | 13.0 | 189.0 | |
| 手术入路 | 0.95 | ||||||
| 微创 | 160 | 51.8 | 23.9 | 42.0 | 13.0 | 162.0 | |
| 开放 | 68 | 52.6 | 28.0 | 45.0 | 16.0 | 189.0 | |
| 手术方式 | 0.89 | ||||||
| 三切口(McKeown) | 187 | 52.1 | 25.2 | 43.0 | 13.0 | 189.0 | |
| 两切口(Ivor-Lewis) | 41 | 51.5 | 25.3 | 43.0 | 16.0 | 135.0 | |
| 病理T分期 | 0.85 | ||||||
| T1+T2 | 39 | 49.7 | 21.2 | 42.0 | 29.0 | 114.0 | |
| T3 | 166 | 52.7 | 26.9 | 43.0 | 13.0 | 189.0 | |
| T4a | 23 | 50.8 | 17.8 | 46.0 | 26.0 | 84.0 | |
| 淋巴结病理状态 | 0.40 | ||||||
| 阳性(N+) | 162 | 53.5 | 26.5 | 43.0 | 26.0 | 189.0 | |
| 阴性(N-) | 66 | 48.4 | 21.2 | 40.5 | 13.0 | 135.0 | |
| 注 *均数比较 | |||||||
| 变量 | B | S.E. | χ2值 | HR | 95%CI | P值 |
| 术后恢复预期肿瘤治疗开始周数 | 0.08 | 0.03 | 7.29 | 1.09 | 1.02~1.15 | 0.01 |
| 年龄 | 0.01 | 0.02 | 0.12 | 1.01 | 0.97~1.04 | 0.73 |
| 性别(男性vs女性) | -0.01 | 0.40 | 0.00 | 0.99 | 0.45~2.17 | 0.99 |
| 肿瘤部位(胸中段vs胸上下段) | 0.02 | 0.22 | 0.01 | 1.02 | 0.67~1.57 | 0.92 |
| 手术入路(微创vs开放) | -0.33 | 0.37 | 0.82 | 0.72 | 0.35~1.48 | 0.37 |
| 手术方式(三切口vs两切口) | -0.54 | 0.42 | 1.71 | 0.58 | 0.26~1.31 | 0.19 |
| 病理T分期(T3 vs T1+T2) | 0.46 | 0.40 | 1.30 | 1.58 | 0.72~3.48 | 0.26 |
| 病理T分期(T4a vs T1+T2) | 0.69 | 0.57 | 1.48 | 2.00 | 0.66~6.08 | 0.22 |
| 淋巴结病理状态(阳性vs阴性) | 0.49 | 0.32 | 2.31 | 1.62 | 0.87~3.04 | 0.13 |
| 术后住院时间 | -0.02 | 0.03 | 0.53 | 0.98 | 0.93~1.03 | 0.47 |
局部晚期食管鳞癌的最佳治疗策略一直存在争议[11-13],在不同国家其治疗方案也有所不同。在中国,术后辅以化疗或放化疗在真实世界中更为常见[14-17],特别是在2018年以前,尽管其作用仍存在争议[14-20]。RIOT是一个较新的概念,目前国内尚无中文翻译,笔者将其翻译为术后恢复预期肿瘤治疗。本研究可能是在国内首次采用RIOT的概念,并用其研究食管癌术后化疗的RIOT特点及其与预后的关系。
利用RIOT比例和RIOT时间来评价肿瘤手术的质量,如微创手术和开放手术,是一种新策略。因为高RIOT比例和短RIOT时间通常意味着患者术后并发症更少和恢复更快,并与更好的预后相关[1]。在Aloia等[1]的研究中,接受微创肝肿瘤切除术的患者比开放手术患者具有更高的RIOT率(100% vs 75%,P < 0.01)和更短的RIOT时间(15 d vs 42 d,P < 0.01)。另一项结肠癌研究也报道,微创手术的RIOT时间较短(机器人组25.2 d,腹腔镜组27.8 d,开放组36.0 d,P < 0.01)[21]。然而,本研究中,与开放食管手术比较,微创食管手术在RIOT比例和RIOT时间上并没有明显的优势。笔者分析可能有2个原因:(1)与其他部位的微创手术比较,食管癌微创手术是一种创伤范围更大的手术,因为其涉及到颈部、胸部和腹部3个部位,患者可能需要更长的恢复时间;(2)与开放手术比较,食管癌微创手术的并发症发生率相似甚至更高[22-23],这将导致RIOT比例降低和RIOT时间延长。
与之前报道的研究一致[14-16, 24],本研究显示,接受术后化疗的局部晚期食管癌患者比单纯手术的患者有更好的OS。虽然术后单纯化疗的总体有效率不高,对患者身体影响大,但是部分患者仍可从中获益。目前食管癌术后辅助治疗的最佳开始时间尚无明确共识。在临床实践中,食管癌术后辅助治疗的开始时间通常在术后1个月左右,而在已发表的相关研究中为2~12周[14-16, 18, 20, 25]。既往在结肠癌中的回顾性研究显示,在术后8周内开始化疗可提高患者生存率[5]。本研究中食管癌患者术后化疗的RIOT时间为13~189 d,且每推迟1周,患者的死亡风险就增加9%。这一结果表明,早期进行RIOT对OS有潜在的益处。因此,临床上制定提高RIOT比例和RIOT时间的策略,将有可能改善局部晚期食管鳞癌患者的长期预后。
本研究有一定的局限性:(1)由于回顾性的研究设计,患者术前功能状态、术后并发症、未进行RIOT或延迟RIOT的原因等信息未能准确统计,从而未能更深入分析RIOT的影响因素;(2)本研究仅纳入了术后化疗,而未将术后其他辅助治疗类型纳入,其主要原因是2018年前的术后放化疗比例相对较低;(3)本研究对患者术后是否完成全部周期的化疗也未能随访明确,这导致了对RIOT的描述尚不全面;(4)本研究是单中心研究,且随访时间短,其结论的普适性和有效性有待进一步研究。
综上所述,本研究以局部晚期食管鳞癌患者术后化疗RIOT为例,发现微创食管手术并不优于开放食管手术的RIOT,更早的RIOT时间与更好的OS独立相关。本研究结论有待在多中心、前瞻性的研究中进一步验证。
| [1] |
Aloia TA, Zimmitti G, Conrad C, et al. Return to intended oncologic treatment (RIOT): a novel metric for evaluating the quality of oncosurgical therapy for malignancy[J]. J Surg Oncol, 2014, 110(2): 107-114. DOI:10.1002/jso.23626 |
| [2] |
Finnerty DT, Buggy DJ. Return to intended oncologic therapy: a potentially valuable endpoint for perioperative research in cancer patients?[J]. Br J Anaesth, 2020, 124(5): 508-510. DOI:10.1016/j.bja.2020.02.013 |
| [3] |
Kiong KL, Moreno A, Vu CN, et al. Enhanced recovery after surgery (ERAS) in head and neck oncologic surgery: impact on return to intended oncologic therapy (RIOT) and survival[J]. Oral Oncol, 2022, 130: 105906. DOI:10.1016/j.oraloncology.2022.105906 |
| [4] |
Lillemoe HA, Marcus RK, Kim BJ, et al. Severe preoperative symptoms delay readiness to return to intended oncologic therapy (RIOT) after liver resection[J]. Ann Surg Oncol, 2019, 26(13): 4548-4555. DOI:10.1245/s10434-019-07719-8 |
| [5] |
Kim YW, Choi EH, Kim BR, et al. The impact of delayed commencement of adjuvant chemotherapy (eight or more weeks) on survival in stage Ⅱ and Ⅲ colon cancer: a national population-based cohort study[J]. Oncotarget, 2017, 8(45): 80061-80072. DOI:10.18632/oncotarget.17767 |
| [6] |
Garcia-Nebreda M, Zorrilla-Vaca A, Ripollés-Melchor J, et al. Early return to intended oncologic therapy after implementation of an enhanced recovery after surgery pathway for gastric cancer surgery[J]. Langenbecks Arch Surg, 2022, Epub.
|
| [7] |
Tankou JI, Foley O, Falzone M, et al. Enhanced recovery after surgery protocols improve time to return to intended oncology treatment following interval cytoreductive surgery for advanced gynecologic cancers[J]. Int J Gynecol Cancer, 2021, 31(8): 1145-1153. DOI:10.1136/ijgc-2021-002495 |
| [8] |
Mickel TA, Kutlu OC, Silberfein EJ, et al. Factors associated with inability to return to intended oncologic treatment in pancreatic cancer[J]. Am J Surg, 2022, 224(1 Pt B): 635-640. |
| [9] |
Ramos MFKP, de Castria TB, Pereira MA, et al. Return to intended oncologic treatment (RIOT) in resected gastric cancer patients[J]. J Gastrointest Surg, 2020, 24(1): 19-27. DOI:10.1007/s11605-019-04462-z |
| [10] |
律方. 食管癌第6版AJCC分期与第七版AJCC分期的比较研究[D]. 北京: 北京协和医学院研究生院, 2011: 1-50.
|
| [11] |
Sohda M, Kuwano H. Current status and future prospects for esophageal cancer treatment[J]. Ann Thorac Cardiovasc Surg, 2017, 23(1): 1-11. DOI:10.5761/atcs.ra.16-00162 |
| [12] |
张斯渊, 董信春, 韩松辰, 等. 精准医疗: 中晚期食管癌放疗技术进展浅谈[J]. 实用肿瘤杂志, 2021, 36(4): 368-374. |
| [13] |
张柏文, 何丽娜, 涂水平. 食管癌相关多原发癌的研究进展[J]. 实用肿瘤杂志, 2022, 37(2): 191-195. |
| [14] |
Qin RQ, Wen YS, Wang WP, et al. The role of postoperative adjuvant chemotherapy for lymph node-positive esophageal squamous cell carcinoma: a propensity score matching analysis[J]. Med Oncol, 2016, 33(4): 31. DOI:10.1007/s12032-016-0746-8 |
| [15] |
Zhang LZ, Li WW, Lyu X, et al. Adjuvant chemotherapy with paclitaxel and cisplatin in lymph node-positive thoracic esophageal squamous cell carcinoma[J]. 中国癌症研究: 英文版, 2017, 29(2): 149-155. |
| [16] |
Lyu X, Huang J, Mao YS, et al. Adjuvant chemotherapy after esophagectomy: is there a role in the treatment of the lymph node positive thoracic esophageal squamous cell carcinoma?[J]. J Surg Oncol, 2014, 110(7): 864-868. DOI:10.1002/jso.23716 |
| [17] |
Chen HL, Wu ZY, Chen JX, et al. Postoperative adjuvant therapy for resectable thoracic esophageal squamous cell carcinoma: a retrospective analysis of 426 cases[J]. Med Oncol, 2015, 32(1): 417. DOI:10.1007/s12032-014-0417-6 |
| [18] |
Ando N, Iizuka T, Ide H, et al. Surgery plus chemotherapy compared with surgery alone for localized squamous cell carcinoma of the thoracic esophagus: a Japan Clinical Oncology Group Study: JCOG9204[J]. J Clin Oncol, 2003, 21(24): 4592-4596. DOI:10.1200/JCO.2003.12.095 |
| [19] |
Pasquer A, Gronnier C, Renaud F, et al. Impact of adjuvant chemotherapy on patients with lymph node-positive esophageal cancer who are primarily treated with surgery[J]. Ann Surg Oncol, 2015, 22(3_suppl): S1340-S1349. |
| [20] |
Lee J, Lee KE, Im YH, et al. Adjuvant chemotherapy with 5-fluorouracil and cisplatin in lymph node-positive thoracic esophageal squamous cell carcinoma[J]. Ann Thorac Surg, 2005, 80(4): 1170-1175. DOI:10.1016/j.athoracsur.2005.03.058 |
| [21] |
Jung YB, Kang J, Park EJ, et al. Time to initiation of adjuvant chemotherapy in colon cancer: comparison of open, laparoscopic, and robotic surgery[J]. J Laparoendosc Adv Surg Tech A, 2016, 26(10): 799-805. DOI:10.1089/lap.2016.0293 |
| [22] |
Takeuchi H, Miyata H, Gotoh M, et al. A risk model for esophagectomy using data of 5354 patients included in a Japanese nationwide web-based database[J]. Ann Surg, 2014, 260(2): 259-266. DOI:10.1097/SLA.0000000000000644 |
| [23] |
Sihag S, Kosinski AS, Gaissert HA, et al. Minimally invasive versus open esophagectomy for esophageal cancer: a comparison of early surgical outcomes from the society of thoracic surgeons national database[J]. Ann Thorac Surg, 2016, 101(4): 1281-1288; discussion1288-1289.
|
| [24] |
Wang QF, Peng L, Li T, et al. Postoperative chemotherapy for thoracic pathological T3N0M0 esophageal squamous cell carcinoma[J]. Ann Surg Oncol, 2020, 27(5): 1488-1495. DOI:10.1245/s10434-019-08112-1 |
| [25] |
Ando N, Kato H, Igaki H, et al. A randomized trial comparing postoperative adjuvant chemotherapy with cisplatin and 5-fluorouracil versus preoperative chemotherapy for localized advanced squamous cell carcinoma of the thoracic esophagus (JCOG9907)[J]. Ann Surg Oncol, 2012, 19(1): 68-74. DOI:10.1245/s10434-011-2049-9 |
 2022, Vol. 37
2022, Vol. 37


