文章信息
- 许晓明, 董学妍, 陈岳明, 余道军, 王贤军
- Xu Xiaoming, Dong Xueyan, Chen Yueming, Yu Daojun, Wang Xianjun
- 富含脯氨酸小蛋白2A对胃癌细胞增殖和迁移能力的影响
- Effects of small proline-rich protein 2A on proliferation and migration of human gastric cancer cells
- 实用肿瘤杂志, 2020, 35(6): 511-517
- Journal of Practical Oncology, 2020, 35(6): 511-517
基金项目
- 杭州市医药卫生科技计划项目(2015Z01);浙江省中医药科技计划项目(2016ZA158);浙江省医药卫生科技计划(2020KY688)
-
作者简介
- 许晓明(1982-),男,黑龙江伊春人,主治医师,博士生,从事肝胆胰和消化道病理诊断研究.
-
通信作者
- 董学妍,E-mail:dongxueyan82@163.com
-
文章历史
- 收稿日期:2019-12-18
2. 浙江大学医学院附属杭州市第一人民医院检验科,浙江 杭州 310006
2. Department of Clinical Laboratory, Affiliated Hangzhou First People's Hospital of Zhejiang University School of Medicine, Hangzhou 310006, China
胃癌是常见的恶性肿瘤之一。2018年全球癌症数据统计显示,全球胃癌死亡率居所有恶性肿瘤第3位[1-2]。随着医疗水平的提高,近年来胃癌发病率出现下降趋势,且平均发病年龄出现后移趋势,但胃癌转移仍是导致胃癌患者死亡的重要原因[3-5],因此寻找影响胃癌增殖和迁移的相关基因,对于胃癌诊断、有效治疗及准确判断预后具有重要意义。
富含脯氨酸小蛋白2A(small prolin-rich proteins 2A,SPRR2A)是在表皮分化复杂区域中编码的10个SPRR基因家族中的成员之一。SPRR基因家族编码一类与细胞分化相关的蛋白[6],和其他分化相关基因(involucrin、loricrin和late envelope proteins)共同构成表皮分化复合物(epidermal differentiation complex, EDC),影响细胞分化[7-8]。SPRR2A在胃癌细胞中的研究尚未见报道,本研究前期基因芯片结果显示,SPRR2A在胃癌组织中的表达增加,与癌旁正常胃黏膜组织比较表达差异高达12倍,表明SPRR2A可能在胃癌的发展中起重要作用。因此,本研究拟通过检测SPRR2A在胃癌细胞中的表达以及转染靶向SPRR2A的RNAi质粒和SPRR2A表达质粒后检测SPRR2A的表达情况,探讨SPRR2A对胃癌细胞增殖和迁移的影响。
1 材料与方法 1.1 实验材料及仪器胃癌细胞株SGC-7901、MKN-28和BGC-823以及胃上皮细胞株GES-1来自中科院上海富恒细胞库。pcDNA3.1、ex-SPRR2A-pcDNA3.1质粒、干扰RNA(si-SPRR2A)和对照干扰RNA(si-NC)均购自上海吉满生物科技有限公司。DMEM培养液、RPMI-1640培养液和胎牛血清购自美国Gibco公司。体外转染试剂盒购自美国jetPRIME公司。总蛋白提取试剂盒购自北京碧云天生物技术有限公司。β-actin抗体购自北京中杉金桥生物技术有限公司。引物由上海生工生物工程有限公司合成。CCK8检测试剂盒购自北京金克隆生物公司,Trizol试剂购自北京Bioteke生物技术有限公司。qRT-PCR SYBR Green PCR试剂购自南京Vazyme生物公司。Transwell小室购自美国Corning公司。ABI 7500实时荧光定量PCR仪购自美国应用生物系统公司。Image Quant LAS4000 mini化学发光成像仪购自美国通用电气医疗集团。FLx800荧光发光酶联仪购自北京Biotek公司。
1.2 实验方法 1.2.1 细胞培养胃癌细胞株SGC-7901和MKN-28用含10% 胎牛血清的DMEM培养液培养,胃癌细胞株BGC-823和永生化胃上皮细胞株GES-1用含10%胎牛血清的RPMI-1640培养液培养,所有细胞均置于37℃ 5%CO2培养箱中培养,细胞生长至80%~90%时,按1∶2传代培养。
1.2.2 实时定量PCRTrizol法提取细胞总RNA,微量核酸蛋白测定仪检测RNA的浓度和纯度,制备引物终浓度为2 μmol/L的RNA 20 μL反应体系。ABI 7500实时荧光定量PCR仪进行反转录和PCR。反应参数:50℃3 min;95℃5 min;95℃10 s,60℃30 s,40个循环。GAPDH数据为内参,SPRR2A mRNA相对表达量用2-ΔΔCt表示。SPRR2A上游引物为5’- AGTCAAAGTATCCACCGAAGAGC-3’,下游引物为5’- AGGGATCATCATGGGCAGATTACTG-3’。GAPDH上游引物为5’- AGAAGGCTGGGGCTCATTTG-3’,下游引物为5’-AGGGGCCATCCACAGTCTTC-3’。
1.2.3 Western blot法提取各类细胞的总蛋白,二奎啉甲酸(bicinchoninic acid,BCA)法定量检测。采用10%十二烷基硫酸钠聚丙烯酰胺凝胶电泳(sodium dodecyl sulfate polyacrylamide gel electrophoresis,SDS-PAGE)预制胶进行电泳分离并转至聚偏二氟乙烯膜(polyvinylidene fluoride,PVDF)膜,用新鲜配制的10%脱脂奶粉/TBST(TRIS-HCL 200 mmol/L、氯化钠9%或1.5 mol/L和Tween20组成)摇床上封闭1 h,加入SPRR2A抗体(美国Abcam公司)及抗β-actin抗体,4℃反应过夜。TBST液洗涤3次,每次15 min,加入辣根过氧化物酶标记的二抗,室温孵育1 h,用TBST液进行3次洗涤,每次15 min,最后用化学发光法检测,结果用灰度值表示。
1.2.4 细胞转染胃癌细胞株SGC-7901和BGC-823,细胞数量达到80%后,换成不含胎牛血清的DMEM培养液进行转染。实验分为未转染任何质粒的空白对照组、ex-SPRR2A-pcDNA3.1质粒转染组(ex-SPRR2A组)和pCDNA3.1的空载质粒转染组(空载质粒组),SPRR2A靶向siRNA干扰组(si-SPRR2A组) 及对照干扰RNA组(si-NC组)。参照DNA & siRNA体外转染试剂盒操作说明,将对照组(si-NC组或空载质粒组)、转染组(ex-SPRR2A组或si-SPRR2A组)分别转染至胃癌细胞中。转染6 h后更换为10%胎牛血清的培养液中继续培养36 h。实验重复≥3次。
1.2.5 细胞增殖和毒性检测(cell counting kit-8,CCK-8)实验SGC-7901和BGC-823细胞转染24 h后,胰酶消化后重悬计数,按1×103细胞/mL分别接种100 μL至96孔板,每组6个复孔。分别培养24 h、48 h、72 h和96 h,加入CCK-8试剂10 μL,37℃培养箱培养2 h后检测450 nm处吸光度。实验重复3次。
1.2.6 实时无标记细胞分析技术(real time cellular analysis,RTCA)法检测细胞增殖能力将各组细胞计数后接种于RTCA系统的E-Plate 16板各孔中,每组平行4个复孔,加入50 μL培养液,将E-Plate 16放入仪器中,完成1 min的稳定性检测。37℃5%CO2培养箱中培养48 h,观察细胞增殖曲线。
1.2.7 Transwell实验用胰酶消化收集各转染组细胞,加入无血清培养液制成细胞悬液,计数,按2×104细胞/孔的浓度接种水化后的transwell小室,每孔约100 μL, 每组平行3个复孔。先在下室中加入500 μL含10%胎牛血清的培养液,然后放入transwell小室,静置5 min让膜充分湿润;放入培养箱中培养24 h,取出小室,在磷酸缓冲盐溶液(phosphate buffer saline,PBS)溶液中放置5 s,冲洗3次,用棉签拭去上室内多余的细胞,正反各转动约5次,用95%甲醇固定15 min,0.1%结晶紫染色20 min,用PBS冲洗。最后均移至显微镜(×200)下拍照,计随机3个视野内细胞数量。实验重复3次。挑选3个视野拍照计数。
1.3 统计学分析采用SPSS 21.0统计学软件进行数据分析。计量资料采用均数±标准差(x±s)表示,组间比较采用独立样本t检验。以P < 0.05为差异具有统计学意义。
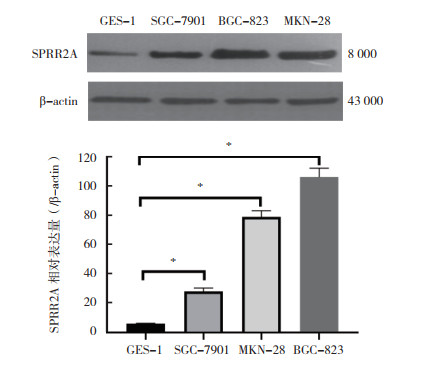
2 结果 2.1 SPRR2A在胃癌细胞株中的表达情况通过实时荧光定量PCR和Western blot法观察不同分化胃癌细胞株和正常胃黏膜细胞中SPRR2A的表达水平。RT-PCR法检测胃癌细胞BGC-823、MKN-28和SGC-7901以及正常胃黏膜GES-1细胞中SPRR2A的相对表达量分别为(849.22±0.04)、(77.17± 0.26)、(1.73±0.07)和(1.05±0.06)。胃癌细胞中SPRR2A的相对表达量均高于GES-1细胞(均P < 0.05)。Western blot结果显示,SPRR2A在BGC-832细胞中高表达,在SGC-7901细胞中低表达(图 1),胃癌细胞中SPRR2A表达均高于胃上皮细胞GES-1(均P < 0.05)。因此,本研究选取BGC-832和SCG-7901细胞用于后续研究。
|
| * P < 0.05 图 1 Western blot法检测GES-1细胞和胃癌细胞中SPRR2A蛋白的表达水平 Fig.1 SPRR2A expression in different gastric cancer lines and GES-1 cells by Western blot |
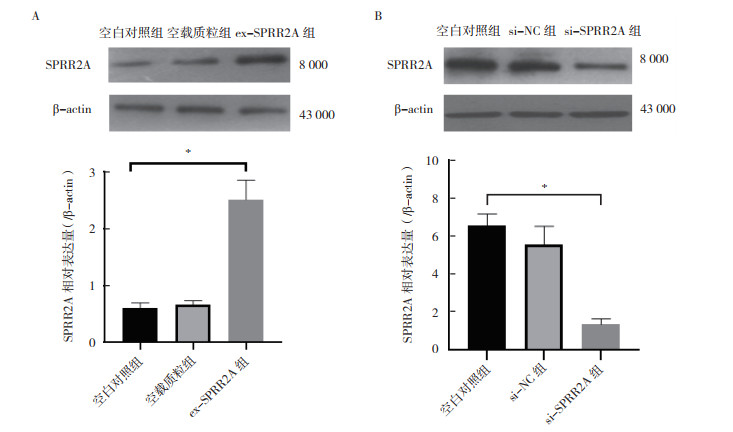
建立过表达SPRR2A质粒转染组(ex-SPRR2A组)和pCDNA3.1空载体组(空载质粒组)的SGC-7901细胞株。转染36 h后,Western blot法检测ex-SPRR2A组、空载质粒组和空白对照组中SPRR2A表达水平,ex-SPRR2A组中SPRR2A的表达水平高于空载质粒组和空白对照组(均P < 0.05,图 2A)。
|
| 注 A:Western blot法检测SGC-7901细胞中SPRR2A过表达后转染效率;B:Western blot法检测BGC-823细胞中沉默SPRR2A后转染效率;* P < 0.05 图 2 Western blot法检测空白对照组、空载质粒组/si-NC组和SPRR2A转染组(ex-SPRR2A组/si-SPRR2A组)细胞中SPRR2A的表达情况 Fig.2 Expression of SPRR2A in the control group, empty vector transfected group/si-NC group and SPRR2A transfected group (ex-SPRR2A group/si-SPRR2A group) by Western blot |
通过RNA干扰法建立SPRR2A siRNA(si-SPRR2A组)及对照干扰(si-NC组)的BGC-823细胞株。转染36 h后,用Western blot法检测si-SPRR2A组、si-NC组和空白对照组中SPRR2A表达水平,与si-NC组和空白对照组比较,si-SPRR2A组中SPRR2A的表达水平降低(均P < 0.05),表明SPRR2A表达受到抑制(图 2B)。
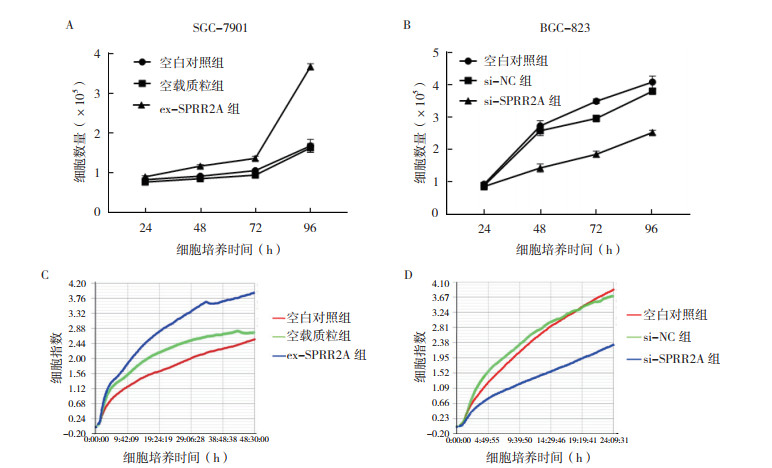
2.3 SPRR2A对胃癌细胞增殖能力的影响通过RTCA和CCK8实验绘制表达/沉默干扰SPRR2A转染后的胃癌细胞增殖曲线。CCK8实验结果显示,转染ex-SPRR2A后培养48 h、72 h和96 h时,SGC-7901细胞数量较空白对照组和空载质粒组均增多(均P < 0.05);RTCA结果显示,转染后48 h内,ex-SPRR2A组SGC-7901细胞数量较空白对照组和空载质粒组增多(图 3)。与空白对照组和si-NC组比较,BGC-823细胞转染si-SPRR2A后培养48 h、72 h和96 h,细胞增殖指数均下降(均P < 0.05);RTCA结果显示,在24 h内,转染si-SPRR2A的BGC-823细胞数量较空白对照组和si-NC组降低(图 3)。
|
| 注 A:CCK-8实验示上调SPRR2A表达后对SGC-7901细胞增殖能力的影响;B:CCK-8实验示沉默SPRR2A表达后对BGC-823细胞增殖能力的影响;C:实时无标记细胞分析技术示上调SPRR2A表达后对SGC-7901细胞增殖能力的影响;D:实时无标记细胞分析技术示沉默SPRR2A表达后对BGC-823细胞增殖能力的影响 图 3 SPRR2A对胃癌细胞增殖能力的影响 Fig.3 Effect of SPRR2A on the proliferation of gastric cancer cells |
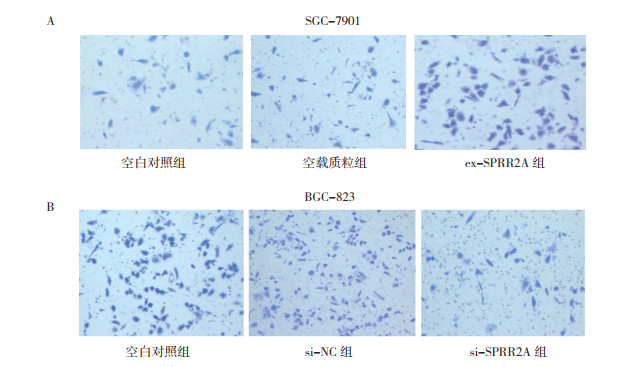
Transwell细胞迁移实验结果表明,ex-SPRR2A组SGC-7901细胞迁移数为(102.33±23.89)个,与空白对照组的(50.20±12.34)个和空载质粒组(62.46±19.33)个细胞比较,ex-SPRR2A组细胞迁移能力均增强(均P < 0.05)。si-NC组BGC-823细胞迁移细胞数量为(32.03±1.87)个,si-SPRR2A组细胞迁移数量为(16.81±2.28)个,与空白对照组的(40.01±3.46)个比较,si-SPRR2A组细胞迁移能力下降(P < 0.05,图 4)。
|
| 注 A:上调SPRR2A表达后对SGC-7901细胞迁移能力的影响;B:沉默SPRR2A表达后对BGC-823细胞迁移能力的影响 图 4 Transwell法检测SPRR2A对胃癌细胞迁移能力的影响(×200) Fig.4 Effect of SPRR2A on the migration of gastric cancer cells by transwell assay (×200) |
SPRR家族广泛存在于机体不同组织器官的上皮及屏障系统中,通过cDNA微阵列实验分析表明,SPRR2A在胃肠道、前列腺、结肠和乳腺组织中差异性高表达[9-12]。在慢性鼻窦炎中,SPRR通过活性氧干扰细胞迁移,影响组织修复及伤口愈合[13]。关于SPRR2A在肿瘤中的研究较少,主要集中在舌鳞状细胞癌和胆管细胞癌的研究中。SPRR2A在舌鳞状细胞中低表达,诱导过表达SPRR2A可以轻微的增加细胞增殖,但减少舌鳞状癌细胞的远处转移[14]。在胆管细胞癌中过表达SPRR2A可增强肿瘤的局部浸润性,阻止肿瘤的远处转移[15]。SPRR2在人乳头瘤病毒8型(human paplloma viruses 8, HPV8)转基因小鼠的鳞状细胞乳头状瘤形成期间表达增强,而在口腔鳞状细胞癌中呈低表达[16-17]。SPRR2A在肿瘤中发挥着重要作用。
为了检测SPRR2A对于胃癌细胞增殖和迁移能力的影响,本研究选取不同分化能力的人胃癌细胞株(SGC-7901、MKN-28和BGC-823)和正常的人胃黏膜上皮细胞(GES-1),通过实时荧光定量PCR和Western blot法检测各细胞株中SPRR2A表达情况。与人胃黏膜上皮细胞GES-1比较,SPRR2A在BGC-832细胞中高表达,在SGC-7901细胞中低表达,因此选用BGC-832和SCG-7901细胞转染靶向SPRR2A的siRNA片段或表达质粒以构建沉默或过表达SPRR2A的胃癌细胞株。通过RTCA和CCK-8细胞增殖实验和细胞迁移实验检测SPRR2A对胃癌细胞增殖和迁移能力的影响。结果显示,沉默SPRR2A后的BGC-823细胞增殖和迁移能力降低,而上调SPRR2A表达的SCG-7901细胞增殖和迁移能力增加,因此推测SPRR2A基因在胃癌细胞的增殖和迁移过程中起重要作用。有研究显示,在胃硬癌细胞株OCUM-2M中发现SPRR2A表达下调可促进OCUM-2M胃癌细胞株的侵袭和迁移[18],这与本研究结果相反,这可能与实验选取的胃癌细胞组织来源不同有关。胃硬癌为一种低分化癌伴有间质增生及广泛弥漫性浸润,可以找到印戒细胞。而本研究选取的胃癌细胞株为不同分化的普通型腺癌,间质内无显著的增生。这说明在SPRR2A基因表达量不同的胃癌细胞株中,SPRR2A基因所起到的作用具有一定的差异。
本研究结果显示,沉默或过表达SPRR2A可以影响胃癌细胞的增殖和迁移能力。现有的一些研究认为,SPRR2A促进细胞的迁移与上皮间质转化(epithelial-mesenchymal transition, EMT)有关。EMT使肿瘤细胞获得迁移与侵袭、抗凋亡和降解细胞外基质的能力等间质表型,与肿瘤迁移和侵袭密切相关, 提示着预后不良[19]。在人胆管上皮细胞中,过表达SPRR2A可改变胆管上皮细胞形态,向梭形间质细胞转变,并促进细胞迁移[20]。在胆管癌细胞中,过表达SPRR2A导致细胞侵袭性增加,但无法形成转移灶,SPRR2A促进上皮间质转化这一过程,主要与信号传导与转录激活因子3 (signal transducer and activator of transcription,STAT3)激活酪氨酸激酶受体家族成员-表皮生长因子受体(epidermal growth factor receptor,EGFR)和酪氨酸激酶受体2(erb-b2 receptor tyrosine-protein kinase 2,ErbB2)以及上调糖蛋白130 (glycoprotein 130,gp130)有关[21]。目前关于SPRR2A在胃癌中作用具体机制研究很少,笔者推测SPRR2A在胃癌的发生过程中可能通过促进癌组织细胞周围EMT形成,进而促进胃癌细胞的转移和浸润,其具体机制有待进一步验证。
综上所述,SPRR2A能够影响胃癌细胞的增殖及迁移,但具体调控的基因和分子机制尚不清楚。本文初步探讨SPRR2A与胃癌增殖和转移的关系,将有望作为临床上治疗胃癌的新靶点及生物标志物。
| [1] |
Siegel RL, Miller KD, Jemal A. Cancer statistics, 2019[J]. CA Cancer J Clin, 2019, 69(1): 7-34. DOI:10.3322/caac.21551 |
| [2] |
Bray F, Ferlay J, Soerjomataram I, et al. Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J]. CA Cancer J Clin, 2018, 68(6): 394-424. DOI:10.3322/caac.21492 |
| [3] |
倪璐, 邱萌. 胃癌围手术期化疗的现状和研究进展[J]. 实用肿瘤杂志, 2019, 34(5): 390-396. |
| [4] |
Rojas A, Araya P, Gonzalez I, et al. Gastric tumor microenvironment[J]. Adv Exp Med Biol, 2020, 1226: 23-35. |
| [5] |
Sitarz R, Skierucha M, Mielko J, et al. Gastric cancer: epidemiology, prevention, classification and treatment[J]. Cancer Manag Res, 2018, 10(7): 239-248. |
| [6] |
Carregaro F, Stefanini AC, Henrique T, et al. Study of small proline-rich proteins (SPRRs) in health and disease: a review of the literature[J]. Arch Dermatol Res, 2013, 305(10): 857-866. DOI:10.1007/s00403-013-1415-9 |
| [7] |
Sobiak B, Graczyk-Jarzynka A, Lesniak W. Comparison of DNA methylation and expression pattern of S100 and other epidermal differentiation complex genes in differentiating keratinocytes[J]. J Cell Biochem, 2016, 117(5): 1192-1198. |
| [8] |
Abhishek S, Palamadai Krishnan S. Epidermal differentiation complex: a review on its epigenetic regulation and potential drug targets[J]. Cell, 2016, 18(1): 1-6. |
| [9] |
Sun FJ, Kaur S, Ziemer D, et al. Decreased gastric bacterial killing and up-regulation of protective genes in small intestine in gastrin-defificient mouse[J]. Dig Dis Sci, 2003, 48(5): 976-985. DOI:10.1023/A:1023068116934 |
| [10] |
Park YK, Franklin JL, Settle SH, et al. Gene expression profifile analysis of mouse colon embryonic development[J]. Genesis, 2005, 41(1): 1-12. DOI:10.1002/gene.20088 |
| [11] |
Moggs JG, Tinwell H, Spurway T, et al. Phenotypic anchoring of gene expression changes during estrogen-induced uterine growth[J]. Environ Health Perspect, 2004, 112(16): 1589-1606. DOI:10.1289/txg.7345 |
| [12] |
Morris JS, Stein T, Pringle MA, et al. Involvement of axonal guidance proteins and their signaling partners in the developing mouse mammary gland[J]. J Cell Physiol, 2006, 206(1): 16-24. DOI:10.1002/jcp.20427 |
| [13] |
Ramakrishnan VR, Gonzalez JR, Cooper SE, et al. RNA sequencing and pathway analysis identify tumor necrosis factor alpha driven small proline-rich protein dysregulation in chronic rhinosinusitis[J]. Am J Rhinol Allergy, 2017, 31(5): 283-288. DOI:10.2500/ajra.2017.31.4457 |
| [14] |
Fang Z, Zhang S, Wang Y, et al. Long non-coding RNA MALAT-1 modulates metastatic potential of tongue squamous cell carcinomas partially through the regulation of small proline rich proteins[J]. BMC Cancer, 2016, 16(1): 706. DOI:10.1186/s12885-016-2735-x |
| [15] |
Specht S, Isse K, Nozaki I, et al. SPRR2A expression in cholangiocarcinoma increases local tumor invasiveness but prevents metastasis[J]. Clin Exp Metastasis, 2013, 30(7): 877. DOI:10.1007/s10585-013-9589-2 |
| [16] |
Lazic D, Alborzi F, Marcuzzi GP, et al. Ehanced StefinA and SPRR2 expression during papilloma formation in HPV8 transgenic mice[J]. J Dematol Sci, 2011, 62(2): 84-90. |
| [17] |
Pasini FS, Maistro S, Snitcovsky I, et al. Four-gene expression model predictive of lymph node metastases in oral squamous cell carcinoma[J]. Acta Oncol, 2012, 51(1): 77-85. DOI:10.3109/0284186X.2011.620619 |
| [18] |
Hippo Y, Yashiro M, Ishii M, et al. Differential gene expression profiles of scirrhous gastric cancer cells with high metastatic potential to peritoneum or lymph nodes[J]. Cancer Res, 2001, 61(3): 889-895. |
| [19] |
龙景培, 卜贺启, 刘殿雷. 冬凌草甲素对结肠癌LOVO细胞增殖和EMT影响的实验研究[J]. 实用肿瘤杂志, 2019, 34(4): 309-315. |
| [20] |
Demetris AJ, Specht S, Nozaki I, et al. Small proline-rich proteins (SPRR) function as SH3 domain ligands, increase resistance to injury and are associated with epithelial–mesenchymal transition (EMT) in cholangiocytes[J]. J Hepatol, 2008, 48(2): 276-288. DOI:10.1016/j.jhep.2007.09.019 |
| [21] |
Specht S, Isse K, Nozaki I, et al. SPRR2A expression in cholangiocarcinoma increases local tumor invasiveness but prevents metastasis[J]. Clin Exp Metastasis, 2013, 30(7): 877-890. DOI:10.1007/s10585-013-9589-2 |
 2020, Vol. 35
2020, Vol. 35


