文章信息
- 王雪妮, 张兰慧, 黄冬薇, 钱云峰, 董凤英, 胡亚惠
- Wang Xueni, Zhang Lanhui, Huang Dongwei, Qian Yunfeng, Dong Fengying, Hu Yahui
- G3BP1通过稳定PD-L1 mRNA抑制肺腺癌细胞的免疫杀伤
- G3BP1 inhibits immune killing of lung adenocarcinoma cells by stabilizing PD-L1 mRNA
- 实用肿瘤杂志, 2026, 41(2): 128-135
- Journal of Practical Oncology, 2026, 41(2): 128-135
基金项目
- 广东省医学科学技术研究基金项目(B2022230)
-
通信作者
- 胡亚惠,Email:962273809@qq.com
-
文章历史
- 收稿日期:2025-02-24
2. 南方医科大学南方医院惠侨医疗中心, 广东 广州 510515
2. Huiqiao Medical Center, Nangfang Hospital, Southern Medical University, Guangzhou 510515, China
肺癌是全球发病率和死亡率最高的恶性肿瘤,其中非小细胞肺癌(non-small-cell lung cancer, NSCLC)占80%~85%,而肺腺癌作为NSCLC的主要亚型,发病率逐年攀升,5年生存率 < 20%[1-2]。肿瘤免疫逃逸是肺腺癌治疗耐药和预后不良的核心原因,其中程序性死亡受体配体1[programmed death-ligand 1, PD-L1;又名cluster of differentiation 274(CD274)]通过与T细胞表面程序性死亡受体1(programmed death-1, PD-1)结合抑制免疫活性,是免疫逃逸的关键分子[3-4]。尽管PD-L1抑制剂已成为肺腺癌一线治疗方案,但仅30%的患者响应,且耐药机制尚未完全明确[5-6],因此解析PD-L1的调控机制对优化免疫治疗至关重要。
PD-L1的表达受转录、转录后和翻译后多层面调控,其中RNA结合蛋白(RNA-binding protein, RBP)介导的转录后调控因具有细胞特异性和动态性成为近年研究热点[7-8]。Ras-GTP酶激活蛋白SH3结构域结合蛋白1(Ras-GTPase-activating protein SH3 domain-binding protein 1, G3BP1)作为核心RBP,通过调控mRNA稳定性和介导应激颗粒形成参与肿瘤增殖、转移和耐药[9-10]。近年研究显示,G3BP1在多种癌症中高表达并与不良预后相关:在膀胱癌中,G3BP1与SLU7形成复合物通过PI3K/Akt通路下调主要组织相容性复合体Ⅰ类分子(major histocompatibility complex Ⅰ, MHC-Ⅰ)促进免疫逃逸[11];在结直肠癌中,LINC01088通过吸附miR-548b/c-5p上调G3BP1,进而间接调控PD-L1表达[12];在NSCLC中,G3BP1通过降解信号转导及转录活化因子1(signal transducer and activator of transcription 1, STAT1)减少趋化因子分泌,抑制细胞毒性T淋巴细胞(cytotoxic T lymphocyte, CTL)浸润[13]。
目前,尽管已有研究揭示,G3BP1在肿瘤免疫逃逸中具有一定作用,但针对肺腺癌这一特定亚型的相关研究仍存在关键缺口。在调控关系层面,肺腺癌中G3BP1与PD-L1的直接调控关系尚未明确。此前虽有研究报道,结直肠癌中G3BP1可通过间接途径调控PD-L1表达,但对于肺腺癌而言,G3BP1作为RBP,是否能直接结合PD-L1 mRNA,以及如何影响PD-L1 mRNA稳定性,目前仍缺乏直接的实验证据支撑[12]。除此之外,G3BP1对肺腺癌免疫杀伤的直接作用也存在研究空缺。现有研究多聚焦于G3BP1对免疫微环境的间接调控,例如通过影响趋化因子分泌和调节MHC-Ⅰ表达等方式参与免疫逃逸,而针对其是否能通过调控PD-L1表达,进而影响T细胞对肺腺癌细胞直接杀伤效应的功能验证,尚未有相关研究报道[11, 13]。
针对上述研究的不足,本研究在肺腺癌细胞中结合RNA免疫共沉淀(RNA binding protein immunoprecipitation, RIP)实验、免疫荧光-荧光原位杂交(fluorescence in situ hybridization, FISH)实验和RNA稳定性实验证实,G3BP1可直接结合PD-L1 mRNA并增强其稳定性,与膀胱癌和结直肠癌中G3BP1的间接调控通路形成区别;在功能验证上,通过构建G3BP1过表达和G3BP1敲低的肺腺癌细胞模型,结合T细胞杀伤实验,明确G3BP1-PD-L1轴与肺腺癌细胞免疫杀伤的直接关联,为G3BP1成为肺腺癌免疫治疗新靶点提供依据。
1 材料与方法 1.1 实验材料人肺腺癌细胞株A549和H1975均购自美国标准培养收集所(American Type Culture Collection, ATCC)。一抗包括兔抗人G3BP1、PD-L1和甘油醛-3-磷酸脱氢酶(glyceraldehyde-3-phosphate dehydrogenase, GAPDH)单抗均购自美国CST公司。LipofectamineTM 3000购自美国Invitrongen公司。G3BP1-shRNA(包括G3BP1-shRNA1和G3BP1-shRNA2)及其阴性对照NC-shRNA重组慢病毒质粒购自上海英骏生物技术有限公司。真核过表达质粒pcDNA3.1-G3BP1及其对照质粒pcDNA3.1购自上海吉玛制药有限公司。MagnaRIP® RBP免疫沉淀试剂盒购自美国Millipore公司。
1.2 细胞培养和转染将A549和H1975细胞接种于含有10%胎牛血清、100 U/mL青霉素和100 μg/mL链霉素的DMEM培养液的细胞培养皿中。细胞长期培养在含5% CO2的37℃湿润培养箱中,当细胞融合度达到80%~90%时,使用0.25%胰蛋白酶消化细胞并传代培养。根据LipofectamineTM 3000说明书中操作方法将G3BP1-shRNA1、G3BP1-shRNA2和NC-shRNA转染H1975细胞,分为shNC组、shG3BP1#1组和shG3BP1#2组,收集转染6 h后的细胞,其中shG3BP1#1组shRNA靶序列为5’-TTAGTCTTTCACTTCCAATTT-3’,shG3BP1#2组为5’-AGTGCGAGAACAACGAATAAA-3’。将稀释的过表达质粒pcDNA3.1-G3BP1及其对照质粒pcDNA3.1与LipofectamineTM 3000混合液转染至A549细胞中,分别为G3BP1 OE组和Vector组,收集转染6 h后的细胞。
1.3 逆转录聚合酶链反应(reverse transcription polymerase chain reaction, RT-PCR)检测G3BP1和PD-L1的mRNA水平采用总RNA提取试剂盒[天根生化科技(北京)有限公司]提取细胞的总RNA,使用高容量cDNA逆转录试剂盒(Thermo Fisher Scientific,美国)逆转录成cDNA模板。以cDNA作为模板,在冰上进行定量PCR体系添加,使用PrimeSTAR MAX Premix试剂盒(Takara Bio公司,日本)扩增G3BP1、PD-L1(CD274)和内参基因GAPDH。扩增条件:95℃ 10 min预变性,95℃ 15 s变性,60℃ 1 min退火/延伸(45个循环)。使用2-ΔΔCT方法计算G3BP1和CD274相对表达量。G3BP1正向引物为5’-CGGGCGGGAATTTGTGAGA-3’,反向引物为5’-TCTGTCCGTAGACTGCATCTG-3’。CD274正向引物为5’-TATGGTGGTGCCGACTACAA-3’,反向引物为5’-TGCTTGTCCAGATGACTTCG-3’。GAPDH正向引物为5’-GGAGCGAGATCCCTCCAAAAT-3’,反向引物为5’-GGCTGTTGTCATACTTCTCATGG-3’。
1.4 蛋白质印迹法检测G3BP1和PD-L1的蛋白水平通过蛋白提取试剂盒(Thermo Fisher Scientific,美国)提取细胞总蛋白,使用BCA法检测蛋白浓度和质量。将蛋白在10%十二烷基硫酸钠聚丙烯酰胺凝胶电泳(sodium dodecylsulfate-polyacrylamide gel electrophoresis, SDS-PAGE)电泳后转移到聚偏氟乙烯[poly(vinylidene fluoride), PVDF]膜上,PVDF与封闭溶液在室温下孵育以阻断非特异性结合,膜与G3BP1、PD-L1和GAPDH一抗(稀释比例均为1∶1 000)4℃下过夜孵育后,加入辣根过氧化物酶(horseradish peroxidase, HRP)标记的山羊抗兔二抗(Thermo Fisher Scientific,美国;稀释比例1∶10 000)室温下孵育2 h后,增强化学发光(enhanced chemiluminescence, ECL)显色系统中显影,分析条带。
1.5 免疫荧光-FISH实验将细胞接种在共聚焦培养皿中,过夜培养,用4%多聚甲醛固定15 min和0.5% Triton X-100渗透10 min。室温下用10%小牛血清封闭1 h,与G3BP1一抗和PD-L1 mRNA FISH杂交液在4℃孵育过夜。与二抗孵育后,用PBS冲洗细胞,进行FISH,室温下将细胞与15%去离子化甲酰胺在1×柠檬酸钠中预杂交15 min。在37℃杂交缓冲液中孵育过夜。杂交完成后,37℃用15%甲酰胺在1×柠檬酸钠中洗涤30 min,此过程重复3次。最后使用含4’, 6-二脒基-2-苯基吲哚(4', 6-diamidino-2-phenylindole dihydrochloride, DAPI)的FluoroshieldTM封固剂(Sigma,美国)固定,PD-L1 mRNA FISH探针序列为Cy5-CCTTTCATTTGGAGGATGTGCCAGAGGTAGTTCTGGGATG-Cy5。
1.6 RIP实验根据MagnaRIPTM RBP免疫沉淀试剂盒说明书进行实验:细胞在RIP裂解缓冲液中裂解,离心后,上清液与抗G3BP1抗体在4℃条件下孵育过夜,再将磁珠添加到上述混合物中形成免疫沉淀复合物,纯化免疫沉淀复合物,通过RT-PCR检测RNA富集情况。
1.7 RNA稳定性实验2 μg/mL放线菌素D处理细胞0、4、8和12 h后收集细胞,进行RNA提取,采用RT-PCR检测PD-L1 mRNA水平。
1.8 T细胞杀伤实验使用人CD8+ T细胞分离试剂盒(STEMCELL Technologies,加拿大)从人外周血中分离得到CD8+ T细胞,将细胞培养于含有10%胎牛血清、55 μmol/L β-巯基乙醇、1%青霉素/链霉素和10 ng/mL白介素-2(interleukin-2, IL-2)的RPMI 1640培养液中,用3 μg/mL抗CD3和CD28单克隆抗体(Gibco,美国)激活CD8+ T细胞48 h,生成CTL。在T细胞杀伤实验中,转染成功的肺腺癌细胞株与CTL以1∶10比例共同培养48 h,然后用1×PBS冲洗细胞3次去除死亡的细胞和CTL,剩余细胞用4%多聚甲醛固定,结晶紫染色。细胞结晶紫染色强度采用Image J软件分析,从4个独立的实验中分析相对细胞数。
1.9 在线数据库分析2022年8月13日通过在线数据库癌症基因组图谱(The Cancer Genome Atlas, TCGA)分析肺腺癌患者中G3BP1与PD-L1表达的相关性。利用Kaplan-Meier plotter数据库(http://kmplot.com/analysis/)[14]分析G3BP1与PD-L1的表达与肺腺癌患者预后的关系。
1.10 统计学分析应用SPSS 19.0统计学软件分析数据。每组实验重复3次。计量资料采用均数±标准差(x±s)表示,组间比较采用t检验。采用Kaplan-Meier法进行生存分析。以P < 0.05为差异具有统计学意义。
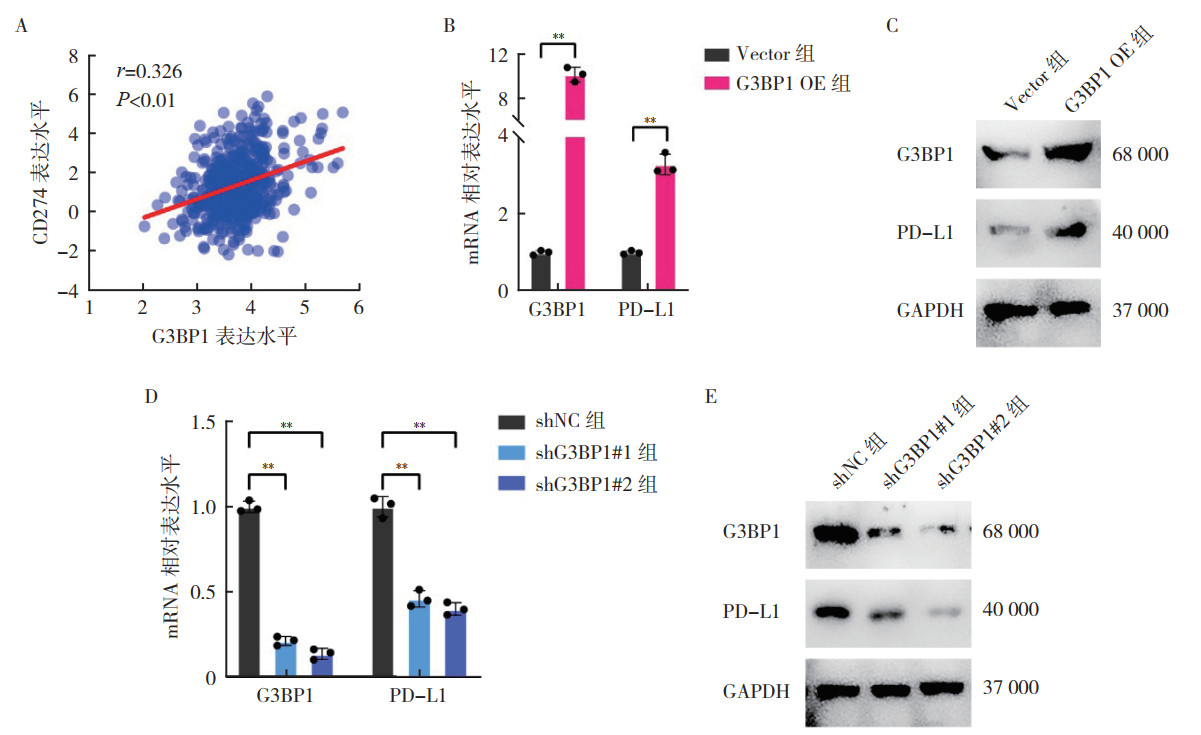
2 结果 2.1 G3BP1促进肺腺癌细胞的PD-L1表达TCGA数据库分析显示,526例肺腺癌患者样本中G3BP1表达水平与PD-L1(CD274)呈正相关(r=0.326,P < 0.01;图 1A)。A549细胞中,利用真核过表达质粒pcDNA3.1-G3BP1构建G3BP1过表达细胞株(G3BP1 OE组),经RT-PCR与蛋白质印迹法检测证实构建成功(图 1B~1C)。与对照Vector组比较,G3BP1 OE组PD-L1的mRNA与蛋白表达水平均上调(均P < 0.05)。H1975细胞中开展反向验证,通过转染G3BP1-shRNA1、G3BP1-shRNA2和NC-shRNA成功构建G3BP1敲低的H1975细胞株及其对照(图 1D~1E)。RT-PCR和蛋白质印迹法显示,与shNC组比较,转染G3BP1-shRNA1和G3BP1-shRNA2的H1975细胞中,PD-L1的mRNA和蛋白表达水平均下降(均P < 0.05)。
|
| 注 A:基于TCGA数据库对526例肺腺癌患者样本中G3BP1的表达水平与CD274(PD-L1)表达水平的相关性分析;B:RT-PCR分析Vector组和G3BP1 OE组A549细胞中G3BP1和PD-L1的mRNA水平;C:蛋白质印迹法检测G3BP1 OE组和Vector组A549细胞中G3BP1和PD-L1的蛋白水平;D:RT-PCR分析shG3BP1#1组、shG3BP1#2组及其对照shNC组H1975细胞中G3BP1和PD-L1的mRNA水平;E:蛋白质印迹法检测shG3BP1#1组、shG3BP1#2组及其对照shNC组H1975细胞中G3BP1和PD-L1的蛋白水平;G3BP1:Ras-GTP酶激活蛋白SH3结构域结合蛋白1(Ras-GTPase-activating protein SH3 domain-binding protein 1);CD274:cluster of differentiation 274;PD-L1:程序性死亡受体配体1(programmed death-ligand 1);GAPDH:甘油醛-3-磷酸脱氢酶(glyceraldehyde-3-phosphate dehydrogenase);**P < 0.01 图 1 G3BP1促进肺腺癌细胞的PD-L1表达 Fig.1 G3BP1 promoted the expression of PD-L1 in lung adenocarcinoma cells |
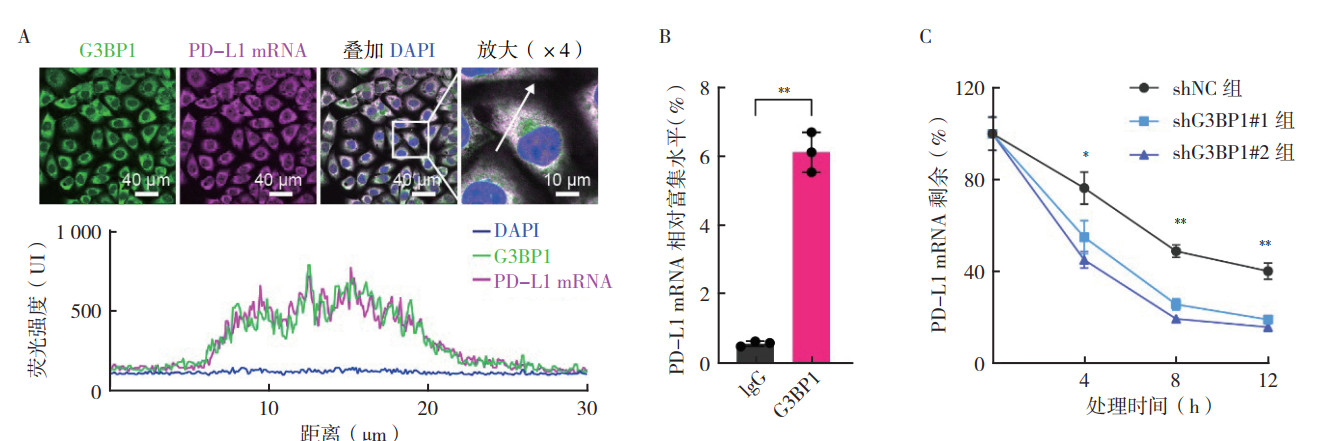
免疫荧光-FISH实验显示,A549细胞中G3BP1蛋白和PD-L1 mRNA存在显著共定位现象(图 2A)。A549细胞中RIP实验表明,与对照组比较,G3BP1抗体组PD-L1 mRNA的富集程度增加(P < 0.01,图 2B),证实G3BP1能特异性结合PD-L1 mRNA。RNA稳定性实验显示,与shNC组比较,敲低G3BP1的H1975细胞中,随着时间的推移,PD-L1 mRNA的稳定性出现明显下降(图 2C)。
|
| 注 A:免疫荧光-荧光原位杂交实验显示,A549细胞中G3BP1蛋白和PD-L1 mRNA存在显著共定位现象;B:RNA免疫共沉淀实验分析A549细胞中对照组(IgG)和G3BP1抗体组PD-L1 mRNA的富集程度;C:RNA稳定性实验分析对照组(shNC组)和G3BP1敲低的shG3BP1#1组和shG3BP1#2组H1975细胞中PD-L1 mRNA的稳定性变化;G3BP1:Ras-GTP酶激活蛋白SH3结构域结合蛋白1(Ras-GTPase-activating protein SH3 domain-binding protein 1);PD-L1:程序性死亡受体配体1(programmed death-ligand 1);DAPI:4’, 6-二脒基-2-苯基吲哚(4', 6-diamidino-2-phenylindole dihydrochloride);*与shG3BP1#1组和shG3BP1#2组比较,均P < 0.05;**与shG3BP1#1组和shG3BP1#2组比较,均P < 0.01 图 2 肺腺癌细胞中G3BP1结合PD-L1的mRNA促进其稳定性 Fig.2 G3BP1 binding to the mRNA of PD-L1 promoted the stability of PD-L1 mRNA in lung adenocarcinoma cells |
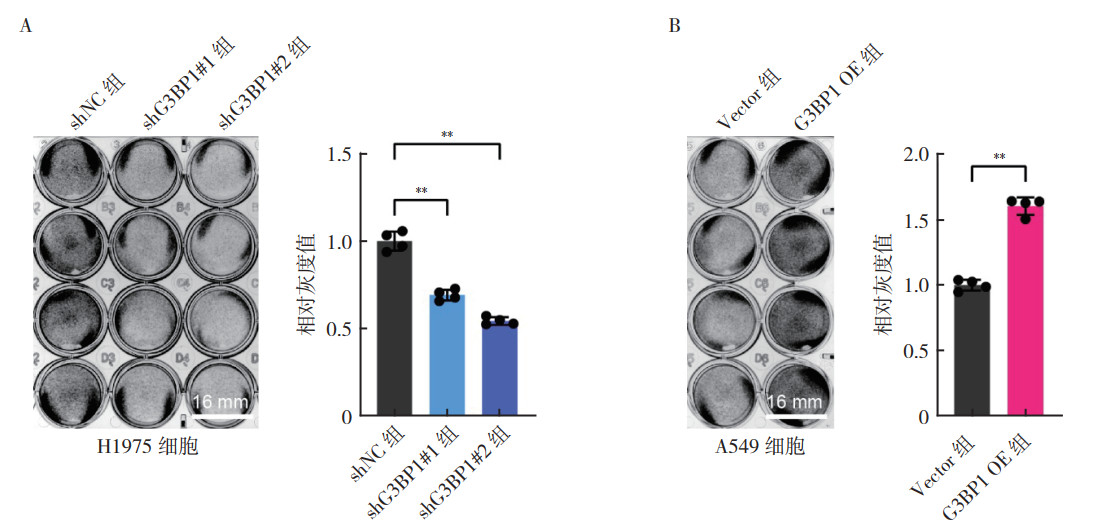
T细胞杀伤实验显示,与CTL共培养48 h后,H1975细胞中,与shNC组比较,shG3BP1#1组和shG3BP1#2组中肿瘤细胞数量均减少(均P < 0.01,图 3A),表明G3BP1表达水平降低可增强肿瘤细胞对T细胞杀伤的敏感性。而过表达G3BP1的A549细胞的肿瘤细胞数量较Vector组增多(P < 0.01,图 3B),表明G3BP1通过抑制人淋巴细胞的杀伤功能降低肺腺癌细胞的免疫原性。
|
| 注 A:T细胞杀伤实验分析shNC组、shG3BP1#1组和shG3BP1#2组H1975细胞中肿瘤细胞数量;B:T细胞杀伤实验分析Vector组和G3BP1 OE组A549细胞中肿瘤细胞数量;G3BP1:Ras-GTP酶激活蛋白SH3结构域结合蛋白1(Ras-GTPase-activating protein SH3 domain-binding protein 1);**P < 0.01 图 3 G3BP1抑制肺腺癌细胞的免疫杀伤 Fig.3 G3BP1 inhibited the immune killing of lung adenocarcinoma cells |
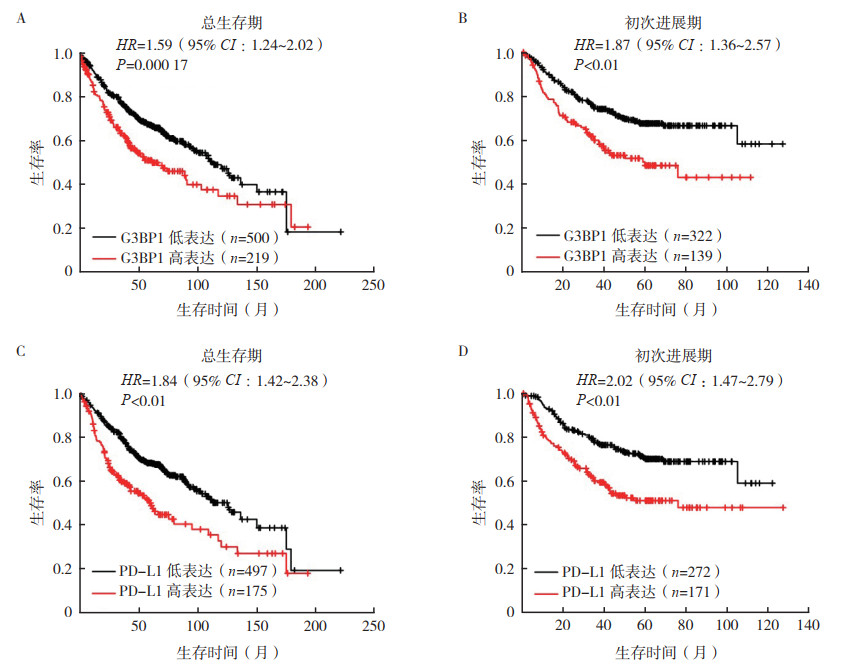
Kaplan-Meier plotter数据库中,以系统自动计算的最佳cutoff值为分界,将G3BP1和PD-L1表达量高于该值的肺腺癌患者定义为高表达组,其余患者为低表达组。G3BP1和PD-L1高表达的肺腺癌患者均较相应低表达患者总生存期(overall survival, OS)和初次进展期(first progression, FP)均缩短(均P < 0.01,图 4)。
|
| 注 A:G3BP1表达与肺腺癌患者总生存期的关系;B:G3BP1表达与肺腺癌患者初次进展期的关系;C:PD-L1表达与肺腺癌患者总生存期的关系;D:PD-L1表达与肺腺癌患者初次进展期的关系;G3BP1:Ras-GTP酶激活蛋白SH3结构域结合蛋白1(Ras-GTPase-activating protein SH3 domain-binding protein 1);PD-L1:程序性死亡受体配体1(programmed death-ligand 1) 图 4 Kaplan-Meier plotter数据库分析显示G3BP1和PD-L1高表达的肺腺癌患者预后不良 Fig.4 Lung adenocarcinoma patients with high G3BP1 or PD-L1 expression had poor prognosis in Kaplan-Meier plotter database |
全球范围内,肺癌已成为严重威胁人类健康的主要恶性肿瘤之一。统计数据表明,NSCLC约占新确诊肺癌患者的80%[15]。其中,肺腺癌作为最常见的病理亚型,约占所有NSCLC病例的50%,且其发病率呈逐年上升态势[16]。肺腺癌起源于支气管黏膜上皮,具备显著的高度浸润性与破坏性生长特性,极易侵袭血管和淋巴系统,致使血液与淋巴转移快速发生,临床病程进展迅猛。尽管当前针对肺腺癌的治疗方案涵盖手术、放化疗、靶向治疗和免疫治疗等多种手段,但整体治疗效果仍差强人意,患者5年OS率长期处于较低水平[17-19]。因此,深入剖析肺腺癌发生和发展的精确分子机制,对于实现疾病的早期诊断和优化临床治疗策略,具有至关重要的意义。
恶性肿瘤的发生与发展主要历经免疫消除、免疫平衡和免疫逃逸3个关键阶段,其中免疫逃逸作为肿瘤持续进展的核心环节,是当前肿瘤研究的重点。PD-L1作为免疫球蛋白超家族中的Ⅰ型跨膜蛋白,由CD274基因编码,在肿瘤免疫逃逸机制中发挥着枢纽作用[20-21]。PD-L1在肺癌[22]、乳腺癌[23]、结肠癌[24]和胃癌[25]等多种恶性肿瘤组织和细胞中均呈高表达状态。其表达水平与肿瘤分期、侵袭转移能力、治疗效果和预后密切相关。本研究利用Kaplan-Meier plotter数据库对肺腺癌患者生存数据进行分析显示,PD-L1高表达的肺腺癌患者OS和FP短于低表达患者,表明PD-L1高表达预示患者预后不良。然而,PD-L1表达调控机制复杂,涉及转录、转录后和翻译后等多个层面。深入探究PD-L1表达调控的分子机制,将为研发新一代抗肿瘤免疫治疗药物提供关键理论依据,对推动肿瘤精准治疗具有重要意义。
G3BP1是一种能与Ras-GTP酶激活蛋白的SH3结构域特异性结合的多功能蛋白,广泛参与细胞生长、转移、分化和凋亡等重要生物学过程,在调节mRNA稳定性和介导应激颗粒形成等方面发挥关键作用[26-27]。近年来,大量研究聚焦G3BP1在肿瘤发生和发展中的作用。G3BP1蛋白在肺癌、结肠癌、乳腺癌、肝癌和胰腺癌等多种恶性肿瘤组织和细胞系中呈高表达[28-31]。在肺癌细胞H1299中,下调G3BP1表达能够抑制Src/黏着斑激酶(focal adhesion kinase, FAK)信号通路,进而抑制肺癌细胞的生长、迁移和侵袭[32]。本研究发现,肺腺癌组织中G3BP1高表达患者预后较差。为进一步探究G3BP1在肺腺癌中的作用机制,本研究成功构建G3BP1过表达的A549细胞株和G3BP1敲低的H1975细胞株,并开展T细胞杀伤实验。结果显示,过表达G3BP1可抑制肺腺癌细胞的免疫杀伤作用,而沉默G3BP1则能增强免疫杀伤效果。上述结果表明,G3BP1与肺腺癌的发生和发展密切相关,抑制其表达有望增强T细胞免疫活性,为肿瘤免疫治疗提供新的潜在靶点。然而,G3BP1抑制肺腺癌细胞免疫杀伤的具体分子机制仍有待深入研究。
T细胞表面PD-1与其配体PD-L1结合后,可抑制机体细胞免疫应答,为肿瘤细胞免疫逃逸创造条件。为探究G3BP1与PD-L1在肺腺癌细胞免疫杀伤中的关联,本研究首先通过TCGA数据库对526例肺腺癌患者样本进行分析发现,G3BP1表达水平与PD-L1呈正相关。进一步通过细胞水平实验验证,在构建的G3BP1过表达肺腺癌细胞株中,PD-L1蛋白表达上调;而在G3BP1沉默细胞株中,PD-L1表达水平降低,证实G3BP1对肺腺癌细胞PD-L1表达具有正向调控作用。基于G3BP1作为RBP的特性,综合运用免疫荧光-FISH、RIP和RNA稳定性检测等发现,G3BP1能够直接结合PD-L1的mRNA,并增强其稳定性。这表明,G3BP1通过稳定PD-L1的mRNA促进PD-L1蛋白表达,实现对肺腺癌细胞免疫杀伤的抑制作用。
综上所述,本研究揭示,G3BP1通过稳定PD-L1 mRNA协同调控肺腺癌细胞免疫逃逸的新机制。这一发现为解析肺腺癌免疫逃逸的分子机制提供崭新视角,为靶向G3BP1的新型免疫治疗策略奠定坚实的理论基础,有望推动肺腺癌精准诊疗领域的突破性进展。值得关注的是,靶向G3BP1的免疫治疗策略构建了“机制-靶点-药物-标志物”的全链条转化路径。随着临床前研究的深入和临床试验数据的持续积累,G3BP1靶向药物有望嵌入肺腺癌免疫治疗的核心体系,成为连接基础研究与临床应用的关键枢纽,为实现肺腺癌的个体化精准治疗开辟全新路径。
利益冲突 所有作者声明无利益冲突
| [1] |
Siegel RL, Miller KD, Wagle NS, et al. Cancer statistics, 2023[J]. CA Cancer J Clin, 2023, 73(1): 17-48. |
| [2] |
Jenkins R, Walker J, Roy UB. 2022 cancer statistics: Focus on lung cancer[J]. Future Oncol, 2024, 22: 1-11. |
| [3] |
Topalian SL, Drake CG, Pardoll DM. Targeting the PD-1/B7-H1(PD-L1) pathway to activate anti-tumor immunity[J]. Curr Opin Immunol, 2012, 24(2): 207-212. DOI:10.1016/j.coi.2011.12.009 |
| [4] |
Cui YN, Li J, Zhang PP, et al. B4GALT1 promotes immune escape by regulating the expression of PD-L1 at multiple levels in lung adenocarcinoma[J]. J Exp Clin Cancer Res, 2023, 42(1): 146. DOI:10.1186/s13046-023-02711-3 |
| [5] |
Dantoing E, Piton N, Salaün M, et al. Anti-PD1/PD-L1 immunotherapy for non-small cell lung cancer with actionable oncogenic driver mutations[J]. Int J Mol Sci, 2021, 22(12): 6288. DOI:10.3390/ijms22126288 |
| [6] |
He JB, Hu Y, Hu MM, et al. Development of PD-1/PD-L1 pathway in tumor immune microenvironment and treatment for non-small cell lung cancer[J]. Sci Rep, 2015, 5: 13110. DOI:10.1038/srep13110 |
| [7] |
Cha JH, Chan LC, Li CW, et al. Mechanisms controlling PD-L1 expression in cancer[J]. Mol Cell, 2019, 76(3): 359-370. DOI:10.1016/j.molcel.2019.09.030 |
| [8] |
Cai ZL, Zhai XX, Xu JD, et al. ELAVL1 regulates PD-L1 mRNA stability to disrupt the infiltration of CD4-positive T cells in prostate cancer[J]. Neoplasia, 2024, 57: 101049. DOI:10.1016/j.neo.2024.101049 |
| [9] |
Yang PG, Mathieu C, Kolaitis RM, et al. G3BP1 is a tunable switch that triggers phase separation to assemble stress granules[J]. Cell, 2020, 181(2): 325-345. DOI:10.1016/j.cell.2020.03.046 |
| [10] |
Guo JY, Huang RY, Mei Y, et al. Application of stress granule core element G3BP1 in various diseases: a review[J]. Int J Biol Macromol, 2024, 282(Pt 5): 137254. |
| [11] |
Zheng XC, Chen JW, Deng MH, et al. G3BP1 and SLU7 jointly promote immune evasion by downregulating MHC-I via PI3K/Akt activation in bladder cancer[J]. Adv Sci, 2024, 11(7): 2305922. DOI:10.1002/advs.202305922 |
| [12] |
Li CM, Pan B, Wang XH, et al. Upregulated LINC01088 facilitates malignant phenotypes and immune escape of colorectal cancer by regulating microRNAs/G3BP1/PD-L1 axis[J]. J Cancer Res Clin Oncol, 2022, 148(8): 1965-1982. DOI:10.1007/s00432-022-03981-8 |
| [13] |
Wang JL, Jia YL, Liu TX, et al. Tumor cell-intrinsic BIN1 deficiency promotes the immunosuppression and impedes ferroptosis of non-small cell lung cancer via G3BP1-mediated degradation of STAT1[J]. J Exp Clin Cancer Res, 2025, 44(1): 141. DOI:10.1186/s13046-025-03404-9 |
| [14] |
Györffy B, Surowiak P, Budczies J, et al. Online survival analysis software to assess the prognostic value of biomarkers using transcriptomic data in non-small-cell lung cancer[J]. PLoS One, 2013, 8(12): e82241. DOI:10.1371/journal.pone.0082241 |
| [15] |
Bray F, Laversanne M, Sung H, et al. Global cancer statistics 2022:GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J]. CA A Cancer J Clin, 2024, 74(3): 229-263. |
| [16] |
Dong HH, Tian YH, Guo YJ, et al. Integrative multiomic and immune profiling of lung adenocarcinoma: molecular landscapes, gene expression, and treatment response insights[J]. Oncologist, 2025, 30(10): oyaf191. DOI:10.1093/oncolo/oyaf191 |
| [17] |
Imielinski M, Berger AH, Hammerman PS, et al. Mapping the hallmarks of lung adenocarcinoma with massively parallel sequencing[J]. Cell, 2012, 150(6): 1107-1120. DOI:10.1016/j.cell.2012.08.029 |
| [18] |
Succony L, Rassl DM, Barker AP, et al. Adenocarcinoma spectrum lesions of the lung: Detection, pathology and treatment strategies[J]. Cancer Treat Rev, 2021, 99: 102237. DOI:10.1016/j.ctrv.2021.102237 |
| [19] |
Zhou CW, Zhong RQ, Zhang L, et al. Exploring the mechanism of rosmarinic acid in the treatment of lung adenocarcinoma based on bioinformatics methods and experimental validation[J]. Discov Oncol, 2025, 16(1): 47. DOI:10.1007/s12672-025-01784-0 |
| [20] |
Lin X, Kang K, Chen P, et al. Regulatory mechanisms of PD-1/PD-L1 in cancers[J]. Mol Cancer, 2024, 23(1): 108. DOI:10.1186/s12943-024-02023-w |
| [21] |
Zhou YJ, Li GL, Wang JY, et al. PD-L1:expression regulation[J]. Blood Sci, 2023, 5(2): 77-91. DOI:10.1097/BS9.0000000000000149 |
| [22] |
Li CL, Li CW, Zhi CC, et al. Clinical significance of PD-L1 expression in serum-derived exosomes in NSCLC patients[J]. J Transl Med, 2019, 17(1): 355. DOI:10.1186/s12967-019-2101-2 |
| [23] |
Monypenny J, Milewicz H, Flores-Borja F, et al. ALIX regulates tumor-mediated immunosuppression by controlling EGFR activity and PD-L1 presentation[J]. Cell Rep, 2018, 24(3): 630-641. DOI:10.1016/j.celrep.2018.06.066 |
| [24] |
Wang LS, Ren F, Wang QF, et al. Significance of programmed death ligand 1 (PD-L1) immunohistochemical expression in colorectal cancer[J]. Mol Diagn Ther, 2016, 20(2): 175-181. DOI:10.1007/s40291-016-0188-1 |
| [25] |
Eto S, Yoshikawa K, Nishi M, et al. Programmed cell death protein 1 expression is an independent prognostic factor in gastric cancer after curative resection[J]. Gastric Cancer, 2016, 19(2): 466-471. DOI:10.1007/s10120-015-0519-7 |
| [26] |
Aulas A, Caron G, Gkogkas CG, et al. G3BP1 promotes stress-induced RNA granule interactions to preserve polyadenylated mRNA[J]. J Cell Biol, 2015, 209(1): 73-84. DOI:10.1083/jcb.201408092 |
| [27] |
Liu ZS, Cai H, Xue W, et al. G3BP1 promotes DNA binding and activation of cGAS[J]. Nat Immunol, 2019, 20(1): 18-28. DOI:10.1038/s41590-018-0262-4 |
| [28] |
Zhang H, Ma Y, Zhang SH, et al. Involvement of Ras GTPase-activating protein SH3 domain-binding protein 1 in the epithelial-to-mesenchymal transition-induced metastasis of breast cancer cells via the Smad signaling pathway[J]. Oncotarget, 2015, 6(19): 17039-17053. DOI:10.18632/oncotarget.3636 |
| [29] |
Lu SA, Du T, Chen H, et al. Diagnostic, prognostic, and immune-related roles of G3BP1 in pan-cancer[J]. Hum Mol Genet, 2025, 34(21): 1808-1828. DOI:10.1093/hmg/ddaf145 |
| [30] |
Dou N, Chen JD, Yu SJ, et al. G3BP1 contributes to tumor metastasis via upregulation of Slug expression in hepatocellular carcinoma[J]. Am J Cancer Res, 2016, 6(11): 2641-2650. |
| [31] |
Zhang H, Zhang SH, He HW, et al. GAP161 targets and downregulates G3BP to suppress cell growth and potentiate cisplaitin-mediated cytotoxicity to colon carcinoma HCT116 cells[J]. Cancer Sci, 2012, 103(10): 1848-1856. DOI:10.1111/j.1349-7006.2012.02361.x |
| [32] |
Zhang H, Zhang SH, He HW, et al. Downregulation of G3BPs inhibits the growth, migration and invasion of human lung carcinoma H1299 cells by suppressing the Src/FAK-associated signaling pathway[J]. Cancer Gene Ther, 2013, 20(11): 622-629. DOI:10.1038/cgt.2013.62 |
 2026, Vol. 41
2026, Vol. 41


