文章信息
- 徐洁, 潘月龙
- 脂联素抑制大肠癌LoVo细胞增殖与侵袭能力
- 实用肿瘤杂志, 2021, 36(1): 33-36
基金项目
- 浙江省医药卫生科技计划项目(2015KYB290);浙江省基础公益研究计划项目(LGF18H160040)
-
通信作者
- 潘月龙,E-mail:hzsyzlkp@sina.com
-
文章历史
- 收稿日期:2020-08-02
2. 浙江大学医学院附属杭州市第一人民医院肿瘤内科,浙江大学医学院附属杭州市肿瘤医院,浙江 杭州 310006
目前的流行病学资料指出,大肠癌在全世界范围内年发病率位列所有恶性肿瘤第3位[1]。肥胖与大肠癌关系密切。脂联素是一种经胰岛素刺激由脂肪组织分泌的特异性血浆激素蛋白,参与糖代谢与脂肪代谢,与肥胖和胰岛素抵抗的发生密切相关[2]。已有研究表明,脂联素可以直接通过抑制细胞生长,如通过大鼠肉瘤病毒癌基因同源物(rat sarcoma viral oncogene homolog,RAS)信号传导[3]和诱导凋亡在大肠癌的发展中起保护作用[4]。一项探讨循环脂联素浓度与大肠癌风险之间关联的前瞻性研究观察18 225例男性血浆脂联素水平发现,血浆脂联素水平与大肠癌危险度呈负相关(RR=0.42,95%CI:0.23~0.78,P=0.01)[5]。本实验旨在研究脂联素对大肠癌细胞的增殖和侵袭能力的影响,探索其可能的作用靶点及机制。
1 材料与方法 1.1 主要试剂重组人脂联素购自美国PEPROTECH公司;基质金属蛋白酶-9(matrix metalloproteinase 9,MMP-9)和E-钙黏附蛋白(E-cadherin,E-cad)购自北京Sino Biological Inc;Ezrin蛋白购自美国Santa Cruz Biotechnology。
1.2 细胞培养大肠癌细胞株LoVo细胞购自浙江大学肿瘤研究所。以LoVo细胞为研究对象,设置空白对照组及4个浓度梯度组(2.5、5、10和20 μg/mL脂联素)。
1.3 细胞实验 1.3.1 MTT法检测细胞增殖抑制率培养LoVo细胞至指数生长期,制成单细胞悬液后以4×105个/mL密度接种于96孔板,待细胞贴壁后加入重组人脂联素使孔中终浓度为2.5、5、10和20 μg/mL(2.5 μg/mL脂联素组、5 μg/mL脂联素组、10 μg/mL脂联素组和20 μg/mL脂联素组),同时设空白对照组,每组设3个复孔,培养24 h,弃上清液,加入90 μL新鲜10%胎牛血清(fetal bovine serum,FBS)培养液,再加入10 μL噻唑蓝(thiazdyl blue tetrazolium bromide,MTT)溶液,继续培养4 h后弃上清液,每孔加入100 μL二甲基亚砜(dimethyl sulfoxide,DMSO),低速振荡10 min,于酶联免疫检测仪490 nm处测量其吸光度(absorbance, A)值。细胞增殖抑制率(%)=(1-实验组细胞A值平均值/对照组细胞A值平均值)×100%。
1.3.2 Transwell小室实验检测细胞侵袭能力在transwell下室面铺纤维黏连蛋白,上室面包被Matrigel 1∶8稀释液,4℃过夜,超净工作台风干,紫外消毒灭菌;吸出培养板中残余液体,每孔加入50 μL含10 mg/mL牛血清蛋白(bovine serum albumin,BSA)的无血清培养液,37℃孵育30 min,形成无基质胶transwell小室。再将LoVo细胞撤血清饥饿12~24 h,0.25%胰酶消化细胞,用含10 mg/mL BSA的无血清培养液重悬,使终密度为5×105个/mL。取细胞悬液200 μL加入小室,同时加入500 μL含不同浓度(2.5、5、10和20 μg/mL)重组人脂联素的FBS培养液,对照组加入等量FBS培养液,24 h后取出小室,甲醇∶冰醋酸(3∶1)固定15 min后用10%Giemsa染色15 min,再用棉签将表面的细胞擦拭去除,然后在10×20倍光学显微镜下随机选取5个视野细胞计数。
1.4 Western Blot法检测E-cad、MMP-9和Ezrin蛋白表达收集指数生长期LoVo细胞,不同浓度(2.5、5、10和20 μg/mL)重组人脂联素处理24 h后,裂解和离心后提取总蛋白,Lowry法测浓度。提取蛋白进行SDS-PAGE凝胶电泳分离,随后电转印至硝酸纤维素(nitrocellulose,NC)膜,分别加入按合适比例稀释的不同分子作为一抗,室温振荡反应1 h,再加入不同的酶标抗体,室温振荡反应1 h,以PBST洗膜3次,每次5 min, 最后加入四甲基联苯胺(tetrabenzidine,TMB)显色液,避光显色至出现条带,记录结果。
1.5 统计学分析采用SPSS 22.0统计学软件分析数据。计量资料采用均数±标准差(x±s)表示,两组间比较采用t检验,多组间比较采用单因素方差分析,组间两两比较采用LSD-t检验。以P < 0.05为差异具有统计学意义。
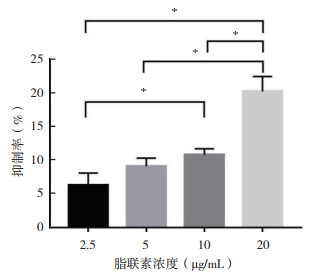
2 结果 2.1 脂联素抑制LoVo细胞增殖能力通过MTT实验发现,2.5、5、10和20 μg/mL的重组人脂联素处理24 h后,LoVo细胞增殖均受到抑制,与空白对照组比较,差异均具有统计学意义(均P < 0.05,表 1,图 1)。组间两两比较显示,20 μg/mL脂联素组细胞增殖抑制率高于其他各组(均P < 0.05),10 μg/mL脂联素组细胞增殖抑制率高于2.5 μg/mL脂联素组(P < 0.05),抑制率呈剂量依赖性。
| 组别 | A值 | 抑制率(%) |
| 空白对照组 | 1.067±0.002 | - |
| 2.5 μg/mL脂联素组 | 1.000±0.019* | 6.3±1.8 |
| 5.0 μg/mL脂联素组 | 0.970±0.012* | 9.1±1.2 |
| 10 μg/mL脂联素组 | 0.952±0.009* | 10.8±0.9 |
| 20 μg/mL脂联素组 | 0.851±0.023* | 20.2±2.2 |
| 注 *与空白对照组比较,P < 0.05 | ||
|
| 注 *P < 0.05 图 1 不同浓度脂联素对LoVo细胞增殖的影响 |
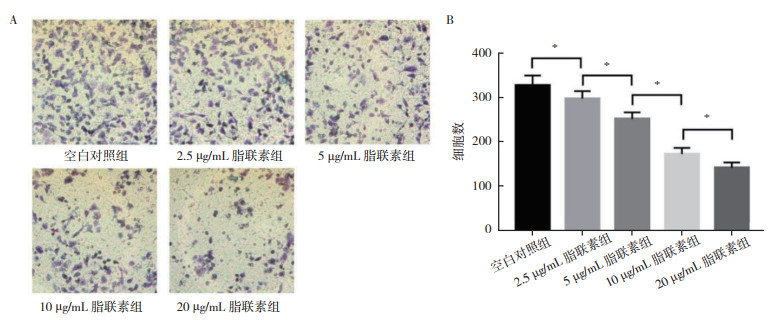
空白对照组、2.5 μg/mL脂联素组、5 μg/mL脂联素组、10 μg/mL脂联素组和20 μg/mL脂联素组LoVo细胞穿膜细胞数分别为(329±22)个、(299±17)个、(253±15)个、(174±14)个和(143±12)个(图 2A)。与空白对照组比较,不同浓度的重组人脂联素作用LoVo细胞24 h后,穿膜细胞数均减少,浓度越高,穿膜细胞数越少,组间两两比较差异具有统计学意义(均P < 0.05,图 2B)。
|
| 注 A:Transwell法检测脂联素对LoVo细胞侵袭能力的影响(Giemsa×200);B:脂联素对LoVo细胞侵袭能力的影响;*P < 0.05 图 2 不同浓度脂联素对LoVo细胞侵袭能力的影响 |
Western blot结果显示,不同浓度(2.5、5、10和20 μg/mL)重组人脂联素作用于LoVo细胞24 h后,可诱导E-cad蛋白表达上调,诱导MMP-9蛋白及Ezrin蛋白下调,且呈剂量依赖性(图 3)。

|
| 注 A:空白对照组;B:2.5 μg/mL脂联素组;C:5 μg/mL脂联素组;D:10 μg/mL脂联素组;E:20 μg/mL脂联素组 图 3 Western blot法检测不同浓度脂联素对LoVo细胞E-cad、Ezrin和MMP-9蛋白表达的影响 |
大肠癌已成为最常见的消化道恶性肿瘤之一[1]。在我国,大肠癌的发病与高蛋白/低纤维饮食及少运动等生活习惯相关,总体呈上升趋势[6]。肥胖是大肠癌患病的高危因素[3]。脂肪组织不仅是储存和释放脂肪的场所,也是一个具有内分泌功能的“器官”,可以分泌多种生物活性分子,其中,血管内皮生长因子、瘦素、肿瘤生长因子-α和白细胞介素-6等能促进血管生成,与多种恶性肿瘤的发生和发展正相关;但脂联素的作用相反,能抑制血管生成,调节炎性反应,与多种恶性肿瘤的发生和发展负相关[7-9]。
现有的大肠癌治疗方法包括手术、化疗、放疗及靶向治疗等。随着化疗药物和靶向治疗药物的进步和多学科协作治疗的发展,大肠癌的治疗效果有明显提高,但肿瘤的侵袭和转移仍是大肠癌患者治疗失败的主要原因[10-11]。因此有必要探索更多的治疗靶点为大肠癌患者带来更好的治疗效果。
侵袭和转移是恶性肿瘤的主要生物学特征,是多因素参与和多步骤完成的生物学过程。恶性肿瘤要实现侵袭转移首先要摆脱细胞间的粘附,才能从原发灶脱落,到达远处器官后形成转移灶[12]。有研究表明,E-cad的表达降低,可以使基质黏附力减低,使肿瘤细胞脱离原发灶,侵犯破坏基底膜及邻近近组织及脉管,造成侵袭和转移[13]。Ezrin是一种膜-细胞骨架链接蛋白,在细胞的运动、迁移和有丝分裂等生理作用中发挥着重要作用。Ezrin的表达可使E-cad向胞内聚集,从而减少膜表面E-cad,影响细胞间的黏附性,并使细胞间隙增宽,运动能力增强。先前有研究发现,与结直肠癌原发肿瘤比较,肝转移灶中Ezrin的表达上调[14];Ezrin基因敲除可抑制表皮生长因子(epidermal growth factor,EGF)诱导的大肠癌肺转移[15]。MMP是一类蛋白水解酶,肿瘤细胞脱离原发灶后,通过释放这种酶降解细胞外基质,从而在肿瘤侵袭和转移中起着重要作用。MMP-9在大肠癌的浸润和转移过程及大肠腺瘤的致癌作用中也发挥着作用,与患者的预后呈负相关[16]。本研究结果显示,脂联素可以促进E-cad的表达,并抑制Ezrin和MMP-9的表达,说明脂联素抑制大肠癌细胞的侵袭迁移可能与此有关。
综上所述,本研究通过重组人脂联素体外作用于大肠癌细胞株LoVo细胞实验,显示脂联素能有效抑制LoVo细胞的增殖及侵袭能力,其机制可能与促进E-cad表达以及抑制MMP-9和Ezrin表达有关。为进一步开展分子机制及信号通路的研究奠定基础,为开展相关治疗新靶点的深入研究和药物开发提供理论支持。
| [1] |
Siegel RL, Miller KD, Jemal A. Cancer statistics, 2019[J]. CA Cancer J Clin, 2019, 69(1): 7-34. DOI:10.3322/caac.21551 |
| [2] |
Yamauchi T, Kamon J, Ito Y, et al. Cloning of adiponectin receptors that mediate antidiabetic metabolic effects[J]. Nature, 2003, 423(6941): 762-769. DOI:10.1038/nature01705 |
| [3] |
Inamura K, Song M, Jung S, et al. Prediagnosis plasma adiponectin in relation to colorectal cancer risk according to KRAS mutation status[J]. J Natl Cancer Inst, 2015, 108(4): djv363. |
| [4] |
Parida S, Siddharth S, Sharma D. Adiponectin, obesity, and cancer: clash of the bigwigs in health and disease[J]. Int J Mol Sci, 2019, 20(10): 2519. DOI:10.3390/ijms20102519 |
| [5] |
Wei EK, Giovannucci E, Fuchs CS, et al. Low plasma adiponectin levels and risk of colorectal cancer in men: A prospective study[J]. J Natl Cancer Inst, 2005, 97(22): 1688-1694. DOI:10.1093/jnci/dji376 |
| [6] |
Gu MJ, Huang QC, Bao CZ, et al. Attributable causes of colorectal cancer in China[J]. BMC Cancer, 2018, 18(1): 38. DOI:10.1186/s12885-017-3968-z |
| [7] |
An W, Bai Y, Deng SX, et al. Adiponectin levels in patients with colorectal cancer and adenoma: a meta-analysis[J]. Eur J Cancer Prev, 2012, 21(2): 126-133. DOI:10.1097/CEJ.0b013e32834c9b55 |
| [8] |
Dalamaga M, Diakopoulos KN, Mantzoros CS. The role of adiponectin in cancer: a review of current evidence[J]. Endocr Rev, 2012, 33(4): 547-594. DOI:10.1210/er.2011-1015 |
| [9] |
Zazzo ED, Polito R, Bartollino S, et al. Adiponectin as link factor between adipose tissue and cancer[J]. Int J Mol Sci, 2019, 20(4): 839. DOI:10.3390/ijms20040839 |
| [10] |
Liska D, Stocchi L, Karagkounis G, et al. Incidence, patterns, and predictors of locoregional recurrence in colon cancer[J]. Ann Surg Oncol, 2017, 24(4): 1093-1099. DOI:10.1245/s10434-016-5643-z |
| [11] |
王湘, 赵林. 结直肠癌辅助化疗回顾与进展[J]. 实用肿瘤杂志, 2019, 34(6): 479-485. |
| [12] |
Blaschuk OW, Devemy E. Cadherins as novel tragets for anticancer therapy[J]. Eur J Pharmacol, 2009, 625(1-3): 195-198. DOI:10.1016/j.ejphar.2009.05.033 |
| [13] |
Repetto O, De Paoli P, De Re V, et al. Levels of soluble E-cadherin in breast, gastric, and colorectal cancers[J]. Biomed Res Int, 2014, 2014: 408047. |
| [14] |
Leiphrakpam PD, Rajput A, Mathiesen M, et al. Ezrin expression and cell survival regulation in colorectal cancer[J]. Cell Signal, 2014, 26(5): 868-879. DOI:10.1016/j.cellsig.2014.01.014 |
| [15] |
Li Y, Lin Z, Chen B, et al. Ezrin/NF-kB activation regulates epithelial- mesenchymal transition induced by EGF and promotes metastasis of colorectal cancer[J]. Biomed Pharmacother, 2017, 92: 140-148. DOI:10.1016/j.biopha.2017.05.058 |
| [16] |
Herszényi L, Hritz I, Lakatos G, et al. The behavior of matrix metalloproteinases and their inhibitors in colorectal cancer[J]. Int J Mol Sci, 2012, 13(10): 13240-13263. |
 2021, Vol. 36
2021, Vol. 36


