文章信息
- 黄香, 刘谦, 吴昕煜, 金楠, 殷咏梅
- Huang Xiang, Liu Qian, Wu Xinyu, Jin Nan, Yin Yongmei
- 地舒单抗对比唑来膦酸治疗乳腺癌骨转移的疗效和安全性:一项倾向评分匹配队列研究
- Efficacy and safety of denosumab versus zoledronic acid for treatment of bone metastasis in breast cancer patients: a propensity score-matched cohort study
- 实用肿瘤杂志, 2024, 39(6): 542-548
- Journal of Practical Oncology, 2024, 39(6): 542-548
-
通信作者
- 殷咏梅, E-mail: ymyin@njmu.edu.cn
-
文章历史
- 收稿日期:2023-08-09
骨骼是晚期乳腺癌常见的转移部位。研究显示,55%~75%的晚期乳腺癌患者可发生骨转移[1]。骨相关事件(skeletal related event, SRE)是指骨转移性恶性肿瘤患者由于疾病进展带来的一系列骨并发症总和,包括病理性骨折、脊髓压迫、骨手术和骨放疗[2-3]。乳腺癌所致骨转移大多为溶骨性改变,易发生SRE,在不使用骨改良药物的情况下,确诊骨转移后3年的SRE发生率可高达80%[4-5]。一项回顾性研究显示,伴发SRE的乳腺癌骨转移患者中位生存期显著缩短[6]。
为了降低骨转移患者的SRE风险,国内外指南均推荐,在发现骨转移后,立即使用骨改良药物治疗,并在整个病程中持续使用[7-10]。目前主要的骨改良药物包括双膦酸盐和地舒单抗[11]。双膦酸盐是治疗乳腺癌骨转移的有效药物。唑来膦酸是使用最为广泛的一种双膦酸盐,但疗效维持时间短,且易发生发热和肾功能损害等不良反应[12],限制其在临床实践中的长期安全应用。地舒单抗则是一种新型的骨改良药物,为人免疫球蛋白G2单克隆抗体,可高亲和性地结合核因子κB受体活化因子配体(receptor activator of nuclear factor-κB ligand, RANKL),阻碍破骨细胞成熟和活化,抑制骨吸收[6]。一项国外随机对照研究显示,与唑来膦酸比较,地舒单抗可延迟乳腺癌骨转移患者的SRE发生时间,降低SRE发生次数,且发热和肾功能损伤等不良事件的发生率更低,耐受性良好[13]。因此国内外指南均以高级别证据一致推荐地舒单抗用于乳腺癌骨转移患者的治疗[7-10]。
由于地舒单抗在国内应用时间不长,价格较为昂贵且未纳入医保,其在乳腺癌骨转移患者中并未得到广泛的应用。目前地舒单抗应用于中国乳腺癌骨转移患者的疗效和安全性数据并不完善,因此本回顾性队列研究通过对比乳腺癌骨转移患者经地舒单抗与唑来膦酸治疗后SRE和不良事件的发生率,进一步确认地舒单抗治疗乳腺癌骨转移患者的有效性和安全性。
1 资料与方法 1.1 纳入标准纳入标准:(1)年龄≥18岁;(2)经组织学或细胞学证实的乳腺癌,影像学检查提示至少有1处骨转移;(3)血常规和肝肾功能检查基本正常,无治疗禁忌证;(4)美国东部肿瘤协作组(Eastern Cooperative Oncology Group, ECOG)体能状态评分≤2分;(5)预计生存期≥3个月;(6)临床资料完整,包括治疗记录、疗效评估和不良事件等。
1.2 一般资料回顾性收集来自南京医科大学第一附属医院肿瘤科的2020年9月至2022年7月经地舒单抗或唑来膦酸治疗的乳腺癌骨转移患者的临床资料,包括年龄、ECOG评分、月经状态、分子分型和转移部位、联合抗肿瘤治疗方案、既往SRE发生情况、初始骨改良药物类型、影像学检查和实验室检验结果等。地舒单抗用法为120 mg皮下注射,每周期1次,28 d为1个周期;唑来膦酸用法为4 mg静脉滴注,每周期1次,28 d为1个周期。本研究已获得南京医科大学第一附属医院伦理委员会审批,批准编号为2022-SR-0459号,患者知情同意予以豁免。
绝经定义为:既往进行过双侧卵巢切除术;年龄≥60岁;年龄 < 60岁,自然停经≥12个月(近1年内未接受化疗、三苯氧胺、托瑞米芬或卵巢去势药物的情况下),卵泡刺激素(follicle stimulating hormone, FSH)和雌二醇(estradiol, E2)水平在绝经后范围内[8, 14]。激素受体(hormone receptor, HR)阳性定义为雌激素受体(estrogen receptor, ER)和(或)孕激素受体(progesterone receptor, PR)阳性[15]。人表皮生长因子受体2(human epidermal growth factor receptor 2, HER2)阴性乳腺癌的定义为原发灶或转移灶组织标本免疫组织化学HER2为0/1+或HER2为2+且荧光原位杂交(fluorescence in situ hybridization, FISH)检测为阴性[16]。HR阴性定义为ER阴性且PR阴性。分子亚型由以上标准分为HR阳性HER2阴性(HR+HER2-)乳腺癌、HER2阳性(HER2+)乳腺癌和三阴性(HR阴性HER2阴性)乳腺癌。
1.3 研究终点疗效终点包括1年无SRE生存率和至首次SRE发生时间。1年无SRE生存率定义为地舒单抗或唑来膦酸治疗后1年无SRE发生的患者比例。至首次SRE发生时间定义为开始地舒单抗或唑来膦酸治疗至首次发生SRE的时间。
安全性终点为患者治疗后与骨改良药物相关的不良事件的发生率和级别,根据美国国立癌症研究所不良反应事件通用术语标准(National Cancer Institute-Common Terminology Criteria for Adverse Events, NCI-CTCAE)5.0进行记录[17]。
1.4 随访随访截至2023年7月20日,随访时间为11.6~34.0个月,中位随访时间为18.3个月。通过检索患者住院病历资料整理基线特征和疗效评估结果,并通过电话随访、线上问诊和面对面访谈随访了解患者使用地舒单抗或唑来膦酸期间的SRE与其他不良反应的发生和经治情况。排除基线、不良反应资料严重缺乏和随访期间脱失患者共32例,最终纳入176例患者。
1.5 统计学分析应用SPSS 27.0和R语言4.3.1软件分析数据。通过倾向评分匹配(propensity score matching, PSM)降低地舒单抗组和唑来膦酸组的混杂偏倚,1∶1进行匹配,混杂协变量包括年龄、ECOG评分、月经状态、分子分型、转移部位和联合抗肿瘤治疗方案,卡钳值设为0.2。采用Kaplan-Meier法作生存曲线,采用log-rank检验进行生存分析。SRE发生风险的因素分析采用Cox风险比例模型。组间不良反应发生比较采用两样本非参数U检验。以P < 0.05为差异具有统计学意义。
2 结果 2.1 基线特征共纳入176例经骨改良药物治疗的乳腺癌骨转移患者,均为女性,其中经地舒单抗治疗者90例,经唑来膦酸治疗者86例,倾向评分匹配前两组患者月经状态的基线特征比较,差异具有统计学意义(P < 0.05,表 1)。经倾向评分匹配后,共纳入132例患者,其中经地舒单抗治疗者66例(地舒单抗组),经唑来膦酸治疗者66例(唑来膦酸组)。两组基线特征均衡。
| 临床特征 | 倾向评分匹配前 | 倾向评分匹配后 | |||||||
| 地舒单抗治疗者(n=90) | 唑来膦酸治疗者(n=86) | SMD | P值 | 地舒单抗组(n=66) | 唑来膦酸组(n=66) | SMD | P值 | ||
| 中位年龄(岁,范围) | 58(23~81) | 53(30~80) | 0.152 | 0.314 | 58(30~81) | 54(30~80) | 0.096 | 0.581 | |
| 月经状态 | 0.397 | 0.015 | 0.064 | 0.855 | |||||
| 已绝经 | 66(73.3) | 47(54.7) | 44(66.7) | 43(65.2) | |||||
| 未绝经 | 24(26.7) | 39(45.3) | 22(33.3) | 23(34.8) | |||||
| ECOG评分 | 0.160 | 0.378 | 0.037 | 1.000 | |||||
| 0~1分 | 65(72.2) | 68(79.1) | 52(77.8) | 51(77.3) | |||||
| 2分 | 25(27.8) | 18(20.9) | 14(21.2) | 15(22.7) | |||||
| 分子分型 | 0.170 | 0.532 | 0.068 | 0.927 | |||||
| HR+HER2- | 44(48.9) | 44(51.2) | 34(51.5) | 36(54.6) | |||||
| HER2+ | 29(32.2) | 31(36.0) | 22(33.3) | 21(31.8) | |||||
| 三阴性 | 17(18.9) | 11(12.8) | 10(15.2) | 9(13.6) | |||||
| 内脏转移 | 0.094 | 0.635 | 0.061 | 0.861 | |||||
| 有 | 44(48.9) | 38(44.2) | 31(47.0) | 30(45.5) | |||||
| 无 | 46(51.1) | 48(55.8) | 35(53.0) | 36(54.5) | |||||
| 联合靶向治疗 | 0.052 | 0.864 | 0.034 | 1.000 | |||||
| 是 | 69(76.7) | 64(74.4) | 48(72.7) | 47(71.2) | |||||
| 否 | 21(23.3) | 22(25.9) | 18(28.3) | 19(28.8) | |||||
| 联合内分泌治疗 | 0.153 | 0.394 | 0.064 | 0.854 | |||||
| 是 | 26(28.9) | 31(36.0) | 21(31.8) | 23(34.8) | |||||
| 否 | 64(71.1) | 55(64.0) | 45(68.2) | 43(65.2) | |||||
| 联合化疗 | 0.033 | 0.947 | 0.063 | 0.856 | |||||
| 是 | 54(60.0) | 53(61.6) | 43(65.2) | 41(62.1) | |||||
| 否 | 36(40.0) | 33(38.4) | 23(34.8) | 25(37.9) | |||||
| 注 SMD:标准化均数差(standardized mean difference);ECOG:美国东部肿瘤协作组(Eastern Cooperative Oncology Group);HR:激素受体(hormone receptor);HER2:人表皮生长因子受体2(human epidermal growth factor receptor 2) | |||||||||
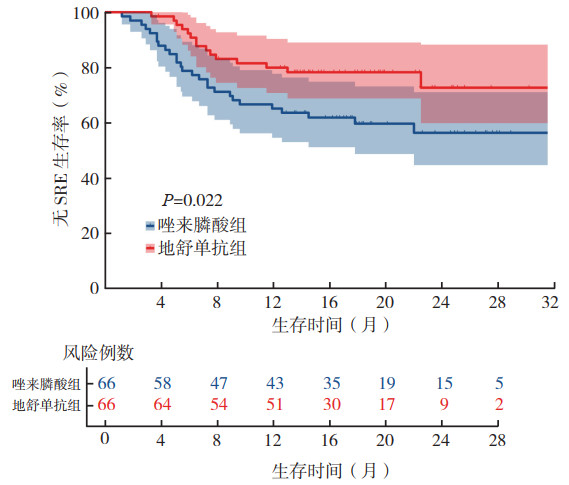
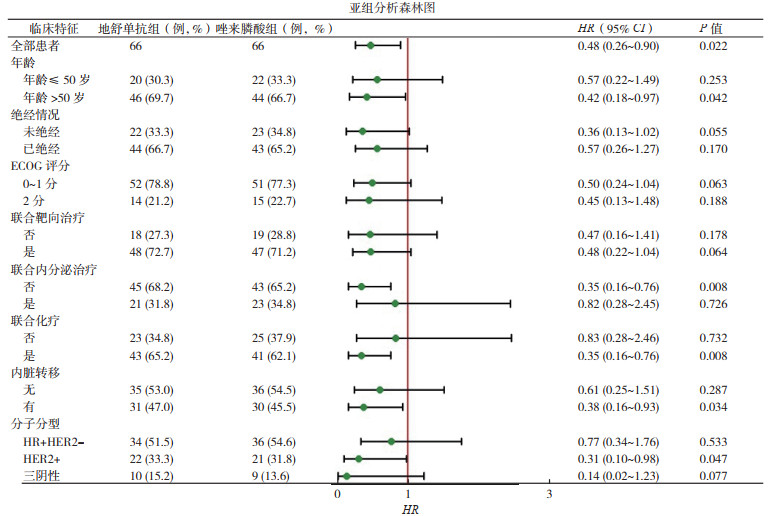
截至2023年7月20日,中位随访时间为18.3个月,两组患者中位至首次SRE发生时间均未达到(图 1)。地舒单抗组SRE发生风险降低(HR=0.48,95% CI:0.26~0.90,P=0.022;图 2)。亚组分析显示,与唑来膦酸组比较,地舒单抗组SRE风险的降低在年龄 > 50岁(P=0.042)、未联合内分泌治疗(P=0.008)、联合化疗(P=0.008)、存在内脏转移(P=0.034)和HRE2阳性(P=0.047)患者中获益(图 2)。
|
| 注 SRE:骨相关事件(skeletal-related event) 图 1 Kaplan-Meier法比较地舒单抗组和唑来膦酸组乳腺癌骨转移患者无SRE生存曲线 Fig.1 SRE-free survival curves of breast cancer patients with bone metastasis treated with denosumab or zoledronic acid using Kaplan-Meier method |
|
| 注 ECOG:美国东部肿瘤协作组(Eastern Cooperative Oncology Group);HR:激素受体(hormone receptor);HER2:人表皮生长因子受体2(human epidermal growth factor receptor 2) 图 2 地舒单抗组和唑来膦酸组乳腺癌骨转移患者SRE发生风险的亚组分析 Fig.2 Subgroup analysis of the risk of skeletal-related events of breast cancer patients with bone metastasis treated with denosumab or zoledronic acid |
地舒单抗组15例发生SRE,其中3例为病理性骨折,7例为骨放疗,4例为骨手术,1例发生脊髓压迫(表 2)。唑来膦酸组27例发生SRE,其中,8例为病理性骨折,12例为骨放疗,6例为骨手术,1例发生脊髓压迫。地舒单抗组和唑来膦酸组1年无SRE生存率分别为80.3%(95% CI:68.7%~89.1%)和63.6%(95% CI:50.9%~75.1%,表 2)。
| SRE特征 | 地舒单抗组(n=66) | 唑来膦酸组(n=66) |
| SRE分布 | ||
| 所有 | 15(22.7) | 27(40.9) |
| 病理性骨折 | 3(4.5) | 8(12.1) |
| 脊髓压迫 | 1(1.5) | 1(1.5) |
| 骨手术 | 4(6.1) | 6(9.1) |
| 骨放疗 | 7(10.6) | 12(18.2) |
| SRE发生 | ||
| 6个月 | 5(7.8) | 15(22.7) |
| 1年 | 13(19.7) | 24(36.4) |
| 中位至首次SRE发生时间 | 未达到 | 未达到 |
| 中位随访时间(月,范围) | 18.0(11.6~34.5) | 18.4(7.5~34.0) |
| 注 SRE:骨相关事件(skeletal-related event) | ||
地舒单抗组最常见相关不良事件为低钙血症(22.7%),其中Ⅲ~Ⅳ级低钙血症发生率为1.5%;其次为牙周炎(13.6%),其中Ⅲ~Ⅳ级牙周炎发生率为1.5%;其他不良事件包括肌肉痛(10.6%)、肾功能损伤(6.1%)、关节痛(3.0%)和下颌骨坏死(3.0%)等,均为Ⅰ~Ⅱ级不良事件;2例(3.0%)分别出现低钙血症和牙周炎的治疗相关性严重不良事件,但是与唑来膦酸组比较,差异无统计学意义(P=0.156,表 3)。唑来膦酸组最常见的相关不良事件同样为低钙血症(15.2%),牙周炎发生率与地舒单抗组相同(13.6%),但是较多患者出现肌肉痛(13.6%)、肾功能损伤(13.6%)、关节痛(13.6%)、发热(9.1%)和注射部位疼痛(6.1%),特别是关节痛发生率与地舒单抗组比较,差异具有统计学意义(P=0.028)。两组均无患者发生死亡事件。
| 不良事件 | 地舒单抗组(n=66) | 唑来膦酸组(n=66) | P值 | |||
| 所有级别 | Ⅲ/Ⅳ级 | 所有级别 | Ⅲ/Ⅳ级 | |||
| 低钙血症 | 15(22.7) | 1(1.5) | 10(15.2) | 0(0.0) | 0.269 | |
| 牙周炎 | 9(13.6) | 1(1.5) | 9(13.6) | 0(0.0) | 1.000 | |
| 肌肉痛 | 7(10.6) | 0(0.0) | 9(13.6) | 0(0.0) | 0.595 | |
| 肾功能损伤 | 4(6.1) | 0(0.0) | 9(13.6) | 0(0.0) | 0.146 | |
| 关节痛 | 2(3.0) | 0(0.0) | 9(13.6) | 0(0.0) | 0.028 | |
| 下颌骨坏死 | 2(3.0) | 0(0.0) | 2(3.0) | 0(0.0) | 1.000 | |
| 注射部位疼痛 | 2(3.0) | 0(0.0) | 4(6.1) | 0(0.0) | 0.405 | |
| 发热 | 1(1.5) | 0(0.0) | 6(9.1) | 0(0.0) | 0.053 | |
| 治疗相关严重不良事件 | 2(3.0) | 0(0.0) | 0.156 | |||
SRE是乳腺癌骨转移患者的严重骨并发症[18]。骨改良药物可有效降低乳腺癌骨转移患者SRE的发生[19]。地舒单抗是一种靶向于RANKL的高特异性和高亲和性的单克隆抗体,欧洲肿瘤内科学会(European Society for Medical Oncology, ESMO)指南、美国国立综合癌症网络(National Comprehensive Cancer Network, NCCN)指南等国外指南共同推荐地舒单抗用于乳腺癌骨转移患者的治疗[7-8]。在国内,《乳腺癌骨转移临床诊疗专家共识》和《中国乳腺癌骨转移和骨相关疾病临床诊疗专家共识(2021版)》等同样将地舒单抗作为乳腺癌骨转移患者的治疗推荐[9-10]。
大型前瞻性随机双盲研究Study 136对比地舒单抗与唑来膦酸治疗晚期乳腺癌骨转移患者的疗效与安全性结果显示,地舒单抗较唑来膦酸延迟至首次SRE发生时间(未到达vs 26.4个月),整体不良事件发生率和严重不良事件发生率相当,但唑来膦酸组肾功能损伤和急性期不良反应发生率更高[13]。有学者汇总分析三项随机、双盲Ⅲ期临床研究共纳入5 723例乳腺癌、前列腺癌和其他实体肿瘤骨转移患者或多发性骨髓瘤患者[患者随机接受地舒单抗(n=2 862)或唑来膦酸(n=2 861)治疗]显示,与唑来膦酸比较,地舒单抗延迟首次SRE的发生时间,中位至首次SRE发生时间分别为19.45和27.66个月,降低了17%的首次SRE风险(HR=0.83,95% CI:0.76~0.90),且地舒单抗使用时不需监测肾功能,不需根据肾功能状态调整剂量或中断治疗[20]。上述研究均提示,与唑来膦酸比较,地舒单抗可进一步降低乳腺癌骨转移患者发生SRE的风险,且肾功能损伤和发热等不良事件发生率更低。
地舒单抗于2019年5月在中国上市,由于价格昂贵且未纳入医保,其在乳腺癌骨转移患者中并未得到广泛的应用。本项回顾性研究进一步明确地舒单抗在中国乳腺癌骨转移患者中应用的疗效与安全性。本研究是在中国乳腺癌骨转移患者中开展的对比地舒单抗和唑来膦酸有效性和耐受性的首项回顾性研究,分别纳入90例经地舒单抗治疗和86例经唑来膦酸治疗的乳腺癌骨转移患者,经倾向评分匹配法平衡基线特征后,地舒单抗组66例,唑来膦酸组66例。Kaplan-Meier生存曲线分析显示,与唑来膦酸组比较,地舒单抗治疗可延长至首次SRE发生时间。亚组分析显示,在年龄 > 50岁、未联合内分泌治疗、联合化疗、存在内脏转移和HRE2阳性人群中地舒单抗能带来一致的获益趋势。
在Study 136研究中,乳腺癌骨转移患者应用地舒单抗治疗后,12个月SRE发生率约为30.0%[21]。本研究中地舒单抗用药后12个月SRE发生率为19.7%,较Study 136研究展现出更低的SRE发生率。原因可能是:本研究开展时间较晚,现有的影像学手段更为敏感,可以在骨转移初期发现骨破坏征象,更早地诊断骨转移并给予骨改良药物治疗;同时现阶段联合的抗肿瘤治疗药物亦更加先进,对肿瘤的治疗更为有效,可进一步降低SRE的发生。
在不良事件方面,本研究显示,地舒单抗治疗乳腺癌骨转移患者耐受性良好,整体的不良事件发生率为48.4%,多为Ⅰ/Ⅱ级不良事件;最常见的Ⅲ/Ⅳ级不良事件为低钙血症(1.5%)和牙周炎(1.5%)。与唑来膦酸组比较,地舒单抗组低钙血症发生率更高,而肌肉痛、肾功能损伤、关节痛、发热和注射部位疼痛等不良事件发生率更低,特别是关节痛发生率显著降低。
本研究中,地舒单抗组患者肌肉痛和关节痛的发生率分别为10.6%和3.0%,低于Study 136研究(肌肉痛20.0%,关节痛24.5%)[21],原因可能在于本研究为回顾性分析,部分患者在本研究入组后开始随访时对其初始接受骨改良治疗期间发生的不良反应有所遗忘,因而造成上述不良反应发生率的低估。此外,本研究中多数患者暂停地舒单抗治疗的原因为严重的低钙血症和牙周炎。地舒单抗应用后患者低钙血症发生率为22.7%,牙周炎发生率为13.6%,高于Study136研究(低钙血症为5.5%,牙周炎为5.6%)。前者的原因在于Study136研究进行时强烈建议参与研究的患者每天补充钙剂和维生素D,而本研究中虽告知患者需常规服用钙片和维生素D,但部分患者未能按医嘱执行,同时本研究入组66.7%的绝经后乳腺癌患者,进一步加重低钙血症的发生风险。牙周炎不良事件的发生可能与入组患者既往口腔卫生情况和原有口腔疾病的恶化有关。Study136研究排除了既往有未愈合的牙科或口腔手术者有关,而本研究未对患者的口腔既往疾病有所限制。
本研究存在一定的局限性。本研究为回顾性分析,因选择偏倚,两组患者间的基线特征不均衡。虽然通过倾向得分匹配法最大程度地保证组间患者基线特征的可比性,但由于回顾性分析的限制,纳入的混杂因素仍不全面,如既往SRE发生情况和骨转移灶数目等。此外,由于本研究随访时间较短,难以观察患者使用地舒单抗的长期不良事件和依从性。
综上所述,对于出现骨转移的晚期乳腺癌患者,与唑来膦酸比较,地舒单抗可降低SRE的发生风险,且肾功能损伤和发热不良事件发生率更低。
| [1] |
Hernandez RK, Wade SW, Reich A, et al. Incidence of bone metastases in patients with solid tumors: analysis of oncology electronic medical records in the United States[J]. BMC Cancer, 2018, 18(1): 44. DOI:10.1186/s12885-017-3922-0 |
| [2] |
Li W, Wu XY, Yu H, et al. A retrospective analysis of denosumab for the treatment of bone metastases in Chinese patients with breast cancer[J]. Clin Med Insights Oncol, 2023, 17: 11795549231182266. DOI:10.1177/11795549231182266 |
| [3] |
Coleman RE. Clinical features of metastatic bone disease and risk of skeletal morbidity[J]. Clin Cancer Res, 2006, 12(20 Pt 2): 6243s-6249s. |
| [4] |
Harbeck N, Penault-Llorca F, Cortes J, et al. Breast cancer[J]. Nat Rev Dis Primers, 2019, 5: 66. DOI:10.1038/s41572-019-0111-2 |
| [5] |
Liu WC, Li MX, Wu SN, et al. Using machine learning methods to predict bone metastases in breast infiltrating ductal carcinoma patients[J]. Front Public Health, 2022, 10: 922510. DOI:10.3389/fpubh.2022.922510 |
| [6] |
Yong M, Jensen AÖ, Jacobsen JB, et al. Survival in breast cancer patients with bone metastases and skeletal-related events: a population-based cohort study in Denmark (1999-2007)[J]. Breast Cancer Res Treat, 2011, 129(2): 495-503. DOI:10.1007/s10549-011-1475-5 |
| [7] |
Coleman R, Hadji P, Body JJ, et al. Bone health in cancer: ESMO clinical practice guidelines[J]. Ann Oncol, 2020, 31(12): 1650-1663. DOI:10.1016/j.annonc.2020.07.019 |
| [8] |
Gradishar WJ, Moran MS, Abraham J, et al. Breast cancer, version 3.2022, NCCN clinical practice guidelines in oncology[J]. J Natl Compr Canc Netw, 2022, 20(6): 691-722. DOI:10.6004/jnccn.2022.0030 |
| [9] |
Jiang ZF, Wang HB, Wang S, et al. Chinese expert consensus statement on the clinical diagnosis and treatment of breast cancer bone metastasis and bone related disease[J]. Transl Breast Cancer Res, 2021, 2: 2. DOI:10.21037/tbcr-20-65 |
| [10] |
中国抗癌协会骨肿瘤和骨转移瘤专业委员会. 乳腺癌骨转移临床诊疗专家共识[J]. 中国肿瘤临床, 2022, 49(13): 660-669. |
| [11] |
Ishikawa T. Differences between zoledronic acid and denosumab for breast cancer treatment[J]. J Bone Miner Metab, 2023, 41(3): 301-306. DOI:10.1007/s00774-023-01408-z |
| [12] |
Jakob T, Tesfamariam YM, Macherey S, et al. Bisphosphonates or RANK-ligand-inhibitors for men with prostate cancer and bone metastases: a network meta-analysis[J]. Cochrane Database Syst Rev, 2020, 12(12): CD013020. |
| [13] |
Stopeck AT, Lipton A, Body JJ, et al. Denosumab compared with zoledronic acid for the treatment of bone metastases in patients with advanced breast cancer: a randomized, double-blind study[J]. J Clin Oncol, 2010, 28(35): 5132-5139. DOI:10.1200/JCO.2010.29.7101 |
| [14] |
严雪绮, 黄香, 李薇, 等. 晚期乳腺癌内分泌分层治疗进展[J]. 实用肿瘤杂志, 2023, 38(2): 105-109. |
| [15] |
Hammond ME, Hayes DF, Wolff AC. Clinical Notice for American Society of Clinical Oncology-College of American Pathologists guideline recommendations on ER/PgR and HER2 testing in breast cancer[J]. J Clin Oncol, 2011, 29(15): e458. DOI:10.1200/JCO.2011.35.2245 |
| [16] |
Wolff AC, Somerfield MR, Dowsett M, et al. Human epidermal growth factor receptor 2 testing in breast cancer: ASCO-College of American Pathologists guideline update[J]. J Clin Oncol, 2023, 41(22): 3867-3872. DOI:10.1200/JCO.22.02864 |
| [17] |
U.S. Department of Health and Human Services, National Institutes of Health, National Cancer Institute. Common Terminology Criteria for Adverse Events (CTCAE) version 5.0[EB/OL]. (2017-11-27)[2023-07-29]. https://ctep.cancer.gov/protocoldevelopment/electronic_applications/docs/ctcae_v5_quick_reference_5x7.pdf
|
| [18] |
Niu YM, Yang HB, Yu ZY, et al. Intervention with the bone-associated tumor vicious cycle through dual-protein therapeutics for treatment of skeletal-related events and bone metastases[J]. ACS Nano, 2022, 16(2): 2209-2223. DOI:10.1021/acsnano.1c08269 |
| [19] |
Eisen A, Somerfield MR, Accordino MK, et al. Use of adjuvant bisphosphonates and other bone-modifying agents in breast cancer: ASCO-OH (CCO) guideline update[J]. J Clin Oncol, 2022, 40(7): 787-800. DOI:10.1200/JCO.21.02647 |
| [20] |
Lipton A, Fizazi K, Stopeck AT, et al. Superiority of denosumab to zoledronic acid for prevention of skeletal-related events: a combined analysis of 3 pivotal, randomised, phase 3 trials[J]. Eur J Cancer, 2012, 48(16): 3082-3092. DOI:10.1016/j.ejca.2012.08.002 |
| [21] |
Stopeck AT, Lipton A, Body JJ, et al. Denosumab compared with zoledronic acid for the treatment of bone metastases in patients with advanced breast cancer: a randomized, double-blind study[J]. J Clin Oncol, 2010, 28(35): 5132-5139. DOI:10.1200/JCO.2010.29.7101 |
 2024, Vol. 39
2024, Vol. 39


