文章信息
- 杨立羊, 张新军, 葛嘉欣, 王庆领
- 环状RNA作为微小RNA海绵在结直肠癌中的作用及其临床价值
- 实用肿瘤杂志, 2020, 35(5): 473-478
基金项目
- 宁波市自然科学基金(2016A610121)
-
作者简介
- 杨立羊(1993-), 女, 江西上饶人, 住院医师, 硕士, 从事消化系统肿瘤临床与基础研究.
-
通信作者
- 张新军, E-mail:zxj14@163.com
-
文章历史
- 收稿日期:2019-08-09
2. 宁波大学医学院附属医院消化内科, 浙江 宁波 315020
目前,结直肠癌(colorectal cancer, CRC)已成为全球第三大最常见的癌症(占总病例的10.2%),第二大癌症死亡原因(占癌症死亡总例数的9.2%)[1]。在我国结直肠癌的发病率和死亡率在所有癌症中位居第3位,并且发病率呈上升趋势[2]。结直肠癌的具体机制仍不明确,其早期诊断、精准治疗和预后评估是难题。
非编码RNA(non-coding RNA,ncRNA)是一类数量众多、没有编码蛋白质功能但具有重要生物学活性的RNA分子[3]。环状RNA(circular RNA,circRNA)是其中重要一员,具有共价闭合的环状结构,对核糖核酸酶(ribonuclease,RNase)具有抵抗性,在体内比线性RNA更稳定。此外,circRNA数量众多,在多种物种中高度保守,表现出组织特异性和发育阶段依赖的表达模式[4]。由于这些特性,近年来circRNA得到不少学者的关注。研究发现,人类小脑变性相关蛋白1反义转录物(cerebellar degeneration-related protein 1 antisense,CDR1as)具有miR-7结合位点,在斑马鱼中脑中,CDR1as的过度表达会使其中脑发育受损,这种现象与敲低miR-7效应类似[5]。这说明circRNA具有作为miRNA分子海绵的生物学功能。同时Hansen等[6]在小鼠大脑模型中也有类似发现。此后,circRNA作为miRNA分子海绵功能在生物体内的作用逐渐成为研究领域的热点。本文就circRNA作为miRNA分子海绵在结直肠癌中研究进展进行综述,旨在为探索结直肠癌的发病机制提供思路;为结直肠癌的诊断及预后提供新的生物标志物;为治疗提供潜在的精准治疗靶点。
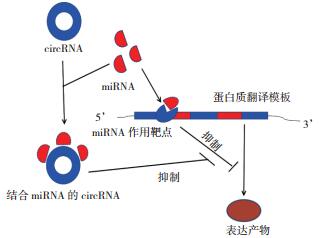
1 circRNA充当miRNA海绵随着生物学技术不断的进展,不少circRNA被发现具有作为miRNA分子海绵、调节基因转录和剪接、调节蛋白质-蛋白质相互作用、参与蛋白质的翻译、形成融合circRNA参与耐药及肿瘤进展等多种重要的生物学功能[7],其中充当miRNA分子海绵这一生物学功能成为近几年关注的焦点。circRNA携带miRNA响应元件(miRNA response element,MRE),可以通过结合miRNA,调节miRNA活性,从而降低miRNA结合和下调蛋白编码转录本的能力[8]。这种过程被称为circRNA分子海绵效应(图 1)。进一步研究发现,circRNA分子海绵效应与疾病,特别是和肿瘤发生与发展关系密切。circ_100290通过miR-29b家族成员来调控细胞周期蛋白依赖性激酶6(cyclin-dependent kinase 6,CDK6)的表达促进口腔癌细胞的增殖[9]。circ_0052112作为miR-125a-5p分子海绵促进乳腺癌细胞迁移和侵袭[10]。circ_PSMC3通过miR-296-5p海绵抑制胃癌的增殖和转移[11]。
|
| 注 circRNA上携带miRNA响应元件,能与相应的miRNA结合,影响miRNA的活性,从而能减弱miRNA与靶基因/靶蛋白作用后产生的对蛋白翻译和表达能力的抑制作用 图 1 circRNA的分子海绵效应 |
目前,大量研究发现,circRNA作为miRNA分子海绵与CRC发生和发展有关,参与CRC细胞的增殖、迁移、侵袭和凋亡等病理过程,并且某些circRNA作为miRNA分子海绵与CRC放疗敏感性有关。表达上调的CDR1as可结合miR-7,增加miR-7的表达,进而抑制miR-7下游靶蛋白表皮生长因子受体(epidermal growth factor receptor,EGFR)、胰岛素样生长因子1型受体(insulin-like growth factor-1 receptor,IGF-1R)和转录因子Ying-Yang1(transcription factor Ying-Yang 1,YY1)的表达,从而在CRC中发挥致癌作用[12-13]。表达下调的circ_0000523可作为miR-31海绵,使miR-31表达上调,间接激活β-catenin Wnt信号通路,从而促进CRC的进展[14]。各种circRNA作为miRNA海绵与CRC的关系如表 1所示[12-31]。circRNA作为miRNA分子海绵在CRC发生、发展、早期诊断及预后评估中具有重要作用。同时由于circRNA具有结构稳定等特性,使其有望成为新的生物标志物用于肿瘤的临床应用。
| circRNA类型 | 表达情况 | 结合的miRNA | 相关的信号通路 | 与CRC相关的病理过程和可能作用 | 参考文献 |
| CDR1as(circ_ciRS-7) | 上调 | miR-7 | CDR1as/miR-7/EGFR/IGF-1R/YY1 | 促进细胞增殖、侵袭和抑制细胞凋亡 | [12-13] |
| circ_0000523(circ_006229) | 下调 | miR-31 | circ_0000523/miR-31/Wnt/β-catenin | 抑制细胞增殖,促进细胞凋亡 | [14] |
| circ_103809 | 下调 | miR-532-3p | circ_103809/ miR-532-3p/FOXO4 | 抑制细胞增殖、迁移和细胞周期进展,促进细胞凋亡 | [15-16] |
| circ_DDX17 | 下调 | miR-21-5p | circ_DDX17/miR-21-5p/KEGG | 抑制细胞增殖、迁移和细胞周期进展,促进细胞凋亡 | [17] |
| circ_VAPA(circ_0006990) | 上调 | miR-101 | circ_VAPA/miR-101/KEGG | 促进细胞增殖、迁移和侵袭 | [18] |
| circ_0136666 | 上调 | miR-136 | circ_0136666/miR-136/SH2B1 | 促进细胞增殖和侵袭 | [19] |
| circ_0071589 | 上调 | miR-600 | circ_0071589/miR-600/EZH2 | 促进细胞增殖、侵袭和迁移 | [20] |
| circ_ACAP2 | 上调 | miR-21-5p | circ_ACAP2/miR-21-5p/Tiam1 | 促进细胞增殖、侵袭和迁移 | [21] |
| circ_001569 | 上调 | miR-145 | circ_001569/miR-145/E2F5/BAG4/FMNL2 | 促进细胞增殖、侵袭和细胞周期进展,抑制细胞凋亡 | [22] |
| circ_ITCH | 下调 | miR-7,miR-20a | circ_ITCH/miR-7/miR-20a/Wnt/β-catenin | 抑制细胞增殖、分化和侵袭 | [23] |
| circ_000984 | 上调 | miR-106b | circ_000984/miR-106b/CDK6 | 促进细胞增殖、迁移和侵袭,促进细胞周期进展 | [24] |
| circ_0026344 | 下调 | miR-21,miR-31 | circ_0026344/miR-21/miR-31 | 抑制细胞增殖、侵袭和促进细胞凋亡 | [25] |
| circ_0020397 | 上调 | miR-138 | circ_0020397/miR-138/TERT/PD-L1 | 提高细胞活性,促进细胞侵袭,抑制细胞凋亡 | [26] |
| circ_0055625 | 下调 | miR-106b | circ_0055625/miR-106b-5p (miR-106b)/ITGB8 | 抑制细胞增殖、迁移和侵袭 | [27] |
| circ_0001313(circ_CCDC66) | 上调 | miR-338-3p | circ_0001313/miR-338-3p/KEGG | 降低细胞对放疗的敏感性 | [28] |
| circ_NSD2 | 上调 | miR-199b-5p | circ_NSD2/miR-199b-5p/DDR1/JAG1 | 促进细胞与基质的相互作用以及细胞迁移和侵袭 | [29] |
| circ_100290 | 上调 | miR-516b | circ_100290/miR-516b/FZD4/Wnt/β-catenin | 促进细胞增殖、迁移和侵袭 | [30] |
| circ_Sry | - | miR-138 | circ_Sry/miR-138/TWIST2 | 促进细胞迁移和侵袭 | [6, 31] |
circRNA在CRC细胞的增殖、分化、凋亡、侵袭和转移等病理过程中发挥着一定作用。这种作用是通过与miRNA及其下游靶基因或靶蛋白相互影响而实现的。circ_001569在CRC组织中表达水平高于邻近正常组织,能推动细胞周期的进展,抑制细胞凋亡,促进CRC细胞增殖和侵袭。在CRC细胞中,新引入miR-145可以抑制circ_001569对CRC细胞增殖和侵袭的促进作用,敲除circ_001569可以抑制细胞增殖和侵袭,而沉默miR-145可以逆转这种作用[22]。E2F转录因子5 (E2F transcription factor 5,E2F5)是E2F转录因子家族的成员之一,能与参与细胞周期调控的靶基因启动子结合。Bcl2相关基因4(Bcl2-associated athanogene 4,BAG4)与癌细胞的增殖和转移有关。甲酸精类蛋白2(formin-like protein 2,FMNL2)促进CRC细胞增殖、侵袭、转移和上皮间质转化。miR-145转录活性的改变可以直接影响E2F5、BAG4和FMNL2的表达,增强miR-145转录活性可以降低E2F5、BAG4和FMNL2表达,而抑制miR-145转录活性则起相反作用。另外,circ_001569与下游靶基因在CRC细胞中的协同作用在随后的试验中也得到论证。蛋白质印迹结果显示,上调circ_001569可以增加E2F5、BAG4和FMNL2表达水平,而下调circ_001569,其表达水平则呈现相反结果[22]。在功能试验中发现,在敲低circ_001569的CRC细胞中,新引入E2F5、BAG4和FMNL2可以增加G2/M期细胞的比例,降低细胞凋亡率,促进细胞侵袭[22]。由此说明,circ_001569通过作为miR-145海绵,调节下游靶基因E2F5、BAG4和FMNL2的表达水平,从而促进CRC的增殖与侵袭。circ_NSD2与CRC的进展和转移有关。circ_NSD2是CRC转移的启动子。其在CRC组织中表达升高,并且在晚期或出现转移的CRC患者中表达升高。功能试验显示,过表达的circ_NSD2在体内和体外能促进CRC的迁移、侵袭和转移,而敲低circ_NSD2在体内外则起抑制作用[29]。研究发现,miR-199b-5p为circ_NSD2的作用靶点,在小鼠肿瘤模型中circ_NSD2表达与miR-199b-5p呈负相关,miR-199b-5p模拟物能成功逆转circ_NSD2对CRC细胞迁移的促进作用,miR-199b-5p抑制剂有效清除circ_NSD2的干扰RNA对CRC细胞迁移的抑制作用[29]。基于这些结果可以看出,circ_NSD2通过作为miR-199b-5p海绵来促进CRC细胞的迁移与侵袭。盘状结构域受体家族成员1重组蛋白(recombinant discoidin domain receptor family member 1,DDR1)和JAGGED1重组蛋白(recombinant jagged 1,JAG1)表达与CRC的上皮间质转化、迁移和转移过程有关。进一步实时定量PCR以及蛋白质印迹分析研究显示,转染miR-199b-5p模拟物后,细胞中的DDR1和JAG1的mRNA和蛋白质水平降低,而转染miR-199b-5p抑制剂后,细胞中的DDR1和JAG1的mRNA和蛋白质水平升高。DDR1和JAG1是miR-199b-5p直接靶点。另外,circ_NSD2与DDR1和JAG1在CRC中的协同关系也在研究中得到论证。综上可知,circ_NSD2作为miR-199b-5p的海绵,通过上调DDR1和JAG1的表达,从而促进CRC的侵袭和转移[29]。除此之外,目前研究表明,还有许多circRNA能通过miRNA海绵在CRC的发生和发展中起重要作用[23-27]。因此circRNA/miRNA/靶基因/靶蛋白轴可能是CRC发病的一个重要原因。通过纠正上游异常分子表达,可能抑制CRC的发生与进展。这为后期CRC分子靶向治疗药物的研究提供潜在方向。
2.2 circRNA作为miRNA分子海绵在结直肠癌早期诊断中的作用结直肠癌的预后与诊断阶段有关。早期诊断的5年生存率为90%,远处转移的5年生存率 < 10%[32],这一下降表明早期发现CRC的重要性。circ_103809在CRC中起着抑癌基因的作用,下调circ_103809表达能够促进CRC细胞的增殖和迁移,并且circ_103809表达水平与淋巴结转移和TNM分期相关。既往研究发现,miR-532-3p在结直肠腺瘤和CRC患者的血清中表达均上调[33-34]。miR-532-3p在CRC组织及细胞中的表达也均上调,并且与circ_103809表达呈负相关。转染circRNA_103809小干扰RNA后,CRC细胞中miR-532-3p表达上调。功能试验表明,敲除circRNA_103809可以逆转miR-532-3p下调抑制CRC细胞增殖和迁移的能力。叉头框O4(forkhead box O4,FOXO4)转录因子调控多种细胞通路,对多种癌症均有抑制作用。生物信息学技术表明,circRNA_103809和FOXO4对miR-532-3p有共同的作用位点。下调miR-532-3p可导致circRNA_103809和FOXO4表达上调。蛋白质印迹分析检测提示,敲除miR-532-3p可以促进FOXO4的表达,敲除circRNA_103809可以逆转这一现象[16]。由此可见,circ_103809作为抑癌基因,通过circRNA_103809 / miR-532-3p/FOXO4轴参与CRC的生物学过程。通过构建受试者工作特征(receiver operating characteristic,ROC)曲线评价其诊断价值,显示其ROC曲线下面积(area under curve,AUC)为0.69[15]。这表明作为miR-532-3p海绵的circRNA_103809对CRC早期诊断具有一定作用,并具有较高的诊断准确性。另外,血浆中的circ_VAPA对CRC的早期诊断也具有重要作用。circ_VAPA不仅在CRC患者组织中表达上调,而且在患者血浆中表达也上调,并且血浆中circ_VAPA表达水平随TNM分期的进展呈上升趋势。荧光素酶报告基因实验表明,circ_VAPA与miR-101之间存在直接的相互作用[18]。进一步研究显示,circ_VAPA对miR-101的表达水平没有影响,miR-101过表达与circ_VAPA沉默具有类似的抑癌作用。此外,miR-101上调能够逆转circ_VAPA过表达介导的CRC细胞增殖、迁移和侵袭。由此可见,circ_VAPA通过作为miR-101分子海绵在CRC中发挥致癌特性[18]。构建ROC曲线评价血浆中circ_VAPA的诊断价值,发现ROC AUC为0.724[18]。这说明血浆中的circ_VAPA是一种早期诊断CRC有前途的生物标志物。
2.3 circRNA作为miRNA分子海绵在结直肠癌预后评估中的作用目前已有不少研究表明,作为miRNA海绵分子的circRNA与肿瘤的进展有关,早期检测这些circRNA对指导临床决策具有重大意义[35-36]。circ_0136666在CRC组织和细胞中均过表达。体外功能检测显示,抑制circ_0136666表达可以抑制CRC细胞的增殖、迁移和侵袭[19]。此外,抑制circ_0136666表达可以抑制体内CRC细胞的生长。荧光素酶报告基因实验显示,miR-136模拟物可降低CRC细胞中circ_0136666的相对荧光素酶活性,然而抑制circ_0136666可增加miR-136在CRC细胞中的表达[19]。由此说明,在CRC细胞中,circ_0136666可以通过作为miR-136海绵发挥作用。近年来研究表明,人类SH2B衔接因子蛋白l(homo sapiens SH2B adaptor protein 1,SH2B1)在肿瘤的发生、发展和转移过程中起着致癌基因的作用[37-38]。相关分析显示,在CRC细胞中SH2B1的表达与circ_0136666表达呈正相关,而与miR-136表达呈负相关[19]。在CRC细胞中,抑制circ_0136666表达可降低SH2B1信使RNA (messenger RNA,mRNA)和蛋白表达,而miR-136抑制剂可逆转这种抑制作用。功能实验表明,抑制circ_0136666表达可降低细胞的增殖和侵袭能力,这种效应可被过表达的SH2B1所逆转[19]。因此可见,异常表达的circ_0136666可以通过结合miR-136,增加下游靶蛋白SH2B1的表达,在CRC细胞中发挥致癌作用[19]。生存分析显示,circ_0136666高表达组总生存率低于circ_0136666低表达组,说明circ_0136666高表达是一个预后不良因素[19]。另外,circ_0071589的表达在CRC组织中高于正常组织,并且表达水平的高低与TMN分期及有无淋巴结转移相关。miR-600通过靶向p53在人类结直肠癌中发挥抑癌作用。进一步的生物信息学分析表明,在circ_0071589中具有miR-600结合位点[20]。miR-600表达与circ_0071589表达呈负相关。生物信息学分析和荧光素酶报告基因分析发现,miR-600能够与ZESTE同源物增强子2(recombinant enhancer of zeste homolog 2,EZH2)结合,敲低circ_0071589能下调EZH2的表达,应用抗miR-600可以消除这种效应[20]。此外,抗miR-600可以逆转circ_0071589敲低诱导的细胞活力下降、增殖受限、侵袭和迁移能力的减弱[20]。由此可见,circ_0071589在CRC组织中表达上调,并通过miR-600/EZH2轴作为致癌因子发挥作用。Kaplan-Meier生存分析和log-rank检验表明,circ_0071589高表达组总生存时间短于circ_0071589低表达组CRC患者[20]。这说明circ_0071589表达水平是决定CRC患者预后状况的重要因素之一。
3 总结与展望随着生物技术的不断发展,已有大量的circRNA在生物体内被发现,并且其作为miRNA分子海绵与miRNA及其靶基因之间相互作用,在各类肿瘤的发病机制中发挥重要作用。circRNA作为miRNA海绵与CRC病理过程及放疗敏感性关系密切,对于CRC的发生、发展、早期诊断及预后评估具有重要作用,这为以后了解CRC的发病机制、寻找CRC新的早期诊断和预后评估标志物方面提供很好的思路,同时也为以后分子靶向药物的研究和实施放疗的个体选择方面提供了很好的方向。但是对于circRNA的海绵作用在肿瘤作用机制上的认识目前还不完善,同时由于circRNA数量多、表达特异以及circRNA/miRNA/靶蛋白轴的复杂性,增加理解其作用机制的难度;此外仅有单次研究的结果,其研究结果的准确性及可重复性有待验证。因此后期还需要更深入的研究,以便明确该作用轴在各类肿瘤中的专一性以及确定性。相信随着科研人员坚持不懈地探索以及科研能力不断地提高,circRNA将在不久的将来能够运用于临床实践,能为CRC的早期诊断、精准治疗和预后评估贡献一份力量。
| [1] |
Bray F, Ferlay J, Soerjomataram I, et al. Global cancer statistics 2018:GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J]. CA Cancer J Clin, 2018, 68(6): 394-424. |
| [2] |
Liu F, Dear K, Huang L, et al. Association between microRNA-27a rs895819 polymorphism and risk of colorectal cancer:A meta-analysis[J]. Cancer Genet, 2016, 209(9): 388-394. |
| [3] |
Guttman M, Rinn JL. Modular regulatory principles of large non-coding RNAs[J]. Nature, 2012, 482(7385): 339-346. |
| [4] |
Meng S, Zhou H, Feng Z, et al. CircRNA:functions and properties of a novel potential biomarker for cancer[J]. Mol Cancer, 2017, 16(1): 94. |
| [5] |
Memczak S, Jens M, Elefsinioti A, et al. Circular RNAs are a large class of animal RNAs with regulatory potency[J]. Nature, 2013, 495(7441): 333-338. |
| [6] |
Hansen TB, Jensen TI, Clausen BH, et al. Natural RNA circles function as efficient microRNA sponges[J]. Nature, 2013, 495(7441): 384-388. |
| [7] |
Li X, Yang L, Chen LL. The biogenesis, functions, and challenges of circular RNAs[J]. Mol Cell, 2018, 71(3): 428-442. |
| [8] |
Mitra A, Pfeifer K, Park KS. Circular RNAs and competing endogenous RNA (ceRNA) networks[J]. Transl Cancer Res, 2018, 7(Suppl 5): S624-628. |
| [9] |
Chen L, Zhang S, Wu J, et al. circRNA_100290 plays a role in oral cancer by functioning as a sponge of the miR-29 family[J]. Oncogene, 2017, 36(32): 4551-4561. |
| [10] |
Zhang HD, Jiang LH, Hou JC, et al. Circular RNA hsa_circ_0052112 promotes cell migration and invasion by acting as sponge for miR-125a-5p in breast cancer[J]. Biomed Pharmacother, 2018, 107: 1342-1353. |
| [11] |
Rong D, Lu C, Zhang B, et al. CircPSMC3 suppresses the proliferation and metastasis of gastric cancer by acting as a competitive endogenous RNA through sponging miR-296-5p[J]. Mol Cancer, 2019, 18(1): 25. |
| [12] |
Tang W, Ji M, He G, et al. Silencing CDR1as inhibits colorectal cancer progression through regulating microRNA-7[J]. Onco Targets Ther, 2017, 10: 2045-2056. |
| [13] |
Zhang N, Li X, Wu CW, et al. microRNA-7 is a novel inhibitor of YY1 contributing to colorectal tumorigenesis[J]. Oncogene, 2013, 32(42): 5078-5088. |
| [14] |
Jin Y, Yu LL, Zhang B, et al. Circular RNA hsa_circ_0000523 regulates the proliferation and apoptosis of colorectal cancer cells as miRNA sponge[J]. Braz J Med Biol Res, 2018, 51(12): e7811. |
| [15] |
Zhang P, Zuo Z, Shang W, et al. Identification of differentially expressed circular RNAs in human colorectal cancer[J]. Tumour Biol, 2017, 39(3): 1010428317694546. |
| [16] |
Bian L, Zhi X, Ma L, et al. Hsa_circRNA_103809 regulated the cell proliferation and migration in colorectal cancer via miR-532-3p/FOXO4 axis[J]. Biochem Biophys Res Commun, 2018, 505(2): 346-352. |
| [17] |
Li XN, Wang ZJ, Ye CX, et al. RNA sequencing reveals the expression profiles of circRNA and indicates that circDDX17 acts as a tumor suppressor in colorectal cancer[J]. J Exp Clin Cancer Res, 2018, 37(1): 325. |
| [18] |
Li XN, Wang ZJ, Ye CX, et al. Circular RNA circVAPA is up-regulated and exerts oncogenic properties by sponging miR-101 in colorectal cancer[J]. Biomed Pharmacother, 2019, 112: 108611. |
| [19] |
Jin C, Wang A, Liu L, et al. Hsa_circ_0136666 promotes the proliferation and invasion of colorectal cancer through miR-136/SH2B1 axis[J]. J Cell Physiol, 2019, 234(5): 7247-7256. |
| [20] |
Yong W, Zhuoqi X, Baocheng W, et al. Hsa_circ_0071589 promotes carcinogenesis via the miR-600/EZH2 axis in colorectal cancer[J]. Biomed Pharmacother, 2018, 102: 1188-1194. |
| [21] |
He JH, Li YG, Han ZP, et al. The circRNA-ACAP2/Hsa-miR-21-5p/Tiam1 regulatory feedback circuit affects the proliferation, migration, and invasion of colon cancer SW480 cells[J]. Cell Physiol Biochem, 2018, 49(4): 1539-1550. |
| [22] |
Xie H, Ren X, Xin S, et al. Emerging roles of circRNA_001569 targeting miR-145 in the proliferation and invasion of colorectal cancer[J]. Oncotarget, 2016, 7(18): 26680-26691. |
| [23] |
Huang G, Zhu H, Shi Y, et al. cir-ITCH plays an inhibitory role in colorectal cancer by regulating the Wnt/beta-catenin pathway[J]. PLoS One, 2015, 10(6): e0131225. |
| [24] |
Xu XW, Zheng BA, Hu ZM, et al. Circular RNA hsa_circ_000984 promotes colon cancer growth and metastasis by sponging miR-106b[J]. Oncotarget, 2017, 8(53): 91674-91683. |
| [25] |
Yuan Y, Liu W, Zhang Y, et al. CircRNA circ_0026344 as a prognostic biomarker suppresses colorectal cancer progression via microRNA-21 and microRNA-31[J]. Biochem Biophys Res Commun, 2018, 503(2): 870-875. |
| [26] |
Zhang XL, Xu LL, Wang F. Hsa_circ_0020397 regulates colorectal cancer cell viability, apoptosis and invasion by promoting the expression of the miR-138 targets TERT and PD-L1[J]. Cell Biol Int, 2017, 41(9): 1056-1064. |
| [27] |
Zhang J, Liu H, Zhao P, et al. Has_circ_0055625 from circRNA profile increases colon cancer cell growth by sponging miR-106b-5p[J]. J Cell Biochem, 2019, 120(3): 3027-3037. |
| [28] |
Wang L, Peng X, Lu X, et al. Inhibition of hsa_circ_0001313(circCCDC66) induction enhances the radio-sensitivity of colon cancer cells via tumor suppressor miR-338-3p:Effects of cicr_0001313 on colon cancer radio-sensitivity[J]. Pathol Res Pract, 2019, 215(4): 689-696. |
| [29] |
Chen LY, Zhi Z, Wang L, et al. NSD2 circular RNA promotes metastasis of colorectal cancer by targeting miR-199b-5p-mediated DDR1 and JAG1 signalling[J]. J Pathol, 2019, 248(1): 103-115. |
| [30] |
Fang G, Ye BL, Hu BR, et al. CircRNA_100290 promotes colorectal cancer progression through miR-516b-induced downregulation of FZD4 expression and Wnt/beta-catenin signaling[J]. Biochem Biophys Res Commun, 2018, 504(1): 184-189. |
| [31] |
Long L, Huang G, Zhu H, et al. Down-regulation of miR-138 promotes colorectal cancer metastasis via directly targeting TWIST2[J]. J Transl Med, 2013, 11(1): 275. |
| [32] |
Coppede F, Lopomo A, Spisni R, et al. Genetic and epigenetic biomarkers for diagnosis, prognosis and treatment of colorectal cancer[J]. World J Gastroenterol, 2014, 20(4): 943-956. |
| [33] |
Moschetta A, Luo X, Stock C, et al. Identification and evaluation of plasma microRNAs for early detection of colorectal cancer[J]. PLoS One, 2013, 8(5): e62880. |
| [34] |
Kanaan Z, Roberts H, Eichenberger M R, et al. A plasma microRNA panel for detection of colorectal adenomas[J]. Ann Surg, 2013, 258(3): 400-408. |
| [35] |
Shan G, Shao B, Liu Q, et al. circFMN2 sponges miR-1238 to promote the expression of LIM-homeobox gene 2 in prostate cancer cells[J]. Mol Ther Nucleic Acids, 2020, 21: 133-146. |
| [36] |
Wu Y, Zhang Y, Zheng X, et al. Circular RNA circCORO1C promotes laryngeal squamous cell carcinoma progression by modulating the let-7c-5p/PBX3 axis[J]. Mol Cancer, 2020, 19(1): 99. |
| [37] |
Wang S, Cheng Y, Gao Y, et al. SH2B1 promotes epithelial-mesenchymal transition through the IRS1/beta-catenin signaling axis in lung adenocarcinoma[J]. Mol Carcinog, 2018, 57(5): 640-652. |
| [38] |
Cheng Y, Duan C, Zhang C. New perspective on SH2B1:An accelerator of cancer progression[J]. Biomed Pharmacother, 2020, 121: 109651. |
 2020, Vol. 35
2020, Vol. 35


