文章信息
- 李济馨, 谭文华
- Li Jixin, Tan Wenhua
- miRNA27a对子宫颈癌细胞迁移和侵袭的影响
- Effects of miRNA27a on migration and invasion of cervical cancer cells
- 实用肿瘤杂志, 2020, 35(3): 223-227
- Journal of Practical Oncology, 2020, 35(3): 223-227
-
作者简介
- 李济馨(1994-), 女, 黑龙江绥化人, 硕士生, 从事妇科肿瘤临床和基础研究.
-
通信作者
- 谭文华, E-mail:tanwenhua1962@126.com
-
文章历史
- 收稿日期:2019-07-29
近年来, 恶性肿瘤发病率和死亡率不断升高。子宫颈癌、卵巢癌和子宫内膜癌已成为危害女性生命健康的常见肿瘤[1]。子宫颈癌的早期预防、及时诊断和有效治疗尤为重要。微小RNA(microRNA, miRNA)是一类非编码单链小分子RNA, 长度约为20~22个核苷酸, 为目前新的研究热点[2]。miRNA广泛存在于许多生物体中, 遍布于植物、动物乃至于病毒中[3]。miRNA在多种肿瘤中发挥重要作用。上调乳腺癌MCF-7细胞的miR-27a-3p表达促进细胞增殖、侵袭和迁移[4]。miRNA152通过作用于抑癌因子叉头状转录因子O1(fork head transcription factor O1, FOXO1), 使细胞周期调控失调和凋亡反应受损, 从而促进子宫内膜癌的发展[5]。而miR-145在卵巢癌中呈低表达, 通过靶向作用于高迁移率蛋白A2(high-mobility group protein A2, HMGA2)而发挥作用, 进而抑制肿瘤细胞的生长和迁移, 并促进卵巢癌细胞的凋亡[6]。本研究组前期已经证实miRNA27a在子宫颈癌组织中呈低表达。本研究着重于探讨miRNA27a对子宫颈癌细胞迁移和侵袭能力的影响。
1 材料与方法 1.1 细胞培养分别取子宫颈癌HeLa细胞株和SiHa细胞株(中国科学院上海细胞库)置于含10%胎牛血清及青霉素、链霉素双抗溶液的DMEM培养液中, 并放于37℃、5% CO2恒温培养箱中进行培养。观察细胞生长状态, 定期更换培养液, 待细胞处于对数生长期时进行传代及后续操作。
1.2 细胞转染miRNA27a模拟物(miRNA27a mimic)序列:上游引物为5'-UUCACAGUGGCUAAGUUCCGC-3', 下游引物为5'-GGAACUUAGCCACUGUGAAUU-3'; miRNA27a模拟物无关序列(miRNA27a negative control, miRNA27a NC):上游引物为5'-UUCUCCGAACGUGUCACGUTT-3', 下游引物为5'-ACGUGACACGUUCGGAGAATT-3'。序列的设计和合成均来源于上海吉玛生物技术有限公司。子宫颈癌HeLa细胞和SiHa细胞分别分为3组:未转染组细胞常规培养, 定期换液; mimic-miRNA27a组转染miRNA27a模拟物, mimic-NC组细胞转染miRNA27a模拟物无关序列。操作步骤参照脂质体2000(Invitrogen公司, 美国)试剂说明书, 采用荧光定量聚合酶链反应(realtime polymerase chain reaction, RT-PCR)检测确定细胞成功转染。
1.3 RT-PCR通过Trizol-离心柱法(Trizol试剂购于美国Invitrogen公司)提取出细胞总RNA, 借助于Merinton SMA4000紫外分光光度仪(Thermo公司, 美国)检测, 观察A260 nm/A280 nm比值, 计算目标RNA溶液浓度, 判断目标RNA提取质量。运用RNA反转录试剂盒(Roche公司, 瑞士)将RNA反转录为cDNA, miRNA27a PCR引物序列(上海生工生物工程有限公司):上游引物为5'-CGGCGGTTTCACAGTGGCTAAG-3', 下游引物为5'-CCAGTGCAGGGTCC GAGGTAT-3'。反应程序中, 扩增曲线:95℃ 5 min 1次; 95℃ 5 s, 60℃ 30 s共40次循环。熔解曲线:95℃ 15 s, 60℃ 30 s, 95℃ 15 s。
1.4 Transwell肿瘤细胞迁移实验将transwell小室(孔径为8 μm; BD Biosciences公司, 美国)置入24孔板中, 聚碳酸脂膜(polycarbonate membrane, PC膜)上层为无血清培养液, 下室为含10%胎牛血清(fetal bovine serum, FBS)的培养液, 取1×105个转染24 h的细胞重悬于上层无血清培养液中, 将细胞混合液贴壁放置于小室上层, 在37℃、5% CO2条件下进行培养15 h, 将小室取出, 去除24孔板下室中的培养液, 棉签擦去transwell小室上层细胞, 用磷酸盐缓冲液(phosphate buffered saline, PBS)冲洗3次, 于室温下用甲醇固定5 min, 用0.5%结晶紫进行5 min染色后, 用清水浸洗5~8次, 倒置晾干, 用刀片将PC膜取下, 封片, 于高倍镜下每孔随机选取3个视野拍照, 并对穿膜细胞进行计数。实验重复3次后, 进行统计分析。
1.5 Transwell肿瘤细胞侵袭实验将transwell小室置入24孔板中, 在小室的聚碳酸脂膜上加入1 mg/mL Matrigel(MG)基质胶40 μL(MG/PC膜), 取2×105个转染24 h的细胞重悬于上层无血清培养液中, 将细胞混合液加到基质胶上层, 将含20%FBS的培养液加到小室下层, 在37℃、5%CO2条件下培养24 h后将小室取出, 去除24孔板下室中的培养液, 擦拭掉上层细胞并用PBS冲洗3次, 室温下用甲醇固定, 用结晶紫染色, 清水浸洗后晾干, 封片。于高倍镜下每孔随机选取3个视野拍照, 并对穿膜细胞进行计数。实验重复3次后, 进行统计分析。
1.6 Western blot实验收集2×105个呈对数生长期的细胞, 利用蛋白提取试剂盒(上海碧云天生物技术有限公司)分别提取各组细胞总蛋白, 用聚氰基丙烯酸正丁酯(butyleyanoacrylate, BCA)蛋白定量试剂盒(Thermo公司, 美国)检测蛋白浓度。提取总蛋白进行SDS-PAGE凝胶电泳分离, 进行电转将电泳产物转至聚偏二氟乙烯膜(polyvinylidene fluoride, PVDF)膜上, 封闭5%脱脂牛奶1 h, 分别将1:1 000和1:2 000稀释的基质金属蛋白酶2 (matrix metalloproteinase 2, MMP-2)、MMP-9及对照蛋白特异性一抗(CST公司, 美国)加入, 于4℃下孵育过夜, 用Tris盐酸盐缓冲液(tris buffered saline tween, TBST)进行漂洗4次, 每次4 min, 将相应浓度二抗(CST公司, 美国)加入后, 于室温下静置1 h, 再用TBST漂洗4次, 每次4 min, 加入发光液(electrochemiluminescence, ECL; 上海天能科技有限公司)进行化学发光显影, 凝胶成像仪(上海天能科技有限公司)对蛋白条带进行观察, 获得图像, 并通过灰度分析(Image Lab软件), 记录灰度值, 计算目的蛋白与内参蛋白的灰度比值。甘油醛-3-磷酸脱氢酶(glyceraldehyde-3- phosphate dehydrogenase, GAPDH)蛋白(Santa公司, 美国)作为内参照。实验重复3次后, 进行统计分析。
1.7 统计学分析采用SPSS26.0统计软件作数据分析。计量资料采用均数±标准差(
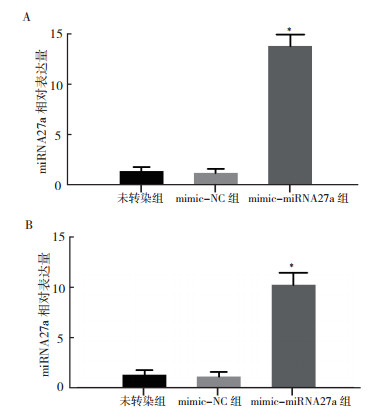
子宫颈癌HeLa和SiHa细胞转染24 h后, RT-PCR结果均显示, mimic-miRNA27a组的miRNA27a相对表达量高于mimic-NC组和未转染组, 差异均具有统计学意义(均P < 0.05);而mimic-NC组和未转染组miRNA27a相对表达量比较, 差异均无统计学意义(均P>0.05, 图 1)。
|
| 注 A:HeLa细胞;B:SiHa细胞;*与未转染组和mimicNC组比较,均P < 0.05 图 1 HeLa细胞和SiHa细胞miRNA27a模拟物转染24 h后miRNA27a相对表达量 Fig.1 Relative expression of miRNA27a in HeLa cells and SiHa cells after 24 h transfection with miRNA27a mimic |
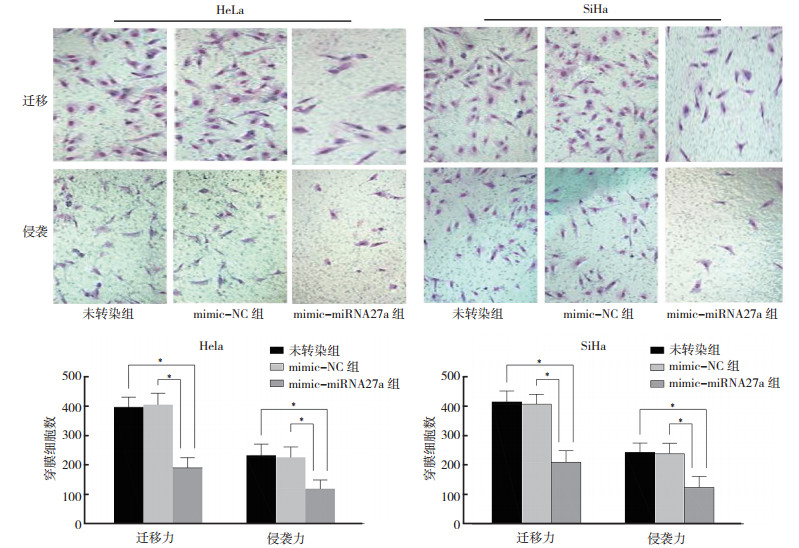
Transwell小室迁移实验检测子宫颈癌HeLa细胞和SiHa细胞迁移能力显示, 转染24 h后, mimic-miRNA27a组与mimic-NC组、未转染组比较, 2种细胞的穿膜细胞数均减少, 差异均具有统计学意义(均P < 0.05)。而mimic-NC组与未转染组比较, 差异均无统计学意义(均P>0.05, 图 2)。
|
| 注 *P < 0.05 图 2 miRNA27a模拟物转染24 h后对HeLa细胞和SiHa细胞迁移和侵袭能力的影响(×200) Fig.2 Migration and invasion of HeLa cells and SiHa cells after 24 h transfection with miRNA27a mimic (×200) |
Transwell小室侵袭实验显示, 在子宫颈癌HeLa细胞和SiHa细胞中, 转染24 h后, mimic-miRNA27a组与mimic-NC组、未转染组比较, 2种细胞的穿膜细胞数均减少, 差异均具有统计学意义(均P < 0.05, 图 2); mimic-NC组与未转染组比较, 差异均无统计学意义(均P>0.05)。
2.4 上调miRNA27a可影响MMP-2和MMP-9蛋白的表达Western blot实验显示, 转染24 h后, 在HeLa细胞和SiHa细胞中, mimic-miRNA27a组与mimicNC组、未转染组比较, 2种细胞中MMP-2和MMP-9蛋白表达量均降低, 差异均具有统计学意义(均P < 0.05, 图 3); mimic-NC组与未转染组比较, 差异均无统计学意义(均P>0.05)。

|
| 注 A:HeLa细胞;B:SiHa细胞;* P < 0.05 图 3 miRNA27a模拟物转染24 h对HeLa细胞和SiHa细胞MMP-2和MMP-9蛋白表达量的影响 Fig.3 Effect of 24 h miRNA27a mimic transfection on MMP-2 and MMP-9 expression in HeLa cells and SiHa cells |
子宫颈癌如果早发现并早治疗, 预后良好, 早期子宫颈癌的5年生存率达90%以上, 而中期和局部晚期子宫颈癌易出现复发转移, 治疗效果欠佳, 生存率低。肿瘤的转移是肿瘤细胞从原发肿瘤组织中分裂出来, 通过血液循环, 种植于远处, 并在新部位建立细胞血供, 逐步生长形成危及生命的肿块的过程, 多种生长因子及细胞因子都参与其中并发挥重要的作用[7-8]。目前, 对miRNA27a在子宫颈癌的研究甚少, 其在子宫颈癌迁移和侵袭过程中的具体机制仍不明确。miRNA27a是miRNA家族的一个重要成员, 在肿瘤的发生和发展中起到重要的作用, 在对胃癌的研究中发现, 上调胃癌SGC-7901细胞中miRNA27a的表达, 凋亡相关蛋白BCL-2表达上调, p53水平下降, 与miRNA27a靶向抑制FOXO1基因表达有关[9]。对于卵巢癌的预后而言, miRNA27a通过对P-gp在翻译水平的抑制, 提高卵巢癌细胞对顺铂的敏感性[10]。本研究证实, 在子宫颈癌细胞的迁移和侵袭过程中miRNA27a发挥着极其重要的作用。本研究组前期研究证实, miRNA27a在子宫颈癌组织中呈低表达。本研究采用transwell细胞迁移和侵袭实验证实, miRNA27a对子宫颈癌细胞的迁移和侵袭能力有抑制作用。
MMP-9是基质金属蛋白酶家族中重要一员, 其与肿瘤的浸润和转移有关[11]。MMP-9作为一种Ⅳ型的胶原蛋白, 主要作用是降解细胞外基质(extracellular matrix, ECM)。ECM是防止恶性肿瘤细胞侵袭和转移的重要生理屏障, 对防止肿瘤细胞的扩散有重要作用, 因此MMP-9在肿瘤的转移过程中有一定意义[12-13]。MMP-2同样也是基质金属蛋白酶家族中的一员, 参与许多恶性肿瘤的侵袭迁移, 为治疗肿瘤的一个新的靶点[14]。研究表明, 中医药黄芩苷可通过调节p38信号通路下调MMP-2和MMP-9的表达, 进而抑制子宫颈癌HeLa细胞侵袭和转移[15]。
本研究显示, 上调miRNA27a后子宫颈癌细胞MMP-2和MMP-9的相对表达量减少, 表明miRNA27a对MMP-2和MMP-9的表达起抑制作用。后期本研究组将建立裸鼠子宫颈癌异种移植模型, 进一步探索上调miRNA27a对在体子宫颈癌细胞迁移和侵袭的影响及其相关的分子机制, 从而为子宫颈癌的靶向治疗提供科学依据。
综上所述, miRNA27a在子宫颈癌组织中呈低表达, 上调miRNA27a的表达抑制子宫颈癌细胞的迁移和侵袭能力。本研究对子宫颈癌的迁移和侵袭的机制研究提供新的思路, 为子宫颈癌在临床诊疗过程中提供理论基础及潜在的分子靶向位点。
| [1] |
Siegel RL, Miller KD, Jemal A. Cancer statistics, 2019[J]. CA Cancer J Clin, 2019, 69(1): 7-34. |
| [2] |
王焱, 唐博. MiRNA与肝癌密切关系的研究进展[J]. 世界最新医学信息文摘, 2018, 18(94): 27-30. |
| [3] |
Shi M, Guo N. MicroRNA expression and its implications for the diagnosis and therapeutic strategies of breast cancer[J]. Cancer Treat Rev, 2009, 35(4): 328-334. |
| [4] |
蒋雪梅, 权毅. 上调miRNA-27a-3p对乳腺癌MCF-7细胞增殖、侵袭和迁移能力的影响[J]. 郑州大学学报:医学版, 2019, 54(2): 279-283. |
| [5] |
Myatt SS, Wang J, Monteiro LJ, et al. Definition of microRNAs that repress expression of the tumor suppressor gene FOXO1 in endometrial cancer[J]. Cancer Res, 2010, 70(1): 367-377. |
| [6] |
Kim TH, Song JY, Park H, et al. MiR-145, targeting high-mobility group A2, is a powerful predictor of patient outcome in ovarian carcinoma[J]. Cancer Lett, 2015, 356(2 Pt B): 937-945. |
| [7] |
Steeg PS. Cancer biology:emissaries set up new sites[J]. Nature, 2005, 438(7069): 750-751. |
| [8] |
刘永刚, 闫一敏, 杨荣松. 血清miRNA复发分子标志物检测与鼻咽癌复发远处转移的相关性[J]. 实用肿瘤杂志, 2018, 33(4): 354-358. |
| [9] |
张悦, 管叙文, 王婧雅, 等. MiR-27a对胃癌细胞凋亡影响的体外研究[J]. 天津医科大学学报, 2018, 24(6): 469-473. |
| [10] |
高慧. 转染miRNA27a抑制物对卵巢癌耐药细胞系顺铂敏感性的研究[J]. 山东医学高等专科学校学报, 2015, 37(3): 201-205, 241. |
| [11] |
王志凯, 张超, 白军伟, 等. CD147及MMP-7在胆管癌中的表达及其临床意义[J]. 实用肿瘤杂志, 2019, 34(1): 35-38. |
| [12] |
Hou Y. Protein expression and clinical significance of COX2, p21and MMP-9 in cervical cancer tissue[J]. J Central South Med Sci, 2016, 44(6): 664-666. |
| [13] |
Shen XG, Guo ZY, Zhao GP, et al. Clinical pathologic significance and prognostic value of upregulated MMP-7 expression in gastric cancer[J]. Clin J Practical Hospital, 2017, 14(5): 128-131. |
| [14] |
Pei J, Park IH, Ryu HH, et al. Sublethal dose of irradiation enhances invasion of malignant glioma cells through p53-MMP 2 pathway in U87MG mouse brain tumor model[J]. Radiat Oncol, 2015, 10(10): 164. |
| [15] |
张悦, 符乔珊, 刘韡, 等. 黄芩苷对宫颈癌HeLa细胞侵袭转移的抑制作用及其机制[J]. 西安交通大学学报:医学版, 2016, 37(4): 599-603. |
 2020, Vol. 35
2020, Vol. 35


