文章信息
- 何平, 宋辉, 梁杰雄, 邵天松, 张钊, 李洋
- He Ping, Song Hui, Liang Jiexiong, Shao Tiansong, Zhang Zhao, Li Yang
- MiR-200c调节人结肠癌SW480细胞迁移与侵袭的分子机制研究
- Molecular mechanisms of miR-200c regulating invasion and migration of human colon cancer SW480 cells
- 实用肿瘤杂志, 2019, 34(3): 210-214
- Journal of Practical Oncology, 2019, 34(3): 210-214
基金项目
- 国家自然科学基金(30972886)
-
作者简介
- 何平(1972-), 男, 北京人, 副主任医师, 博士, 消化道肿瘤的基础与临床研究.
-
通信作者
- 何平, E-mail: 149155918@qq.com
-
文章历史
- 收稿日期:2017-11-24
结直肠癌的发病率呈逐年攀升的趋势,是发病率较高的胃肠道肿瘤。结肠肿瘤可沿肠壁进行环形发展,向肠壁深层浸润或沿肠管纵轴上下蔓延,不但能够进行局部侵犯,还能够进行扩散与转移。虽然还没有完全清楚结肠癌的发病机制,但值得指出的是结肠癌的发生和发展与癌前疾病、环境和遗传因素密切相关。结肠癌的侵袭与迁移可能与miR-200家族成员的作用相关。miR-200c属于miR-200家族成员之一[1-3],上皮间质转化(epithelial-mesenchymal transition,EMT)可能与上述miR-200家族成员的异常表达密切相关,也就是说在上皮细胞转化为间质细胞的过程中,细胞具有入侵与转移的功能,这些功能不但参与器官纤维化和受损组织的愈合等生理过程,还参与癌症的发生和发展。我国目前尚无关于miR-200c参与癌症发生与发展的系统性研究。外源性微小核糖核酸(microribonucleic acid,miRNA)包括miRNA类似物与抑制物目前已经成功应用于探索干扰靶基因的功能和表达等方面。本文通过miRNA类似物以及抑制物改变结肠肿瘤细胞miR-200c表达探讨miR-200c对结肠肿瘤细胞生物学行为的影响以及其作用机制,以期为结肠癌治疗提供思路和理论支持。
1 材料与方法 1.1 试剂及细胞株L-15培养液(上海哈灵公司);脂质体2000(上海拜力生物科技有限公司);miR-200c类似物(miR-200c mimics)及miR-200c抑制物(miR-200c核酸抑制剂)(上海拜力生物科技有限公司);人结肠癌细胞株SW480(上海拜力生物科技有限公司)。
1.2 实验方法 1.2.1 细胞培养采用L-15培养液(含有10%胎牛血清),5%CO2 37℃条件下进行SW480细胞培养。
1.2.2 分组SW480细胞分为类似物转染组(转染miR-200c类似物)、抑制物转染组(转染miR-200c核酸抑制剂)、类似物阴性对照组(转染miR-200c类似物的无义序列)、抑制物阴性对照组[加入miR-200c核酸抑制剂的载体(不含miR-200c核酸抑制剂)]以及空白组(不进行任何处理)。
1.2.3 细胞转染实验于6孔细胞培养板上接种处于对数期生长且经消化后的细胞,每孔的细胞数为(4~5)×105个。当细胞融合50%~60%时,按照脂质体2000说明书操作步骤转染SW480细胞,无义序列和miR-200c类似物以50 nmo/L为终浓度进行转染,无义序列和miR-200c抑制物以100 nmo/L为终浓度进行转染;总RNA的提取采用Trizol法,选择miR-200c特异性引物和反转录酶进行cDNA的合成,保存于-20℃冰箱中备用。miR-200c表达水平的检测采用荧光定量PCR,具体反应条件如下:95℃预变性20 s,95℃变性10 s,60℃退火20 s,70℃延伸10 s,共40个循环。采用2-ΔΔCt进行数据分析。
1.2.4 Western blot检测对转染24 h以及48 h的细胞进行收集,核蛋白提取采用核蛋白提取试剂盒(生工生物工程上海股份有限公司)并严格按照说明书中具体步骤操作;核蛋白分离采用聚丙烯酰胺凝胶电泳,80 V恒压向PVDF膜转移;以BSA进行1 h的封闭,分别加入羊抗人β-catenin抗体(按照1 :300稀释,购自上海优宁维生物科技有限公司)和E-cadherin抗体(按照1 :300稀释,购自北京义翘神州科技有限公司),在4℃的条件下过夜培养。第2天在室温条件下培养0.5 h,洗膜,加入二抗(辣根过氧化酶标记,按照1 :200稀释),室温条件下培养1 h。图像通过凝胶成像系统进行采集。
1.2.5 细胞划痕实验转染后细胞于5% CO2 37℃条件下过夜培养。第2天采用移液枪头在6孔板上垂直划线,以磷酸盐缓冲液洗涤3次,加入不含血清培养液;分别于0 h、12 h和24 h时对划痕处细胞迁移情况进行观察,拍摄照片;伤痕的宽度使用Image-proplus 6.0进行检测。SW480细胞伤痕平均面积与SW480细胞伤痕长度之比即为SW480细胞伤痕宽度。
1.2.6 Transwell细胞侵袭实验在培养小室上铺采用L-15培养液8倍稀释的Matrigel基质胶,对稀释后SW480细胞进行接种;下室加入500 μL浓度为15%血清的L-15培养液,每组均设置3个复孔,5% CO2 37℃条件下培养24 h和48 h后,将transwell小室取出,将孔中的培养液弃去,以PBS进行3次洗涤,染色采用浓度为0.1%的结晶紫,25 min后以棉签将膜上层细胞去除。10倍镜下随机选择5个视野计数,取平均数。所有实验重复3次。聚碳酸酯滤膜孔径为8 μm。
1.3 统计学分析采用SPSS 20.0统计学软件作数据分析。计量资料采用均数±标准差(x±s)表示,多组间比较采用单因素方差分析或重复测量的方差分析,组间两两比较采用LSD-t检验。计数资料采用频数(百分比)表示,多组间比较采用χ2检验。以P < 0.05为差异具有统计学意义。
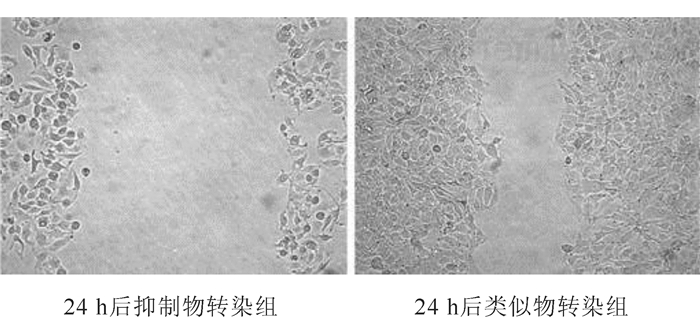
2 结果 2.1 miR-200c对SW480细胞迁移能力的影响细胞划痕实验显示(图 1),12 h后类似物转染组和类似物阴性对照组伤痕宽度分别为(589.60±17.28)μm和(465.32±16.60)μm(P < 0.05)。24 h后类似物转染组和类似物阴性对照组伤痕宽度分别为(523.82±57.13)μm和(393.98±7.53)μm(P < 0.05)。12 h后抑制物转染组和抑制物阴性对照组伤痕宽度分别为(430.92±20.76)μm和(485.63±16.65)μm(P < 0.05)。24 h后抑制物转染组和抑制物阴性对照组伤痕宽度分别为(221.37± 44.37)μm和(441.21±22.40)μm(P < 0.05)。
|
| 图 1 miR-200c对SW480细胞迁移能力的影响(×100) Fig.1 Effect of miR-200c on the migration of SW480 cells(×100) |
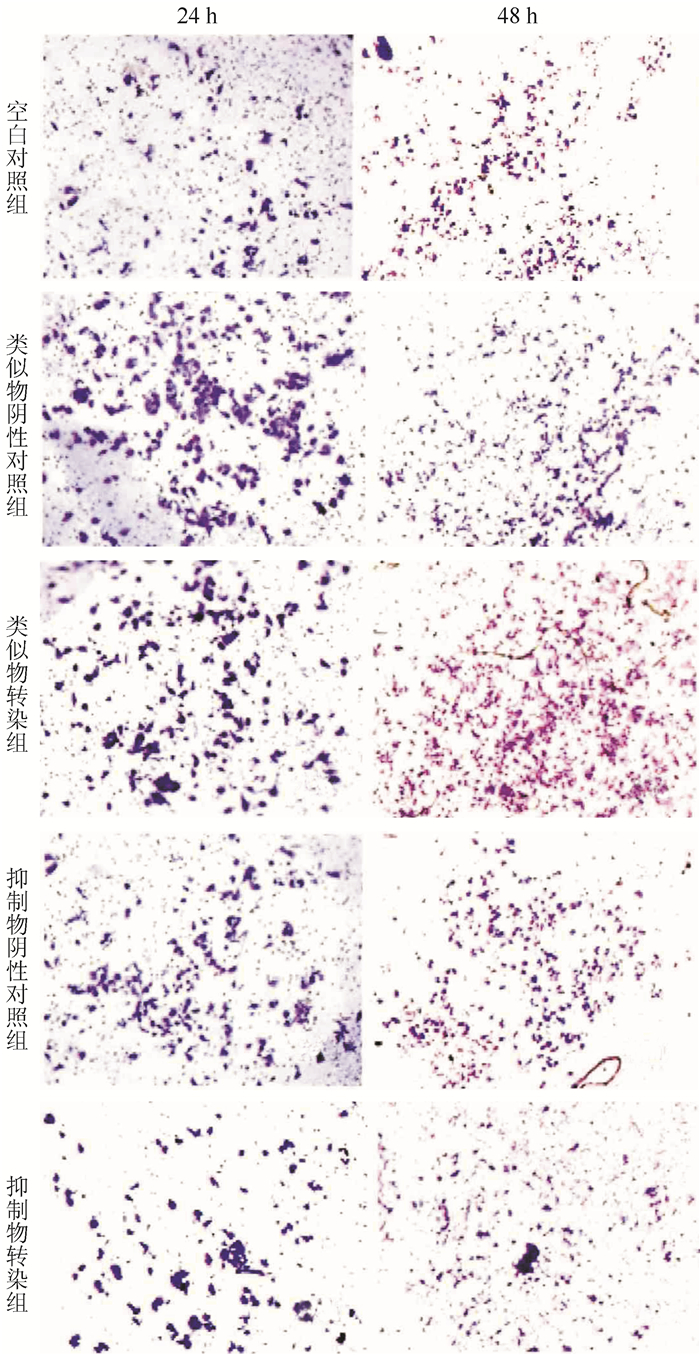
Transwell侵袭实验显示,24 h和48 h后类似物转染组通过8 μm孔径的细胞数目降低,与类似物阴性对照组以及空白对照组间比较,差异均具有统计学意义(均P < 0.05,图 2)。抑制物转染组细胞通过数目增加,高于抑制物阴性对照组以及空白对照组(均P < 0.05)。提示miR-200c的过表达对SW480细胞侵袭产生抑制,miR-200c的低表达能够促进SW480细胞的侵袭。
|
| 图 2 miR-200c对SW480细胞侵袭能力的影响(×200) Fig.2 Effect of miR-200c on the invasion of SW480 cells(×200) |
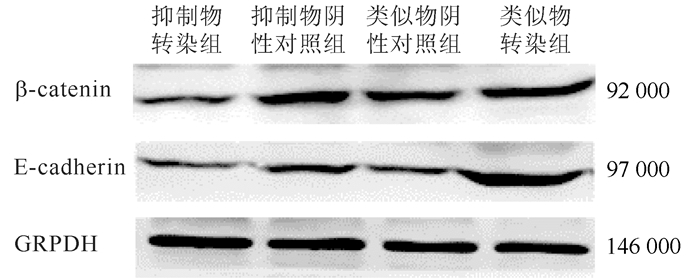
类似物转染组细胞β-catenin和E-cadherin蛋白表达均升高(均P < 0.05),抑制物转染组细胞β-catenin和E-cadherin蛋白表达均降低(均P < 0.05,图 3)。
|
| 图 3 miR-200c对SW480细胞β-catenin和E-cadherin表达的影响 Fig.3 Effect of miR-200c on the expression of β-catenin and E-cadherin in SW480 cells |
在肿瘤EMT、侵袭和转移的过程中miR-200家族扮演重要角色[4-6]。EMT与胚胎发育、组织重建、慢性炎性反应、肿瘤转移以及纤维化疾病密切相关,主要特征包括细胞角蛋白细胞骨架向波形蛋白为主的细胞骨架的转化、细胞黏附分子表达水平降低以及具有间充质细胞的形态特征等。上皮细胞通过上皮向间质转化丧失细胞极性,丧失连接基底膜等上皮表型,具有较高的侵袭、迁移、抗凋亡能力以及对细胞外基质进行降解的能力。EMT是来源于上皮细胞的恶性肿瘤细胞得到迁移与侵袭能力的主要生理过程。
本研究细胞划痕实验显示,类似物转染组12 h和24 h后伤痕宽度高于miR-200类似物阴性对照组,抑制物转染组低于抑制物阴性对照组。Transwell实验显示,与类似物阴性对照组和抑制物阴性对照组比较,类似物转染组24 h和48 h通过8 μm孔径的细胞数减少,抑制物转染组增多。已知miR-200家族成员的上调可促进细胞转移[7-9],转录因子GA-TA结合蛋白-3(GA-TA-binding protein-3,GATA3)可通过抑制miR-200的表达对肿瘤细胞的转移起促进作用[10]。miR-200c抑制SW480细胞侵袭与迁移的机制可能与靶向抑制转录因子锌指结构蛋白1(zinc-finger E-box-binding homeobox 1,ZEB1)相关[11-12]。转录因子ZEB1能够对多种基因的表达产生抑制作用,并可能通过降低E-cadherin的表达,促进EMT,最终起到促进肿瘤细胞侵袭的作用。若miR-200c的表达水平增加,蛋白水平与mRNA水平的ZEB1表达水平均降低。
细胞质中存在2种catenin间的平衡状态的变化可能与肿瘤细胞的侵袭与迁移能力相关。β-catenin不仅与E-cadherin结合成复合体参与细胞的黏附,还是Wnt/β-catenin信号通路的重要成员[13]。在各种肿瘤细胞中均发现E-cadherin/catenin与组织学特征密切相关[14]。本研究发现,类似物转染组β-catenin和E-cadherin的表达均升高,抑制物转染组各蛋白表达下降。这说明miR-200可调节EMT过程。miR-200家族成员能够对转录因子ZEB1与ZEB2的表达产生抑制作用,而ZEB1与ZEB2同样能够反过来抑制miR-200家族成员的表达[15-17],即miR-200家族成员可通过反馈调节对EMT过程起抑制作用[18-20],本研究与此相互印证。
Wnt/β-catenin信号通路是参与调控EMT的重要通路之一[21-22]。当Wnt/β-catenin信号途径被激活时,E-cadherin/catenin复合物稳定性遭到破坏,核内聚集大量的β-catenin并与T细胞因子组合成为复合体,通过影响EMT相关蛋白的表达量,最终引起EMT发生。Wnt/β-catenin信号通路的主要标志包括细胞内β-catenin的异常表达。β-catenin核内积聚多发生在肿瘤组织侵袭边缘的去分化肿瘤组织中,而EMT发生的主要部位之一即肿瘤侵袭边缘。
综上所述,本研究显示,过表达miR-200c对SW480细胞的侵袭与迁移能力产生抑制,增加E-cadherin和β-catenin的表达水平。miR-200c表达水平降低则促进SW480细胞的侵袭与迁移能力,并降低E-cadherin和β-catenin的表达水平。这提示可通过Wnt/β-catenin信号通路抑制SW480细胞的侵袭和迁移,EMT中miRNA的复杂调节可能可以通过miR-200c的信号转导来解释。
| [1] |
Gao HX, Yan L, Li C, et al. miR-200c regulates crizotinib-resistant ALK-positive lung cancer cells by reversing epithelial-mesenchymal transition via targeting ZEB1[J]. Mol Med Rep, 2016, 14(5): 4135-4143. DOI:10.3892/mmr.2016.5770 |
| [2] |
Meng X, Müller V, Milde-Langosch K, et al. Circulating cell-free miR-373, miR-200a, miR-200b and miR-200c in patients with epithelial ovarian cancer[J]. Adv Exp Med Biol, 2016, 924(1): 3-8. |
| [3] |
Damiano V, Brisotto G, Borgna S, et al. Epigenetic silencing of miR-200c in breast cancer is associated with aggressiveness and is modulated by ZEB1[J]. Genes Chromosomes Cancer, 2016, 56(2): 147-158. |
| [4] |
Li Q, Zhang C, Chen R, et al. Disrupting MALAT1/miR-200c sponge decreases invasion and migration in endometrioid endometrial carcinoma[J]. Cancer Lett, 2016, 383(1): 28-40. DOI:10.1016/j.canlet.2016.09.019 |
| [5] |
Guo E, Wang Z, Wang S. MiR-200c and miR-141 inhibit ZEB1 synergistically and suppress glioma cell growth and migration[J]. Eur Rev Med Pharmacol Sci, 2016, 20(16): 3385-3391. |
| [6] |
Sulaiman SA, AbMutalib NS, Jamal R, et al. miR-200c regulation of metastases in ovarian cancer:potential role in epithelial and mesenchymal transition[J]. Front Pharmacol, 2016, 7(8): 271. |
| [7] |
Muto Y, Suzuki K, Kato T, et al. Heterogeneous expression of zinc-finger E-box-binding homeobox 1 plays a pivotal role in metastasis via regulation of miR-200c in epithelial-mesenchymal transition[J]. Int J Oncol, 2016, 49(3): 1057-1067. DOI:10.3892/ijo.2016.3583 |
| [8] |
Jiang Z, Tao JH, Zuo T, et al. The correlation between miR-200c and the severity of interstitial lung disease associated with different connective tissue diseases[J]. Scand J Rheumatol, 2016, 16(7): 1-8. |
| [9] |
Guo J, Fang W, Sun L, et al. Reduced miR-200b and miR-200c expression contributes to abnormal hepatic lipid accumulation by stimulating JUN expression and activating the transcription of srebp1[J]. Oncotarget, 2016, 7(24): 36207-36219. |
| [10] |
Yang Y, Ahn YH, Gibbons DL, et al. The Notch ligand Jagged2 promotes lung adenocarcinoma metastasis through a miR-200-dependent pathway in mice[J]. J Clin Invest, 2011, 121(4): 1373-1385. DOI:10.1172/JCI42579 |
| [11] |
Yang Y, Ahn YH, Chen Y, et al. ZEB1 sensitizes lung adenocarcinoma to metastasis suppression by PI3K antagonism[J]. J Clin Invest, 2014, 124(6): 2696-2708. DOI:10.1172/JCI72171 |
| [12] |
Del Vecchio G, De Vito F, Saunders SJ, et al. RNA-binding protein HuR and the members of the miR-200 family play an unconventional role in the regulation of c-Jun mRNA[J]. RNA, 2016, 22(10): 1510-1521. DOI:10.1261/rna.057588.116 |
| [13] |
Jenkins LM, Singh P, Varadaraj A, et al. Altering the proteoglycan state of TβRⅢ/Betaglycan modulates canonical Wnt/β-catenin signaling[J]. J Biol Chem, 2016, 291(49): 25716-25728. DOI:10.1074/jbc.M116.748624 |
| [14] |
Kitase Y, Shuler CF. Microtubule disassembly prevents palatal fusion and alters regulation of the E-cadherin/catenin complex[J]. Int J Dev Biol, 2013, 57(1): 55-60. DOI:10.1387/ijdb.120117yk |
| [15] |
Cheng Y, Zhang X, Li P, et al. MiR-200c promotes bladder cancer cell migration and invasion by directly targeting RECK[J]. Onco Targets Ther, 2016, 9(8): 5091-5099. |
| [16] |
Jepsen RK, Novotny GW, Klarskov LL, et al. Investigating intra-tumor heterogeneity and expression gradients of miR-21, miR-92a and miR-200c and their potential of predicting lymph node metastases in early colorectal cancer[J]. Exp Mol Pathol, 2016, 101(2): 187-196. DOI:10.1016/j.yexmp.2016.08.003 |
| [17] |
Peng Y, Zhu X, Qiu L, et al. Electroneutral composite polymersomes self-assembled by amphiphilic polyphosphazenes for effective miR-200c in vivo delivery to inhibit drug resistant lung cancer[J]. Biomaterials, 2016, 106(11): 1-12. |
| [18] |
Li Y, Nie Y, Tu S, et al. Epigenetically deregulated miR-200c is involved in a negative feedback loop with DNMT3a in gastric cancer cells[J]. Oncol Rep, 2016, 36(4): 2108-2116. DOI:10.3892/or.2016.4996 |
| [19] |
Shan W, Zhang X, Li M, et al. Over expression of miR-200c suppresses invasion and restores methotrexate sensitivity in lung cancer A549 cells[J]. Gene, 2016, 593(2): 265-271. DOI:10.1016/j.gene.2016.07.038 |
| [20] |
Yoshimatsu G, Takita M, Kanak MA, et al. MiR-375 and miR-200c as predictive biomarkers of islet isolation and transplantation in total pancreatectomy with islet autotransplantation[J]. J Hepatobiliary Pancreat Sci, 2016, 23(9): 585-594. DOI:10.1002/jhbp.377 |
| [21] |
Xiao C, Wu CH, Hu HZ, et al. LncRNA UCA1 promotes epithelial-mesenchymal transition (EMT) of breast cancer cells via enhancing Wnt/beta-catenin signaling pathway[J]. Eur Rev Med Pharmacol Sci, 2016, 20(13): 2819-2824. |
| [22] |
Ma X, Yan W, Dai Z, et al. Baicalein suppresses metastasis of breast cancer cells by inhibiting EMT via downregulation of SATB1 and Wnt/β-catenin pathway[J]. Drug Des Devel Ther, 2016, 10(4): 1419-1441. |
 2019, Vol. 34
2019, Vol. 34


