文章信息
- 李长江, 洪琛
- Li Changjiang, Hong Chen
- 肿瘤源性外泌体miR-21对胃癌细胞增殖和凋亡的影响
- Effect of tumor-derived exosome miR-21 on proliferation and apoptosis of gastric cancer cells
- 实用肿瘤杂志, 2022, 37(2): 123-127
- Journal of Practical Oncology, 2022, 37(2): 123-127
-
通信作者
- 李长江,E-mail:lichangjiang5555@163.com
-
文章历史
- 收稿日期:2021-02-07
胃癌是一种常见的恶性肿瘤病变。近5年胃癌发病率呈上升趋势[1]。胃癌位居全国肿瘤发病的第二位,仅次于肺癌。胃癌的主要治疗手段包括手术、化疗以及放疗,由于在我国胃癌早期检出率较低,多数患者就诊时已处于中晚期,传统手段治疗下胃癌5年生存率始终偏低[2-3]。深入研究胃癌的发生和发展机制对改善胃癌患者的生存质量具有重大意义。
外泌体是一种直径约40~100 nm的膜性囊泡网[4]。外泌体可介导多种信号传导,例如细胞与细胞间的信息传递等[5-6]。外泌体特异性蛋白分子主要包括白细胞分化抗原群63(cluster of differentiation 63,CD63)、CD9和肿瘤易感基因101蛋白(tumor susceptibility gene 101 protein,TSG101)等。因此,在实验研究中通过特异性检测相关标志物有助于外泌体的提取与分离[7]。研究发现,外泌体的宿主来源具有不同的分子调控作用,其中肿瘤细胞来源外泌体可通过调控细胞间信号传导,促进血管新生等细胞生物学行为,影响肿瘤细胞代谢状态和侵袭增殖能力等,是目前肿瘤学研究的重点和热点之一[8]。但是目前有关肿瘤外泌体对肿瘤细胞的调节机制尚不完全清楚。本研究拟探讨肿瘤源性外泌体miR-21对胃癌细胞增殖和凋亡的影响,为进一步探索胃癌发生和发展过程的分子作用机制提供理论支持。
1 材料与方法 1.1 实验细胞与主要试剂人胃癌细胞株SGC-7091来自美国ATCC细胞库。胎牛血清和细胞培养液购于美国Gibco公司。荧光定量实时PCR(real-time PCR,RT-PCR)试剂盒购自日本Takara公司。PCR引物由广州锐博公司合成。外泌体提取试剂盒购自美国System Biosciences公司。B淋巴细胞瘤-2(B-cell lymphoma-2,Bcl-2)和caspase-3单克隆抗体购自美国Cell Signaling Technology公司。兔抗人细胞周期素D1(cyclin D1)购自美国Santa Cruz公司。兔抗人TSG101和CD63购自英国Abcam公司。兔抗人β-actin单克隆抗体购自武汉Proteintech公司。TUNEL染色试剂盒购自上海碧云天公司。
1.2 实验主要仪器和设备PCR仪器购自武汉赛默飞ABI公司。TWK-FST32型细胞组织匀浆仪购自武汉泰普拓公司。Micro17R型高速冷冻离心机和FC型全自动多功能酶标检测仪购自武汉赛默飞世尔科技(中国)有限公司。GPJ9-TS100-F型倒置荧光显微镜购自日本Nikon公司。1658033型电泳仪和ChemiDoc XRS+成像系统购自美国Bio-Rad公司。
1.3 细胞培养与外泌体共培养处理将实验细胞分为两组,分别为对照组和外泌体组。37℃ 5% CO2及饱和湿度条件下培养,细胞贴壁生长,之后每2天换液1次。待细胞长满瓶底后进行细胞传代处理(0.25%的胰蛋白酶消化2 min)。其中外泌体组采用与细胞培养液混合方式加入终浓度为0.50 μg/μL的外泌体处理细胞24 h,对照组细胞常规细胞培养液培养24 h。
1.4 肿瘤细胞外泌体提取采用处理完成的无外泌体的血清完全培养液培养48 h,收集细胞上清液并进行离心处理。按照试剂盒进行外泌体提取。首先将培养完成的细胞上清液转移至无菌培养皿,并与等体积ExoQuick exosome precipitation solution(SBI,美国)充分混合,将混合完成4 ℃条件下静置20 h,混悬液以3 000 r/min离心20 min,弃去细胞上清后1 500 r/min离心10 min,收集得到外泌体沉淀物。
1.5 外泌体检测 1.5.1 电子显微镜观察外泌体2%戊二醛重悬并固定外泌体,PBS清洗2次,1%的饿酸固定时长1 h,PBS清洗2次,乙醇脱水,将乙醇与环氧丙烷等比例混匀,室温条件下浸泡10 min,后转移至环氧丙烷中再浸泡10 min,最后将所取标本浸透、干燥、包埋、聚合、切片和染色,电子显微镜下观察外泌体形态学特征。
1.5.2 Western blot检测外泌体样品定量,对外泌体标志性蛋白CD63和TSG101进行定量检测。对细胞上清液进行高速离心30 000 r/min,离心30 min,得到细胞上清液沉淀; 加入细胞裂解液于冰上裂解10 min; BCA法测定蛋白质浓度; 定量上样,电泳,转膜,孵育对应抗体; 显影定量检测上清液沉淀物CD63和TSG101表达情况。
1.6 TUNEL染色倾去细胞培养液,按照TUNEL染色试剂盒说明书进行相关检测。
1.7 MTT检测细胞增殖将消化后的SGC-7091细胞按照1×104/孔接种于96孔板,细胞贴壁生长24 h后,加入终浓度为0.50 μg/μL的外泌体处理细胞24 h,每个浓度设置6个复孔,每孔加入MTT溶液10 μL继续培养1 h,酶标仪设定波长为570 nm检测各孔的吸光度(absorbance,A)值。
1.8 RT-PCR检测miR-21表达使用紫外分光光度计检测RNA样品浓度及260 nm与280 nm处的A值比值,之后进行RNA样品浓度标化; 按照RNA反转录试剂盒说明书,配置mRNA反转录混合体系。U6上游引物: 5'-CCTCACTGTCCACCTTCCA-3';下游引物: 5'-GGGTGTAAAACGCAGCTCA-3'。miR-21上游引物:5'-GGGCCCAGTGTTCAGACTAC-3';下游引物: 5'-GTGCAGGGTCCGAGGT-3'。将qPCR反应参数设置为:92℃,30 s; 92℃,5 s; 60℃,31 s,共进行30个循环。采用7300 System SDS Software分析数据,根据2-△△Ct值相对定量样本中miR-21表达。
1.9 Western blot实验将处理完成的SGC-7091放置于1.5 mL的组织研磨管内并按照1∶4比例加入细胞裂解液放置在已经预冷后的细胞组织匀浆仪中进行研磨; 4℃ 12 000 r/min离心10 min,收集细胞上清液,并进行蛋白质浓度定量检测; 每孔上样量为40 μg进行蛋白质凝胶电泳实验,根据目的蛋白相对分子质量大小以及蛋白marker指示进行切胶,湿转转膜法将蛋白转移至PVDF膜上,脱脂牛奶封闭2 h,孵育对应Bcl-2(1∶1 000)、caspase-3(1∶1 000)、cyclin D1(1∶500)和β-actin(1∶5 000)置于4℃条件下过夜,孵育各自对应二抗(1∶5 000)1~2 h,于摇床摇晃洗膜,TPBS洗涤后加入ECL,使用胶片曝光,图片扫描后用Image J软件计算各条带的灰度值,以各目标条带灰度值与内参β-actin条带灰度值的比值表示目标蛋白的相对表达量。
1.10 统计学分析采用SPSS 20.0软件进行数据分析。数据采用均数±标准差(x±s)表示,多组之间比较采用ANOVA分析方法,两组间差异比较采用t检验。以P < 0.05为差异具有统计学意义。
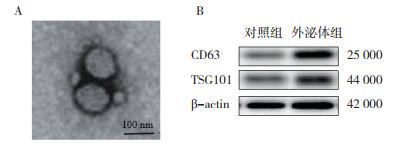
2 结果 2.1 肿瘤细胞外泌体提取与鉴定透射电子显微镜观察胃癌细胞株SGC-7091源性外泌体呈椭圆形或部分圆形形状,粒径大小为40~100 nm。与对照组比较,外泌体组高表达CD63和TSG101,表明成功提取到SGC-7091外泌体(图 1)。
|
| 注 A:透射电子显微镜下肿瘤细胞外泌体形态特征; B:Western blot检测提示外泌体标志蛋白CD63及TSG101表达升高 图 1 肿瘤细胞源性外泌体提取与鉴定 Fig.1 Extraction and identification of tumor cell-derived exosomes |
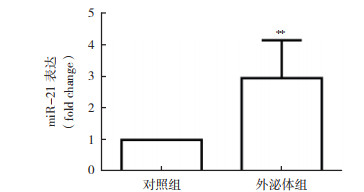
与对照组比较,外泌体组SGC-7091细胞miR-21表达增加(P < 0.01,图 2)。
|
| 注 **与对照组比较,P < 0.01 图 2 外泌体组SGC-7091细胞miR-21表达增加 Fig.2 The increased expression of miR-21 in SGC-7091 cells in the exosome group |
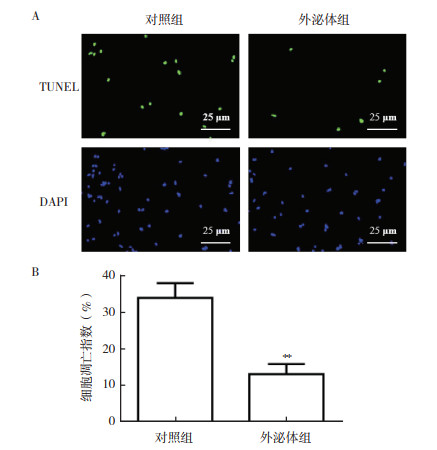
TUNEL染色检测胃癌细胞株SGC-7091凋亡情况显示,与对照组比较,外泌体组细胞凋亡降低(P < 0.01,图 3)。
|
| 注 A:TUNEL染色检测结果; B:细胞凋亡统计图; **与对照组比较,P < 0.01 图 3 TUNEL染色检测外泌体组和对照组SGC-7091细胞凋亡情况 Fig.3 TUNEL staining to detect the apoptosis of SGC-7091 cells in the exosome group and control group |
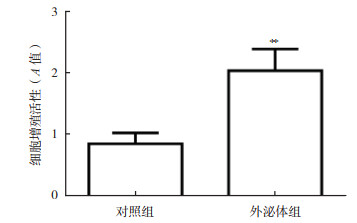
MTT染色检测SGC-7091细胞增殖情况显示,与对照组比较,外泌体组细胞增殖活性升高(P < 0.01,图 4)。
|
| 注 **与对照组比较,P < 0.01 图 4 MTT检测示外泌体组细胞增殖活性升高 Fig.4 MTT assay showed increased cell proliferation activity in the exosome group |
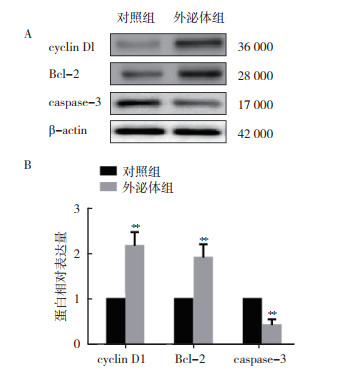
Western blot检测增殖蛋白cyclin D1以及凋亡蛋白caspase-3和Bcl-2的表达显示,与对照组比较,外泌体组cyclin D1和Bcl-2表达增加(均P < 0.01),caspase-3表达降低(P < 0.01,图 5)。
|
| 注 A:Western blot检测cyclin D1、Bcl-2和caspase-3表达; B:相关蛋白表达统计图; **与对照组比较,P < 0.01 图 5 外泌体处理对细胞凋亡和增殖相关蛋白表达影响 Fig.5 Effects of exosome treatment on the expression of apoptosis and proliferation-related proteins |
胃癌是全球肿瘤患者死亡的第二大因素。幽门螺杆菌、慢性胃炎、环境因素以及遗传因素等是造成胃癌的主要原因[9]。近年来研究发现,胃癌患者血液中外泌体相对健康人高出近1倍,其中不同肿瘤组织和细胞来源外泌体中所包含的生物活性物质如mRNA、蛋白质和miRNA等可以递送至特异性细胞,进而抑制肿瘤细胞的增殖和迁移[10]。其中外泌体源性miRNA具有较好的稳定性,可能成为一种新的肿瘤标志物[11]。因此,外泌体源性miRNA有望成为胃癌早期诊断的检测靶标,为胃癌患者开拓新的治疗策略。
miRNA是一类内源性的小分子RNA,不具有蛋白质编码功能。miRNA可以通过靶向目标蛋白,抑制其翻译,从而降低靶基因的表达水平,进而参与相关基因表达。既往研究发现,miR-21是与胃癌发生和发展密切相关的miRNA。进一步体外培养胃癌细胞株,通过抑制miR-21可以促进细胞凋亡,抑制细胞增殖[12]。胃癌细胞株MGC-803细胞中,miR-21表达上调。姜黄素可以通过miR-21/PTEN/Akt信号通路抑制肿瘤细胞增殖,促进细胞凋亡[13]。miR-21在胃癌的发生和发展中发挥重要作用。外泌体具有体积小和分布均匀等特点,适合作为纳米级别药物载体,在胃癌的治疗中发挥重要的作用。转染miR-21抑制剂可以抑制巨噬细胞外泌体对胃癌细胞BGC-823的作用,促进细胞凋亡,抑制细胞迁移[14-15]。但是目前有关肿瘤自身外泌体源性miR-21与肿瘤的增殖和凋亡的关系尚不完全明确。本实验前期通过提取胃癌细胞株SGC-9071外泌体,探究其内含物质miR-21对自身细胞功能的影响。结果发现,外泌体直径大小为40~100 nm,高表达TSG101和CD63,是一种双层膜状囊泡。在成功提取肿瘤细胞外泌体并将其与胃癌SGC-9071细胞共培养后,本研究组通过RT-PCR检测发现,与对照组比较,外泌体组细胞miR-21表达上升,提示肿瘤外泌体可能通过递送miR-21影响细胞相关生物学功能。为了进一步明确外泌体miR-21对胃癌细胞的影响,本研究通过TUNEL染色发现,外泌体与肿瘤细胞共培养可以降低细胞凋亡率,同时Western blot检测也发现,caspase-3表达降低,Bcl-2和cyclin D1表达上升,提示外泌体miR-21可能通过作用细胞凋亡和增殖影响胃癌的发生和发展。
综上所述,本研究通过探究肿瘤外泌体源性miR-21与肿瘤细胞凋亡和增殖的关系发现,肿瘤细胞外泌体源性miR-21可能通过抑制细胞凋亡和促进细胞增殖加快胃癌的进程。
| [1] |
柏玉蓉, 陆一丹, 孙杨承, 等. 预防性腹腔热灌注化疗治疗进展期胃癌临床疗效的meta分析[J]. 实用肿瘤杂志, 2021, 36(4): 306-313. |
| [2] |
Siegel RL, Miller KD, Jemal A. Cancer statistics[J]. CA Cancer J Clin, 2016, 66(1): 7-30. DOI:10.3322/caac.21332 |
| [3] |
左婷婷, 郑荣寿, 曾红梅, 等. 中国胃癌流行病学现状[J]. 中国肿瘤临床, 2017, 44(1): 52-58. |
| [4] |
张东焕, 张素云, 杨升. 外泌体在胃肠道肿瘤诊治中的应用[J]. 实用肿瘤杂志, 2021, 36(4): 300-305. |
| [5] |
Zhang L, Yu D. Exosomes in cancer development, metastasis, and immunity[J]. Biochim Biophys Acta Rev Cancer, 2019, 1871(2): 455-468. DOI:10.1016/j.bbcan.2019.04.004 |
| [6] |
Chen X, Zhang S, Du K, et al. Gastric cancer-secreted exosomal X26nt increases angiogenesis and vascular permeability by targeting VE-cadherin[J]. Cancer Sci, 2021, 112(5): 1839-1852. DOI:10.1111/cas.14740 |
| [7] |
Zhu L, Sun HT, Wang S, et al. Isolation and characterization of exosomes for cancer research[J]. J Hematol Oncol, 2020, 13(1): 152. |
| [8] |
林锋, 王海娟, 李春晓, 等. 食管癌细胞来源的外泌体对肿瘤细胞迁移及侵袭能力的影响及机制研究[J]. 解放军医学杂志, 2017, 42(4): 307-313. |
| [9] |
Matsuzaki J, Tsugawa H, Suzuki H. Precision medicine approaches to prevent gastric cancer[J]. Gut Liver, 2021, 15(1): 3-12. DOI:10.5009/gnl19257 |
| [10] |
Hoshino A, Costa-Silva B, Shen TL, et al. Tumour exosome integrins determine organotropic metastasis[J]. Nature, 2015, 527(7578): 329-335. DOI:10.1038/nature15756 |
| [11] |
宋健, 杨松林, 李琳, 等. 外泌体对胃癌转移的作用及其在诊断中的应用研究进展[J]. 中国肿瘤临床, 2018, 45(22): 1164-1168. DOI:10.3969/j.issn.1000-8179.2018.22.953 |
| [12] |
Gu Y, Fei Z, Zhu R. miR-21 modulates cisplatin resistance of gastric cancer cells by inhibiting autophagy via the PI3K/Akt/mTOR pathway[J]. Anticancer Drugs, 2020, 31(4): 385-393. |
| [13] |
陈泽慧, 安静, 魏玥, 等. 消痞颗粒对胃癌前病变模型大鼠胃黏膜组织miR-21-PTEN-PI3K/AKT信号通路的影响[J]. 中医杂志, 2020, 61(18): 1628-1632. |
| [14] |
Wang JJ, Wang ZY, Chen R, et al. Macrophage-secreted exosomes delivering miRNA-21 inhibitor can regulate BGC-823 cell proliferation[J]. Asian Pac J Cancer Prev, 2015, 16(10): 4203-4209. |
| [15] |
Li L, Wang X, Li W, et al. miR-21 modulates prostaglandin signaling and promotes gastric tumorigenesis by targeting 15-PGDH[J]. Biochem Biophys Res Commun, 2018, 495(1): 928-934. |
 2022, Vol. 37
2022, Vol. 37


