文章信息
- 刘首鹏, 赖佳路, 周阳, 刘登洪, 姜筱璇, 钟仁明
- Liu Shoupeng, Lai Jialu, Zhou Yang, Liu Denghong, Jiang Xiaoxuan, Zhong Renming
- 单双部分弧有无均整器模式VMAT与IMRT在食管癌放疗中的剂量学比较
- A dosimetric study of single-arc and double partial-arc VMAT with and without flattening filter and IMRT for esophageal cancer
- 实用肿瘤杂志, 2022, 37(5): 450-456
- Journal of Practical Oncology, 2022, 37(5): 450-456
基金项目
- 四川省科技厅项目(2021JDKP0070);四川大学华西医院学科卓越发展1·3·5工程临床研究孵化项目(2021HXFH029)
-
通信作者
- 钟仁明, E-mail: zrm_100@163.com
-
文章历史
- 收稿日期:2021-08-27
食管癌是我国常见的胸部肿瘤之一,放疗在食管癌治疗中扮演着重要角色。随着放疗技术的发展,调强技术已经广泛应用于食管癌放疗。调强分为静态调强放疗(intensity modulated radiotherapy,IMRT)和容积旋转调强放疗(volumetric modulated arc therapy,VMAT)。国内外多数食管癌在均整模式(flattening filter,FF)下使用多野IMRT或双弧VMAT进行治疗[1-3]。该模式下最高剂量率为600机器跳数(monitor unit,MU)/min。根据报道,治疗时间的长短与分次内误差相关,且食管在放疗过程中会发生移动[4-5]。因此,在影像引导放疗技术下,进一步缩短放疗的时间具有减少分次内误差及提高临床效率的价值。
目前部分直线加速器配备无均整器(flattening filter free,FFF)出束方式,6 MV和10 MV光子在FFF模式下最高剂量率分别可达1 400 MU/min和2 200 MU/min,能减少治疗时间。本研究拟比较FFF模式双弧间断出束VMAT技术(VMAT-3F2A)、FF模式双弧间断出束VMAT技术(VMAT-2F2A)、FFF模式单弧间断出束VMAT技术(VMAT-3F1A)和FFF模式IMRT技术(IMRT-3F)在食管癌放疗剂量学和治疗效率方面的差异,为临床食管癌放疗调强技术的选择提供参考依据。
1 资料与方法 1.1 一般资料选择2020年5月至9月在四川大学华西医院放疗科行食管癌放疗的患者15例。所有病例均经细胞病理学或免疫组织化学证实为鳞癌,无肿瘤放疗相关禁忌证。9例患者靶区范围包含上段食管,其余6例为中下段;病理类型均为鳞癌;计划靶区体积(planning target volume,PTV)范围211.49~658.50 cm3,平均体积为442.48 cm3;男性15例,女性0例;年龄52~75岁,平均年龄65.6岁;TNM分期范围: T1-3,N0-3,M0。为每例患者分别设计VMAT-3F2A、VMAT-2F2A、VMAT-3F1A和IMRT-3F这4种计划,其中IMRT-3F为临床治疗实施计划。比较4种计划类型的剂量学差异。本研究经本院生物医学伦理审查委员会审批通过。
1.2 CT模拟定位及靶区勾画 1.2.1 CT模拟定位患者仰卧平躺于碳纤维固定床板上,双手交叉举过头顶置于抓手杆,将定位热塑膜(四川瑞迪医疗科技有限公司)置于恒温水箱,温度设置为70℃,待热塑膜软化,去除多余水分,根据患者体表轮廓塑形,15 min后待热塑膜完全冷却定型。再应用高压注射器注射80~100 mL碘海醇造影剂,开始螺旋CT扫描。CT扫描参数:管电压120 kV,管电流375 mA,扫描层厚5 mm,扫描范围自颅底至第二腰椎下缘。扫描的图像均通过DICOM网络传至计划系统进行靶区和危及器官(organs at risk,OARs)的勾画。
1.2.2 靶区勾画肿瘤靶区勾画由放疗主管医师根据CT采集图像,参考ICRU第62号报告[6],在计划系统上勾画大体肿瘤体积(gross tumor volume,GTV)、临床靶区体积(clinical target volume,CTV)、PTV和OARs。OARs包括双侧肺(lungs)、食管(esophagus)、心脏(heart)和脊髓(spinal cord)等。GTV参考X线钡餐、胃镜、CT和PET/CT等影像勾画肿瘤区和阳性淋巴结。CTV为GTV前后左右外扩5 mm、上下方向外扩30 mm。PTV为CTV在上下方向外扩10 mm,前后左右方向外扩5 mm生成;PTV处方剂量均为50.4 Gy,分次为28次。
1.3 计划设计该15例患者均在RayStation(v4.7.5.4)计划系统进行计划设计,每例设计VMAT-3F2A、VMAT-2F2A、VMAT-3F1A和IMRT-3F这4个计划,其中IMRT-3F为临床治疗计划。采用3 mm×3 mm×3 mm的计算网格,采用三维共面调强技术照射。3个VMAT计划机架旋转范围均为181°~225°、315°~45°和135°~179°。VMAT-3F2A计划采用FFF模式,顺时针和逆时针双弧照射,每4°为1个控制点;VMAT-2F2A计划采用FF模式,顺时针和逆时针双弧照射,每4°为1个控制点;VMAT-3F1A计划采用FFF模式,顺时针单弧照射,每2°为1个控制点。IMRT-3F计划射野个数5~7,中下段食管癌采用5野,射野角度分别为210°、330°、0°、40°和140°;上段食管癌7野射野角度分别为210°、280°、330°、0°、40°、80°和140°,其中80°和280°射野采用铅门固定技术,照射范围仅为锁骨以上靶区;采用FFF模式,子野最小跳数设为4 MU,最小子野面积设为4 cm2,最大子野个数设为50。同1例患者4个计划采用相同的目标优化函数,为方便各个计划间的比较,所有计划均归一至处方剂量覆盖95%的靶区体积。加速器选用医科达Versa HD(Elekta linear accelerator,瑞典),射线为6 MV X线,剂量率采用FF模式或FFF模式,配置Agility型80对多叶准直器(multi-leaf collimator,MLC)。MLC在等中心处宽度为5 mm,MLC叶片最大运动速度65 mm/s;最大照射野为40 cm×40 cm。靶区优化设计目标:≥95%的靶区体积接受100%的处方剂量,107%的处方剂量覆盖的体积 < 1%,PTV最大剂量 < 110%的处方剂量。OARs剂量限值具体约束条件分别为:脊髓剂量最大值(maximum dose,Dmax) < 45 Gy;双肺V5 < 60%、V20 < 30%、V30 < 20%,双肺平均剂量(mean dose,Dmean) < 15 Gy;心脏V30 < 40%、V40 < 30%;并且在此基础之上再尽可能降低OARs和正常组织的受量。Dmax的含义是靶区或OARs所接受的最大照射剂量。Vx的含义是接受超过x Gy剂量照射的体积占OARs总体积的百分比。
1.4 计划评估 1.4.1 靶区的评估参数根据计划的剂量体积直方图(dose volume histogram,DVH)来评价靶区的剂量学参数,包括均匀性指数(heterogeneity index,HI)、适形性指数(conformity index,CI)、最大值Dmax和PTV体积(VPTV)。
HI计算公式为HI=(D2-D98)/D50,Dx代表x%的靶区体积所受到的剂量。HI取值范围为0~1,越接近0,说明PTV的剂量分布越均匀。CI计算公式为CI=V50.4 Gy/VPTV,V50.4 Gy的含义是50.4 Gy的处方等剂量线包绕的体积;CI取值范围为0~1,越接近1,说明靶区与处方等剂量曲线越适形。
1.4.2 OARs的评估参数食管肿瘤放疗计划主要评估的OARs包括双侧肺、食管、心脏和脊髓等。肺的评估指标为V5、V20、V30和Dmean。心脏的评估指标为V30、V40和Dmean。脊髓的评估指标为Dmax。
1.4.3 治疗效率治疗效率的评价包括计划总MU和治疗实施时间,其中治疗实施时间为计划质量保证(quality assurance,QA)时执行时间,指开始出束至结束的时间,不包括摆位和图像引导的时间。
1.5 统计学分析采用SPSS 20.0软件对剂量学参数进行统计学分析。计量资料先行单样本Shapiro-Wilk正态性检验。若符合正态分布则计量资料以均数±标准差(x±s)表示,并对符合正态分布的资料行配对样本t检验;若不符合正态分布则计量资料采用中位数(四分位间距)[M(Q1~Q3)]方式表示,并采用配对Wilcoxon秩和检验对数据进行分析。P < 0.05为差异具有统计学意义。
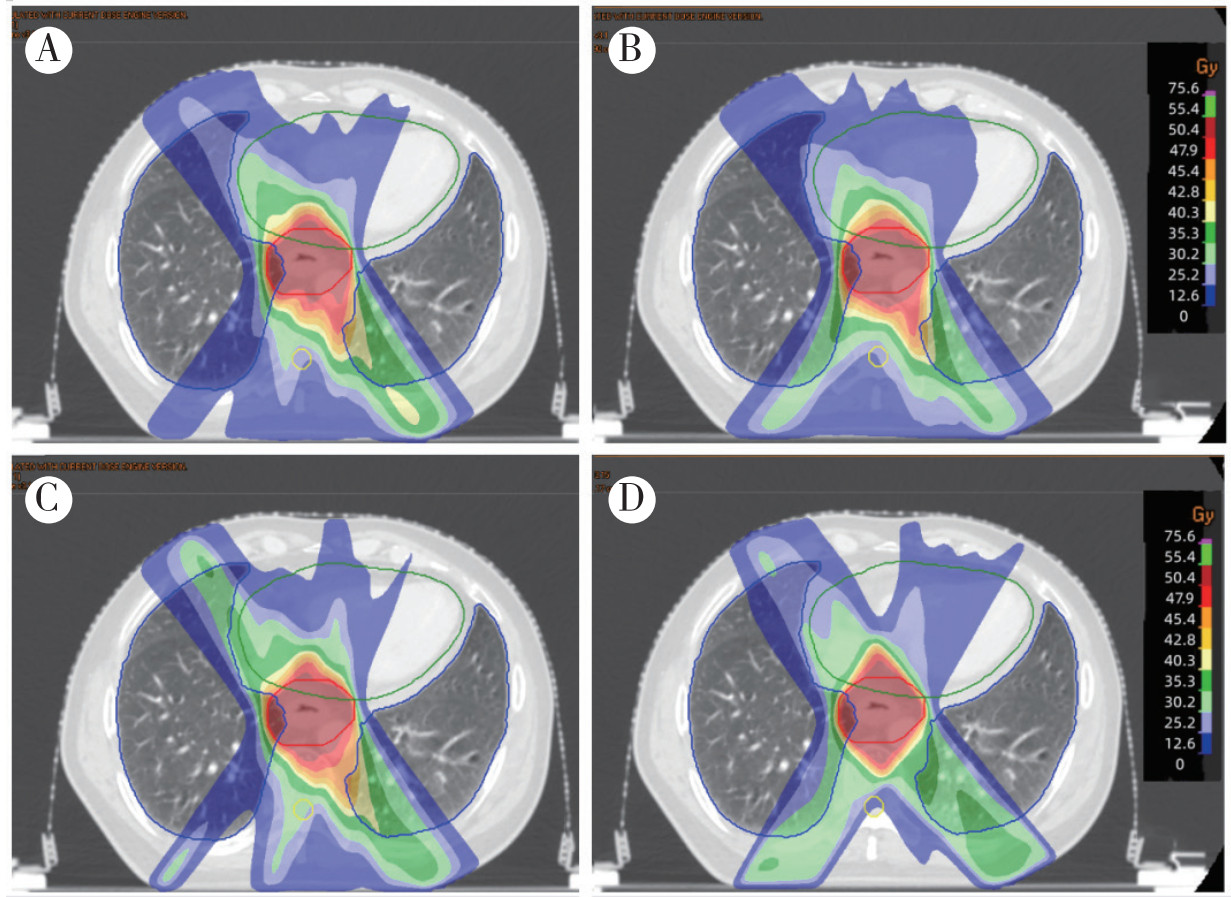
2 结果 2.1 靶区剂量分布比较15例患者4个计划的靶区剂量均能满足临床要求。在靶区覆盖率相同的前提下,VMAT-3F1A计划的CI值低于VMAT-3F2A和VMAT-2F2A计划(均P < 0.01,表 1),HI值和Dmax值均高于VMAT-3F2A和VMAT-2F2A计划(均P < 0.01)。同1例食管癌患者4种放疗计划的横断面剂量分布比较图例见图 1。
| 项目 | VMAT-3F2A | VMAT-2F2A | VMAT-3F1A | IMRT-3F | P值a | P值b | P值c | P值d | P值e | P值f |
| PTV | ||||||||||
| CI | 0.79±0.05 | 0.79±0.05 | 0.76±0.05 | 0.77±0.05 | 0.840 | 0.002 | 0.087 | 0.010 | 0.108 | 0.531 |
| HI | 0.09±0.02 | 0.09±0.02 | 0.10±0.02 | 0.10±0.02 | 0.161 | < 0.01 | 0.014 | 0.004 | 0.085 | 0.133 |
| Dmax(Gy) | 54.23.±0.99 | 54.37±1.08 | 55.11±1.14 | 54.71±1.23 | 0.334 | < 0.01 | 0.020 | 0.010 | 0.171 | 0.085 |
| 双肺 | ||||||||||
| V5(%) | 45.54±9.99 | 47.07±10.41 | 45.96±10.29 | 45.08±10.35 | < 0.01 | 0.034 | 0.494 | < 0.01 | 0.010 | 0.153 |
| V20(%) | 20.90±4.60 | 21.23±4.44 | 21.48±4.78 | 22.03±4.93 | 0.023 | 0.006 | 0.001 | 0.319 | 0.024 | 0.005 |
| V30(%) | 10.20±3.98 | 10.28±3.93 | 10.40±3.97 | 10.38±4.08 | 0.600 | 0.216 | 0.617 | 0.272 | 0.750 | 0.940 |
| Dmean(Gy) | 10.51±2.27 | 10.71±2.29 | 10.64.±2.32 | 10.52±2.40 | < 0.01 | 0.001 | 0.793 | 0.078 | 0.053 | 0.059 |
| 脊髓 | ||||||||||
| Dmax(Gy) | 42.47±2.64 | 42.52±2.88 | 43.40±2.62 | 43.08±2.69 | 0.665 | < 0.01 | 0.042 | 0.005 | 0.108 | 0.315 |
| 心脏 | ||||||||||
| V30(%) | 23.88±12.99 | 24.33±13.47 | 24.97±13.76 | 25.03±14.30 | 0.139 | 0.090 | 0.087 | 0.148 | 0.170 | 0.908 |
| V40(%) | 12.60±7.37 | 12.63±7.58 | 13.03±7.62 | 13.11±8.03 | 0.845 | 0.100 | 0.309 | 0.168 | 0.331 | 0.867 |
| Dmean(Gy) | 18.02±9.63 | 18.28±9.67 | 18.35±9.84 | 18.24.±10.08 | < 0.01 | 0.010 | 0.367 | 0.505 | 0.863 | 0.612 |
| MU | 557.50±82.01 | 451.69±55.47 | 494.60±63.42 | 958.96±229.75 | < 0.01 | 0.001 | < 0.01 | 0.010 | < 0.01 | < 0.01 |
| 治疗时间(s) | 241.0±6.30 | 244.3±8.00 | 124.4±6.79 | 425.4±21.48 | 0.192 | < 0.01 | < 0.01 | < 0.01 | < 0.01 | < 0.01 |
| 注 aVMAT-3F2A与VMAT-2F2A比较;bVMAT-3F2A与VMAT-3F1A比较;cVMAT-3F2A与IMRT-3F比较;dVMAT-2F2A与VMAT-3F1A比较;eVMAT-2F2A与IMRT-3F比较;fVMAT-3F1A与IMRT-3F比较;VMAT:容积旋转调强放疗(volume modulated arc therapy);IMRT:静态调强放疗(intensity modulated radiation therapy);PTV:计划靶区体积(planning target volume);CI:适形性指数(conformity index);HI:均匀性指数(heterogeneity index);Dmax:剂量最大值(maximum dose);Dmean:平均剂量(mean dose);MU:机器跳数(monitor unit) | ||||||||||
|
| 注 A:VMAT-3F2A计划;B:VMAT-2F2A计划;C:VMAT-3F1A计划;D:IMRT-3F计划;VMAT:容积旋转调强放疗(volume modulated arc therapy);IMRT:静态调强放疗(intensity modulated radiation therapy) 图 1 1例食管癌下段患者VMAT-3F2A、VMAT-2F2A、VMAT-3F1A和IMRT-3F放疗计划的横断面剂量分布比较 Fig.1 Comparison of transverse-section dose distribution of VMAT-3F2A、VMAT-2F2A、VMAT-3F1A and IMRT-3F radiotherapy plans in a patient with lower esophageal cancer |
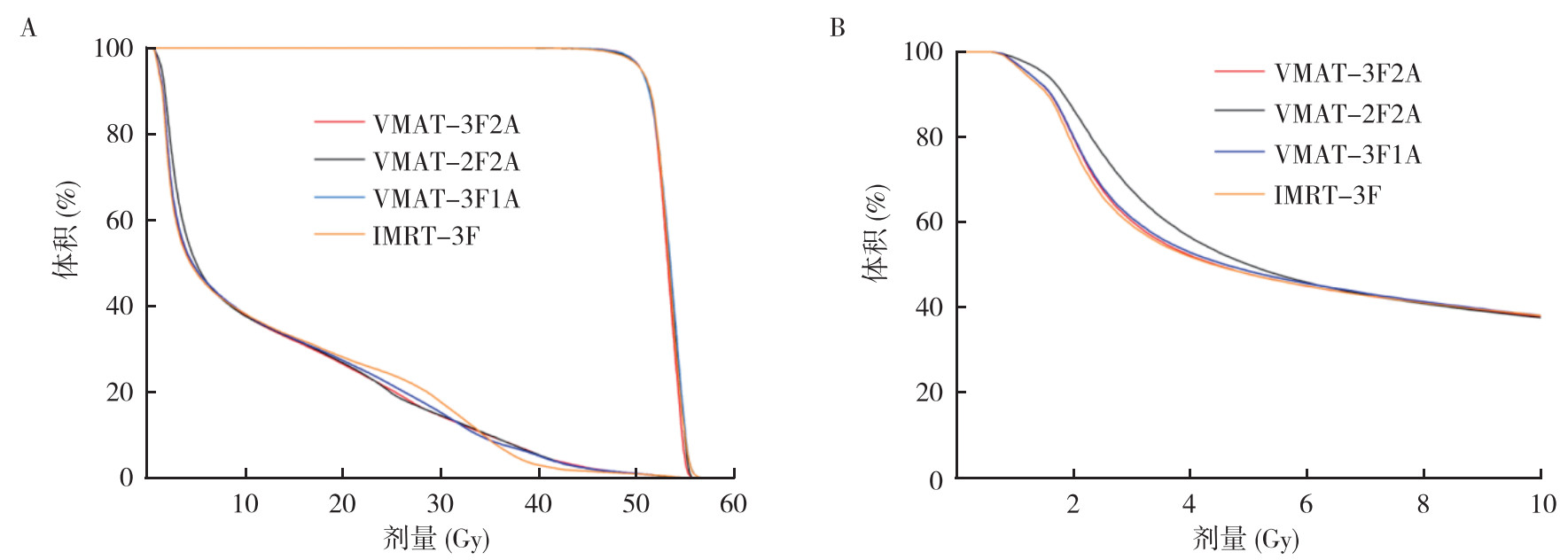
15例患者的靶区和双肺受照剂量的结果在DVH图上均呈现出良好的一致性。在高剂量区(V20和V30),IMRT-3F计划双肺的高剂量区高于其他3个计划(均P < 0.05),VMAT-3F2A与VMAT-2F2A曲线基本重合(P=0.600),VMAT-3F1A计划稍高于VMAT-3F2A与VMAT-2F2A计划(P=0.006,P=0.319;图 2A)。在低剂量区(≤V5)IMRT-3F与VMAT-3F2A及VMAT-3F1A计划均基本重合(均P > 0.05),VMAT-3F2A计划稍低于VMAT-3F1A计划(P=0.034),VMAT-2F2A计划双肺的低剂量区高于其他3个计划(均P < 0.05,图 2B)。
|
| 注 A:未缩放比例图;B:双肺低剂量区域放大图;VMAT:容积旋转调强放疗(volume modulated arc therapy);IMRT:静态调强放疗(intensity modulated radiation therapy) 图 2 1例食管癌患者VMAT-3F2A、VMAT-2F2A、VMAT-3F1A和IMRT-3F放疗计划的靶区和双肺受量DVH比较 Fig.2 Comparison of DVH of the target volumn and bilateral lung dosages of VMAT-3F2A、VMAT-2F2A、VMAT-3F1A and IMRT-3F radiotherapy plans in patient with esophageal cancer |
IMRT-3F与VMAT-3F2A和VMAT-3F1A计划在双肺V5方面比较,差异均无统计学意义(均P > 0.05,表 1)。VMAT-2F2A计划双肺V5均高于其他3个计划(均P < 0.05)。IMRT-3F计划双肺V20均高于其他3个计划(均P < 0.05)。VMAT-3F2A计划双肺V20均低于其他3个计划(均P < 0.05)。
2.2.2 脊髓和心脏受量比较与VMAT-3F1A和IMRT-3F计划比较,VMAT-3F2A计划的脊髓Dmax分别降低0.93 Gy和0.62 Gy(均P < 0.01,表 1)。VMAT-2F2A计划的脊髓Dmax与VMAT-3F1A计划比较,降低0.87 Gy(P=0.005),其他计划间脊髓Dmax比较,差别均无统计学意义(均P > 0.05)。
4个计划间在心脏V30和V40方面比较,差异均无统计学意义(均P > 0.05)。在心脏Dmean方面比较,VMAT-3F2A计划较VMAT-2F2A和VMAT-3F1A计划分别降低0.26 Gy和0.33.Gy(均P < 0.05);其他计划间比较,差异均无统计学意义(均P > 0.05)。
2.3 MU和治疗时间比较IMRT-3F、VMAT-3F2A、VMAT-3F1A和VMAT-2F2A4计划在MU方面依次递减,两两间比较,差异均具有统计学意义(均P < 0.05,表 1)。VMAT-2F2A、VMAT-3F2A和VMAT-3F1A与IMRT-3F计划比较,MU分别减少52.90%、41.86%和48.42%。
VMAT-3F2A与VMAT-2F2A计划治疗时间比较,差异无统计学意义(P=0.192,表 1)。IMRT-3F计划治疗时间最长,与VMAT-3F2A、VMAT-2F2A和VMAT-3F1A计划比较,治疗时间分别增加76.35%、74.13%和241.96%(均P < 0.01)。VMAT-3F1A计划治疗时间最短,与VMAT-3F2A、VMAT-2F2A和IMRT-3F计划比较,治疗时间分别减少48.38%、49.08%和70.76%(均P < 0.01)。
3 讨论虽然与三维适形放射治疗(3 dimensional conformal radiotherapy,3DCRT)比较,IMRT具有更好的靶区适形性,能更好地保护OARs[7],但与VMAT比较,具有治疗实施时间长、MU高和导致第二原发肿瘤概率高等缺点。VMAT能在保证相同计划质量前提下,具有“快、准、优”的特点[8];与IMRT比较,VMAT导致更多的组织受到低剂量的照射[9-10]。临床上预测放射性肺损伤发生率最常用的剂量学参数包括V5、V20、V30和Dmean,其中最相关的参数是肺V5体积[11-12],这也是国内在胸部肿瘤放疗中很慎重考虑使用全弧VMAT技术的原因之一。王清鑫等[2]采用弧内间断出束容积旋转调强(finite discontinuous-volume modulated arc therapy,FD-VMAT)疗法用于胸中下段食管癌,发现此技术不但具有VMAT保护肺V20和V30的优点,还同时具有IMRT保护肺V2和V5的优点。与本研究结果一致。
本研究发现,VMAT-3F2A、VMAT-2F2A、VMAT-3F1A和IMRT-3F计划均能满足临床要求,虽然VMAT-3F1A计划的靶区参数(CI、HI和Dmax值)略差于VMAT-3F2A和VMAT-2F2A计划,但与临床治疗计划IMRT-3F无差异。VMAT-3F2A计划靶区的HI和Dmax值好于临床治疗计划IMRT-3F。在肺保护方面,在低剂量区,VMAT-2F2A计划双肺的V5高于其他3个计划;在高剂量区,IMRT-3F计划双肺的V20值高于其他3个计划;VMAT-3F2A计划双肺的V20值低于其他3个计划;VMAT-3F2A计划比VMAT-2F2A和VMAT-3F1A计划双肺的Dmean分别低0.20 Gy和0.14 Gy。在脊髓保护方面,VMAT-3F2A计划优于VMAT-3F1A和IMRT-3F计划;在心脏保护方面,VMAT-3F2A计划与VMAT-2F2A和VMAT-3F1A比较,心脏的Dmean分别降低0.26 Gy和0.33 Gy。
综上所述,4个计划综合评价发现,VMAT-3F2A计划无论是靶区还是OARs的参数都优于其他3个计划,可能有以下3个方面的原因:(1)与VMAT-2F2A计划比较,VMAT-3F2A计划选用FFF模式减少机头的散射线和电子污染,有利于对肺低剂量区和心脏的保护[13];(2)与VMAT-3F1A比较,选用双弧照射增加计划的自由度,使得计划质量更高[14];(3)与IMRT-3F比较,可能是因为治疗技术的差异,采用VMAT技术具有更多可选择的射线入射角度,计划的可调制度增加[15]。
VMAT-3F2A计划与VMAT-2F2A计划比较,在保证靶区剂量覆盖的情况下,能降低OARs的受量,虽然会导致MU增加23.45%,但两者治疗时间并无差异。相关研究也发现,FFF模式与FF模式比较,具有降低OARs的受量、剂量计算更准确以及电子和中子污染降低等优点[16-17]。但Sun等[13]研究发现,虽然FFF计划的MU数量较FF计划增加21.83%,但FFF计划的治疗时间减少11.90%。此结果与本研究有差异,分析原因可能是本研究采用的分段弧VMAT治疗技术,而Sun等[13]采用完整的360°旋转弧,使FFF模式在较短的旋转出束范围体现出的优势不明显。
VMAT-3F1A计划与IMRT-3F比较,在靶区剂量学参数无差别的前提下,VMAT-3F1A计划不但具有IMRT-3F保护肺低剂量区的优点,同时还能降低肺高剂量区的受量,分析原因可能也是因为治疗技术的差异,采用VMAT技术具有更多的射线入射角度选择,计划的可调制度增加[15]。此外与IMRT-3F比较,MU减少48.42%,治疗时间减少70.76%,故在临床中配置FFF模式的加速器可考虑使用VMAT-3F1A计划,能进一步提高临床实际治疗效率,缓解医疗资源紧张的状态。
在治疗效率上,IMRT-3F计划机器总MU和治疗时间高于其他3个计划;随着机器总MU的增加,患者发生第二原发肿瘤的概率会增加[18];同时随着治疗时间的延长,患者的劳损和分次内的运动也会增加[19-20],“三精”放疗之一的精确实施将很难得到保证。VMAT-3F2A和VMAT-3F1A计划MU分别高于VMAT-2F2A计划23.45%和9.52%,分析其原因,可能是因为采用了FFF模式,其剂量分布在射野边缘极不均匀,为了实现靶区内的均匀照射,无疑将会增加许多小野补偿,导致MU增加。相关研究也发现,采用FFF模式的VMAT计划MU比采用FF模式的VMAT计划高20%[15]。
此外,本研究也设计了采用FFF模式、顺时针单弧照射、每4°为1个控制点的计划和采用FF模式、顺时针单弧照射、每2°为1个控制点的计划;都因靶区参数不能满足临床研究,所以并未纳入研究比较。分析其原因可能是受机架的转速和MLC的运动速度等机械因素的限制。
本研究不足之处是:由于RayStation计划系统不支持跳弧的功能,每1段小弧治疗完成后,都需要治疗师手动切换到下1个弧,造成机架旋转的终止,然后再启动,这将增加治疗时间;如果合并后将在弧间不出束的范围机架以最大旋转速度转动,将会减少治疗实施时间。经测试每2个弧之间切换时间为12 s左右(6段小弧之间需要切换5次,3段小弧之间需要切换2次),如果部分弧VMAT计划合并成1个整弧,治疗时间将会进一步减少0.5~1.0 min。Eclipse计划系统具有规避扇区功能,可以定义在整个旋转治疗中,不出束的具体机架范围;或者也可以像王清鑫等[2]一样通过Matlab软件编写程序将3个间断弧控制点的信息合并成1个完整弧。
综上所述,VMAT-3F1A与临床治疗计划IMRT-3F比较能减少肺低剂量受照体积(V5)及肺高剂量受照体积(V20),且具有更高的治疗效率。VMAT-3F2A计划与其他3个计划比较,能进一步降低双肺、脊髓和心脏的受照射量。
| [1] |
张斯渊, 董信春, 韩松辰, 等. 精准医疗: 中晚期食管癌放疗技术进展浅谈[J]. 实用肿瘤杂志, 2021, 36(4): 368-374. DOI:10.13267/j.cnki.syzlzz.2021.076 |
| [2] |
王清鑫, 江波, 孙佳娜, 等. 胸中下段食管癌弧内间断出束VMAT计划研究[J]. 中华放射肿瘤学杂志, 2016, 25(11): 1238-1243. DOI:10.3760/cma.j.issn.1004-4221.2016.11.020 |
| [3] |
牟艳红, 刘强, 方志祥, 等. 胸中段食管癌调强放疗的临床疗效分析[J]. 实用肿瘤杂志, 2020, 35(5): 450-453. DOI:10.13267/j.cnki.syzlzz.2020.05.013 |
| [4] |
Hadj Henni A, Gensanne D, Roge M, et al. Evaluation of inter- and intra-fraction 6D motion for stereotactic body radiation therapy of spinal metastases: influence of treatment time[J]. Radiat Oncol, 2021, 16(1): 168. DOI:10.1186/s13014-021-01892-5 |
| [5] |
Jin P, Hulshof MC, de Jong R, et al. Quantification of respiration-induced esophageal tumor motion using fiducial markers and four-dimensional computed tomography[J]. Radiother Oncol, 2016, 118(3): 492-497. DOI:10.1016/j.radonc.2016.01.005 |
| [6] |
Stroom J, Heijmen B. Geometrical uncertainties, radiotherapy planning margins, and the ICRU-62 report[J]. Radiother Oncol, 2002, 64(1): 75. DOI:10.1016/S0167-8140(02)00140-8 |
| [7] |
Sauter M, Lombriser N, Bütikofer S, et al. Improved treatment outcome and lower skin toxicity with intensity-modulated radiotherapy vs. 3D conventional radiotherapy in anal cancer[J]. Strahlenther Onkol, 2020, 196(4): 356-367. DOI:10.1007/s00066-019-01534-6 |
| [8] |
胡彩容, 阴晓娟, 张秀春, 等. 不同调强方式在胸中上段食管癌放疗中的剂量学研究[J]. 中华放射医学与防护杂志, 2014, 34(3): 220-224. DOI:10.3760/cma.j.issn.0254-5098.2014.03.016 |
| [9] |
Paudel NR, Narayanasamy G, Han EY, et al. Dosimetric and radiobiological comparison for quality assurance of IMRT and VMAT plans[J]. J Appl Clin Med Phys, 2017, 18(5): 237-244. DOI:10.1002/acm2.12145 |
| [10] |
Radhakrishnan S, Chandrasekaran A, Sarma Y, et al. Dosimetric comparison between single and dual arc-volumetric modulated arc radiotherapy and intensity modulated radiotherapy for nasopharyngeal carcinoma using a simultaneous integrated boost technique[J]. Asian Pac J Cancer Prev, 2017, 18(5): 1395-1402. |
| [11] |
Tomohiro I, Shinji S, Ryuji M, et al. Evaluation of the relationship between the range of radiation-induced lung injury on CT images after IMRT for stage Ⅰ lung cancer and dosimetric parameters[J]. Ann Med, 2021, 53(1): 267-273. DOI:10.1080/07853890.2020.1869297 |
| [12] |
Szejniuk WM, Nielsen MS, Takács-Szabó Z, et al. High-dose thoracic radiation therapy for non-small cell lung cancer: a novel grading scale of radiation-induced lung injury for symptomatic radiation pneumonitis[J]. Radiat Oncol, 2021, 16(1): 131. DOI:10.1186/s13014-021-01857-8 |
| [13] |
Sun WZ, Chen L, Yang X, et al. Comparison of treatment plan quality of VMAT for esophageal carcinoma with: flattening filter beam versus flattening filter free beam[J]. J Cancer, 2018, 9(18): 3263-3268. DOI:10.7150/jca.26044 |
| [14] |
Vivekanandan N, Sriram P, Kumar SA, et al. Volumetric modulated arc radiotherapy for esophageal cancer[J]. Med Dosim, 2012, 37(1): 108-113. DOI:10.1016/j.meddos.2011.01.008 |
| [15] |
Nicolini G, Ghosh-Laskar S, Shrivastava SK, et al. Volumetric modulation arc radiotherapy with flattening filter-free beams compared with static gantry IMRT and 3D conformal radiotherapy for advanced esophageal cancer: a feasibility study[J]. Int J Radiat Oncol Biol Phys, 2012, 84(2): 553-560. DOI:10.1016/j.ijrobp.2011.12.041 |
| [16] |
Hrbacek J, Lang S, Graydon SN, et al. Dosimetric comparison of flattened and unflattened beams for stereotactic ablative radiotherapy of stage Ⅰ non-small cell lung cancer[J]. Med Phys, 2014, 41(3): 031709. DOI:10.1118/1.4866231 |
| [17] |
Meshram MN, Pramanik S, Ranjith CP, et al. Dosimetric properties of equivalent-quality flattening filter-free (FFF) and flattened photon beams of Versa HD linear accelerator[J]. J Appl Clin Med Phys, 2016, 17(3): 358-370. DOI:10.1120/jacmp.v17i3.6173 |
| [18] |
罗云秀, 林少民. 放疗诱发第二原发肿瘤[J]. 中华放射医学与防护杂志, 2021, 41(7): 552-556. DOI:10.3760/cma.j.issn.0254-5098.2021.07.015 |
| [19] |
Hoekstra N, Habraken S, Swaak-Kragten A, et al. Intrafraction motion during partial breast irradiation depends on treatment time[J]. Radiother Oncol, 2021, 159: 176-182. DOI:10.1016/j.radonc.2021.03.029 |
| [20] |
Xhaferllari I, El-Sherif O, Gaede S. Comprehensive dosimetric planning comparison for early-stage, non-small cell lung cancer with SABR: fixed-beam IMRT versus VMAT versus TomoTherapy[J]. J Appl Clin Med Phys, 2016, 17(5): 329-340. DOI:10.1120/jacmp.v17i5.6291 |
 2022, Vol. 37
2022, Vol. 37


