-
项目名称
- 国网青海省电力有限公司科技项目“青海高原荒漠地区电网工程迹地植被拟原生态营建技术研究与应用”(52283022000G)
-
第一作者简介
- 王文昌(1986—), 男, 本科生, 高级工程师。主要研究方向: 脆弱生态修复。E-mail: wangwc_qinghai@163.com
-
通信作者简介
- 荆可(1992—), 男, 硕士, 高级工程师。主要研究方向: 电网生态修复。E-mail: jinke_19920705@163.com
-
文章历史
-
收稿日期:2023-12-11
修回日期:2024-01-02
荒漠(desert)占地球陆地面积的约1/3[1-2]。该地区降水贫乏、炎热干燥,导致植被稀疏、土壤贫瘠、侵蚀频发[3];然而,在如此恶劣的土壤生境中却包含着丰富而多样的土壤微生物类群,如细菌、古菌、真菌、病毒等[4-5]。这些微生物不仅是荒漠地区生物多样性的重要组分,还是土壤物质和能量循环的关键调解者[6]。其中,自养微生物还能利用光能或化学能合成有机物,为生态系统中的其他生物提供能量和有机物;根际有益菌帮助植物吸收水分和养分、抵抗病菌侵害,对植物生长、健康和逆境适应性具有重要意义。总之,土壤微生物在维持土壤生态系统的平衡、促进植被生长、抵御环境压力等方面扮演着非常关键的生态角色,而这些生态功能也是过去研究所忽视的[7-8]。
随着微生物测序技术的发展,过去10余年对荒漠地区土壤微生物群落物种组成、结构,开展广泛研究,主要集中在中国北方沙区[9]、纳米布[10]、莫哈维[11]、阿塔卡玛[12]和澳大利亚西部沙漠[13]等地区。荒漠地区土壤环境极其脆弱,容易受到气候改变、土壤侵蚀、人类活动等各种因素破坏干扰[5, 9-11],其土壤微生物群落主要受到干燥度、pH值、盐分、降雨和植被类型等因素的影响[2, 4-6, 14]。这些研究主要聚焦在表层土壤微生物群落的变化,然而鉴于土壤垂直方向的异质性,深层土壤微生物群落对环境干扰的响应显著不同[15-16]。这意味着仅仅针对表层土壤微生物群落的研究成果并不足以完全了解土壤生态功能,只有全面深入研究土壤生态系统的复杂性和人类活动的影响,才能更好地保护和利用土壤资源,实现可持续的农业发展和生态环境的保护[17]。
随着“沙戈荒”绿色电能项目的陆续开展,输变电工程建设极易引发土壤侵蚀和生态系统的退化。过去关于输电线路对生态环境的影响主要集中在水土流失和灾害等方面[18-20],强调土地利用变化对生态系统的潜在影响,而对土壤微生物却鲜有关注。韩晓锐[21]评估输电线路对环境的影响及污染防治策略,也揭示输电线路可能引起的环境污染问题。工程建设不仅仅引起大量水土流失,伴随这一过程的还有生物多样性降低,特别是土壤微生物,从而降低土壤功能和影响土壤生态稳定性维持;然而,工程建设干扰对土壤微生物多样性、群落结构组成和特征等方面的影响,目前并不清楚。
共和盆地位于青藏高原腹地,过去关于这个区域的土壤微生物的研究主要集中在环境梯度下的变化[22-23],而对土地干扰和土地利用类型改变对土壤微生物群落结构(特别是深层土壤微生物)影响的认识相对薄弱。笔者以共和盆地荒漠区输电塔基建设干扰区为研究对象,结合目前先进的微生物测序技术和生态学方法,分析塔基建成2 a后深层土壤群落多样性和结构特征,并进一步分析其关键土壤影响因子,以期为高寒荒漠区生产建设水土保持和生态恢复提供理论参考和技术支持。
1 研究区概况研究选择在青海省海南藏族自治州共和盆地西部进行。该区域处于黄河二级阶地上,地形平坦,地势较开阔,地面高程约为2 880 m,属于高原大陆性气候,平均气温在1.0~2.4 ℃之间,日照时间长、辐射强;冬季漫长、夏季凉爽;气温日较差大,年较差小;降水量少,干燥多风,多年降雨量约为385 mm,年均潜在蒸发约为1 700 mm。土壤主要为棕钙土、栗钙土、盐土和风沙土。
由于生境条件恶劣,共和盆地西部沙区植被分布稀少,植物群落结构简单,主要有沙蒿(Artemisia desertorum)、小叶锦鸡儿(Caragana microphylla)、乌柳(Salix cheilophila)、沙棘(Hippophaer hamnoides)等灌木;沙生旱生草本植物包括赖草(Leymus secalinus)、针茅(Stipa capillata)、甘草(Glycyrrhiza uralensis)、骆驼蓬(Peganum harmala)、双叉细柄茅(Ptilagrostisdichotoma)、芨芨草(Neotrinia splendens)、阿拉善马先蒿(Pedicularis alaschanica)、狗牙根(Cynodon dactylon)和披针叶野决明(Thermopsis lanceolata)等。
2 材料与方法 2.1 样地选择2022年8月,选择塔拉—海南—西宁Ⅲ回750千伏输变电工程塔基干扰区和临近未干扰区域深层土壤微生物为研究对象。该输电工程工期为2019年8月—2021年1月。为调查工程建设对荒漠区深层土壤的影响,在该工程共和盆地沙珠玉段选择5个塔基建设工程干扰区为研究样地,在每个塔基下建立5个5 m×5 m样方;同时,在距离塔基100 m未被干扰的区域,建立5个5 m×5 m样方为对照,在研究中,共建成50个5 m×5 m的样方。
2.2 土壤样品采集样品采集在2022年8月22日完成。在每个样方内,用直径为5 cm的土钻采集60~80 cm土层土壤样品,并将每个塔基临近5个样方内的土壤混合成一个混合样品,分别装入无菌10号自封袋,标记、装入冷藏箱中迅速运回实验室。将每份土壤样品分成3份,一份鲜土用于微生物碳和微生物氮的测定;一份自然风干研磨后,测定理化性质;一份装入50 mL离心管中用干冰保存寄往广州进行微生物DNA测序。在每个取样点,用环刀采集60~80 cm土层原位土,每个土壤剖面收集3个环刀,土壤密度计算取平均值。
2.3 基因测序和生物信息分析首先利用E.Z.N.A. ® soil DNA Kit土壤试剂盒(Omega Bio-tek公司, 美国)提取土壤样品中所有DNA,用ThermoNanoDrop One检测DNA的纯度和浓度[24];利用带barcode的特异引物对515F/806R(515F: 5′-GTGCCAGCMGCCGCGGTAA; 806R: 5′-GGACTACHVGGGTWTCTAAT)[25]进行V4区PCR扩增(BioRad S1000; Bio-Rad Laboratory, CA),每个样品进行3个重复,并将PCR产物混合。按照NEBNext ® UltraTM Ⅱ DNA Library Prep Kit for Illumina ®(New England Biolabs,USA)标准流程进行建库操作。利用fastp和cutadapt软件对数据进行质控处理,在QIIME2平台使用UPARSE进行OTU(operational taxonomic units)聚类,将每个OTU的代表序列与SILVA库进行比对获得物种注释信息[26-27]。利用R语言对所有样品重抽样至最少样本的reads数(89004)。
2.4 土壤理化性质测定土壤密度采用环刀烘干法测定。微生物量碳、氮采用氯仿熏蒸法- K2SO4浸提法,分别用重铬酸钾氧化—外加热法和紫外分光光度计比色法对提取液进行碳氮测定[28]。土壤其他化学性质测定参考《土壤农业化学分析》[29],有机碳、全氮、全钾和总磷质量分数分别用重铬酸钾氧化—外加热法、硫酸—高氯酸消化开氏定氮法、氧化钾法和硫酸—过氧化氢消解法进行测定。有效磷和有效钾质量分数分别用树脂吸附法和铵醋提取法测定。
2.5 数据处理采用双比率Z检验(two-proportions Z-test)检验塔基干扰区和未干扰区深层土壤细菌门和科相对丰度差异;采用t检验比较细菌α多样性和土壤理化性质差异;基于LEfSe分析塔基干扰区和未干扰区深层土壤细菌群落组成差异。利用非参数多元方差(Adonis, 999次蒙特卡洛随机置换)检验2种处理条件细菌群落结构差异;利用FastTree软件,构建细菌系统进化树,并用零模型分析细菌的构建方式;通过计算Pearson相关系数,进行细菌群落和土壤理化性质之间的Mantel分析;并构建结构方程模型,解析塔基建设对土壤理化性质和细菌群落结构的影响机制。除进化树构建,本研究所有分析和制图均用R 4.2.3完成(https://www.r-project.org/)。
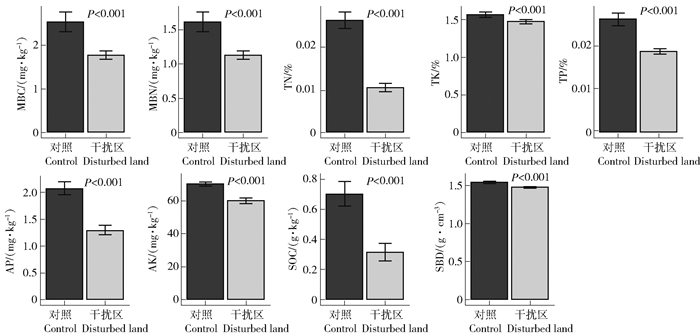
3 结果与分析 3.1 塔基建设对深层土壤物理化学性质的影响如图 1所示,通过对土壤物理化学性质进行显著性检验发现,塔基建设显著降低土壤密度、微生物量碳、微生物量氮、有机碳、总氮、总磷、总钾、有效磷和有效钾的质量分数(P<0.05)。
|
MBC:微生物量碳,MBN:微生物量氮,TN:总氮,TK:总钾,TP:总磷,AP:有效磷,AK:有效钾,SOC:土壤有机碳,SBD:土壤密度。 MBC: Microbialbiomass carbon; MBN: microbialbiomass nitrogen; TN: total nitrogen; TK: total kalium; TP: total phosphorus; AP: available phosphorus; AK: available kalium; SOC: soil organic carbon; SBD: soil bulk density 图 1 塔基建设干扰区和未干扰区深层土壤物理化学性质差异 Fig. 1 Differencesin thephysical and chemical traits ofdeepsoil layers in the disturbed area for transmission tower construction and undisturbed area |
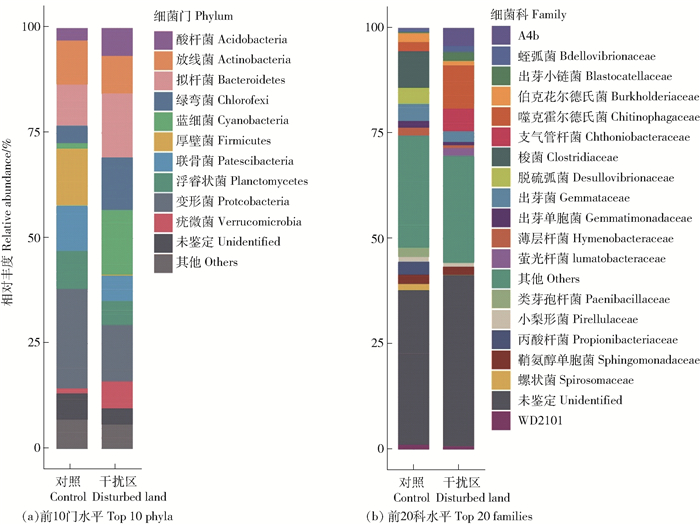
塔基建成2 a后,建设干扰区深层土壤细菌组成与附近未干扰区显著不同(图 2)。门水平主要表现为酸杆菌(Acidobacteria)、拟杆菌(Bacteroidetes)、绿弯菌(Chloroflexi)、蓝细菌(Cyanobacteria)和疣微菌(Verrucomicrobia)等相对丰度显著增加;变形菌(Proteobacteria)、厚壁菌(Firmicutes)和髌骨菌(Patescibacteria)则明显降低(Z-test; P<0.05)。科水平主要是A4b、Chitinophagaceae和Chthoniobacteraceae相对丰度显著增加,而Clostridiaceae显著降低(Z-test; P<0.05)。
|
图 2 塔基建设干扰区和未干扰区深层土壤前10细菌门水平和前20科水平相对丰度 Fig. 2 Relative abundances of the top 10 phyla and the top 20 families in the bacterial communities of deep soil layers between in the disturbed area for transmission tower construction and undisturbed area |
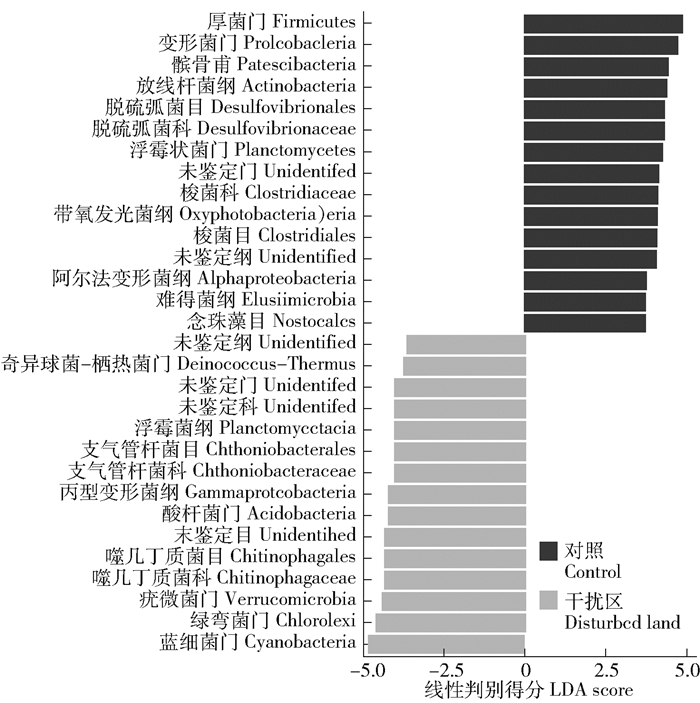
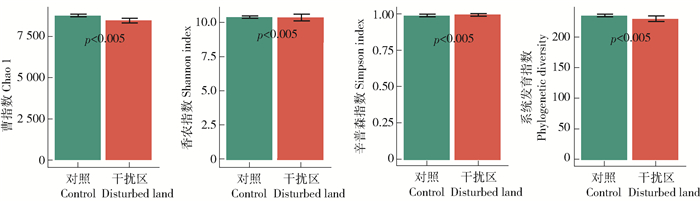
线性判别分析发现,塔基建设干扰后,Firmicutes、Proteobacteria、Planctomycetes、Cyanobacteria、Chloroflexi和Verrucomicrobia等细菌门具有显著差异(图 3;P<0.01);Desulfovibrionaceae、Clostridiaceae、Chitinophagaceae和Chthoniobacteraceae等科也具有显著差异(P<0.01)。尽管塔基建设并未明显改变深层土壤细菌群落香农指数和辛普森指数(P>0.05),但干扰区Chao1和系统发育多样性却显著降低(图 4;P<0.05)。
|
LDA为线性判别分。 LDA: Linear discriminant analysis. 图 3 基于LEfSe塔基建设干扰区和细菌物种差异分析 Fig. 3 Species difference analysis between in the disturbed area for transmission tower construction and undisturbed area based on LEfSe |
|
图 4 塔基建设干扰区和未干扰区深层土壤细菌α多样性差异 Fig. 4 Bacterial α-diversity difference of deep soil layers in the disturbed area for transmission tower construction and undisturbed area |
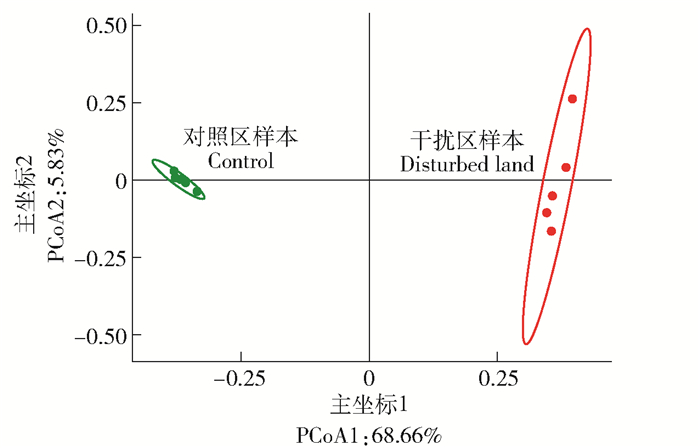
PCoA(principal coordinates analysis)分析显示,塔基建设后深层土壤细菌群落结构显著不同。采用ANOSIM检验后发现,干扰区和未干扰区土壤细菌群落β多样性差异显著(R2=0.68, P=0.009)。由图 5显示,塔基建设导致深层土壤细菌群落组内差异的变异性显著增加。
|
图 5 基于OTU水平塔基建设干扰区和未干扰区深层土壤细菌β多样性差异(Bray-Curtis距离) Fig. 5 Bacterial β-diversity difference (Bray-Curtis distance) of deep soil layers in the disturbed area for transmission tower construction and undisturbed area based on OTU |
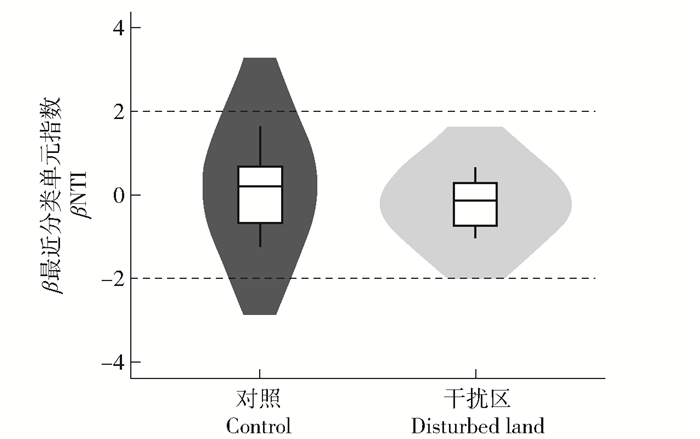
通过构建零模型,计算βNTI (beta nearest-taxon-index)量化细菌群落构建机制。结果发现,尽管未干扰区深层土壤细菌群落的构建受到21.1%的比例决定过程的影响,但塔基建设区深层土壤细菌群落的构建主要由随机过程影响(图 6)。而且,当塔基假设干扰后,深层土壤细菌群落构建100%受到随机过程的影响。显然,塔基建设增加了深层土壤细菌群落组装的随机性。
|
图 6 塔基建设干扰区和未干扰区深层土壤细菌组建的决定和随机过程 Fig. 6 Deterministic and stochastic processes for bacterial communities of deep soil layers in the disturbed area for transmission tower construction and undisturbed area |
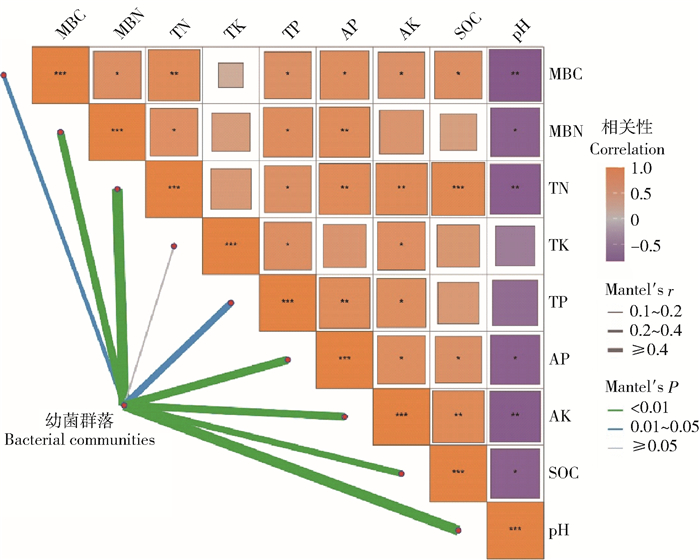
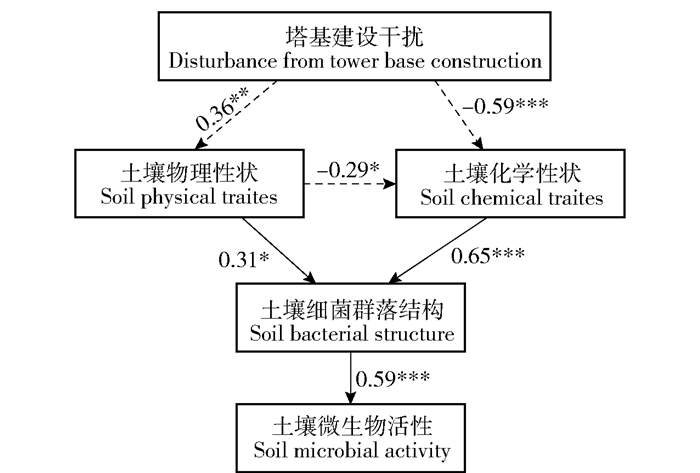
Mantel分析显示,塔基建设干扰后引起的细菌群落结构的变化,主要受到pH、总氮、有效磷、有效钾、微生物氮、有机碳、总磷和微生物碳的影响(图 7)。其中,总钾对细菌群落结构无显著性影响,pH、总氮和有效磷是影响细菌群落结构差异的主要控制因素。塔基建设主要通过改变深层土壤化学性质而不是物理性质,并进一步间接影响细菌群落结构和微生物活性(图 8)。
|
线条粗细代表Mantel的r值的大小。 图 7 细菌群落与土壤化学性质的Mantel相关性分析 Fig. 7 Mantel correlation analysis between bacterial community structure and soil chemical traits |
|
土壤微生物活性用微生物量碳和氮含量;土壤物理性质用土壤密度、机械组成和紧实度的主成分分析的第一轴表征;土壤化学性质用pH、总氮、总磷、总钾、有效磷和有效钾的主成分分析的第一轴表征;土壤细菌群落结构用PCoA第一轴表征;实线和虚线分别代表正相关和负相关。 Soil microbial activity is represented by MBC and MBN; soil physical properties are characterized by the first principal component analysis of soil bulk density, mechanical composition, and compaction; soil chemical properties are represented by the first principal component analysis of pH, TN, TP, TK, AP, and AK; soil bacterial community structure is represented by the first axis of PCoA; solid and dashed lines represent positive correlation and negative correlation, respectively. 图 8 结构方程模型检验塔基建设通过影响土壤理化性质影响深层土壤细菌群落结构 Fig. 8 Structural equation modelling (SEM) verifying that affecting the bacterial community structure of deep soil layers affected by impacts to soil physicochemical property |
研究发现,与未被干扰的自然区域比较,塔基建设区域深层土壤细菌群落物种组成显著不同(图 2和图 3)。在未干扰区深层土壤细菌具有更高比例的厌氧细菌类群。过去的研究证实,变形菌门、芽胞杆菌门和绿弯菌门包含多个厌氧细菌类群,其在深层土壤碳、氮、硫等元素的循环过程发挥着重要作用[30]。本研究还发现厌氧细菌绿弯菌科、氨氧化细菌科和孢杆菌科相对丰度也显著高于干扰区。深层土壤被翻动后,土壤结构发生较大改变,特别是通气性增加,导致土壤孔隙中含有更高的氧气浓度,使原本缺氧的环境更趋向于氧化。这样的改变可能不利于厌氧细菌的生存[31]。总的来说,深层土壤被干扰后,导致厌氧细菌门类减少的主要原因是土壤氧化、污染、结构破坏、温度和水分变化等因素的相互作用。这种减少可能对土壤生态系统的功能和稳定性产生负面影响。在氧气环境中,相比于厌氧细菌,喜氧细菌具有更加旺盛的新陈代谢,有机质降解速率也更快[32]。这可能解释干扰区深层土壤多项化学性质指标显著低于未干扰区(图 1)。显然,厌氧细菌门类比例的减少可能对土壤功能和稳定性带来负面影响。未来的研究应更加关注土壤结构性破坏后,微生物群落结构变化对土壤功能的影响,并探讨可行的土壤管理策略,促进土壤生态系统的恢复。
4.2 深层土壤细菌群落结构变化塔基建设显著降低深层土壤细菌Chao1和系统发育指数(图 4)。过去的研究证实,土地利用类型显著改变荒漠生态系统深层土壤细菌多样性[33]。工程建设干扰后的深层土壤水分流失引起的干旱可能是土壤细菌多样性降低的原因之一。有研究也发现,土地利用类型的改变和气候变化加剧深层土壤的干旱,并降低细菌多样性[34]。PCoA分析和ANOSIM检验还发现,工程建设干扰后显著改变土壤深层细菌群落结构(图 5)。其他干旱区的研究也证实,土壤结构的扰动也显著改变土壤细菌、真菌和古菌群落结构[35]。一些细菌(比如,厌氧和喜氧细菌)可能因为土地结构的破坏和其他环境变化而受到不同程度的影响,导致整体群落结构的变化。因此,土壤扰动引起的结构破坏和水分流失,影响微生物的栖息环境和相互作用,从而对微生物多样性产生严重影响。本研究的结果进一步强调,土壤微生物对于环境变化的高度敏感性。在未来的研究中,应该关注多种微生物,包括真菌、古菌和病毒等,对土壤环境变化的响应,以期更加深入了解整个土壤生态系统对环境的响应机制。
零模型分析发现,干扰区和未干扰区深层土壤细菌组装机制主要受随机过程的影响。这个结果与过去荒漠区土壤细菌的研究[36]相似,JIAO等发现荒漠细菌群落主要由随机过程驱动而不是决定过程。这意味着微生物的空间分布和相互作用更多地是由随机事件引起,而不是受到特定环境条件或相互作用的决定性影响。随机过程可能包括漂移、扩散和随机死亡等事件,使得微生物在土壤中的分布呈现出较大的随机性[37]。荒漠地区的环境具有不稳定的特征,比如降水的偶发性和温度的剧烈波动等[6-7]。这可能导致细菌群落的形成更容易受到随机事件的左右。另外,其他研究[38]也发现,相较于其他微生物种类,细菌生长迅速,对环境的变化更加敏感。组装过程的量化分析更加证实,塔基建设对土壤环境干扰后,增加深层土壤细菌群落组装的随机性(图 6)。这可能是因为塔基建设导致土壤环境变得更加动态和不稳定。这也意味着土壤环境的随机动态变化影响着深层土壤细菌群落的形成和演变。
4.3 深层土壤细菌群落的环境驱动因子Mantel分析显示,塔基建设干扰区和未干扰区深层土壤细菌群落主要受pH、总氮和有效磷含量的影响(图 7)。以往的研究证实,细菌群落的组成与土壤pH密切相关[36, 39]。这是因为不同的细菌群体对酸碱环境有不同的适应性,酸碱环境的变化可以直接影响土壤中可溶性离子的浓度,从而改变土壤的生物和化学性质,因此,土壤pH的变化会导致细菌群落组成和结构的调整[40]。本研究发现,塔基建设导致深层土壤pH显著增加,可能是由于建筑工程过程中需要使用化学物质或者混凝土等材料。这些物质可能会对土壤产生影响,使得土壤的化学性质发生变化。另一方面,由于建设过程对塔基深层土壤结构的扰动,也会影响其化学性质。氮磷元素往往是荒漠贫瘠土壤中限制生物生长的主要因素之一,微生物通常需要适应这种低养分环境,采取各种策略来获取有限的氮和磷[41]。氮和磷是微生物生长和代谢的重要组成部分,因此土壤中总氮和磷的变化可能会直接影响细菌群落的丰度和多样性[41-42]。一些研究表明,养分丰富的土壤可能支持更丰富的微生物多样性;相反,养分贫瘠的土壤可能导致微生物多样性减少,只有适应养分限制的微生物能够在这样的环境中生存[43-44]。这些结果反映微生物对于生存和繁殖在不同生环境中的差异化适应,不同的环境中包含有特定的微生物类群。这一高适应特性不仅使微生物成为生态系统中丰富的多样性组分,同时也为它们在面对环境变化时提供一种灵活的适应策略[45]。
结构方程模型进一步验证,塔基建设直接改变土壤物理和化学性质,进而影响细菌群落多样性和结构(图 8)。塔基建设导致土壤结构的破坏和孔隙度的变化,可能引起水分保持能力、通透性等方面的变化。土壤侵蚀程度的增加直接导致有机质和养分的流失,pH、氮、磷等土壤化学性质改变又影响细菌群落的丰度、结构和构建方式。显然,工程施工对土壤环境的影响是多方面的,在生态修复过程中应该对受到影响的土壤提供更为精细的措施和细致的管理。
5 结论1) 共和盆地荒漠区深层土壤细菌群落的组成、丰度、多样性和结构受到塔基建设的显著影响。输电塔基建设引起深层土壤细菌群落的显著变化,对深层土壤细菌的多样性和群落丰度产生负面影响。
2) 输电塔基建设增加深层土壤细菌组建的随机性,塔基建设对细菌群落结构的改变可能受到多种因素的影响,使细菌群落构建更加随机和不确定。
3) 土壤的pH值、氮和磷含量是主要的控制因子,土壤化学性质的变化是塔基建设影响细菌群落的主要驱动因素。
这本研究揭示深层土壤细菌群落对环境干扰的响应变化,强调人类活动对土壤微生物群落结构和生态系统功能的潜在影响,同时为人为导致的水土流失管理提供更广泛和深入的理解。在进行土地利用规划和基础设施建设时,需要综合考虑对土壤生物资源和生态系统的潜在影响,并采取适当的管理和保护措施。
| [1] |
MIDDLETON N, THOMASS D. (Eds.). World atlas of desertification[M]. 2nd ed. United Nations Environment Programme, 1997: 35.
|
| [2] |
NEILSON J W, CALIFF K, CARDONA C. Significant impacts of increasing aridity on the arid soil microbiome[J]. mSystems, 2017, 2(3): 1128. |
| [3] |
MARTÍNEZ-VALDERRAM J, GUIRADO E, MAESTRE F T. Desertifying deserts[J]. Nature Sustainability, 2020, 3(8): 572. DOI:10.1038/s41893-020-0561-2 |
| [4] |
ZHANG Kaoping, SHI Yu, CUI Xiaoqing, et al. Salinity is a key determinant for soil microbial communities in a desert ecosystem[J]. mSystems, 2019, 4(1): 10. |
| [5] |
DELGADO-BAQUERIZO M, DOULCIER G, ELDRIDGE D J, et al. Increases in aridity lead to drastic shifts in the assembly of dryland complex microbial networks[J]. Land Degradation & Development, 2020, 31(3): 346. |
| [6] |
MAESTRE F T, DELGADO-BAQUERIZO M, JEFFRIES T C, et al. Increasing aridity reduces soil microbial diversity and abundance in global drylands[J]. Proceedings of the National Academy Sciences of United States of America, 2015, 112(51): 15684. DOI:10.1073/pnas.1516684112 |
| [7] |
STEVEN B, PHILLIPS M L, BELNAP J, et al. Resistance, resilience, and recovery of dryland soil bacterial communities across multiple disturbances[J]. Frontiers in Microbiology, 2021, 12: 8. |
| [8] |
张力斌, 何明珠, 张克存, 等. 干旱风沙区植被重建初期对土壤微生物群落结构的影响[J]. 干旱区地理, 2022, 45(6): 1916. ZHANG Libin, HE Mingzhu, ZHANG Kecun, et al. Effect of preliminary vegetation reconstruction on soil microorganism community structure in arid desert area[J]. Arid Land Geography, 2022, 45(6): 1916. |
| [9] |
WANG Xiaobo, LÜ Xiaotao, YAO Jing, et al. Habitat-specific patterns and drivers of bacterial β-diversity in China's drylands[J]. The ISME Journal, 2017, 11(6): 1345. DOI:10.1038/ismej.2017.11 |
| [10] |
COWAN D A, HOPKINS D W, JONES B E, et al. Microbiomes of Namib desert habitats[J]. Extremophiles, 2020, 24(1): 17. DOI:10.1007/s00792-019-01122-7 |
| [11] |
FISHER K, JEFFERSON J S, VAISHAMPAYAN P. Bacterial communities of Mojave Desert biological soil crusts are shaped by dominant photoautotrophs and the presence of hypolithic niches[J]. Frontiers in Ecology and Evolution, 2020, 7: 518. DOI:10.3389/fevo.2019.00518 |
| [12] |
SCHULZE-MAKUCH D, WAGNER D, KOUNAVES S P, et al. Transitory microbial habitat in the hyperarid Atacama Desert[J]. Proceedings of the National Academy of Sciences, 2018, 115(11): 2670. DOI:10.1073/pnas.1714341115 |
| [13] |
LEUNG P M, BAY S K, MEIER D V, et al. Energetic basis of microbial growth and persistence in desert ecosystems[J]. mSystems, 2020, 5(2): 1110. |
| [14] |
TRIPATHI B M, STEGEN J C, KIM M, et al. Soil pH mediates the balance between stochastic and deterministic assembly of bacteria[J]. The ISME Journal, 2018, 12(4): 1072. DOI:10.1038/s41396-018-0082-4 |
| [15] |
WU Ying, CHEN Dima, DELGADO-BAQUERIZO M, et al. Long-term regional evidence of the effects of livestock grazing on soil microbial community structure and functions in surface and deep soil layers[J]. Soil Biology and Biochemistry, 2022, 168: 6. |
| [16] |
YANG Xihang, YUE Linyan, WU Ying, et al. The validity of ecological hypotheses concerning aboveground organisms for soil microbial biomass and diversity across soil depths on the Mongolian Plateau[J]. Applied Soil Ecology, 2023, 181: 104679. |
| [17] |
ZHANG Qiufang, QIN Wenkuan, FENG Jiguang, et al. Whole-soil-profile warming does not change microbial carbon use efficiency in surface and deep soils[J]. Proceedings of the National Academy of Sciences, 2023, 120(32): 10. |
| [18] |
洪倩, 陈晓枫, 余蔚青, 等. 输电线路塔基施工余土的改良及其植物生长试验[J]. 中国水土保持科学, 2022, 20(4): 126. HONG Qian, CHEN Xiaofeng, YU Weiqing, et al. An experimental study on improvement of residual soil and the plant growth in transmission line tower foundation construction[J]. Science of Soil and Water Conservation, 2022, 20(4): 126. DOI:10.16843/j.sswc.2022.04.016 |
| [19] |
刘继武, 韩恺, 闫炜炀. 山西采动影响区输电线路塔基区水土流失特点及防治措施[J]. 山西电力, 2021(5): 23. LIU Jiwu, HAN Kai, YAN Weiyang. Study on water and soil erosion characteristics and control measures of transmission line tower base in mining-affected area of Shanxi province[J]. Shanxi Electric Powe, 2021(5): 23. |
| [20] |
丰佳, 陈晓刚, 王文龙, 等. 云南土石山区输变电线路工程水土流失特征研究[J]. 中国水土保持, 2022(7): 31. FENG jia, CHEN Xiaogang, WANG Wenlong, et al. Soil and water loss characteristics of transmission and transformation line project in Yunnan earth-rock mountain area[J]. Soil and Water Conservation in China, 2022(7): 31. |
| [21] |
韩晓锐. 输电线路涉及环境敏感区的环境影响及污染防治措施研究[J]. 环境与发展, 2019, 31(7): 32. HAN Xiaorui. Study on environmental impacts and pollution prevention measures of transmission lines in environmentally sensitive areas[J]. Environment and Development, 2019, 31(7): 32. |
| [22] |
张曼玉, 王志涛, 邓磊, 等. 共和盆地不同灌木群落生物土壤结皮理化性质差异[J]. 干旱区研究, 2023, 40(11): 1797. ZHANG Manyu, WANG Zhitao, DENG Lei, et al. Differences in the physical and chemical properties of biological soil crusts in different shrub communities in the Gonghe Basin[J]. Arid Zone Research, 2023, 40(11): 1797. |
| [23] |
王伦, 周鸿玉, 杨秀玲, 等. 共和盆地不同恢复年限人工混交林表层土壤微生物群落特征[J]. 青海大学学报, 2023, 41(2): 1. WANG Lun, ZHOU Hongyu, YANG Xiuling, et al. Characteristics of soil microbial communities of artificial mixed forest with different restoration years in Gonghe basin[J]. Journal of Qinghai University, 2023, 41(2): 1. |
| [24] |
CHEN Yongjian, NEILSON J W, KUSHWAHA P, et al. Life-history strategies of soil microbial communities in an arid ecosystem[J]. The ISME Journal, 2021, 15(3): 649. |
| [25] |
MORENO-JIMÉNEZ E, PLAZA C, SAIZ H, et al. Aridity and reduced soil micronutrient availability in global drylands[J]. Nature Sustainability, 2019, 2(5): 371. |
| [26] |
YEH Y C, MCNICHOL J, NEEDHAM D M, et al. Comprehensive single-PCR 16S and 18S rRNA community analysis validated with mock communities, and estimation of sequencing bias against 18S[J]. Environmental Microbiology, 2021, 23: 3240. |
| [27] |
CAPORASO J G, LAUBER C L, WALTERS W A, et al. Ultra-high-throughput microbial community analysis on the Illumina HiSeq and MiSeq platforms[J]. The ISME Journal, 2012, 6(8): 1621. |
| [28] |
周桦, 宇万太, 马强, 等. 氯仿薰蒸浸提法测定土壤微生物量碳的改进[J]. 土壤通报, 2009, 40(1): 154. LU Hua, YU Wanta, MA Qiang, et al. A modified fumigation extraction method for the determination of soil microbial biomass carbon[J]. Chinese Journal of Soil Science, 2009, 40(1): 154. |
| [29] |
鲁如坤. 土壤农业化学分析方法[M]. 北京: 中国农业科技出版社, 2000: 330. LU Rukun. Methods of soil agricultural chemical analysis[M]. Beijing: China Agricultural Science and Technology Press, 2000: 330. |
| [30] |
NAYLOR D, MCCLURE R, JANSSON J. Trends in microbial community composition and function by soil depth[J]. Microorganisms, 2022, 10(3): 540. |
| [31] |
SUI Biao, WANG Li, WANG Hongbin, et al. Deep tillage inhibits microbial species interactions and exhibits contrasting roles in bacterial and fungal assembly[J]. Agriculture, Ecosystems & Environment, 2023, 357: 108679. |
| [32] |
CRǎCIUN N, NEGREA B, POP C E, et al. Experimental research compared aquaculture of certain species of the Lemna genus with demonstration of environmental requirements and of the adaptations to environmental conditions specific to aquatic eutroph-polytroph ecosystems[J]. Scientific Annals of the Danube Delta Institute, 2020, 25: 33. |
| [33] |
KONG Weibo, WEI Xiaorong, WU Yonghong, et al. Afforestation can lower microbial diversity and functionality in deep soil layers in a semiarid region[J]. Global Change Biology, 2022, 28(20): 6086. |
| [34] |
ZHOU Zixuan, WANG Yunqiang. Global patterns of dried soil layers and environmental forcing[J]. Land Degradation & Development, 2023, 11(15): 3364. |
| [35] |
HU Yigang, WANG Zengru, ZHANG Zhishan, et al. Alteration of desert soil microbial community structure in response to agricultural reclamation and abandonment[J]. Catena, 2021, 207: 105678. |
| [36] |
JIAO Shuo, CHU Haiyan, ZHANG Baogang, et al. Linking soil fungi to bacterial community assembly in arid ecosystems[J]. iMeta, 2022, 1(1): 1. |
| [37] |
KU Yongli, HAN Xiaoting, LEI Yuting, et al. Different sensitivities and assembly mechanisms of the root-associated microbial communities of Robinia pseudoacacia to spatial variation at the regional scale[J]. Plant and Soil, 2023, 486: 621. |
| [38] |
JANSSON J K, HOFMOCKL K S. Soil microbiomes and climate change[J]. Nature Reviews Microbiology, 2020, 18(1): 35. |
| [39] |
ROUSK J, BÅÅTH E, BROOKES P C, et al. Soil bacterial and fungal communities across a pH gradient in an arable soil[J]. The ISME Journal, 2010, 4(10): 1340. |
| [40] |
PHILIPPOT L, CHENU C, KAPPLER A, et al. The interplay between microbial communities and soil properties[J]. Nature Reviews Microbiology, 2023, 1: 226. |
| [41] |
LI Jiwei, XIE Jianbo, ZHANG Yu, et al. Interactive effects of nitrogen and water addition on soil microbial resource limitation in a temperate desert shrubland[J]. Plant and Soil, 2022, 475(1/2): 361. |
| [42] |
LI Jiabo, SHEN Zehao, LI Chaonan, et al. Stair-step pattern of soil bacterial diversity mainly driven by pH and vegetation types along the elevational gradients of Gongga Mountain, China[J]. Frontiers in Microbiology, 2018, 9: 569. |
| [43] |
YIN Yue, WANG Xiaojie, HU Yuanan, et al. Soil bacterial community structure in the habitats with different levels of heavy metal pollution at an abandoned polymetallic mine[J]. Journal of Hazardous Materials, 2023, 442: 130063. |
| [44] |
孙欣. 半干旱草原微生物物种组成和功能基因对降水变化的响应[D]. 北京: 清华大学, 2015: 67. SUN Xin. Responses of microbial community taxonomic composition and functional genes to precipitation changes in semi-arid grasslands[D]. Beijing: Tsinghua University, 2015: 67. |
| [45] |
SHU Wensheng, HUANG Linan. Microbial diversity in extreme environments[J]. Nature Reviews Microbiology, 2022, 20(4): 219. |
 2024, Vol. 22
2024, Vol. 22 
