文章信息
- 金迪, 张明如, 王佳佳, 侯平
- JIN Di, ZHANG Mingru, WANG Jiajia, HOU Ping
- 遮阴和氮素梯度处理对芒萁光合生理的影响
- Effects of shading and nitrogen gradient treatments on photosynthetic physiology of potted Dicranopteris dichotoma
- 森林与环境学报,2020, 40(4): 412-419.
- Journal of Forest and Environment,2020, 40(4): 412-419.
- http://dx.doi.org/10.13324/j.cnki.jfcf.2020.04.011
-
文章历史
- 收稿日期: 2020-03-31
- 修回日期: 2020-05-23
2. 浙江农林大学风景园林与建筑学院, 浙江 杭州 311300
2. School of Landscape and Architecture, Zhejiang Agriculture and Forestry University, Hangzhou, Zhejiang 311300, China
光照和氮素是植物生长发育的重要环境因子。光照强度的变化会影响植物的生长速率、生理特性和表观形态特征等[1],氮素的获取直接影响器官间的营养分配,对叶绿素含量、光合关键酶活性等产生影响[2]。氮素对植物光合生理的影响具有一定的阈值效应[3],适量添加氮素能提高植物的净光合速率和光化学效率[4],促进植株生长和拓殖[5]。
芒萁[Dicranopteris dichotoma (Thunb.) Berhn.]是我国亚热带低山丘陵区退化植被的“标志种”[6],能够适应从肥沃到瘠薄多种土壤条件[7]。野外调查发现,芒萁可密集生长于土壤相对肥沃的马尾松(Pinus massoniana Lamb.)、杉木[Cunninghamia lanceolata (Lamb.) Hook.]等单优群落下层及林缘,并形成单优草本层片[8-9],亦可定居于土壤贫瘠的全光地段或水土流失的红壤侵蚀区[10],自然分布于多种类型的生境,表明芒萁能适应多种光照强度和土壤条件。芒萁单优草本层片连续密集生长于多种退化群落下层生境,将同时产生系列生态问题:森林群落针阔叶树种种子发芽和幼苗生长困难,枯草期易引发地表火进而诱发林冠火。因此,芒萁单优草本层片属于阻碍疏灌草丛和马尾松单优群落步入进展演替的关键层片。为研究森林植被退化和恢复过程中的光照强度和土壤氮素含量变化对芒萁光合生理的影响,以盆栽芒萁为研究材料,设置遮阴与氮素双因素控制试验,模拟暖性针叶单优群落下层弱光与土壤较肥沃,到林缘、灌草丛光照较强与土壤较贫瘠等不同生境,测定盆栽芒萁光合生理参数和叶绿素荧光动力学参数,比较芒萁对遮阴和氮素梯度处理的光合生理响应特征,分析芒萁的光照强度与氮素双因素组合处理的适应特点,研究结果对于调控芒萁单优草本层片过度发育、促进森林群落的进展演替,具有一定的生态理论价值和林业生产实践意义。
1 材料与方法 1.1 试验设计试验地位于浙江农林大学东湖校区,北纬30°15′28″,东经119°43′35″,全年降水量1 628.6 mm,年平均气温16.4 ℃,全年无霜期约237 d。2019年5月,在浙江省杭州市临安区玲珑山,北纬30°13′05″,东经119°40′23″,海拔200 m处,选取长势良好且高度基本一致的芒萁幼苗120株[株高(11.7±1.8) cm],栽植于40 cm×21 cm×17 cm的长方形花盆内,每盆定植1株,栽培基质为黄壤,土壤全氮含量为1.07 g · kg-1。设置3个不同光照强度的遮阴大棚,分别为轻度遮阴(L1,透光率35.96%)、中度遮阴(L2,透光率13.00%)和高度遮阴(L3,透光率4.75%)。将芒萁幼苗放置于L2条件下缓苗,两个月后将成活的盆栽芒萁随机分成12组,每组10盆,移至不同遮阴强度的大棚内。根据前人对草本植物的研究[11-12],综合调整盆栽芒萁氮素处理量,在每个遮阴处理下设置1个对照(不施氮)和3个梯度氮素处理,分别为不施氮(N0)、低氮(N1)、中氮(N2)和高氮(N3)。N1、N2和N3三个处理每盆芒萁每次施氮量分别为0.1、0.2和0.3 g (以纯氮含量计),共施放3次,间隔10 d。将对应氮含量的硫酸铵分析纯溶解于200 mL纯水,均匀喷入盆内土壤表面,不施氮处理组喷入等量纯水。处理90 d后,选取长势一致的功能叶片,测定其光合参数和叶绿素荧光参数,并测定光合色素含量。
1.2 测定方法 1.2.1 光响应进程的测定处理90 d后,用Li-6400XT光合仪于晴天上午8:30—11:30,测定芒萁叶片光响应进程。将待测叶片置于饱和光(1 500 μmol · m-2 · s-1)下照射30 min,使叶片充分适应。设定光照强度依次为2 000、1 500、1 200、1 000、800、500、300、100、50、30、10和0 μmol · m-2 · s-1,测定净光合速率(net photosynthesis rate, Pn)、气孔导度(stomatal conductance, Gs)、蒸腾速率(transpiration rate, Tr)和胞间CO2浓度(inter-cellular CO2 concentration, Ci)。每个处理选择3盆芒萁,每盆重复打点3次,计算平均值。利用光合助手(Photosynth Assistant)对Pn-光响应曲线进行拟合[13],计算光补偿点(light compensation point, LCP)、光饱和点(light saturation point, LSP)、表观量子效率(apparent quantum efficiency, AQY)、最大净光合速率(Pnmax)和暗呼吸速率(dark respiration rate, Rd)。
1.2.2 叶绿素荧光诱导动力学曲线的绘制利用便携式动态荧光仪YZQ-500,测定不同处理下芒萁成熟叶片的叶绿素荧光动力学曲线(O-J-I-P曲线),测定前将待测芒萁暗处理40 min,每个处理测3盆,每盆重复测定3次。从O-J-I-P曲线上可以直接得到荧光强度(fluorescence intensity, F):初始荧光FO=F50 μs;J点荧光FJ=F2 ms;I点荧光FI=F30 ms;P点荧光FP=Fmax。计算得到以下参数[14]:J点相对可变荧光(relatively variable fluorescence at point J, VJ)、初始斜率(initial slope, MO)、最大光化学效率(maximum photochemical efficiency, φPo)、电子传递效率(electron transfer efficiency,ψO)、电子传递量子产额(quantum yield of electron transport, φEo)、热耗散量子比率(quantum yield of dissipation, φDo)、光合性能指数(performance index, IP)。
1.2.3 光合色素含量的测定采用乙醇浸提法测定光合色素含量[15],称取0.2 g新鲜成熟芒萁叶片,剪成0.2 cm左右宽的小块,置于试管中,加入体积分数95%的乙醇10 mL,室温下置暗处浸提至叶组织完全变白,将叶绿体色素提取液倒入光径1 cm的比色杯内,用UV-2550型紫外分光光度计在665、649和470 nm的波长下测定吸光度,并计算光合色素含量。
1.3 数据处理用Excel和SPSS 22.0软件进行数据处理,采用单因素方差分析法(one-way ANOVA)和最小显著差数法(least significant difference, LSD)进行显著性检验和多重比较分析。
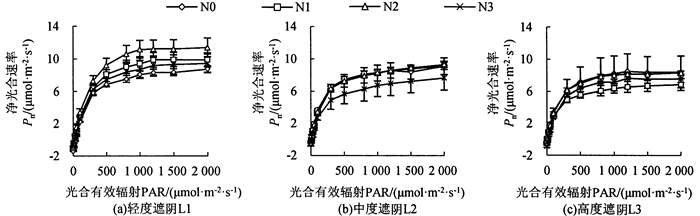
2 结果与分析 2.1 遮阴和氮素梯度处理对芒萁光响应曲线的影响遮阴和氮素梯度处理下芒萁的光响应曲线变化如图 1~图 4所示。从图 1可以看出,L1处理下,芒萁的Pn大小为N2>N1>N3>N0,当光合有效辐射(photosynthetically active radiation,PAR)大于300 μmol · m-2 · s-1时,N2的Pn上升幅度较大,当PAR为1 000 μmol · m-2 · s-1时,N2的Pn较N0上升37.9%;L2处理下,芒萁的Pn大小为N2>N1>N0>N3,PAR大于100 μmol · m-2 · s-1后, N3的Pn增速开始减缓,在PAR为1 000 μmol · m-2 · s-1时,N3的Pn较N0下降18.3%;L3处理下,芒萁的Pn大小为N0>N2>N3>N1,3种施氮量均对芒萁的Pn产生负面影响。
|
图 1 遮阴和氮素梯度处理对芒萁净光合速率的影响 Fig. 1 Effects of shading and nitrogen concentration gradient on the net photosynthesis rate of D. dichotoma |
|
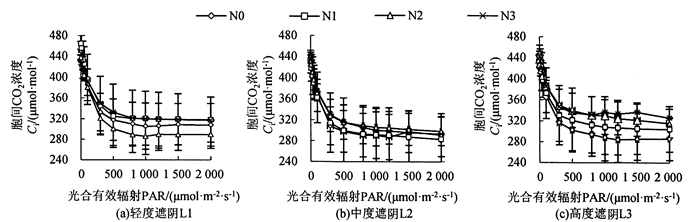
图 2 遮阴和氮素梯度处理对芒萁胞间CO2浓度的影响 Fig. 2 Effects of shading and nitrogen concentration gradient on the inter-cellular CO2 concentration of D. dichotoma |
|
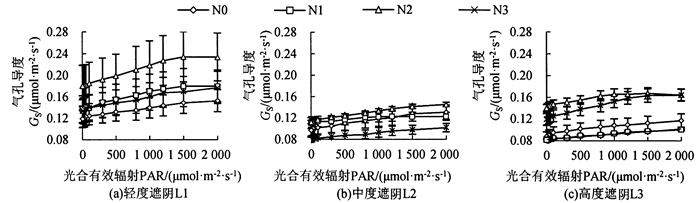
图 3 遮阴和氮素梯度处理对芒萁气孔导度的影响 Fig. 3 Effects of shading and nitrogen concentration gradient on the stomatal conductance of D. dichotoma |
|
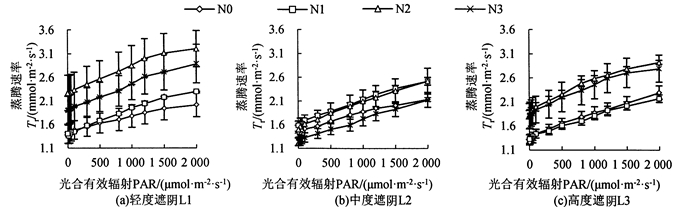
图 4 遮阴和氮素梯度处理对芒萁蒸腾速率的影响 Fig. 4 Effects of shading and nitrogen concentration gradient on the transpiration rate of D. dichotoma |
遮阴和氮素梯度处理对芒萁胞间CO2浓度的影响如图 2所示,当PAR小于300 μmol · m-2 · s-1时,芒萁的Ci下降迅速,而后趋缓,与Pn变化呈负相关。L1处理下,Ci大小为N1>N3>N0>N2;L2处理下,芒萁Ci的变化受施氮影响较小;L3处理下,Ci的大小为N3>N2>N1>N0,即芒萁Ci随施氮量增大而上升。
遮阴和氮素梯度处理对芒萁Gs的影响如图 3所示,L1处理下,芒萁的Gs大小为N2>N1>N3>N0,N2显著提升了芒萁的Gs (P < 0.05),当PAR为1 500 μmol · m-2 · s-1时,N2的Gs较N0上升57.3%,施氮有助于芒萁打开气孔,从而促进Pn升高。L2处理下,芒萁的Gs均低于L1处理,且各施氮处理间的变化差异较小。L3处理下,芒萁的Gs大小为N2>N3>N0>N1,当PAR为2 000 μmol · m-2 · s-1时,N2和N3的Gs较接近,约为N0的1.4倍,N1为N0的85.5%。
遮阴和氮素梯度处理对芒萁Tr的影响如图 4所示,L1处理下,芒萁的Tr大小为N2>N3>N1>N0,其中N2和N3明显高于N0。L2处理下,芒萁的Tr大小为N1>N2>N0>N3。L3处理下,芒萁的Tr大小为N2>N3>N0>N1,其中N2和N3相近,N0和N1相近。Tr的变化主要受Gs影响。
2.2 遮阴和氮素梯度处理对芒萁光合特征参数的影响表 1为遮阴和氮素梯度处理下芒萁的光合特征参数。L1处理下,芒萁LSP和Pnmax的大小顺序为N2>N1>N3>N0,LCP和Rd则在N2出现最小值;与N0相比,N1和N2的AQY上升,而N3的AQY则下降;N0的Rd显著高于其他处理(P < 0.05),为1.43 μmol · m-2 · s-1,说明较高光照强度下芒萁消耗碳水化合物较多,而施氮可以有效降低芒萁的Rd。L2处理下,芒萁的LSP随施氮量增加而增大,AQY和Pnmax则在N2出现最大值,LCP和Rd在N2出现最小值;Rd总体较低,施氮对耐荫性的影响不大。L3处理下,施氮降低了芒萁的LSP,但差异不显著(P>0.05);N1的LCP、Pnmax和Rd均为各处理中的最低值;N3处理则显著降低了芒萁的AQY (P < 0.05),同时LCP和Rd显著增大(P>0.05),分别是N0的1.60和1.67倍。在遮阴处理间,芒萁的LSP和Pnmax随光照强度减弱而降低,L2的AQY最高,Rd最低。
| 遮阴处理 Shading treatment |
氮素处理 Nitrogen treatment |
光饱和点LSP/(μmol·m-2·s-1) | 光补偿点LCP/(μmol·m-2·s-1) | 表观量子效率AQY/(μmol·mol-1) | 最大净光合速率Pnmax/(μmol·m-2·s-1) | 暗呼吸速率Rd/(μmol·m-2·s-1) |
| L1 | N0 | 961.2±17.3abcd | 30.0±0.7a | 0.052±0.001cde | 10.40±0.35bc | 1.43±0.01a |
| N1 | 1 047.2±97.7abc | 20.0±2.7bc | 0.054±0.003c | 11.64±1.22ab | 1.05±0.18b | |
| N2 | 1 121.6±75.5a | 16.0±2.7c | 0.058±0.004abc | 12.97±1.19a | 0.84±0.07b | |
| N3 | 989.6±106.7abcd | 22.0±3.3b | 0.048±0.003de | 10.77±1.24bc | 0.89±0.09b | |
| L2 | N0 | 917.6±59.2bcd | 10.0±2.0d | 0.054±0.001bc | 9.78±1.23bcd | 0.56±0.09c |
| N1 | 973.2±24.9abcd | 8.0±1.3d | 0.062±0.004a | 10.12±0.70bc | 0.52±0.10c | |
| N2 | 1 065.4±45.0ab | 7.2±1.6d | 0.062±0.006a | 10.32±0.35bc | 0.46±0.06c | |
| N3 | 1 112.0±29.0a | 8.0±0.0d | 0.057±0.002abc | 9.28±1.03cd | 0.46±0.03c | |
| L3 | N0 | 884.8±21.8cd | 10.0±2.0d | 0.056±0.005abc | 9.24±1.78cd | 0.52±0.08c |
| N1 | 857.6±116.0d | 6.0±2.0d | 0.060±0.002ab | 7.89±1.05d | 0.43±0.05c | |
| N2 | 865.2±135.2d | 8.0±1.3d | 0.053±0.004cd | 9.33±0.65cd | 0.50±0.08c | |
| N3 | 852.8±111.6d | 16.0±1.3c | 0.047±0.001e | 8.94±0.45cd | 0.87±0.05b | |
| 注:表中数据为平均值±标准误差,小写字母表示同一指标在不同处理之间差异显著(P < 0.05)。Note: the data are presented as means ± standard errors; lowercase letters indicate significant differences between treatments (P < 0.05). | ||||||
表 2为遮阴和氮素梯度处理下芒萁的光合色素含量。L1处理下,芒萁叶片的叶绿素a (chlorophyll a, Chl a)、叶绿素b (chlorophyll b, Chl b)和总叶绿素(total chlorophyll, Ct)含量均随施氮量增加而上升,但差异不显著(P>0.05),同时类胡萝卜素(carotenoid, Car)含量、叶绿素a与叶绿素b的比值(ratio of chlorophyll a and b, Chl a/Chl b)在各施氮处理间变化较小。L2处理下,芒萁叶片的Chl a、Chl b和Ct含量均在N2出现最大值,Car含量和Chl a/Chl b在各施氮处理间变化较小。L3处理下,N3与N0在Chl a、Chl b、Ct和Car的含量差异均达到显著水平(P < 0.05);施氮导致Chl a/Chl b下降。随遮阴程度提高,各氮素处理下芒萁的Chl a和Ct含量均显著增加(P < 0.05);L1和L2各处理的Car含量变化不明显,L3的Car含量则显著高于L1和L2 (P < 0.05);Chl a/Chl b呈现下降趋势,N3处理下降低幅度最大,L3分别比L1和L2低33.7%和28.6%。
| 遮阴处理 Shading treatment |
氮素处理 Nitrogen treatment |
叶绿素a含量 Chl a content/(mg·g-1) |
叶绿素b含量 Chl b content/(mg·g-1) |
总叶绿素含量 Ct content/(mg·g-1) |
类胡萝卜素含量 Car content/(mg·g-1) |
叶绿素a/叶绿素b Chl a/Chl b |
| L1 | N0 | 0.78±0.18e | 0.25±0.06d | 1.03±0.24f | 0.27±0.04cd | 3.13±0.11a |
| N1 | 0.84±0.18e | 0.27±0.05cd | 1.12±0.24ef | 0.23±0.04d | 3.11±0.11ab | |
| N2 | 0.95±0.06de | 0.30±0.01cd | 1.26±0.07def | 0.27±0.02cd | 3.14±0.06a | |
| N3 | 1.09±0.09cde | 0.35±0.04cd | 1.44±0.13cdef | 0.28±0.01cd | 3.09±0.1ab | |
| L2 | N0 | 1.26±0.28cd | 0.44±0.10cd | 1.70±0.38cde | 0.28±0.03cd | 2.85±0.02abc |
| N1 | 1.38±0.30c | 0.48±0.11cd | 1.86±0.41c | 0.29±0.03cd | 2.86±0.11abc | |
| N2 | 1.42±0.11c | 0.52±0.05c | 1.94±0.16c | 0.30±0.02c | 2.76±0.07bc | |
| N3 | 1.36±0.13c | 0.47±0.04cd | 1.83±0.17cd | 0.28±0.03cd | 2.87±0.04abc | |
| L3 | N0 | 1.96±0.15b | 0.75±0.09b | 2.71±0.24b | 0.38±0.02b | 2.62±0.10cd |
| N1 | 2.23±0.20ab | 1.01±0.25a | 3.24±0.44ab | 0.43±0.03ab | 2.29±0.36de | |
| N2 | 2.30±0.05ab | 0.97±0.05ab | 3.27±0.09ab | 0.45±0.00a | 2.38±0.06d | |
| N3 | 2.38±0.06a | 1.19±0.20a | 3.57±0.26a | 0.46±0.01a | 2.05±0.29e | |
| 注:表中数据为平均值±标准误差,小写字母表示同一指标在不同处理之间差异显著(P < 0.05)。Note: the data are presented as means ± standard errors; lowercase letters indicate significant differences between treatments (P < 0.05). | ||||||
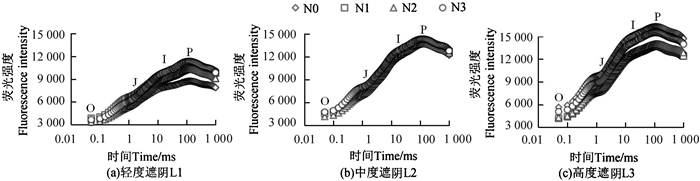
遮阴和氮素梯度处理下芒萁的叶绿素荧光诱导曲线如图 5所示。不同处理下,芒萁叶片的叶绿素荧光诱导曲线均具有O、J、I、P的典型特征位点,随遮阴程度提高,F呈上升趋势。L1处理下,各施氮处理的F大小变化为N1>N3>N2>N0,可知施氮处理后芒萁叶片获得更大的荧光产量。L2处理下,各施氮处理的F在I点后趋同,FP的差异仅为3.88%。L3处理下,芒萁F大小为N0>N3>N2>N1,N0从O点开始F高于其他处理,施氮影响了芒萁光系统Ⅱ (photosynthetic system Ⅱ, PSⅡ)反应中心受体侧原初醌受体(primary quinone, QA)的积累。
|
图 5 遮阴和氮素梯度处理对芒萁叶绿素荧光诱导曲线的影响 Fig. 5 Effects of shading and nitrogen concentration gradient on chlorophyll fluorescence induction curve of D. dichotoma |
表 3为遮阴和氮素梯度处理对芒萁VJ、MO和电子传递量子产额的影响,VJ反映照光2 ms时PSⅡ的活性反应中心关闭的程度。L1处理下,N0的VJ最高,N2和N3处理显著降低了VJ (P < 0.05),施氮有利于芒萁PSⅡ的反应中心保持活性。L2和L3处理下,VJ的最小值分别出现在N2和N1,但氮梯度间差异不显著(P>0.05)。MO代表QA被还原的最大速率,L1和L2处理下,N2处理显著降低了芒萁的MO (P < 0.05),此时芒萁的光合反应中心较为活跃;L3N0的MO在各处理中最高,说明该处理下PSⅡ向下游电子传递链传递电子的能力降低。φPo、ψO和φEo反映PSⅡ受体侧的变化,L1处理下,N0的φPo最低,N2和N3处理显著提高了芒萁的φPo (P < 0.05),施氮增强了芒萁PSⅡ原初光能转换能力。L2处理下,φPo差异不显著(P>0.05)。L3处理下,N1和N2的φPo显著高于N0 (P < 0.05)。L1N0的ψO和φEo最小,反应中心吸收的光能用于电子传递的份额较低。随遮阴程度提高,芒萁叶片的ψO先升高后降低。L1N0的φDo在所有处理中最高,芒萁叶片启动了光防御机制,施氮或提高遮阴度均能使芒萁更高效地利用光能。
| 遮阴处理 Shading treatment |
氮素处理 Nitrogen treatment |
J点相对可变荧光VJ | 初始斜率MO | 最大光化学效率φPo | 电子传递效率ψO | 电子传递量子产额φEo | 热耗散量子比率φDo |
| L1 | N0 | 0.495±0.038a | 0.743±0.128abc | 0.622±0.027c | 0.505±0.038e | 0.315±0.037d | 0.378±0.027a |
| N1 | 0.463±0.042abc | 0.745±0.132ab | 0.646±0.029bc | 0.537±0.042cde | 0.348±0.042cd | 0.354±0.029ab | |
| N2 | 0.408±0.020e | 0.534±0.031e | 0.675±0.015ab | 0.592±0.020a | 0.400±0.020a | 0.325±0.015bc | |
| N3 | 0.423±0.031cde | 0.603±0.110cde | 0.675±0.029ab | 0.577±0.031abc | 0.391±0.038abc | 0.325±0.029bc | |
| L2 | N0 | 0.421±0.025de | 0.712±0.155abc | 0.668±0.034ab | 0.579±0.025ab | 0.388±0.035abc | 0.332±0.034bc |
| N1 | 0.402±0.020e | 0.666±0.140bcd | 0.674±0.021ab | 0.598±0.020a | 0.403±0.026a | 0.326±0.021bc | |
| N2 | 0.397±0.017e | 0.562±0.061de | 0.697±0.018a | 0.603±0.017a | 0.420±0.022a | 0.303±0.018c | |
| N3 | 0.421±0.014de | 0.704±0.090abc | 0.669±0.024ab | 0.579±0.014ab | 0.388±0.022abc | 0.331±0.024bc | |
| L3 | N0 | 0.469±0.056ab | 0.823±0.121a | 0.654±0.043bc | 0.531±0.056de | 0.350±0.054bcd | 0.346±0.043ab |
| N1 | 0.436±0.014bcde | 0.722±0.057abc | 0.696±0.028a | 0.564±0.014abcd | 0.393±0.024ab | 0.304±0.028c | |
| N2 | 0.451±0.052abcd | 0.730±0.099abc | 0.695±0.032a | 0.549±0.052bcde | 0.382±0.048abc | 0.305±0.032c | |
| N3 | 0.438±0.017bcde | 0.778±0.048ab | 0.673±0.023ab | 0.562±0.017abcd | 0.379±0.020abc | 0.327±0.023bc | |
| 注:表中数据为平均值±标准误差,小写字母表示同一指标在不同处理之间差异显著(P < 0.05)。Note: the data are presented as means ± standard errors; lowercase letters indicate significant differences between different treatments (P < 0.05). | |||||||
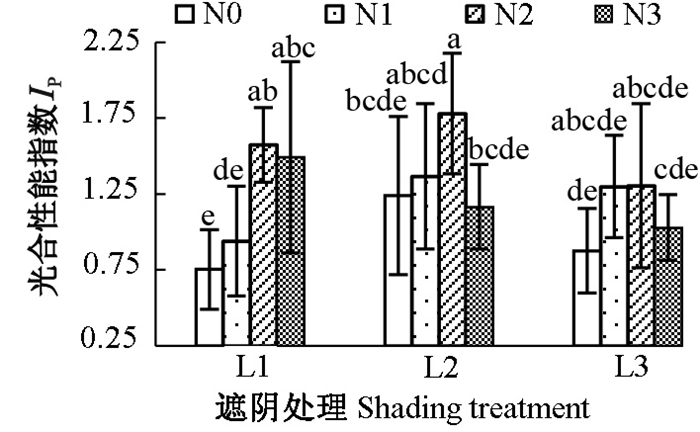
图 6为遮阴和氮素梯度处理对芒萁IP的影响。L1处理下,N2和N3处理芒萁IP显著高于N0 (P<0.05),分别为N0的2.07和1.98倍。L2处理下,IP的差异减小,且与N0相比,但N3的IP出现下降,N2仍有显著提高(P<0.05),且为所有处理的最高值,达到1.78。L3的IP相较L2有所下降,且施氮对芒萁PSⅡ活性的促进作用未达显著水平(P>0.05)。N0、N1和N2三种氮素条件下,随遮阴程度提高,芒萁PSⅡ活性先增强后减弱;N3条件下,芒萁的IP随光照强度减弱而下降。
|
注:小写字母表示同一指标在不同处理之间的差异显著(P < 0.05)。 Note: lowercase letters indicate significant differences between different treatments (P < 0.05). 图 6 遮阴和氮素梯度处理对芒萁光合性能指数的影响 Fig. 6 Effects of shading and nitrogen concentration gradient on performance index of leaves of D. dichotoma |
不同遮阴条件下,施氮对芒萁的光响应进程产生不同程度的影响。L1处理下,施氮增加了芒萁的Pn、Gs和Tr,以N2处理的促进作用最明显。L2处理下,N3的情况与L1不同,随PAR增大,Ci下降幅度最小,且Pn、Gs和Tr均小于N0。L3处理下,N1和N3处理的芒萁Pn下降,弱光环境施氮会对芒萁光利用能力产生负面作用。植物的LSP和LCP是衡量植物光利用能力的重要指标,AQY代表植物的耐荫性[16]。芒萁的LSP在852.8~1 121.6 μmol · m-2 · s-1的范围内变化,LCP在6.0~30.0 μmol · m-2 · s-1的范围内变化,与前期研究结果相近[12, 17]。L1处理下,N2条件对芒萁LSP、AQY和Pnmax的提升最明显,同时使LCP和Rd降低幅度最大,拓宽了芒萁的光照强度生态幅。L2处理下,N2条件同样属于芒萁适宜的土壤肥力条件,与L1N2相比,LSP和Pnmax降低,即强光利用能力稍弱;LCP和Rd显著降低,有利于芒萁在光照强度减弱后维持生长[18],保持较好的碳平衡[19]以积累光合产物。L3处理下,N1增强了芒萁的耐荫性,LCP和Rd为各处理中最低,但同时降低了芒萁的光合潜能,Pnmax为各处理中最低;N3处理的LCP和Rd大幅上升,AQY明显下降,说明芒萁耐荫性下降,可能需要更充足的光照维持光合作用。
3种施氮强度处理下,芒萁的Chl a、Chl b和Ct含量均随遮阴程度的提高而增大,弱光生境中芒萁羽叶需要更多叶绿素以捕获更多的光能。Chl a/Chl b随遮阴程度的提高而降低,高度遮阴显著提高了Car含量,芒萁叶片增强了对蓝紫光的吸收能力,以此适应弱光环境[20];施氮对叶绿素含量的提高有一定促进作用,轻度和中度遮阴下叶绿素含量的提高都有助于芒萁Pn的增大。
叶绿素荧光动力学分析能够反映植物光系统内部的调节过程[21]。L1N0的芒萁荧光强度最低,较强光照下芒萁会出现光抑制现象[22]。施氮处理有效缓解L1处理下芒萁的光抑制,但会降低L3处理下芒萁的荧光强度。未施氮条件下,L1的VJ和φDo最大,φPo、ψO和φEo最小,芒萁光保护能力较弱[23],反应中心吸收的光能较多用来还原QA,PSⅡ向下游传递电子的能力降低[24];芒萁叶片以热能形式耗散过剩激发,从而避免强光伤害。各遮阴条件下,施氮均可降低芒萁的VJ、MO和φDo,利于反应中心数目和活性的增加,同时提高芒萁的φPo、ψO和φEo,即促进PSⅡ电子传递能力和最大光化学效率,优化能量分配和利用效率[25],其中,轻度和中度遮阴下中氮作用最明显,高度遮阴下低氮最佳。IP综合反映光系统活性,相较φPo对环境因子变化的响应更敏感[26],L2N2的IP在各处理中最高,即PSⅡ活性最高;施氮后只有L2N3的IP下降,说明中度遮阴下高氮使芒萁PSⅡ的结构和功能受到伤害[27]。
综上所述,轻度遮阴条件下, 芒萁受到一定的光抑制,此时施氮能有效缓解芒萁的光抑制以及提高芒萁的PSⅡ活性,轻度遮阴与中氮处理组合下芒萁的光照强度生态幅最宽,光合潜力最高。中度遮阴条件下,芒萁的暗呼吸速率较低,施氮优化了芒萁PSⅡ的能量利用效率,中度遮阴与中氮组合处理是最适宜芒萁积累光合产物、PSⅡ活性最高。高度遮阴条件下,施氮引起芒萁净光合速率和叶绿素荧光强度下降,芒萁需要更多光能维持生长。
| [1] |
DUTILLEUL P, HAN L W, VALLADARES F, et al. Crown traits of coniferous trees and their relation to shade tolerance can differ with leaf type:a biophysical demonstration using computed tomography scanning data[J]. Frontiers in Plant Science, 2015, 6: 172. |
| [2] |
吴雅薇, 李强, 豆攀, 等. 氮肥对不同耐低氮性玉米品种生育后期叶绿素含量和氮代谢酶活性的影响[J]. 草业学报, 2017, 26(10): 188-197. |
| [3] |
BOUSSADIA O, STEPPE K, ZGALLAI H, et al. Effects of nitrogen deficiency on leaf photosynthesis, carbohydrate status and biomass production in two olive cultivars 'Meski' and 'Koroneiki'[J]. Scientia Horticulturae, 2010, 123(3): 336-342. |
| [4] |
武姣娜, 魏晓东, 李霞, 等. 植物氮素利用效率的研究进展[J]. 植物生理学报, 2018, 54(9): 1401-1408. |
| [5] |
WANG H Y, WANG Z W, DING R, et al. The impacts of nitrogen deposition on community N:P stoichiometry do not depend on phosphorus availability in a temperate meadow steppe[J]. Environmental Pollution, 2018, 242: 82-89. |
| [6] |
CHEN Z Q, CHEN Z B, YAN X Y, et al. Stoichiometric mechanisms of Dicranopteris dichotoma growth and resistance to nutrient limitation in the Zhuxi watershed in the red soil hilly region of China[J]. Plant and Soil, 2016, 398(1): 367-379. |
| [7] |
王敬哲, 陈志强, 陈志彪, 等. 南方红壤侵蚀区不同植被恢复年限下芒萁叶功能性状对土壤因子的响应[J]. 生态学报, 2020, 40(3): 900-909. |
| [8] |
张明如, 温国胜, 张汝民, 等. 千岛湖森林群落下层芒萁层片发育机理初步判断[J]. 内蒙古农业大学学报, 2010, 31(3): 28-34. |
| [9] |
张明如, 何明, 温国胜, 等. 芒萁种群特征及其对森林更新影响评述[J]. 内蒙古农业大学学报, 2010, 31(4): 303-308. |
| [10] |
任寅榜, 吕茂奎, 江军, 等. 侵蚀退化地植被恢复过程中芒萁对土壤可溶性有机碳的影响[J]. 生态学报, 2018, 38(7): 2288-2298. |
| [11] |
彭扬, 彭培好, 李景吉. 模拟氮沉降对矢车菊属植物Centaurea stoebe种群生长和竞争能力的影响[J]. 植物生态学报, 2016, 40(7): 679-685. |
| [12] |
王佳佳, 张明如, 许焱, 等. 光强和氮素对芒萁光响应及叶绿素荧光参数的影响[J]. 浙江农林大学学报, 2019, 36(6): 1199-1207. |
| [13] |
FARQUHAR G D, VON CAEMMERER S, BERRY J A. Models of photosynthesis[J]. Plant Physiology, 2001, 125(1): 42-45. |
| [14] |
李鹏民, 高辉远, STRASSER R J. 快速叶绿素荧光诱导动力学分析在光合作用研究中的应用[J]. 植物生理与分子生物学学报, 2005, 31(6): 559-566. |
| [15] |
LICHTENTHALER N K. Chlorophylls and carotenoids: pigments of photosynthetic membranes[M]//COLOWICK S P, KAPLAN N O. Methods in Enzymology. San Diego: Academic Press, 1987: 350-382.
|
| [16] |
陆燕元, 马焕成, 李昊民, 等. 土壤干旱对转基因甘薯光合曲线的响应[J]. 生态学报, 2015, 35(7): 2155-2160. |
| [17] |
金桂宏, 张明如, 王立竹, 等. 光强对盆栽芒萁光响应过程与抗氧化酶系统的影响[J]. 浙江农林大学学报, 2018, 35(5): 836-844. |
| [18] |
郭品湘, 尹婷, 粟春青, 等. 遮阴对双色木番茄幼苗生理特性的影响[J]. 森林与环境学报, 2020, 40(1): 76-82. |
| [19] |
殷东生, 沈海龙. 森林植物耐荫性及其形态和生理适应性研究进展[J]. 应用生态学报, 2016, 27(8): 2687-2698. |
| [20] |
廖飞勇, 李鹄鸣. 植物对光强适应机制的研究进展[J]. 经济林研究, 2008, 26(4): 104-108. |
| [21] |
ZHAO J, LANG Y, ZHANG S Y, et al. Photosynthetic characteristics and chlorophyll a fluorescence transient in Lonicera japonica under drought stress[J]. Acta Physiologiae Plantarum, 2019, 41(7): 124. |
| [22] |
ZIVCAK M, BRESTIC M, KALAJI H M, et al. Photosynthetic responses of sun-and shade-grown barley leaves to high light:is the lower PSⅡ connectivity in shade leaves associated with protection against excess of light?[J]. Photosynthesis Research, 2014, 119(3): 339-354. |
| [23] |
KROMDIJK J, GŁOWACKA K, LEONELLI L, et al. Improving photosynthesis and crop productivity by accelerating recovery from photoprotection[J]. Science, 2016, 354(6314): 857-861. |
| [24] |
黄秋娴, 赵顺, 刘春梅, 等. 遮荫处理对铁尾矿基质臭柏实生苗快速叶绿素荧光特性的影响[J]. 林业科学, 2015, 51(6): 17-26. |
| [25] |
HOLLAND V, KOLLER S, BRVGGEMANN W. Insight into the photosynthetic apparatus in evergreen and deciduous European oaks during autumn senescence using OJIP fluorescence transient analysis[J]. Plant Biology, 2014, 16(4): 801-808. |
| [26] |
MA J, LV C F, XU M L, et al. Analysis of chlorophyll a fluorescence and proteomic differences of rice leaves in response to photooxidation[J]. Acta Physiologiae Plantarum, 2017, 39(2): 46. |
| [27] |
李杨, 潘珉, 何锋, 等. 不同底质对海菜花叶绿素荧光诱导动力学参数及净光合速率的影响[J]. 生态学报, 2017, 37(8): 2809-2817. |

 2020, Vol. 40
2020, Vol. 40


