文章信息
- 莫荣海, 丁贵杰, 罗仙英, 陈龙
- MO Ronghai, DING Guijie, LUO Xianying, CHEN Long
- 不同家系马尾松苗木对持续干旱的响应
- Response to sustained drought of seedlings of different families of Pinus massoniana
- 森林与环境学报,2018, 38(4): 473-480.
- Journal of Forest and Environment,2018, 38(4): 473-480.
- http://dx.doi.org/10.13324/j.cnki.jfcf.2018.04.014
-
文章历史
- 收稿日期: 2018-02-07
- 修回日期: 2018-03-30
2. 贵州省森林资源与环境研究中心, 贵州 贵阳 550025
2. Institute for Forest Resources & Environment of Guizhou, Guiyang, Guizhou 550025, China
干旱是严重影响和制约农林发展的重要因素, 研究植物的耐旱机理, 选择耐旱品种、家系或无性系进行培育和推广, 是摆脱干旱影响的有效途径之一。干旱胁迫下, 植物叶片、枝条、主茎、苗高及干物质的积累均受到抑制, 光合速率下降, 细胞膜损伤等, 植物可通过自身的形态生长变化及生理反应来减轻胁迫造成的伤害及适应环境[1-2], 如减缓生长速率, 减少叶片及枝条数[3], 调节细胞渗透物质含量, 增强保护酶活性等来抵御干旱带来的伤害[4]。
马尾松(Pinus massoniana Lamb.)在我国南方分布范围广, 具有速生、丰产、耐瘠薄等优良特性, 是我国南方最主要的用材树种之一[5-6]。贵州是我国南方重要的马尾松用材林产区, 该区域虽年降水量充足, 但时空分布不均且常伴有多发季节性干旱[7], 再加上土壤水分容易下渗、地表蓄水性能弱, 容易造成地表干旱[8], 严重制约马尾松用材林的发展。因此, 对马尾松耐旱家系的选择及抗旱性研究具有十分重要的现实意义。近年来, 一些学者对马尾松苗木的形态生长[7, 9-10]、生理指标[4, 7, 11]和菌根化[12]等方面进行抗旱性研究, 但多数未从家系水平上进行比较和分析, 即使有用家系苗木, 数量也很少, 且研究指标较单一, 结合野外生长表现进行筛选的更少。为此, 通过对21个1年生不同家系马尾松苗进行野外栽培试验, 连续3 a调查其生长状况, 从中初步选出6个生长较优良和存活率较高的马尾松优良家系, 并以这6个优良家系的1年生苗来进行温室土培盆栽模拟干旱环境试验, 比较不同家系的抗旱能力, 为选择马尾松优良耐旱家系进行推广造林及分析适合栽培的水分环境提供一定的理论与生产实践依据。
1 材料与方法 1.1 试验材料供试材料均来源于贵州省都匀市马鞍山林场国家马尾松良种基地, 并经子代测定。在野外田间21个家系连续跟踪测定的基础上, 于2017年3月初, 选择表现较好的6个家系(DF3、DH34、DC2、DH26、DDF4、DY1), 移栽至温室大棚的花盆里, 容器规格为28 cm×20 cm, 土壤用适合马尾松生长的黄壤土, pH值为5.3, 并混入少量的松针, 每盆土量一致, 约8 kg, 然后存放在贵州大学林学院温室大棚内进行管护。试验前缓苗期为45 d, 并适时补水。
1.2 试验设计试验采取随机区组设计, 设6个家系水平, 每个家系24盆, 每盆3株, 共72株。2017年4月21日, 开始做胁迫处理, 处理前给苗木浇透水, 自然干旱一直持续35 d。分别在试验处理的第0、7、14、21、28、35天的相同时间点测定每株苗高和地径, 同时取6株长势均匀的苗木进行各项指标测定, 各指标重复测定3次。在每个测定时间点上, 测得的土壤相对含水量分别为100%、70.6%、48.3%、35.2%、28.7%、19.2%, 对应干旱等级为湿润、轻微干旱、中度干旱、重度干旱、极重度干旱、极端干旱。
1.3 测定指标与方法用钢卷尺测定苗高, 精确到0.1 cm; 游标卡尺测定地径, 精确到0.01 mm。用整株烘干称重法计算生物量, 各家系最终干物质积累量=第35天的总生物量-第0天的总生物量。叶绿素含量的测定采用直接浸提法[13]; 超氧化物歧化酶(superoxide dismutase, SOD)活性测定采用氮蓝四唑(nitroblue tetrazolium, NBT)法, 过氧化物酶(peroxidase, POD)活性测定采用愈创木酚比色法[14]; 游离脯氨酸(free proline, Pro)含量测定采用酸性茚三酮显色法[15]; 可溶性糖含量测定采用蒽酮比色法[14]; 丙二醛(malonaldehyde, MDA)含量测定采用硫代巴比妥酸(thiobarbituric acid, TBA)法[15]。
1.4 数据处理与分析数据用Excel 2016软件进行计算作图, SPSS 20.0进行方差分析。采用模糊隶属函数法比较各家系的抗旱能力, 用灰色关联分析法计算关联度。
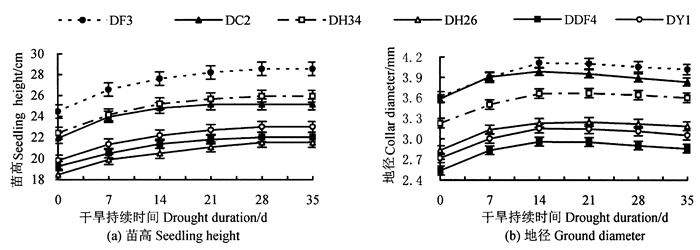
2 结果与分析 2.1 持续干旱对不同家系马尾松苗木生长指标的影响持续干旱胁迫下, 不同家系马尾松苗木苗高、地径变化如图 1所示。随干旱加剧, 6个家系马尾松苗木苗高、地径生长均变缓, 直至停止。从图 1 (a)可知, DC2家系苗高在干旱前期生长最快, 但随干旱时间延长, 最先呈生长缓慢及停止生长的现象。处理结束时, DF3家系苗高增幅与DDF4、DC2、DH26、DY1家系差异显著(P < 0.05), DH34与DDF4差异显著(P < 0.05), 其中, DF3和DH34家系苗高增幅最大, 分别为4.06和3.50 cm, DDF4家系增幅最小, 为2.73 cm, DC2、DH26、DY1家系苗高增幅无显著差异, 分别为3.18、3.04、3.17 cm。从图 1(b)可知, 在干旱0~14 d, DC2, DF3家系地径生长量与其它4个家系差异显著(P < 0.05);干旱14 d后, DC2家系地径生长先受到抑制, 地径生长量明显下降, 其它5个家系在干旱21 d后地径生长量才明显下降; 第35天, DF3家系地径增长量最大, 为0.40 mm, DC2家系最小, 为0.25 mm。各家系地径总增长量比较小, 可能是因为在干旱胁迫后期, 苗木失水严重, 地径生长量的积累受到严重抑制。
|
图 1 持续干旱胁迫下不同家系马尾松苗木苗高、地径的变化 Fig. 1 Seedling height and ground diameter change of different families under continuous drought stress |
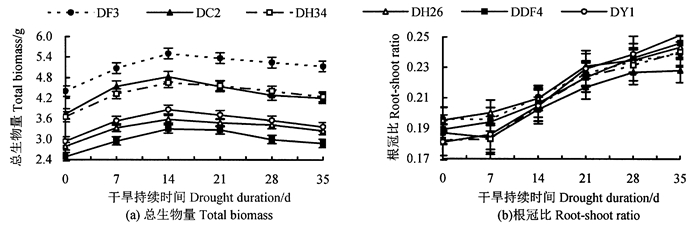
持续干旱胁迫下不同家系马尾松苗木总生物量、根冠比的变化如图 2所示, 在不同程度干旱胁迫下, 各家系根冠比和DDF4、DY1家系总生物量积累存在显著差异(P < 0.05)。由图 2 (a)可知, 随干旱加剧, 6个家系马尾松苗木总生物量积累均呈先升后降趋势, 这可能是因为在干旱前期至中期, 苗木生长受抑制较小, 生物量合成大于消耗, 有一定的积累, 而在干旱后期, 生长受抑制, 生物量消耗大于合成, 造成生物量减少。由图 2(b)可知, 根冠比在干旱前期变化不明显, 在干旱中期至后期, 根冠比随干旱加剧不断增大, 表明在此时期干旱胁迫抑制苗木地上部分生长比地下部分更显著。胁迫结束后, DF3家系最终干物质积累量最大, 达0.72 g, 与DC2、DH26、DY1和DDF4家系存在显著差异(P < 0.05), DDF4家系最小, 为0.39 g, DH34家系最终干物质积累量与DY1和DDF4家系存在显著差异(P < 0.05)。
|
图 2 持续干旱胁迫下不同家系马尾松苗木总生物量、根冠比的变化 Fig. 2 Total biomass and root-shoot ratio change of different families under continuous drought stress |
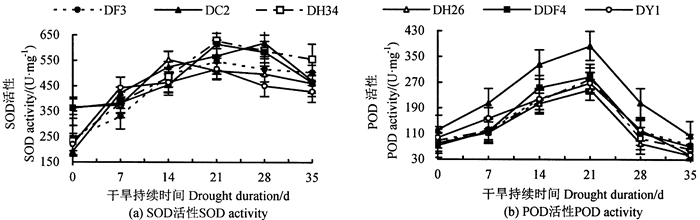
持续干旱胁迫下不同家系马尾松苗木SOD、POD活性如图 3所示, 6个家系SOD、POD活性均随干旱胁迫加剧呈先升后降趋势。0~7 d, 保护酶系统开始响应, DC2、DH34、DY1家系SOD活性上升较大; 7~14 d, DH26家系SOD活性上升较快, 与DDF4、DY1家系差异显著(P < 0.05);第21天, DF3、DH34、DDF4、DY1家系SOD活性上升到最大值; 第28天, DY1家系SOD活性与DC2、DDF4、DH34这3个家系差异均显著(P < 0.05);28~35 d, 6个家系SOD活性均下降, 其中DC2家系下降幅度最大; 第35天, DY1家系SOD活性与DC2、DDF4、DH34这3个家系差异显著(P < 0.05), DY1家系活性保持最低, DH34家系活性最高。第7天, DC2与DH26家系的POD活性差异极显著(P < 0.01), 与DF3、DH34、DDF4家系的POD活性差异显著(P < 0.05);14~21 d, 各家系POD活性升到最大, 第14、21天, DC2与DH26家系的POD活性差异极显著(P < 0.01), 与DF3、DH34、DY1家系的POD活性差异显著(P < 0.05), DF3和DC2家系POD活性仍较高, 与其余家系差异极显著(P < 0.01);第35天, DC2家系POD活性与DF3家系差异显著(P < 0.05), 与其余家系差异极显著(P < 0.01), 此时, DC2家系POD活性增幅最大, 为279.05 U·mg-1, DF3家系最小, 为194.94 U·mg-1。总体看, 随干旱加剧, 各家系通过提高SOD、POD活性来清除植物体产生的自由基, 以适应干旱环境。
|
图 3 持续干旱胁迫下不同家系马尾松苗木SOD和POD活性的变化 Fig. 3 SOD and POD activitiy change of different families under continuous drought stress |
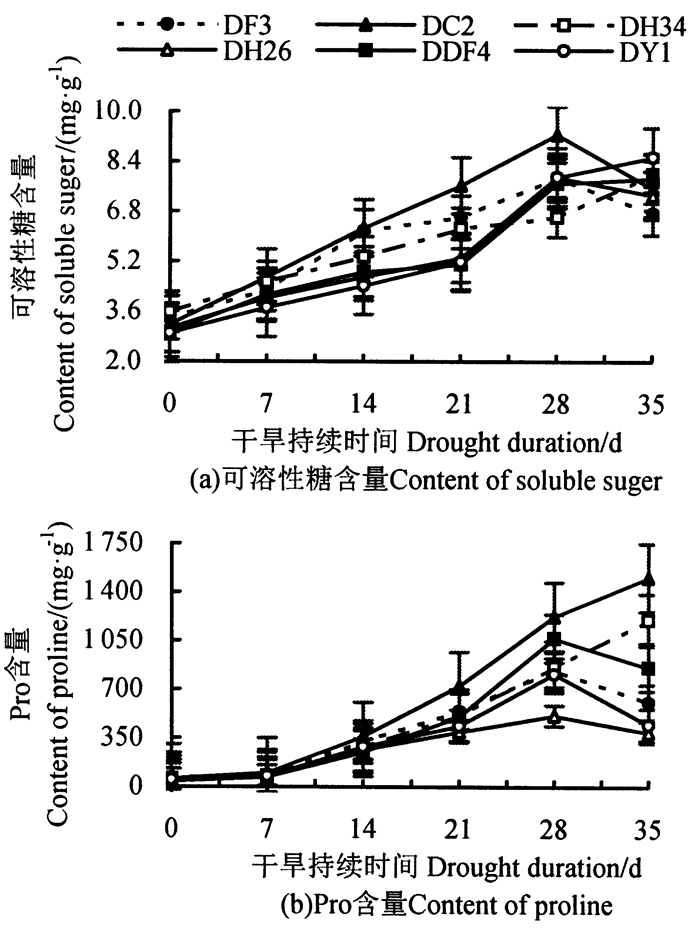
持续干旱胁迫下不同家系马尾松苗木可溶性糖和Pro含量的变化如图 4所示。从图 4可知, 随干旱加剧, DH34、DDF4、DY1家系可溶性糖含量持续上升, DF3、DC2、DH26家系先升后降, DC2和DH34家系Pro含量在整个干旱过程中持续上升, 其余家系先升后降, 6个家系可溶性糖、Pro含量在不同干旱胁迫下存在极显著差异(P < 0.01)。由图 4 (a)可知, 7~14 d, DF3家系可溶性糖含量开始显著上升, DF3、DC2与DH26、DDF4、DY1家系均存在极差异显著(P < 0.01), 7~28 d, DC2家系对干旱响应迅速, 可溶性糖含量上升显著, 均保持最高; 28~35 d, DH34家系上升最快, 在极重度干旱后期大量增加来抵御干旱胁迫的伤害, DC2家系大幅下降, 这可能是因为此时干旱胁迫对其产生很严重的伤害。处理结束时, DC2家系可溶性糖含量增幅最大, 为6.08 mg·g-1, DH34家系最小, 为4.34 mg·g-1。由图 4(b)可知, 0~14 d, 各家系Pro含量上升不大, 差异不显著; 14~21 d, DC2家系上升最明显, 第21天, DC2与DH34、DH26、DY1家系差异极显著(P < 0.01), 且21 d后DC2家系Pro含量比其它家系大; 第28天, DF3、DH26、DDF4、DY1家系Pro含量达到最大, 之后呈下降趋势; 第35天, DC2和DH34家系Pro含量达到最大, 此时, DC2家系Pro含量上升最大(25.27倍), 这可能是因为干旱胁迫对DC2家系伤害最大, 从而产生更多的Pro。
|
图 4 持续干旱胁迫下不同家系马尾松苗木可溶性糖和Pro含量变化 Fig. 4 Soluble sugar and Pro content change of different families under continuous drought stress |
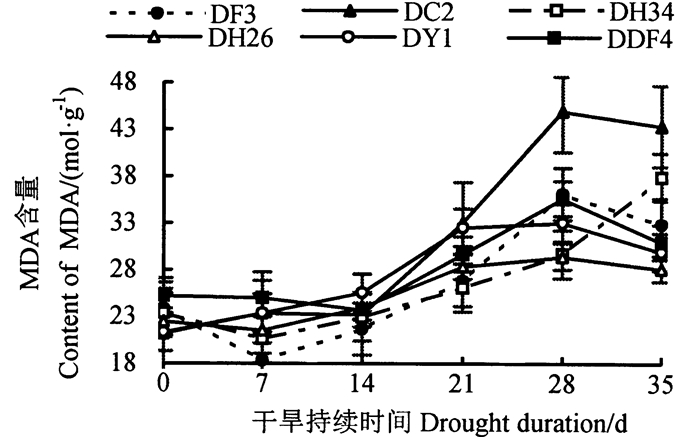
持续干旱胁迫下不同家系马尾松苗木MDA含量的变化情况如图 5所示, 6个家系均发生膜脂过氧化, 各家系MDA含量均上升。0~14 d, 各家系MDA含量变化较小, 表明此时期膜系统未受到损伤; 14~28 d, 各家系MDA含量均升高, 出现膜脂过氧化, DF3、DC2、DH26、DDF4、DY1家系上升到最大, 第28天, DC2家系与其余家系差异均极显著(P < 0.01);28~35 d, DH34家系MDA含量上升到最大, 与DF3、DH26、DDF4、DY1家系差异达极显著水平(P < 0.01), 第35天, DC2家系与DF3、DDF4、DY1家系差异极显著(P < 0.01), 与DH34家系差异显著(P < 0.05)。处理结束时, DC2家系MDA含量增幅最大, 为23.72 mol·g-1, DH26家系最小, 为6.94 mol·g-1。
|
图 5 持续干旱胁迫下不同家系马尾松苗木MDA含量变化 Fig. 5 MDA content change of different families under continuous drought stress |
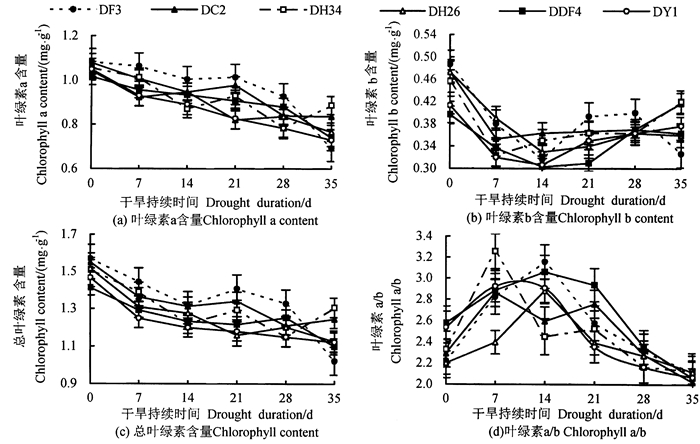
持续干旱胁迫下不同家系马尾松苗木叶绿素a、叶绿素b、总叶绿素含量和叶绿素a/b值的变化如图 6所示, 随干旱加剧, 各家系叶绿素a、叶绿素b、总叶绿素含量和叶绿素a/b值均下降, 在不同干旱胁迫下存在显著差异(P < 0.05)。DF3、DC2和DH26家系叶绿素a随干旱加剧呈先降后升又降的趋势, DH34家系从第7天后呈先降后升又降又升的趋势, DDF4、DY1家系一直呈下降趋势, 其中, DF3家系降幅最大, 达36.00%, DH34家系最小, 为16.09%。DF3、DDF4家系叶绿素b呈先降后升又降的趋势, DH26、DY1、DC2、DH34家系呈先降后升的趋势, 其中, DF3家系降幅最大, 为32.87%, DH34家系最小, 为8.04%。各家系总绿素的变化趋势与叶绿素a变化趋势一致, 叶绿素a/b值呈先升后降趋势, DC2、DH34、DY1家系在第7天上升到最大, DF3、DH26、DDF4家系在第14天升到最大, 整个干旱过程中, DDF4家系叶绿素a/b值降幅最大, 为19.92%, DH26家系最小, 为3.78%。
|
图 6 持续干旱胁迫下不同家系马尾松苗木叶绿素的变化 Fig. 6 Change of chlorophyll of different families under continuous drought stress |
干旱胁迫影响植物生长及生理生化特性, 植物的抗旱性是一个复合性状[4], 因此, 对各家系各指标进行模糊隶属函数分析, 选择苗高、地径、总生物量、根冠比、干物质积累量、可溶性糖含量、Pro含量、SOD活性、POD活性、MDA含量以及叶绿素等指标来比较不同家系的抗旱能力, 计算14个指标的隶属度平均值, 如该值越大, 表明抗旱性越强。各家系马尾松抗旱指标隶属函数值如表 1所示, 6个家系抗旱性大小为:DY1>DH26>DDF4>DH34>DF3>DC2。
| 家系 Family |
隶属函数值Subordinate function value | 抗旱排序 Order |
||||||||||||||
| 叶绿素a含量 Chlorophyll a content |
叶绿素b含量 Chlorophyll b content |
总叶绿素含量 Total chlorophyll content |
叶绿素a/b Chlorophyll a/b |
Pro含量 Pro content |
可溶性糖含量 Soluble sugar content |
MDA含量 MDA content |
POD活性 POD activity |
SOD活性 SOD activity |
苗高 Seedling height |
地径 Ground diameter |
干物质积累量 Dry matter accumulation |
总生物量 Total biomass |
根冠比 Root-shoot ratio |
平均值 Mean value |
||
| DF3 | 0.565 | 0.508 | 0.500 | 0.420 | 0.495 | 0.490 | 0.533 | 0.468 | 0.475 | 0.498 | 0.438 | 0.360 | 0.446 | 0.529 | 0.480 | 5 |
| DC2 | 0.475 | 0.520 | 0.450 | 0.500 | 0.462 | 0.497 | 0.480 | 0.482 | 0.513 | 0.348 | 0.387 | 0.365 | 0.456 | 0.464 | 0.457 | 6 |
| DH34 | 0.482 | 0.438 | 0.468 | 0.538 | 0.530 | 0.455 | 0.483 | 0.467 | 0.532 | 0.418 | 0.473 | 0.513 | 0.511 | 0.462 | 0.481 | 4 |
| DH26 | 0.480 | 0.493 | 0.483 | 0.507 | 0.465 | 0.477 | 0.498 | 0.478 | 0.537 | 0.427 | 0.498 | 0.520 | 0.520 | 0.475 | 0.490 | 2 |
| DDF4 | 0.460 | 0.500 | 0.480 | 0.518 | 0.493 | 0.512 | 0.528 | 0.453 | 0.557 | 0.457 | 0.436 | 0.439 | 0.568 | 0.438 | 0.489 | 3 |
| DY1 | 0.577 | 0.485 | 0.557 | 0.548 | 0.488 | 0.527 | 0.525 | 0.442 | 0.510 | 0.402 | 0.476 | 0.488 | 0.537 | 0.465 | 0.502 | 1 |
灰色关联分析是分析不同因素间关联程度大小的一种量化分析方法, 利用各抗旱指标均值与抗旱隶属函数均值两因素间进行灰色关联分析, 计算两因素间的关联程度, 如关联度越大, 则表明该指标与抗旱性的关系越密切[7]。通过计算各家系抗旱指标均值和隶属函数平均值, 并对其进行标准化处理, 即可获得表 2计算结果。由表 2得出各指标与抗旱性关联度的大小排序为:根冠比>叶绿素b含量>SOD活性>总生物量>苗高>Pro含量>干物质积累量>叶绿素a/b>叶绿素a含量>总叶绿素含量>MDA活性>地径>可溶性糖含量>POD活性, 这表明根冠比对不同家系马尾松苗木的抗旱性影响较大, 而POD活性对不同家系马尾松苗木抗旱性的影响相对较小。
| 家系 Family |
关联系数 Correlative modulus | |||||||||||||
| 干物质积累量 Dry matter accumulation |
总生物量 Total biomass |
苗高 Seedling height |
地径 Ground diameter |
根冠比 Root-shoot ratio |
POD活性 POD activity |
SOD活性 SOD activity |
叶绿素a含量 Chlorophyll a content |
叶绿素b含量 Chlorophyll b content |
总叶绿素含量 Total chlorophyll content |
叶绿素a/b Chlorophyll a/b |
Pro含量 Pro content |
可溶性糖含量 Soluble sugar content |
MDA含量 MDA content |
|
| DF3 | 0.556 | 0.826 | 0.598 | 0.931 | 0.587 | 0.890 | 0.385 | 0.541 | 0.513 | 0.504 | 0.547 | 0.798 | 0.843 | 0.456 |
| DC2 | 0.729 | 0.616 | 0.679 | 0.566 | 0.470 | 0.438 | 0.463 | 0.904 | 0.933 | 0.899 | 0.620 | 0.350 | 0.428 | 0.947 |
| DH34 | 0.917 | 0.942 | 0.953 | 0.588 | 0.941 | 0.701 | 0.590 | 0.776 | 1.000 | 0.912 | 0.960 | 0.462 | 0.504 | 0.690 |
| DH26 | 0.435 | 0.808 | 0.503 | 0.360 | 0.380 | 0.447 | 0.468 | 0.435 | 0.456 | 0.398 | 0.526 | 0.582 | 0.421 | 0.758 |
| DDF4 | 0.548 | 0.350 | 0.441 | 0.474 | 0.759 | 0.469 | 0.922 | 0.389 | 0.387 | 0.441 | 0.395 | 0.993 | 0.574 | 0.736 |
| DY1 | 0.377 | 0.412 | 0.380 | 0.644 | 0.463 | 0.474 | 0.720 | 0.520 | 0.502 | 0.507 | 0.465 | 0.807 | 0.556 | 0.334 |
| 关联度 Correlative degree |
0.593 7 | 0.658 8 | 0.592 4 | 0.593 8 | 0.600 2 | 0.569 9 | 0.591 4 | 0.594 2 | 0.631 7 | 0.610 2 | 0.585 5 | 0.665 4 | 0.554 5 | 0.653 7 |
| 关联序 Correlative order |
9 | 2 | 10 | 8 | 6 | 13 | 11 | 7 | 4 | 5 | 12 | 1 | 14 | 3 |
研究表明, 随干旱加剧, 植物通过减少叶密度、叶面积、枝条总长度和总数量等来降低蒸腾失水, 以增强植物自身抗旱性, 同时, 苗高生长量、地径生长量、生物量积累受到的抑制作用变大, 根冠比增大[3-4, 9]。在重度干旱下, 根系生长减缓甚至停止, 根的吸水能力降低, 蒸腾大幅度下降[16]。在干旱前期, 由于土壤含水量高, 苗木生长没有受到明显抑制, 苗高、地径生长较快, 生物量积累较大, 随干旱加剧, 苗木出现水分亏缺, 生长开始受到抑制, 苗高、地径生长和生物量积累减缓, 在极端干旱后期, 苗木水分亏缺更加严重, 生长受到严重抑制, 苗高、地径生长和生物量积累趋于停止, 同时地径大小在干旱后期稍微偏小, 可能是因为主茎干枯缩水。因此, 长期干旱胁迫将会抑制植物生长, 造成植物减产甚至死亡。
3.2 不同家系马尾松苗木在持续干旱下的生理响应POD、SOD作为植物的抗氧化性酶, 对植物细胞起保护作用[12]; MDA是衡量膜质过氧化的一个重要指标, 能反映膜系统受损伤程度[14, 17-19]; Pro与可溶性糖作为植物的渗透调节物质, 对植物的渗透性起到调节作用。研究表明, 在干旱初期, 植物通过增加POD、SOD酶活性保护自身不受胁迫伤害, 随干旱加剧, POD、SOD活性开始下降, 自由基大量积累, 植物膜系统受到损伤, MDA、Pro、可溶性糖含量逐渐升高, 以此来维持细胞水势, 减轻胁迫伤害[3, 7, 20-23]。水分胁迫抑制叶绿素合成, 迫使叶绿素降解, 诱导叶绿体发生膜质过氧化, 产生活性氧和MDA, 并对叶绿素造成破坏, 使叶绿素质量分数下降, 使植物光合作用受到抑制[11, 24-25]。在干旱0~14 d, 各家系SOD、POD活性开始上升, MDA、Pro与可溶性糖含量变化幅度较小; 在干旱14~21 d, 除DH26家系以外, 其余家系SOD、POD活性仍持续上升, MDA开始积累, 说明此时自由基大量产生, 由于保护酶活性未能及时全部清除, 过多的自由基对膜系统产生伤害, 出现膜脂过氧化, 同时, Pro与可溶性糖含量上升趋势明显, 细胞吸水能力及渗透调节增强, 以此来抵御干旱对细胞的损害; 在干旱21~28 d, 除DC2家系以外, 其余家系SOD、POD活性开始下降, 导致氧自由基未能及时清除而大量产生, 膜系统受损伤程度加剧, 膜质过氧化加重, MDA含量持续上升; 在干旱28~35 d, 细胞水分亏缺严重, 导致其结构功能受损, 生理机能下降, 除DH34外, 6个家系SOD、POD活性持续下降, 大部分家系MDA也出现下降, 这可能是因为自由基减少, 膜质过氧化减弱, 导致MDA也出现下降, 此时, 马尾松为了维持机体生命活动, Pro和可溶性糖含量持续大量积累, 进一步增强细胞吸水能力以及渗透调节, 减轻膜渗透的伤害。在干旱0~7 d, 6个家系马尾松苗木总叶绿素、叶绿素a、叶绿素b含量均下降, 可能是因为在干旱前期水分减少较快, 植物用来合成叶绿素的水分变少, 合成受阻; 在干旱7~35 d, 部分家系总叶绿素、叶绿素a、叶绿素b含量下降, 可能是因为干旱胁迫抑制叶绿素的合成, 使其降解速率加大, 而部分家系含量上升, 可能是因为在一定干旱条件下, 植物为避免因水分亏缺导致自身受到损伤, 通过提高叶绿素含量来适应环境, 以此来增强自身的抗旱性。随干旱加剧, 6个家系叶绿素a/b值总体上呈现出先升后降趋势, 可能是因为干旱后期叶绿素的合成受阻, 导致该比值下降。
4 结论持续干旱下, 6个家系马尾松苗木苗高生长量、地径生长量及生物量积累均受到不同程度的抑制。随干旱加剧, 苗高生长量、地径生长量、生物量积累减缓, 在重度到极端干旱后期, 根冠比增大, 苗木生长停止, 部分逐渐枯死。随干旱加剧, 叶绿素合成受阻, 部分家系叶绿素含量下降, 而部分家系上升, 6个家系叶绿素a/b值总体上呈现出先升后降趋势。在轻度到中度干旱下(7~14 d), 保护酶系统在马尾松苗木抵御干旱胁迫上发挥主要作用, 在中度到重度干旱下(14~21 d), 保护酶系统和渗透调节物质共同发挥主要作用来抵御干旱胁迫, 在重度到极重度干旱下(21~35 d), 渗透调节物质在马尾松应对干旱胁迫上发挥主要作用。
综合评价可知, DY1家系耐旱性最高, DH26家系其次, DDF4和DH34家系耐旱性适中, DF3家系较低, DC2家系耐旱能力最低。这可能是由于不同家系的遗传特性不同所致, 也可能与它们的苗木形态(苗高、地径、根系)有一定关系, 具体是什么原因导致它们具有不同的耐旱能力, 还有待做更深入的系统研究。
| [1] | AROCA R. Plant responses to drought stress[M]. Berlin: Springer, 2012. |
| [2] | 吴金山, 张景欢, 李瑞杰, 等. 植物对干旱胁迫的生理机制及适应性研究进展[J]. 山西农业大学学报(自然科学版), 2017, 37(6): 452–456. DOI:10.3969/j.issn.1671-8151.2017.06.014 |
| [3] | 黄华, 梁宗锁, 韩蕊莲. 持续干旱胁迫对女贞形态与生长的影响[J]. 林业科学, 2008, 44(8): 145–148. DOI:10.3321/j.issn:1001-7488.2008.08.026 |
| [4] | 黄承玲, 陈训, 高贵龙. 3种高山杜鹃对持续干旱的生理响应及抗旱性评价[J]. 林业科学, 2011, 47(6): 48–55. |
| [5] | 丁贵杰, 周志春, 王章荣. 马尾松纸浆用材林培育与利用[M]. 北京: 中国林业出版社, 2006. |
| [6] | 周政贤. 中国马尾松[M]. 北京: 中国林业出版社, 2001. |
| [7] | 杜明凤, 丁贵杰, 赵熙州. 不同家系马尾松对持续干旱的响应及抗旱性[J]. 林业科学, 2017, 53(6): 21–29. |
| [8] | 张和喜.贵州区域干旱演变特征及预测模型研究[D].沈阳: 沈阳农业大学, 2013. |
| [9] | 胡晓健, 欧阳献, 喻方圆. 干旱胁迫对不同种源马尾松苗木生长及生物量的影响[J]. 江西农业大学学报, 2010, 32(3): 510–516. DOI:10.3969/j.issn.1000-2286.2010.03.018 |
| [10] | KHANNA S M, TAXAK P C, JAIN P K, et al. Glycolytic enzyme activities and gene expression in Cicer arietinum exposed to water-deficit stress[J]. Applied Biochemistry and Biotechnology, 2014, 173(8): 2 241–2 253. |
| [11] | 唐小平.水分胁迫对草莓光合作用的影响[D].长沙: 湖南农业大学, 2008. |
| [12] | 王艺, 丁贵杰. 马尾松菌根化苗木对干旱的生理响应及抗旱性评价[J]. 应用生态学报, 2013, 24(3): 639–645. |
| [13] | 张宪政. 植物叶绿素含量测定:丙酮乙醇混合液法[J]. 辽宁农业科学, 1986(3): 26–28. |
| [14] | 张治安, 张美善, 蔚荣海. 植物生理学实验指导[M]. 北京: 中国农业科学技术出版社, 2004. |
| [15] | 郝建军, 康宗利, 于洋. 植物生理学实验技术[M]. 北京: 化学工业出版社, 2007. |
| [16] | HUANG B R, FRY J D. Root anatomical, physiological, and morphological responses to drought stress for tall fescue cultivars[J]. Crop Science, 1998, 38(4): 1 017–1 022. DOI:10.2135/cropsci1998.0011183X003800040022x |
| [17] | 陈贵, 胡文玉, 谢甫绨, 等. 提取植物体内MDA的溶剂及MDA作为衰老指标的探讨[J]. 植物生理学通讯, 1991, 27(1): 44–46. |
| [18] | DOUNAVI A, NETZER F, CELEPIROVIC N, et al. Genetic and physiological differences of European beech provenances (F. sylvatica L.) exposed to drought stress[J]. Forest Ecology and Management, 2016, 361: 226–236. |
| [19] | LIU C C, LIU Y G, GUO K, et al. Effect of drought on pigments, osmotic adjustment and antioxidant enzymes in six woody plant species in Karst habitats of southwestern China[J]. Environmental and Experimental Botany, 2011, 71(2): 174–183. DOI:10.1016/j.envexpbot.2010.11.012 |
| [20] | 袁小凤, 施积炎, 丁贵杰. 不同种源马尾松幼苗对水分胁迫的生理响应[J]. 浙江林学院学报, 2008, 25(1): 42–47. DOI:10.3969/j.issn.2095-0756.2008.01.009 |
| [21] | 崔豫川, 张文辉, 李志萍. 干旱和复水对栓皮栎幼苗生长和生理特性的影响[J]. 林业科学, 2014, 50(7): 66–73. |
| [22] | 宋丽梅, 代微然, 任健, 等. 干旱胁迫及复水处理对百脉根叶片丙二醛含量及抗氧化酶活性的影响[J]. 云南农业大学学报, 2014, 29(1): 37–42. DOI:10.3969/j.issn.1004-390X(n).2014.01.008 |
| [23] | NGUYEN-QUEYRENS A, BOUCHET-LANNAT F. Osmotic adjustment in three-year-old seedlings of five provenances of maritime pine (Pinus pinaster) in response to drought[J]. Tree Physiology, 2003, 23(6): 397–404. DOI:10.1093/treephys/23.6.397 |
| [24] | 李莉, 钟章成, 缪世利, 等. 诸葛菜对水分胁迫的生理生化反应和调节适应能力[J]. 西南师范大学学报(自然科学版), 2000, 25(1): 33–37. DOI:10.3969/j.issn.1000-5471.2000.01.009 |
| [25] | 赵静, 张世民, 张雷, 等. 水分胁迫对棉花叶绿素含量的影响[J]. 天津农业科学, 2017, 23(6): 5–8. DOI:10.3969/j.issn.1006-6500.2017.06.002 |

 2018, Vol. 38
2018, Vol. 38


