2. 大洋渔业资源可持续开发教育部重点实验室, 上海 201306;
3. 国家远洋渔业工程技术研究中心, 上海 201306;
4. 农业农村部大洋渔业开发重点实验室, 上海 201306
太平洋褶柔鱼(Todarodes pacificus)广泛分布在日本海、太平洋沿岸以及我国的黄海和东海海域[1]。作为重要的大洋性经济头足类, 它是日本、韩国、中国和俄罗斯重要的商业开发物种之一, 商业开发始于20世纪60年代, 并在60和90年代捕捞产量出现过2次高峰期, 这4个国家的年总产量为70万t, 其中底拖网和围网等捕捞方式占比达60%[2]。21世纪初, 由于海洋环境的变化, 产卵场水温异常, 太平洋褶柔鱼资源量逐年减少, 产量呈大幅度下降趋势。
根据产卵时间可将太平洋褶柔鱼分为3个种群, 即夏生群体、秋生群体和冬生群体, 其中冬生群的数量最大。冬生群体产卵场主要分布在日本九州西南部东海大陆架外缘区域, 密集区在东海东北部。随季节变化, 夏季北上索饵, 秋冬季南下产卵洄游。其卵孵化温度为14~26℃, 最佳适宜温度为14.7~22.2℃[3]。吴梦瑶等[4]选择平均海表面温度(sea surface temperature, SST)利用Schaefer模型和Fox模型对太平洋褶柔鱼秋生群渔获量进行分段评估。谢恩阁等[5]建立基于产卵场和索饵场SST的Schaefer模型分析SST对太平洋褶柔鱼冬生群资源量的影响。汪金涛等[6]对基于产卵场和索饵场SST的Schaefer剩余产量模型进行比较与分析。以上评估模型主要从资源量角度进行分析, 对环境与物种的生物参数涉及较少[7]。为此, 将考虑影响其资源丰度的关键环境因子, 结合贝叶斯方法构建基于环境因子的剩余产量模型, 评估太平洋褶柔鱼资源状况, 为其资源可持续利用提供参考。
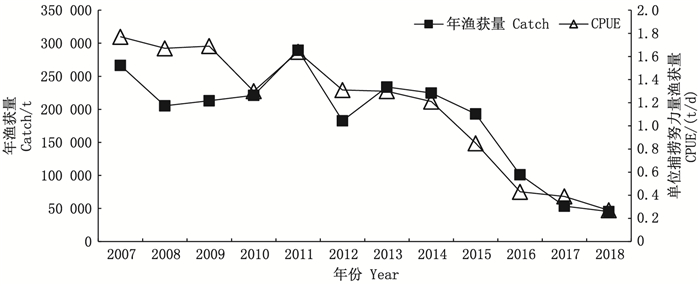
1 材料与方法 1.1 数据来源2007—2018年太平洋褶柔鱼冬生群年资源丰度(catch per unit effort, CPUE)数据来自加賀敏樹等[8]的2019年太平洋褶柔鱼冬生群资源评估报告(图 1)(http://abchan.fra.go.jp/digests2019/html/2019_18.html)。SST来自OceanWatch网站(https://oceanwatch.pifsc.noaa.gov/erddap/griddap/CRW_sst_v1_0_monthly.html), 时间为2007—2018年1—3月, 空间范围为25°N~45°N和125°E~145°E海域, 时间分辨率为月, 空间分辨率为0.5°×0.5°。
|
图 1 2007—2018年太平洋褶柔鱼冬生群CPUE的年间变动 Fig. 1 Inter-annual changes in the CPUE of the winter-spawning cohort for Todarodes pacificus from 2007 to 2018 |
太平洋褶柔鱼冬生群产卵场SST范围为18~26℃, 最适产卵SST范围为14.7~22℃[9]。据此计算2007—2018年1—3月各月最适产卵温度面积占总产卵场面积比例(Ps):
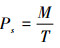
式中: M为产卵场最适温度范围的面积; T为产卵场总面积。
1.2.2 剩余产量模型假设SST对太平洋褶柔鱼种群的环境容纳量K和内禀自然增长率r起着关键性作用[10], 相关性分析结果: 产卵场SST与CPUE显著相关(P < 0.05), 将Ps加到剩余产量模型, 分别构建3种基于SST的剩余产量模型: 产卵场Ps对r影响的模型2、产卵场Ps对K影响的模型3、产卵场Ps对r和K同时影响的模型4, 并将其与传统的剩余产量模型(模型1)进行对比分析, 探究Ps对太平洋褶柔鱼种群动态影响。传统剩余产量模型1:
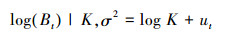 (1)
(1)
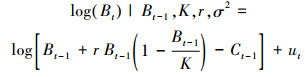 (2)
(2)
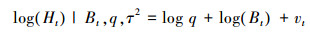 (3)
(3)
模型2:
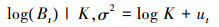 (4)
(4)
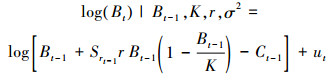 (5)
(5)
模型3:
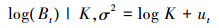 (6)
(6)
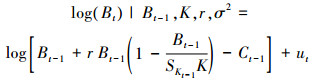 (7)
(7)
模型4:
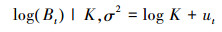 (8)
(8)
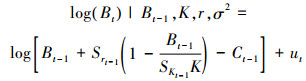 (9)
(9)
式中: Bt为第t年的生物量; r为内禀自然增长率; K为环境容纳量; q为可捕系数; Ht是第t年的CPUE; Ct-1为t-1年的产量;Bt和Ht的误差项分别为参数ut和vt, ut和vt相互独立且服从独立正态分布IID N (0, σ2)。
1.2.3 似然函数概率密度函数最大化用于估算模型参数[11], 假设Bt和太平洋褶柔鱼冬生群年CPUE服从对数正态分布, 似然函数表达式为
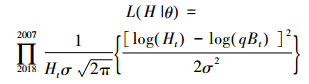 (10)
(10)
式中: H为观测数据; θ为模型参数组成的矢量; σ为标准差, 因渔获量和CPUE的时间序列过短无法估算标准差σ,将其设置为0.2[12]。根据前人研究结果[11], 假设Schaefer剩余产量模型参数K、r和q其先验分布均服从均匀分布, 具体数值见表 1。同时,假设初始生物量为34.5万t[13]。

|
表 1 剩余产量模型参数在MCM迭代计算的初始值设置 Tab.1 Initial value of the surplus production model parameters in the MCMC iterative calculation |
模型参数r、K、q后验概率分布估计采用蒙特卡洛马尔科夫(MARKOV CHAIN MONTE CARLO, MCMC)链的方法。设置3个MCMC链, 总迭代50000次, 丢弃前10000次, 后40000次该模型每40次迭代分析储存一次结果, 共计1 000次结果。

|
表 2 太平洋褶柔鱼冬生群的生物学参考点 Tab.2 Biological reference points of winter-spawning cohort for Todarodes pacificus |
利用偏差信息准则(deviance information criterion, DIC)比较不同模型精度和复杂性, DIC值越小则模型性能越好。
1.2.6 生物学参考点计算的生物学参考点(biological reference point, BRP)包括限制水平捕捞死亡率(F0.1)、最大可持续产量(maximum sustainable yield, MSY)、MSY水平捕捞死亡率(FMSY)和MSY水平生物量(BMSY, 为资源的限制参考点), 并绘制Kobe图, 评估种群的资源状况。统计分析用R 4.1.0语言软件处理, 涉及的packages主要有coda、rjags、R2jags。
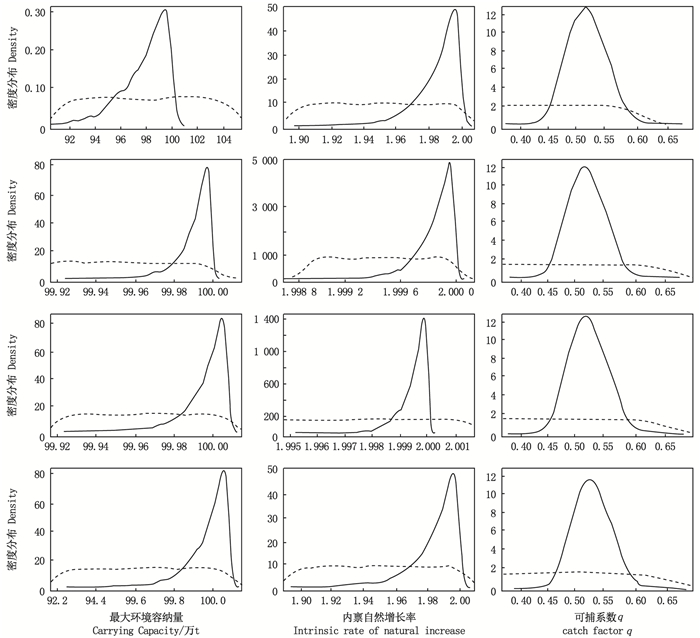
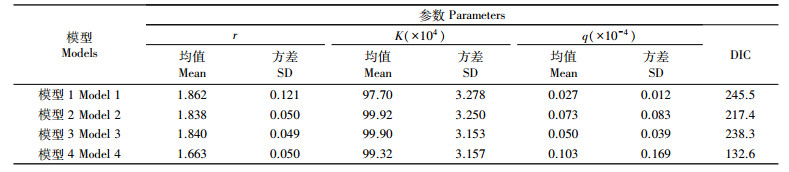
2 结果 2.1 模型对比分析4种剩余产量模型参数的先验分布和后验分布之间存在较大差异, 参数先验分布对后验分布的影响较小, 说明模型获得了较多的太平洋褶柔鱼冬生群的渔业信息(图 2)。每个模型的后验分布均不相同, 后验分布参数r为0.650~1.117、K为43.925×104~48.445×104、q为1.071×10-4~2.320×10-4, 其中r最小值分布在模型3和模型4中, 模型3和模型4的K值相近且以模型3为最小, q最小值分布在模型1中, 模型4的DIC值最小, 为132.6(表 3)。
|
图中实线表示先验分布, 虚线表示后验分布;从上到下模型顺序依次为: 模型1、模型2、模型3和模型4的r、K、q的先验和后验分布。 The solid line in the figure represents the prior distribution, and the dotted line represents the posterior distribution; The order of the models from top to bottom is: Prior and posterior distributions of r, K, q for Model 1, Model 2, Model 3, and Model 4. 图 2 4种剩余产量模型中的先验分布和后验分布对比图 Fig. 2 Comparison of prior distribution and posterior distribution in the four surplus production models |
|
表 3 太平洋褶柔鱼冬生群剩余产量模型中参数统计表 Tab.3 Statistics of parameters in the surplus production model of Todarodes pacificus |
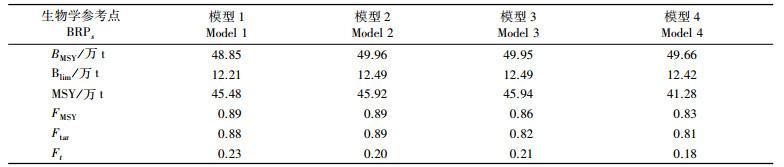
太平洋褶柔鱼冬生群资源评估模型结果显示, 模型1估算的最大可持续产量MSY为45.48万t, BMSY为48.85万t。模型2的MSY为45.92万t, BMSY为49.96万t。模型3的MSY为45.94万t, BMSY为49.95万t。模型4的MSY为41.28万t, BMSY为49.66万t。其中模型1的BMSY值为4个模型最小值, 模型4的MSY和FMSY为4个模型最小值。
评估认为, 模型1的Ftar为0.89, FMSY为0.88, Ftar和FMSY均为4个模型中最大值。2007—2018年在4个剩余产量模型中, 太平洋褶柔鱼冬生群的捕捞死亡率Ft为最小值, 且太平洋褶柔鱼冬生群的实际捕捞量低于MSY(表 4)。
|
表 4 2007—2018年4个模型得出的生物参考点统计表 Tab.4 Statistics of biological reference points derived from four models from 2007 to 2018 |
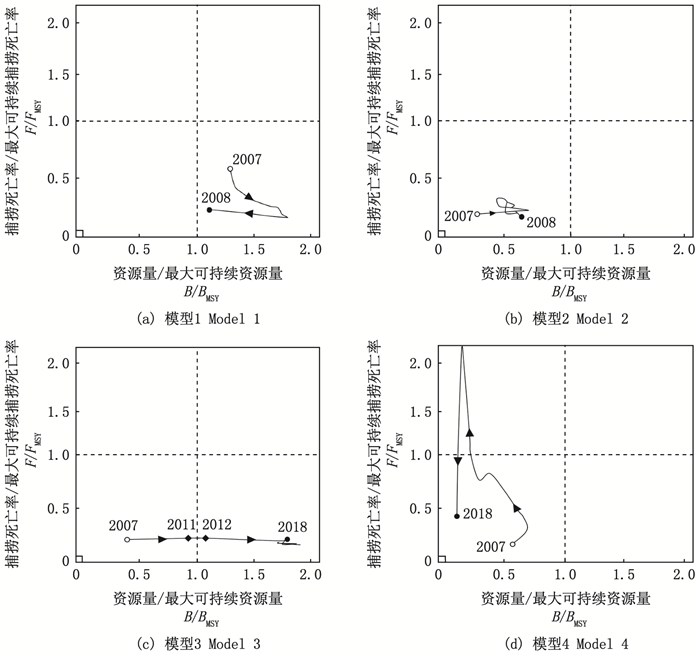
4个模型对太平洋褶柔鱼冬生群资源评估状况来看, 模型1评估结果显示太平洋褶柔鱼冬生群的资源状况良好(B/BMSY>1, F/FMSY < 1), 没有出现过度捕捞的现象(图 3)。Sr-ED模型1中显示资源过度性捕捞, 当前生物量处于较低水平(B/BMSY < 1, F/FMSY < 1)(图 3)。模型4显示, 该种群存在资源型过度捕捞和捕捞型过度的现象, 但资源正在逐渐恢复状态(图 3)。
|
图 3 2007—2018年4种剩余产量模型对太平洋褶柔鱼冬生种群资源评估状态 Fig. 3 Resource status of Todarodes pacificus in four surplus production models from 2007 to 2018 |
太平洋褶柔鱼作为一年生的短生命周期物种, 其资源极易受到海洋环境的影响。据FAO统计, 太平洋褶柔鱼年际产量波动大, 1986年后产量呈现逐年上升趋势, 2015年后, 产量大幅度逐年下降。已有研究[10-14]显示, 太平洋褶柔鱼资源补充量受环境影响显著, 因此探究环境变化对资源的影响, 为资源可持续发展的管理提供参考。SAKURAI等[3]认为太平洋褶柔鱼资源变化主要受产卵场环境影响。水温影响其胚胎发育的时间和发育速度, 对其产卵、孵化生长有明显的影响[11], 产卵场环境变化被认为是太平洋褶柔鱼数量变动的关键因素[15]。因此, 在太平洋褶柔鱼的资源评估中, 需要重点考虑和分析产卵场温度变化对其种群动态的影响。
同时, 环境变化使太平洋褶柔鱼的生物学数据获取受限[16], 造成无法利用传统的评估模型对其进行资源评估[17]。剩余产量模型不需要资源群体本身的生物学数据, 仅需渔获量、捕捞努力量或CPUE[18]。为提高模型评估的准确性, 采用贝叶斯统计方法考虑先验信息, 降低了参数估计的不确定性, 因此,采用Schaefer剩余产量模型对太平洋褶柔鱼冬生群进行资源评估, 具有一定的科学性和可操作性。
3.2 不确定性分析渔业资源评估的不确定性主要来源于原始数据的不确定性, 模型参数的不确定性, 以及数据时间序列等方面。为了降低原始数据的不确定性, 采用了2019年日本水产厅关于太平洋褶柔鱼冬生群的资源评估报告, 该数据本身具有科学性和可靠性, 但是在生物量原始数据选择方面可能存在一定的不确定性, 本研究假设模型参数参数初始量为34.5万t, 不同初始量值对渔业资源评估可能会有一定的影响。
在模型参数的不确定性方面, 假设CPUE标准差σ设为0.2, 该值的假设对评估模型和评估结果产生的影响还待研究。基于环境因子的资源评估模型中, 在模型参数估计的过程中不仅仅是定值, 更多是随着时间变化其生物学参数也会发生变化, 如自然死亡率、资源可捕性等对种群资源状况的影响。因此,模型建立的过程中要考虑随时间变化的生物学参数的变动。
在数据年限限制方面, 本研究建立的剩余产量模型是基于2007—2018年日本鱿钓船的渔业生产数据, 因此基于上述年限估算出的模型参数, 通常只能计算上述年限的种群资源状况, 这是由于太平洋褶柔鱼本身是短生命周期物种, 其资源状况和个体生长状况极易受环境变化影响, 因此用于预测2007—2018年之外的渔业资源状况可能存在一定的风险。
3.3 太平洋褶柔鱼资源状况评价从评估结果可以看出, 2007—2018年太平洋褶柔鱼年渔获量保持在4.5万~31.5万t, 平均值为19.5万t。2000年的31.5万t为最高渔获量, 其次是2011年的29.5万t, 2017年为5.3万t,2018年4.5万t。这说明太平洋褶柔鱼的渔获量年间波动较大, 并且近年来其渔获量呈大幅度下降趋势。
结合4种剩余产量模型, 从渔业捕捞状况来看, Ft的值均小于Ftar的值, 这说明其捕捞强度在渔业资源可承受范围内。从资源量分析来看, 模型1在2007—2018年Bt均大于BMSY(图 6a), 该模型评估结果显示, 太平洋褶柔鱼资源状况良好, 没有呈现过度捕捞趋势, 资源目前处于尚未充分开发, 这与其他3个模型评估结果呈现明显差异。
评估模型1显示, 太平洋褶柔鱼冬生群资源出现过度捕捞(B/BMSY < 1, F/FMSY < 1), 有必要留意因捕捞而引起的资源减少(图 6b)。
评估模型3显示, 2007—2011年B/BMSY>1, F/FMSY < 1;2012—2018年B/BMSY < 1, F/FMSY < 1, 这说明此期间太平洋褶柔鱼冬生群资源的开发需要采取一定的保护措施(图 6d)。
评估模型4显示, 太平洋褶柔鱼冬生群资源的起始年份和终止年份均出现B/BMSY < 1、F/FMSY < 1的现象, 而在2007—2018年期间存在B/BMSY < 1, F/FMSY>1的现象, 这说明太平洋褶柔鱼冬生群资源中出现了过度捕捞的现象, 而在起始年份则出现资源较好的状况, 这可能与捕捞强度较少以及海洋环境的影响有关。
研究认为, 加入环境因子的评估比不加入环境因子的评估结果更具有现实性意义, 且当太平洋褶柔鱼种群资源受环境影响时, 会直接影响种群动态r和K的参数值, 进而影响评估结果, 当动态的模型参数r和K发生变化时, 相关管理部门需及时调整现有的捕捞强度, 避免因捕捞过度影响种群资源的合理开发和可持续利用。
| [1] |
KIDOKORO H, GOTO T, NAGASAWA T, et al. Impact of a climate regime shift on the migration of Japanese common squid (Todarodes pacificus) in the Sea of Japan[J]. ICES Journal of Marine Science, 2010, 67(7): 1314-1322. DOI:10.1093/icesjms/fsq043 |
| [2] |
加賀敏樹, 山下紀生, 岡本俊. 平成29(2017)年度スルメイカ秋季発生系群の資源評価. 北海道区水産研究所, 2017. KAGA T, YAMASHITA N, OKAMOTO S. Evaluation of the resources of the autumn cohort of Todarodes pacificus in 2017. Hokkaido Fisheries Research Institute, 2017. |
| [3] |
SAKURAIY, BOWER J R, NAKAMURA Y, et al. Effects of temperature on development and survival of Todarodes pacificus embryos and paralarvae[J]. American Malacological Bulletin, 1996, 13(1/2): 89-95. |
| [4] |
吴梦瑶, 田思泉. 基于海表面温度SST的剩余产量模型评估太平洋褶柔鱼秋生群资源[J]. 上海海洋大学学报, 2019, 28(6): 933-942. WU M Y, TIAN S Q. Stock assessment for autumn cohort of Todarodes pacificus based on surplus yield model with sea surface temperature[J]. Journal of Shanghai Ocean University, 2019, 28(6): 933-942. |
| [5] |
谢恩阁, 陈新军, 汪金涛, 等. 基于水温因子的太平洋褶柔鱼冬生群剩余产量模型研究[J]. 海洋学报, 2019, 41(12): 71-77. XIE E G, CHEN X J, WANG J T, et al. Study on residual yield model of winter fishes of Todarodes pacificus based on water temperature factors[J]. Acta Oceanologica Sinica, 2019, 41(12): 71-77. DOI:10.3969/j.issn.0253-4193.2019.12.007 |
| [6] |
WANG J T, YU W, CHEN X J, et al. Stock assessment for the western winter-spring cohort of neon flying squid (Ommastrephes bartramii) using environmentally dependent surplus production models[J]. Scientia Marina, 2016, 80(1): 69-78. |
| [7] |
LIU J L, YU W, XU L L, et al. Using Bayesian Bio-economic model to evaluate the management strategies of Ommastrephes bartramii in the Northwest Pacific Ocean[J]. Aquaculture and Fisheries, 2021, 6(2): 205-215. DOI:10.1016/j.aaf.2019.10.001 |
| [8] |
加賀敏樹, 山下紀生, 岡本俊, 等. 平成30年度スルメイカ冬季発生系群の資源評価. 平成30年度我が国周辺水域の漁業資源評価, 水産庁·水産研究·教育機構, 2019: 652-697. KAGA T, YAMAAHITA N, OKAMOTO S, et al. Resource evaluation of the 2018 Japanese flying squid winter outbreak group. 2018 Fisheries Resource Evaluation of the Waters Around Japan, Fisheries Agency/Fisheries Research and Education Agency, 2019: 652-697. |
| [9] |
MINOBE S. A 50-70 year climatic oscillation over the North Pacific and North America[J]. Geophysical Research Letters, 1997, 24(6): 683-686. DOI:10.1029/97GL00504 |
| [10] |
唐峰华, 史赟荣, 朱金鑫, 等. 海洋环境因子对日本海太平洋褶柔鱼渔场时空分布的影响[J]. 中国水产科学, 2015, 22(5): 1036-1043. TANG F H, SHI Y R, ZHU J X, et al. Influence of marine environment factors on temporal and spatial distribution of Japanese common squid fishing grounds in the Sea of Japan[J]. Journal of Fishery Sciences of China, 2015, 22(5): 1036-1043. |
| [11] |
JI F, GUO X Y, WANG Y C, et al. Response of the Japanese flying squid (Todarodes pacificus) in the Japan Sea to future climate warming scenarios[J]. Climatic Change, 2020, 159(4): 601-618. DOI:10.1007/s10584-020-02689-3 |
| [12] |
李纲, 陈新军, 官文江, 等. 东黄海鲐鱼资源评估与管理决策研究[M]. 北京: 科学出版社, 2011: 104-128. LI G, CHEN X J, GUAN W J, et al. Stock assessment and management strategies for chub mackerel (Scomber japonicus) in the East China Sea and Yellow Sea[M]. Beijing: Science Press, 2011: 104-128. |
| [13] |
SAKURAI Y, KIYOFUJI H, SAITOHS I, et al. Stock fluctuations of the Japanese common squid, Todarodes pacificus, related to recent climate changes[J]. Fisheries Science, 2002, 68(s1): 226-229. |
| [14] |
李建生, 严利平. 东海太平洋褶柔鱼的数量分布及其与环境的关系[J]. 海洋渔业, 2004, 26(3): 193-198. LI J S, YAN L P. Quantity distribution of Todarodes pacificus and its relation with environment in the East ChinaSea[J]. Marine Fisheries, 2004, 26(3): 193-198. DOI:10.3969/j.issn.1004-2490.2004.03.007 |
| [15] |
THORSON J T, MONNAHAN C C, COPE J M. The potential impact of time-variation in vital rates on fisheries management targets for marine fishes[J]. Fisheries Research, 2015, 169: 8-17. DOI:10.1016/j.fishres.2015.04.007 |
| [16] |
KIDOKORO H, SHIKATA T, KITAGAWA S. Forecasting the stock size of the autumn cohort of Japanese common squid (Todarodes pacificus) based on the abundance of trawl-caught juveniles[J]. Hidrobiológica, 2014, 24(1): 23-31. |
| [17] |
许骆良, 陈新军, 汪金涛, 等. 基于Schaefer模型的东南太平洋茎柔鱼资源评估和管理[J]. 海洋学报, 2015, 37(10): 49-58. XU L L, CHEN X J, WANG J T, et al. Stock assessment and management of Dosidicus gigas in the Southeast Pacific Ocean with Schaefer model[J]. Acta Oceanologica Sinica, 2015, 37(10): 49-58. DOI:10.3969/j.issn.0253-4193.2015.10.005 |
| [18] |
官文江, 田思泉, 朱江峰, 等. 渔业资源评估模型的研究现状与展望[J]. 中国水产科学, 2013, 20(5): 1112-1120. GUAN W J, TIAN S Q, ZHU J F, et al. A review of fisheries stock assessment models[J]. Journal of Fishery Sciences of China, 2013, 20(5): 1112-1120. |
2. Key Laboratory of Sustainable Exploitation of Oceanic Fisheries Resources, Ministry of Education, Shanghai 201306, China;
3. National Engineering Research Center for Oceanic Fisheries, Shanghai 201306, China;
4. Key Laboratory of Oceanic Fisheries Exploration, Ministry of Agriculture and Rural Affairs, Shanghai 201306, China
 2022,
Vol. 31
2022,
Vol. 31


