2. 宜宾市翠屏区农业农村局, 四川 宜宾 644000
稻渔综合种养是一种新型高效的生态循环种养模式,具有优化农业结构、促进农业增收等特点,目前在我国各省均有推广[1]。中华绒螯蟹(Eriocheir sinensis)是我国特有的名优水产品,在我国分布较广,稻蟹种养模式主要分布于我国三北地区,以及江苏、上海、天津等沿海省市,因其能够为中华绒螯蟹后期生长提供充足光照,还扩大了其活动空间,提供良好的生态环境,近年来养殖比例逐渐增加[2]。
肠道菌群被称为是“被遗忘的器官”,是调节自身生理和免疫的重要器官,肠道菌群多样性在维持免疫功能方面发挥着重要作用,投喂肠道益生菌能够增强宿主免疫力,肠道菌群失调可能会增加疾病的风险[3]。有研究发现患白便综合症的虾较健康的虾的肠道菌群多样性较低[4];感染白斑综合征病毒(white spot syndrome virus)的河蟹,肠道微生物类群和丰度发生变化[5]。水产动物微生物菌群受多种因子的影响,如温度、溶氧、养殖模式等[6-8]。目前已有研究[7]发现稻田模式下克氏原螯虾(Procambarus clarkii)肠道的菌群多样性及丰富度在一定程度上高于池塘模式;池塘养殖的中华绒螯蟹的肠道拟杆菌(Bacteroides)的丰富度和总细菌载量大约是野生蟹的4~10倍[8],稻蟹共作模式下的中华绒螯蟹的软壁菌门(Tenericutes)较蟹单作模式的丰富度多21.9%[1]。肠道菌群的变化与宿主营养代谢密切相关,如肥胖、胰岛素抗性及氨基酸代谢等[9],在水产动物上也有所体现。稻田养殖克氏原螯虾4个月后肌肉风味氨基酸含量显著高于池塘养殖,同时稻田虾的肠道拟杆菌门丰度大幅度高于池塘[7];阳澄湖雌蟹其特有鲜味氨基酸显著高于固城湖蟹,与其肠道微生物多样性和丰度高密切相关[10]。因此,养殖模式会改变养殖对象的肠道菌群进而可能对其肠道免疫和肌肉风味造成影响,然而目前仅见不同养殖模式对中华绒螯蟹肠道微生物、免疫或者对其品质的单一或者两两研究,其结合分析的研究不多。本研究从肠道微生物角度,综合研究中华绒螯蟹在稻田养殖模式与池塘集约化养殖下肠道菌群特征与免疫酶活及肌肉氨基酸差异,为探索不同养殖模式下通过微生物菌群调控中华绒螯蟹的肌肉风味的提供基础参考数据。
1 材料与方法 1.1 试验设计与样品采集本试验在吉林白城某养殖基地进行,同一批次蟹分别置入池塘与稻田进行饲养,其中每池塘和稻田3个重复,试验期间池塘养殖每天投喂2次和丰配合蟹饲料,稻田养殖不投喂。蟹养殖密度稻田模式为9 000只/hm2,池塘模式为15 000只/hm2。5月样品为养殖10日后进行取样;5个月后(即10月),分别于池塘与稻田进行取样。5月池塘组(MP)体质量为(15.35±2.81)g,5月稻田组(MR) 体质量为(15.15±4.04)g,10月池塘组(OP) 体质量为(32.52±5.25)g 10月稻田组(OR) 体质量为(26.06±6.38)g。每组取样10只,将全蟹冰运至实验室,迅速取全肠,剔除表面脂肪、结缔组织,肌肉取身体全部肌肉,置于无菌离心管中后于-80 ℃冰箱中保存。
1.2 样品处理 1.2.1 肠道DNA提取根据天根生物公司的粪便基因组DNA提取试剂盒说明,提取4组样品(每组10个样本)肠道粪便微生物基因组DNA。
1.2.2 DNA质量检测、纯化和高通量测序PCR扩增前采用琼脂糖凝胶电泳(AGE)和OD测定法检测DNA纯度和质量。利用结构域特异性引物(341F: 5′-CCTAYGGGRBGCASCAG-3′和806R: 5′-GGACTACNNGGGTATCTAAT-3′)扩增细菌16S rDNA V3-V4高变区。使用Ion Fragment Library Kit 48 rxns (Thermo Scientific)生成测序文库,通过量子位@ 2.0荧光计(Thermo Scientific)进行质量评估,最后在Ion S5 TM XL平台上对文库进行测序,得到400 bp/600 bp的单端序列。采用北京诺禾有限公司IonS5TMXL平台(Thermofisher, USA)进行16S DNA高通量测序。
1.2.3 免疫酶活的测定每组各取出5个肠道组织样品,称重,按质量体积比1∶ 9加入超纯水,匀浆后,用离心机在4 ℃下以3 000 r/minl转速离心10 min,取上清液作为粗酶提取液,分别按照南京建成的检测试剂盒说明书测定溶菌酶(LZM)、超氧化物歧化酶(SOD)、过氧化氢酶(CAT)、碱性磷酸酶(AKP)和酸性磷酸酶(ACP)的酶活。
1.2.4 样品处理与肌肉游离氨基酸测定将OP组和OR组的肌肉样本各取6个样品,将每个肌肉样本分别剪取约0.1 g,加入9倍体积的超纯水匀浆肌肉,将肌肉匀浆以12 000 r/min转速离心10 min,取上清液,以肌肉匀浆上清与磺基水杨酸体积比为300∶ 900混合后静置30 min,将混合液以12 000 r/min转速离心10 min,取上清液,按肌肉游离氨基酸测定方法,使用超高速全自动氨基酸分析仪(LA8080)进行氨基酸含量测定。
1.3 数据处理实验结果肠道微生物测序数据为fastq格式,使用Cutadapt软件进行过滤和条码分割,统计分析使用QIIME,Microbiome Analyst (https://www.microbiomeanalyst.ca)完成。根据OTUs聚类结果,一方面对每个OTU的代表序列进行物种标注,得到相应的物种信息和基于物种的丰度分布,同时计算OTUs丰度、Alpha多样性,得到样本物种丰富度和均匀度信息,以及不同样本或类群之间常见的和唯一的OTUs信息。另一方面,在OTUs上进行多重序列比对,进一步得到不同样本和群体的群落结构差异,并通过PCoA降维图显示出来。
肠道免疫酶活及肌肉氨基酸结果采用平均值±标准差(X ±SD)表示,使用GraphPad Prism v8.0对肠道免疫酶活结果进行方差分析(Two-way ANOVA),对肌肉氨基酸结果进行单因素方差分析(One-way ANOVA),显著水平取P < 0.05。
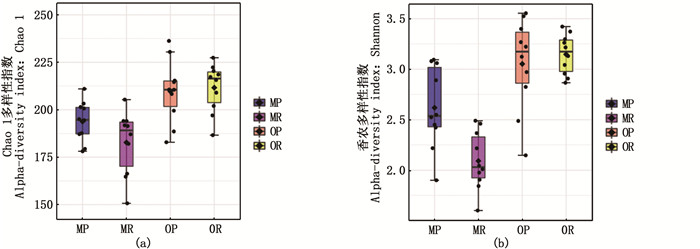
2 结果与分析 2.1 两种养殖模式中华绒螯蟹肠道菌群组成比较从中华绒螯蟹的40份肠道菌群样品中共获得2 151 941条高质量序列和627个细菌OTU。如图 1所示,根据Chao 1指数的结果,5月池塘养殖模式下中华绒螯蟹肠道菌群的丰度高于稻田养殖模式,而10月则相反,为稻田养殖模式下肠道菌群丰度高于池塘养殖模式;Shannon指数显示,池塘养殖模式的肠道菌群物种多样性在5月和10月均高于稻田养殖模式(P < 0.05)。从5月到10月,稻田养殖模式下中华绒鳌蟹肠道菌群的丰度和多样性均出现上升(P < 0.05),而池塘养殖模式下肠道菌群的丰度和多样性则无显著变化(P>0.05)。
|
MP.5月池塘蟹;MR.5月稻田蟹;OP.10月池塘蟹;OR.10月稻田蟹。 图 1 5月和10月池塘、稻田两种养殖模式下中华绒螯蟹肠道菌群α多样性 Fig. 1 Alpha diversity of the intestinal microbiota of Eriocheir sinensis from two modes in May and October |
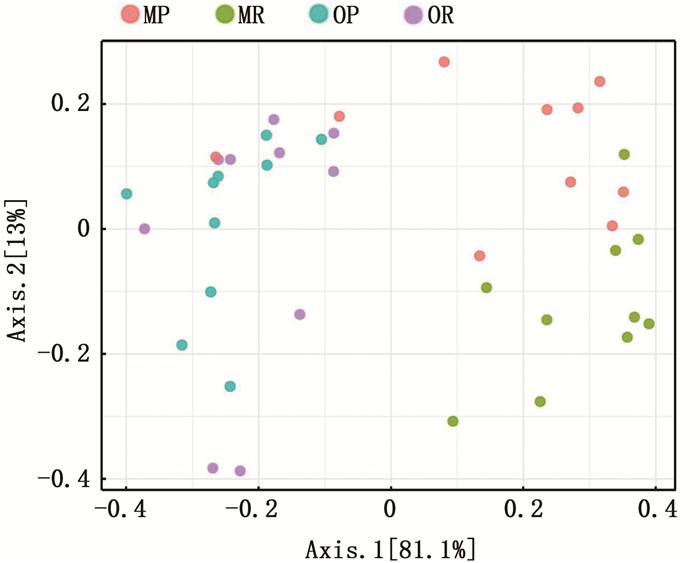
由中华绒螯蟹PCoA分析结果(图 2)可知,不同时间取样的中华绒螯蟹细菌群落相互分开,不同养殖模式下细菌群落难以区别,季节的变化对中华绒螯蟹肠道菌群的影响更大。
|
MP.5月池塘蟹;MR.5月稻田蟹;OP.10月池塘蟹;OR.10月稻田蟹。 图 2 5月和10月池塘、稻田两种养殖模式下中华绒螯蟹肠道菌群PCoA分析 Fig. 2 PCoA of the intestinal microbiota of Eriocheir sinensis from pond and rice field in May and October |
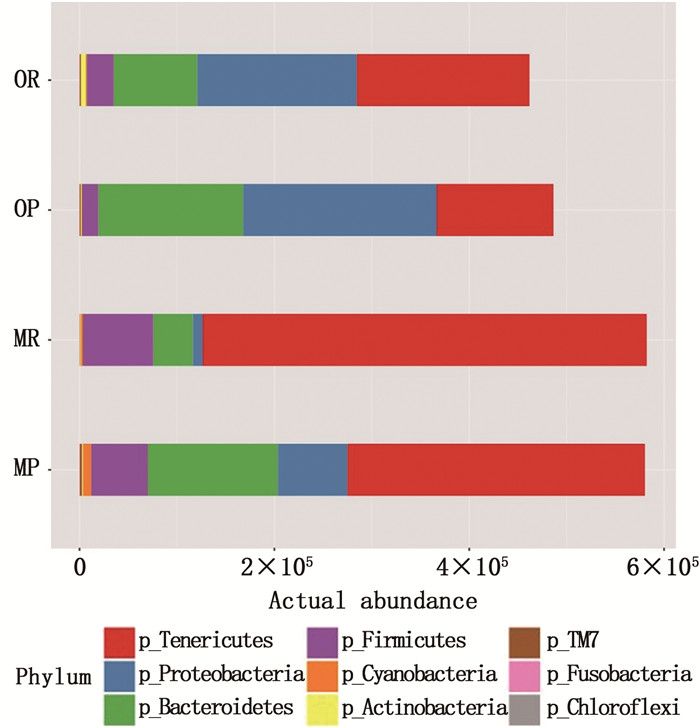
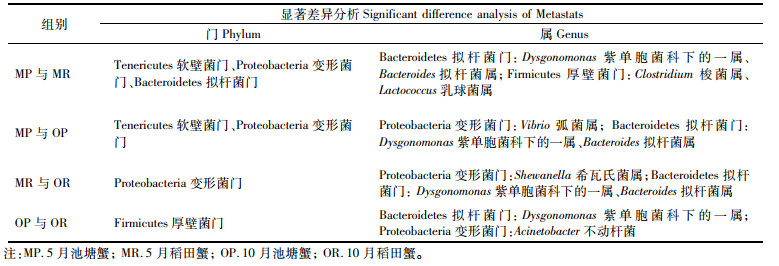
由图 3可知,比较5月和10月两种养殖模式间中华绒螯蟹门水平肠道微生物的组成,两种模式下中华绒螯蟹的优势菌门均为软壁菌门(Tenericutes)、拟杆菌门(Bacteroidetes)、变形菌门(Proteobacteria)和厚壁菌门(Firmicutes),不同时间和养殖模式其门和属的丰度存在差异,并且门和属不一一对应。5月池塘养殖模式下中华绒螯蟹肠道优势菌门为软壁菌门(51.32%)、拟杆菌门(22.24%)、变形菌门(13.14%)和厚壁菌门(10.40%),5月稻田养殖模式下中华绒螯蟹肠道优势菌门为软壁菌门(77.44%)、厚壁菌门(12.63%)、拟杆菌门(7.17%)和变形菌门(1.97%),10月池塘养殖模式下中华绒螯蟹肠道优势菌门为变形菌门(41.62%)、拟杆菌门(29.42%)和软壁菌门(24.78%),10月稻田养殖模式下中华绒螯蟹肠道优势菌门为软壁菌门(37.24%)、变形菌门(36.91%)、拟杆菌门(17.96%)和厚壁菌门(6.12%)。5月和10月,稻田养殖模式下中华绒螯蟹肠道中软壁菌和厚壁菌的丰度均高于池塘养殖模式,变形菌的丰度则为池塘养殖模式高于稻田养殖模式。从5月到10月,软壁菌门的丰度在两种养殖模式下均降低,而变形菌门、拟杆菌门和厚壁菌门的丰度均上升,且池塘的差异菌属主要为Vibrio(弧菌属)、Dysgonomonas(紫单胞菌科下的一属)和Bacteroides(拟杆菌属);5月变形菌门的丰度在稻田养殖模式中较低,仅为1.97%,但在池塘养殖模式下高达13.14%,差异菌属主要为Dysgonomonas、Bacteroides,而在10月,池塘组厚壁菌门丰度和稻田组(6.12%)相比也较低,仅为3.58%(表 1)。
|
MP.5月池塘蟹;MR.5月稻田蟹;OP.10月池塘蟹;OR.10月稻田蟹。 图 3 5月和10月池塘、稻田两种养殖模式下中华绒螯蟹肠道菌群门水平结构特征 Fig. 3 Structural characteristics of intestinal microbiota in Eriocheir sinensis from pond and rice field in May and October |
|
表 1 不同模式下5月和10月具有显著差异菌群汇总 Tab.1 Significantly different bacteria groups in different modes in May and October |
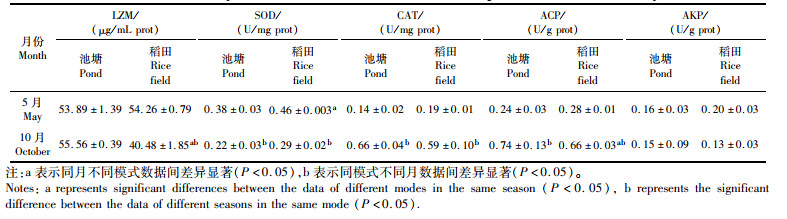
从5月到10月,两种养殖模式下中华绒螯蟹肠道中的SOD在5月的活性均高于10月(P < 0.05),而CAT和ACP的活性则表现为10月高于5月(P < 0.05)。5月,稻田养殖模式下中华绒螯蟹肠道中SOD活性高于池塘养殖模式(P < 0.05);10月,池塘养殖模式下中华绒螯蟹肠道中LZM和ACP活性高于稻田养殖模式(P < 0.05)。见表 2。
|
表 2 5月和10月池塘、稻田两种养殖模式下中华绒螯蟹肠道免疫酶活力 Tab.2 Intestinal immune enzyme activities of Eriocheir sinensis from pond and rice field in May and October |
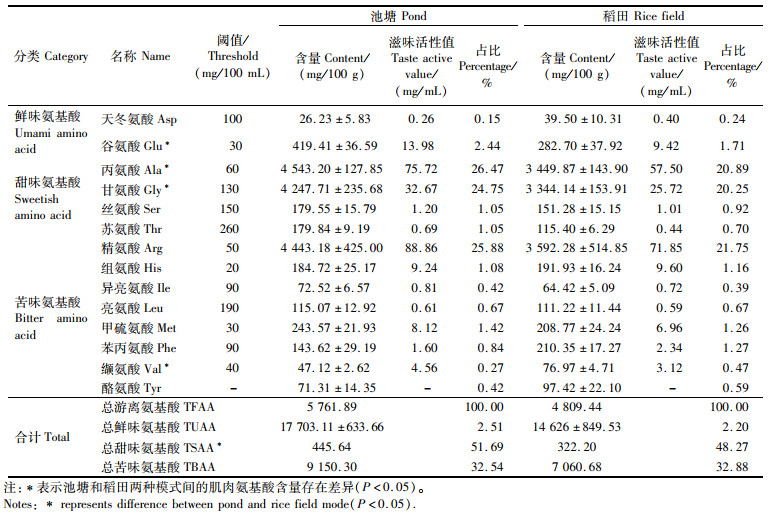
游离氨基酸是一种风味物质,呈鲜、甜、苦等滋味,其对滋味的贡献程度用味道强度值(TAV)表示,当TAV的值大于1时,说明该呈味物质对产品的滋味有显著影响,且数值越大,贡献越大[11]。如表 3所示,在池塘和稻田两种养殖模式下的中华绒螯蟹肌肉中共检出14种呈味氨基酸。在池塘养殖模式下,蟹肌肉中游离氨基酸总量为17 703 mg/100 g,其中丙氨酸(4 543 mg/100 g)、精氨酸(4 443 mg/100 g)和甘氨酸(4 247 mg/100 g)含量较高分别占游离氨基酸总量的26.47%、25.88%和24.75%,谷氨酸、谷氨酰胺和赖氨酸占比分别为2.44%、2.14%和2.03%。其中谷氨酸、丙氨酸、甘氨酸的含量均表现为池塘养殖模式下中华绒螯蟹肌肉中含量高于稻田养殖模式含量,仅缬氨酸的含量均表现为稻田养殖模式下中华绒螯蟹肌肉中含量高于池塘养殖。由表 3可知:总甜味氨基酸(TSAA)﹥总苦味氨基酸(TBAA)﹥总鲜味氨基酸(TUAA)。池塘养殖模式下中华绒螯蟹肌肉中TSAA高于稻田养殖模式(P < 0.05),且池塘养殖模式下中华绒螯蟹肌肉中TFAA(总游离氨基酸)高于稻田养殖模式。这些结果均显示,池塘养殖模式下中华绒螯蟹具有更鲜明的肌肉风味。
|
表 3 10月池塘、稻田两种养殖模式下中华绒螯蟹肌肉中呈味氨基酸的含量 Tab.3 Content of delicious amino acids in fresh muscle of Eriocheir sinensis from pond and rice field in October |
水产动物易受环境条件的影响造成自身的不稳定,从而影响消化道微生物群。摄食和生存环境因子等均可在一定程度上影响鱼类的免疫酶活力,消化道菌群能够通过产物抑制等竞争性作用阻止外源微生物的入侵,有效提高宿主的免疫功能[6-7]。鱼类消化道内存在着一层由微生物构成的保护膜,该微生物层是消化道内的正常微生物菌群。这些微生物菌群在病原体免疫、营养、物理和化学等方面对鱼类具有重要意义[6]。
肠道菌群是一个复杂而动态的系统,高度可变但环境适应性很强,对机体的许多生物过程至关重要,包括消化、葡萄糖代谢、免疫调节和肠屏障功能等[12], 肠道菌群还有助于宿主的营养获取,包括在氨基酸代谢及免疫系统发育方面的贡献[9, 13]。从5月到10月,稻田养殖模式下中华绒鳌蟹肠道菌群的丰度和多样性均上升,肠道菌群多样性的提高会提高机体的健康水平,有利于宿主健康[14], 说明随着时间的延长,稻田养殖环境中华绒螯蟹肠道菌群的多样性提高,进而维持机体健康。
对凡纳滨对虾(Litopenaeus vannamei)的研究发现,Shannon指数越高,细菌群落的稳定性越好,虾对疾病的抵抗力越强[15]。本研究发现池塘养殖模式的肠道菌群Shannon指数在5月和10月均高于稻田养殖模式(P < 0.05),且在5月和10月无显著变化,说明池塘养殖模式下的中华绒螯蟹肠道菌群较稻田养殖模式更稳定。肠道菌群对于调节水生动物的免疫系统和进食习惯以及防止病原微生物的入侵至关重要。从门水平肠道菌群丰度分布结果显示,两种养殖模式下中华绒螯蟹肠道中的优势菌均为软壁菌门、变形菌门、拟杆菌门和厚壁菌门。这与在长江口阳澄湖等地的中华绒螯蟹肠道菌群中的优势菌群结果[16]一致。5月,池塘和稻田养殖模式下软壁菌门的丰度都远高于10月,在5月稻田养殖模式高达77.44%, 而在崇明中华绒螯蟹中则以变形菌门最多为43%~50%[8],差异较大,可能与肠道微生物的分析方法不一样有关,崇明蟹用的是16S rRNA测序,而本文用的16S DNA高通量测序。即使使用同样分析方法,江苏省兴化的成蟹厚壁菌丰度达到90%以上[17],与本研究个体差异较大,因此肠道微生物菌群与个体的大小及发育阶段相关。
10月两种养殖模式下变形菌门的丰度较5月均升高,且5月和10月池塘养殖模式下中华绒螯蟹肠道中变形菌门的丰度都高于稻田养殖模式。有研究[18]表明,变形菌中包含多种致病细菌,同时也被证明与消化密切相关。变形菌门的增加通常被认为是微生物群落不稳定的标志,可能导致宿主营养和代谢紊乱。变形菌门与IL-10和TNF-α的表达密切相关,可引发肠道炎症反应,导致肠道内外环境紊乱,出现生长性能下降[19],其下属的不动杆菌属的细菌是可导致甲壳类动物快速死亡的病原菌[20]。因此其丰度的升高会刺激中华绒螯蟹肠道产生免疫应激反应。10月,两种养殖模式下中华绒螯蟹肠道中厚壁菌的丰度均出现下降,而拟杆菌的丰度出现升高,且两个取样时间点中华绒螯蟹肠道中拟杆菌的丰度均表现为池塘养殖模式高于稻田养殖模式,厚壁菌的丰度则表现为稻田养殖模式高于池塘养殖模式。拟杆菌丰度的变化会影响宿主的能量代谢效率[21-22],厚壁菌与拟杆菌的比值越高,肠道所拥有的营养物质运输和消化的能力就越强。拟杆菌属在维持肠道粘膜免疫系统的动态平衡中起着重要作用,且拟杆菌和厚壁菌的比例与某些疾病的发病有关[23]。拟杆菌属可以产生肠毒素,该肠毒素在被蛋白水解酶处理后会促进肠黏膜的渗透性和细菌吸收[24]。在对不同品质的中华绒螯蟹的肠道菌群的分析中发现,厚壁菌门与拟杆菌门的丰度比降低会导致出现肥满度及肝胰腺指数降低的低品质蟹[17]。而本研究中稻田养殖模式下从5月到10月其厚壁菌门与拟杆菌门的丰度比下降了近80%,也有可能是影响其肌肉品质原因之一,然而本试验未对肠道菌群功能进行分析,有待进一步研究。
3.2 两种养殖模式对中华绒螯蟹肠道免疫酶活的影响在甲壳类动物中,非特异性免疫是抵抗入侵病原体的主要反应,提高免疫功能对抵抗这种压力至关重要[25]。肠道菌群作为宿主细菌生态系统的组成部分,可以影响宿主的健康生长。10月稻田养殖模式下中华绒螯蟹肠道菌群丰度和多样性高于5月,同时,10月稻田养殖模式下中华绒螯蟹肠道SOD活性高于5月(P < 0.05),两者变化趋势一致,说明肠道菌群多样性可在一定程度上反映肠道抗氧化能力。然而在5月稻田养殖模式下中华绒螯蟹肠道菌群丰度和多样性低于池塘模式的情况下,5月稻田养殖模式下中华绒螯蟹肠道中SOD活性高于池塘养殖模式(P < 0.05),说明肠道抗氧化能力除与肠道菌群多样性相关外,可能还有其他因素的作用,如:5月稻田养殖模式下中华绒螯蟹肠道中软壁菌门的丰度(77.44%)高于池塘养殖模式(51.32%),且稻田养殖模式下肠道中SOD活性高于池塘养殖模式(P < 0.05)。软壁菌门是由厚壁菌门进化而来,ZHENG等[26]通过宏基因组测序技术,预测软壁菌具有突出的核酸降解能力,并且对磷、氮等元素的循环有重要驱动作用,而且还能自如应对深海高压和陆地常压环境。因此在5月池塘和稻田中高丰度的软壁菌门有利于适应环境,且稻田相对于池塘环境温度、溶氧等因子变化更快,可能需要更多的软壁菌门进行应对,产生更多的SOD酶活抗应激。在对日本沼虾的研究[27]中发现,虾的肠道微生物群落丰度与非特异性免疫反应(ACP和AKP)呈正相关,由慢性缺氧引起的微生物群改变可以影响虾的肠道免疫反应。10月,池塘养殖模式下肠道菌群丰度低于稻田养殖模式,而池塘养殖模式下中华绒螯蟹肠道中LZM和ACP活性高于稻田养殖模式(P < 0.05),这可能与池塘中较稻田高的变形菌门(41.62%)和拟杆菌门(29.42%)有关。变形菌门和拟杆菌门可引起宿主营养和代谢紊乱[28],可能刺激肠道产生更高活性的LZM和ACP,从而维持池塘养殖模式下5个月肠道菌群丰度和多样性无显著变化(P>0.05),这与之前研究的中华绒螯蟹的肠道菌群在不同环境中具有高可塑性观点[12]一致,然而中华绒螯蟹肠道很多菌群的具体功能仍不明了,亟待进一步研究。
3.3 两种养殖模式对中华绒螯蟹肌肉游离氨基酸的影响对10月两种养殖模式下中华绒螯蟹肌肉中游离氨基酸组成进行分析,结果显示,两种养殖模式下中华绒螯蟹肌肉中均检测出17种游离氨基酸,丙氨酸、甘氨酸、精氨酸的含量在两种养殖模式下均较高。游离氨基酸含量决定中华绒螯蟹肌肉的滋味品质[29]。在对蟹肉有贡献的氨基酸中,池塘养殖模式下呈味氨基酸的含量顺序为甜味(51.69%)>苦味(32.54%)>鲜味(2.51%),稻田养殖模式下的呈味氨基酸的含量顺序为甜味(48.27%)>苦味(32.88%)>鲜味(2.20%),两种养殖模式下中华绒螯蟹肌肉中呈味氨基酸含量比例接近,无显著差别。由表 3可知,在稻田与池塘两种养殖模式下的蟹肌肉中呈现出显著差异的4种氨基酸(Glu, Ala, Gly, Val)均对蟹肉的呈味有显著贡献,均为池塘养殖模式含量高于稻田养殖模式,且池塘养殖模式下中华绒螯蟹肌肉中TSAA的含量显著高于稻田养殖模式,表明池塘养殖模式下的蟹肌肉比稻田养殖模式下的蟹肌肉表现出更加强烈的甜味。池塘养殖模式下,蟹肌肉中谷氨酸、丙氨酸、甘氨酸及缬氨酸的含量均显著高于稻田养殖模式。其中,丙氨酸与甘氨酸均为甜味氨基酸,这两种氨基酸之和占总氨基酸约50%的含量,是肌肉中甜味的主要贡献者,其甜味可使蟹肌肉更接近于大众口味[30]。在使用电子舌和人工感官对稻田和池塘养殖的中华绒螯蟹不同部位的研究中发现,稻田养殖模式下中华绒螯蟹肝胰腺整体喜好高于池塘蟹[2]。本实验中,池塘养殖中华绒螯蟹肌肉风味高于稻田,并且本实验中稻田养殖模式下未额外进行投饵,养殖环境及饵料不同会造成中华绒螯蟹生长性状不同[3, 8, 10]。取样部位、养殖环境及地理位置的不同,可能是导致本试验结果与以上稻田结果出现差异,也是导致本试验中池塘养殖中华绒螯蟹肌肉各呈味氨基酸及游离氨基酸总量高于稻田养殖模式的原因; 同时不同养殖品种对池塘和稻田的适应能力的不同,也会导致其风味出现较大差异[2, 7]。因此,不同养殖模式,选择合适的养殖品种和投喂方式,才能获得理想收益。
| [1] |
成永旭, 刘洪天, 常东, 等. 稻蟹共作与蟹单作模式下中华绒螯蟹肠道及养殖环境细菌群落组成比较[J]. 上海海洋大学学报, 2017, 26(5): 682-690. CHENG Y X, LIU H T, CHANG D, et al. A comparative study of microbiota from the intestine of Chinese mitten crab (Eriocheir sinensis) and their culture environment between rice-crab co-culture and crab monoculture models[J]. Journal of Shanghai Ocean University, 2017, 26(5): 682-690. |
| [2] |
张家奇, 张龙, 王锡昌. 稻田养殖和池塘养殖对中华绒螯蟹滋味品质的影响[J]. 食品工业科技, 2017, 38(13): 229-236. ZHANG J Q, ZHANG L, WANG X C. Effects of rice culture and pond culture on the quality of Chinese mitten crab (Eriocheir sinensis)[J]. Science and Technology of Food Industry, 2017, 38(13): 229-236. DOI:10.13386/j.issn1002-0306.2017.13.044 |
| [3] |
郝向举, 李义. 蟹源地衣芽孢杆菌ESB3对中华绒螯蟹生长及部分免疫指标的影响研究[J]. 饲料工业, 2011, 32(2): 23-27. HAO X J, LI Y. Effect of bacillus licheniformis ESB3 on growth and immunity index for Eriocheir sinensis[J]. Feed Industry, 2011, 32(2): 23-27. DOI:10.3969/j.issn.1001-991X.2011.02.005 |
| [4] |
HOU D W, HUANG Z J, ZENG S Z, et al. Intestinal bacterial signatures of white feces syndrome in shrimp[J]. Applied Microbiology and Biotechnology, 2018, 102(8): 3701-3709. DOI:10.1007/s00253-018-8855-2 |
| [5] |
DING Z F, CAO M J, ZHU X S, et al. Changes in the gut microbiome of the Chinese mitten crab (Eriocheir sinensis) in response to white spot syndrome virus (WSSV) infection[J]. Journal of Fish Diseases, 2017, 40(11): 1561-1571. DOI:10.1111/jfd.12624 |
| [6] |
WANG A R, RAN C, RINGØ E, et al. Progress in fish gastrointestinal microbiota research[J]. Reviews in Aquaculture, 2018, 10(3): 626-640. DOI:10.1111/raq.12191 |
| [7] |
LIU Q, LONG Y N, LI B, et al. Rice-shrimp culture: a better intestinal microbiota, immune enzymatic activities, and muscle relish of crayfish (Procambarus clarkii) in Sichuan Province[J]. Applied Microbiology and Biotechnology, 2020, 104(21): 9413-9420. DOI:10.1007/s00253-020-10797-4 |
| [8] |
LI K, GUAN W, WEI G, et al. Phylogenetic analysis of intestinal bacteria in the Chinese mitten crab (Eriocheir sinensis)[J]. Journal of Applied Microbiology, 2007, 103(3): 675-682. DOI:10.1111/j.1365-2672.2007.03295.x |
| [9] |
MARDINOGLU A, SHOAIE S, BERGENTALL M, et al. The gut microbiota modulates host amino acid and glutathione metabolism in mice[J]. Molecular Systems Biology, 2015, 11(10): 834. DOI:10.15252/msb.20156487 |
| [10] |
TAO H, DU B B, WANG H, et al. Intestinal microbiome affects the distinctive flavor of Chinese mitten crabs in commercial farms[J]. Aquaculture, 2018, 483: 38-45. DOI:10.1016/j.aquaculture.2017.09.031 |
| [11] |
CHEN D W, ZHANG M. Non-volatile taste active compounds in the meat of Chinese mitten crab (Eriocheir sinensis)[J]. Food Chemistry, 2007, 104(3): 1200-1205. DOI:10.1016/j.foodchem.2007.01.042 |
| [12] |
CHEN X W, CHEN H H, LIU Q H, et al. High plasticity of the gut microbiome and muscle metabolome of Chinese mitten crab (Eriocheir sinensis) in diverse environments[J]. Journal of Microbiology and Biotechnology, 2021, 31(2): 240-249. DOI:10.4014/jmb.2011.11018 |
| [13] |
JIN Y X, WU S S, ZENG Z Y, et al. Effects of environmental pollutants on gut microbiota[J]. Environmental Pollution, 2017, 222: 1-9. DOI:10.1016/j.envpol.2016.11.045 |
| [14] |
CLARKE S F, MURPHY E F, O'SULLIVAN O, et al. Exercise and associated dietary extremes impact on gut microbial diversity[J]. Gut, 2014, 63(12): 1913-1920. DOI:10.1136/gutjnl-2013-306541 |
| [15] |
ZHENG L, XIE S W, ZHUANG Z X, et al. Effects of yeast and yeast extract on growth performance, antioxidant ability and intestinal microbiota of juvenile Pacific white shrimp (Litopenaeus vannamei)[J]. Aquaculture, 2020, 530: 735941. |
| [16] |
王晨赫, 周彦锋, 方弟安, 等. 饥饿与重摄食对河蟹肠道菌群结构的影响[J]. 水生生物学报, 2019, 43(4): 748-756. WANG C H, ZHOU Y F, FANG D A, et al. Effects of starvation and refeeding on intestinal microflora of Chinese mitten crab (Eriocheir sinensis)[J]. Acta Hydrobiologica Sinica, 2019, 43(4): 748-756. |
| [17] |
陆宏达, 赵欢, 张小俊, 等. 正常和低品质中华绒螯蟹肠道菌群结构的比较分析[J]. 江苏农业科学, 2020, 48(20): 176-178. LU H D, ZHAO H, ZHANG X J, et al. Comparative analysis of intestinal flora structure between normal and low quality Chinese mitten crab Eriocheir sinensis[J]. Jiangsu Agricultural Sciences, 2020, 48(20): 176-178. |
| [18] |
KITTLE R P, MCDERMID K J, MUEHLSTEIN L, et al. Effects of glyphosate herbicide on the gastrointestinal microflora of Hawaiian green turtles (Chelonia mydas) Linnaeus[J]. Marine Pollution Bulletin, 2018, 127: 170-174. DOI:10.1016/j.marpolbul.2017.11.030 |
| [19] |
SHIN N R, WHON T W, BAE J W. Proteobacteria: microbial signature of dysbiosis in gut microbiota[J]. Trends in Biotechnology, 2015, 33(9): 496-503. DOI:10.1016/j.tibtech.2015.06.011 |
| [20] |
BERGOGNE-BÉRÉZIN E, TOWNER K J. Acinetobacter spp. as nosocomial pathogens: microbiological, clinical, and epidemiological features[J]. Clinical Microbiology Reviews, 1996, 9(2): 148-165. DOI:10.1128/CMR.9.2.148 |
| [21] |
KIM J Y, KWON Y M, KIM I S, et al. Effects of the Brown seaweed Laminaria japonica supplementation on serum concentrations of IgG, triglycerides, and cholesterol, and intestinal microbiota composition in rats[J]. Frontiers in Nutrition, 2018, 5: 23. DOI:10.3389/fnut.2018.00023 |
| [22] |
JIN Y X, ZENG Z Y, WU Y, et al. Oral exposure of mice to carbendazim induces hepatic lipid metabolism disorder and gut microbiota dysbiosis[J]. Toxicological Sciences, 2015, 147(1): 116-126. DOI:10.1093/toxsci/kfv115 |
| [23] |
WALTERS W A, XU Z, KNIGHT R. Meta-analyses of human gut microbes associated with obesity and IBD[J]. FEBS Letters, 2014, 588(22): 4223-4233. DOI:10.1016/j.febslet.2014.09.039 |
| [24] |
TAO J H, DUAN J A, JIANG S, et al. Polysaccharides from Chrysanthemum morifolium Ramat ameliorate colitis rats by modulating the intestinal microbiota community[J]. Oncotarget, 2017, 8(46): 80790-80803. DOI:10.18632/oncotarget.20477 |
| [25] |
BACHÈRE E, GUEGUEN Y, GONZALEZ M, et al. Insights into the anti-microbial defense of marine invertebrates: the penaeid shrimps and the oyster Crassostrea gigas[J]. Immunological Reviews, 2010, 198(1): 149-168. |
| [26] |
ZHENG R K, LIU R, SHAN Y Q, et al. Characterization of the first cultured free-living representative of Candidatus Izemoplasma uncovers its unique biology[J]. The ISME Journal, 2021, 15(9): 2676-2691. DOI:10.1038/s41396-021-00961-7 |
| [27] |
SUN S M, YANG M, FU H T, et al. Altered intestinal microbiota induced by chronic hypoxia drives the effects on lipid metabolism and the immune response of oriental river prawn Macrobrachium nipponense[J]. Aquaculture, 2020, 526: 735431. DOI:10.1016/j.aquaculture.2020.735431 |
| [28] |
YE G L, DONG X H, YANG Q H, et al. Dietary replacement of fish meal with peanut meal in juvenile hybrid grouper (Epinephelus fuscoguttatus ♀×Epinephelus lanceolatus ♂ ): Growth performance, immune response and intestinal microbiota[J]. Aquaculture Reports, 2020, 17: 100327. |
| [29] |
宋黎黎, 高建操, 邵乃麟, 等. 越冬暂养对雌性中华绒螯蟹的营养品质及风味的影响[J]. 上海海洋大学学报, 2021, 30(5): 800-811. SONG L L, GAO J C, SHAO N L, et al. Effects of overwintering cultivation on nutritional quality and flavor of female Eriocheir sinensis[J]. Journal of Shanghai Ocean University, 2021, 30(5): 800-811. |
| [30] |
WU N, FU X Y, ZHUANG K J, et al. Effects of dietary replacement of fish oil by vegetable oil on proximate composition and odor profile of hepatopancreas and gonad of Chinese mitten crab (Eriocheir sinensis)[J]. Journal of Food Biochemistry, 2019, 43(10): e12646. |
2. Agricultural and Rural Bureau of Cuiping District, Yibin 644000, Sichuan, China
 2022,
Vol. 31
2022,
Vol. 31


