2. 上海海洋大学 科技部海洋生物科学国际研究中心, 上海 201306
脂肪酸去饱和酶(fatty acid desaturase,FAD)是在脂肪酸上引入不饱和键的酶。根据FAD所作用的底物,可以将FAD分为3类[1-3]:(1)酰基酯去饱和酶(acyl-lipid desaturase)是与植物叶绿体膜、内质网膜以及蓝藻类囊体膜相结合的FAD[1],将双键引入被酯化于甘油脂上的脂肪酸中。(2)酰基-酰基载体蛋白(acyl carrier protein,ACP)去饱和酶(acyl-ACP desaturase),此类酶多存在于藻类及高等植物叶绿体的基质,在结合于ACP上的脂肪酸中引入双键[4-5]。(3)酰基-CoA去饱和酶(acyl-CoA desaturase),此类酶是一种内质网膜的结合蛋白,多存在于动物和酵母等真菌细胞中,它将双键引入至结合于CoA上的脂肪酸中[6]。
缺刻缘绿藻(Myrmecia incisa Reisigl)属绿藻门(Chlorophyta)共球藻纲(Trebouxiophyceae),藻细胞常呈球形,叶绿体较大,形态常为缺刻状[7]。研究[8]发现,缺刻缘绿藻能够合成大量的花生四烯酸(arachidonic acid,20∶ 4Δ5, 8, 11, 14,ArA),通过缺氮培养藻细胞中ArA可占细胞总脂肪酸的60%、藻体干质量的7%。罗梦柳等[9]和童牧等[10]研究表明,在脂肪酸合成途径中,亚油酸(linoleic acid,18∶ 2Δ9, 12,LA)是Δ6系列脂肪酸合成途径中ArA的前体,同时也是Δ3系列脂肪酸α-亚麻酸(α-linolenic acid,18∶ 3Δ9, 12, 15,ALA)的前体。李慧等[11]研究发现,在酵母中LA转化为ALA时通过ω3系列FAD中Δ15 FAD发挥去饱和作用,于LA碳链上的第15位脱氢生成。但缺刻缘绿藻的ω3 FAD是膜结合蛋白,在缺刻缘绿藻中的叶绿体中发挥主要作用,结合酿酒酵母中进行的Δ15去饱和反应,因此预测缺刻缘绿藻的Δ15 FAD属于酰基酯去饱和酶。
为了探究缺刻缘绿藻中Δ15 FAD与何种脂肪酸结合载体结合产生去饱和功能,选用具有不同脂肪酸结合载体的生物对象进行Δ15 FAD基因的转基因操作,以此来验证Δ15 FAD与何种脂肪酸结合载体结合产生去饱和反应。聚球藻(Synechococcus sp.)PCC7942属于蓝藻门,细胞结构简单,只有核糖体这一细胞器。研究[12-13]发现,聚球藻PCC7942内主要通过酰基载体蛋白去饱和酶以及酰基酯去饱和酶与脂肪酸结合进行去饱和反应,并且藻细胞内只含有Δ9 FAD基因,可以作为酰基-ACP供体来验证Δ15 FAD的功能。酿酒酵母(Saccharomyces cerevisiae)INVSc1胞内缺乏Δ12、ω3等脂肪酸去饱和酶[14-15],脂肪酸组分主要包括棕榈酸(16∶ 0)、软油酸(palmitoleic acid,16∶ 1Δ7)、硬脂酸(18∶ 0)和油酸(oleic acid,18∶ 1Δ9)[11, 16],其脂肪酸主要由酰基-CoA去饱和酶以及酰基酯去饱和酶与脂肪酸结合进行合成。Δ15 FAD功能的研究进一步完善了缺刻缘绿藻ω3系列脂肪酸合成途径,为提高多不饱和脂肪酸产量奠定了基础。
1 材料与方法 1.1 生物材料来源与培养缺刻缘绿藻H4301藻种来源于Culture collection of algae Charles University of Prague(CAUP),由暨南大学张成武教授馈赠。将适量的藻种接种于BG-11培养基[17]中,在温度为25 ℃、光照强度为115 μmol photons/(m2·s)的条件下,每天光照12 h培养。待藻细胞生长至对数期时,在4 ℃下、5 500 r/min离心10 min,收集藻细胞,用灭菌去离子水洗涤2次。液氮速冻后,-80 ℃保存备用。
聚球藻PCC7942购于中国科学院淡水藻种库。置于温度为25 ℃、光照强度为115 μmol photons/(m2·s)的人工培养箱中,使用BG-11培养基,每天光照培养12 h。
载体pMD19-T和pYES2分别购自TaKaRa公司和Thermo公司;载体pCAMBIA1300为实验室保存。酿酒酵母INVSc1菌株(His-、Leu-、Trp-、Ura-缺陷型)购自Thermo公司,于YPD培养基中培养。大肠杆菌(Escherichia coli)DH5α感受态细胞购自天根生化科技(北京)有限公司,于LB培养基中培养。
1.2 缺刻缘绿藻的RNA提取及cDNA合成将液氮冻存的缺刻缘绿藻置于盛满液氮的研钵中进行研磨。然后按照操作说明,按每50 mg藻粉加入1 mL的比例加入TRIzol试剂(Thermo公司);在4 ℃下、以12 000 r/min的转速离心10 min,取上清液加入预冷的氯仿;得到水相并加入异丙醇以沉降RNA,使用75%乙醇洗涤沉淀,在4 ℃下、以8 000 r/min的转速离心5 min。在沉淀中加入适量的DEPC水,溶解RNA,利用Nanodrop2000测定RNA浓度。
使用反转录(RT)-PCR试剂盒(TaKaRa)并按照其说明将提取的总RNA合成为cDNA第一链,作为克隆Δ15 FAD基因(Δ15 FAD)的模板。
1.3 携带缺刻缘绿藻Δ15 FAD基因的重组表达载体构建 1.3.1 克隆载体pMD19T-Δ15FAD的构建根据pCAMBIA1300载体、pYES2载体和缺刻缘绿藻Δ15 FAD基因序列(GenBank登录号:EU658930)设计1对特异性引物:上游引物(Δ15 FAD-F)序列为5′-cgGAATTCATGCAGGCCCCCACTATGT-3′,下游引物(Δ15 FAD -R)序列为5′-gcTCTAGACTACACATCCGAGCCACTG-3′(小写字母为保护碱基,斜体分别为Eco RⅠ和Xba Ⅰ酶切识别位点)。25 μL扩增反应体系中含有2×Taq Plus PCR MasterMix 12.5 μL;上、下游引物(10 μmol/L)各1 μL;模板1 μL;无RNA酶水9.5 μL。PCR反应程序:94 ℃预变性5 min,35个循环包括94 ℃变性1 min、63.8 ℃退火1 min、72 ℃延伸2 min,最后72 ℃延伸10 min,4 ℃保存。
使用琼脂糖凝胶电泳检测PCR产物。胶回收纯化该产物并将其连接至载体pMD19-T以构建质粒pMD19T-Δ15 FAD。然后转化大肠杆菌DH5α感受态细胞,筛选阳性克隆后送至生工生物工程(上海)股份有限公司进行序列分析。
1.3.2 双元表达载体pC-Δ15 FAD的构建使用天根生化科技(北京)有限公司生产的质粒提取试剂盒提取pMD19T-Δ15 FAD质粒;使用限制性内切酶Eco RⅠ和Xba Ⅰ对质粒pCAMBIA1300和pMD19T-Δ15 FAD进行同样的双酶切反应。20 μL的酶切反应体系:10 μmol/L缓冲液2 μL;0.1% BSA 2 μL;DNA(≤2 μg)4 μL;限制性内切酶Eco RⅠ和Xba Ⅰ各1 μL;无RNA酶水10 μL。37 ℃消化反应4 h,琼脂糖凝胶电泳后回收酶切产物。使用T4 DNA连接酶将酶切后的载体片段和目的基因进行连接以构建双元表达载体pC-Δ15FAD。连接反应体系:5×连接反应缓冲液4 μL;载体片段DNA约为3×10-11 mol;Δ15 FAD基因目的片段约9×10-11 mol;T4 DNA连接酶1 μL;无RNA酶的水7 μL。16 ℃下连接反应10~20 h后,转化大肠杆菌DH5α感受态细胞。阳性克隆筛选及菌液PCR验证后,将阳性克隆菌液送至生工生物工程(上海)股份有限公司进行序列分析。测序无误后,-20 ℃保存菌种备用。
1.4 重组表达载体的遗传转化 1.4.1 将重组表达载体pC-Δ15 FAD转化聚球藻PCC7942按1.3节方法利用质粒提取试剂盒自大肠杆菌中提取重组表达质粒pC-Δ15 FAD,利用聚球藻PCC7942藻细胞在天然状态下即可进行遗传转化的特性[18],收集聚球藻细胞并与pC-Δ15FAD混合;利用Bio-Rad公司生产的电穿孔仪,选择Agr程序,电击1次;立即加入1 mL的BG-11培养基,置于人工培养箱中恢复培养4~5 h;然后涂布在含有卡那霉素(Kan)的BG-11固体培养基上进行筛选。挑出在固体平板上生长的聚球藻细胞,接种于BG-11液体培养基中继续培养至稳定生长期。使用十六烷基三甲基溴化铵(CTAB)法[19]提取转基因聚球藻的DNA,利用特异性引物Δ15FAD -F和Δ15FAD -R进行PCR反应以验证。同时使用空载体pCAMBIA1300进行遗传转化以作为阴性对照。
1.4.2 重组表达载体pY-Δ15 FAD的构建及在酿酒酵母中的转化按照李慧等[11]的方法将Δ15 FAD的ORF序列连接至pYES2上以构建pY-Δ15FAD;然后将构建的重组质粒先后转化至大肠杆菌DH5α及酿酒酵母INVSc1菌株,以转空载体pYES2的酿酒酵母作为阴性对照;经菌液PCR及测序验证后,作为实验对象。
1.5 添加外源LA培养转基因细胞系以野生型和转空载体的聚球藻和酿酒酵母为对照,将上述携带缺刻缘绿藻Δ15 FAD基因的转基因聚球藻和转基因酿酒酵母活化培养后,按1∶ 100的比例分别接种于BG-11和含2%半乳糖的SC-U液体培养基中;添加50 μL终质量浓度为200 μg/mL的LA(Sigama),并在培养基加入1%的表面活性剂IGEPAL CA-630(Sigama)以乳化LA便于其进入细胞;置于温度为25 ℃、光照强度为115 μmol photons/(m2·s)的光照培养箱中每天光照12 h,将聚球藻培养至稳定期,或置于28 ℃摇床中以180 r/min的转速将酵母培养36~72 h至稳定期。实验设置3个平行样品,同时设置未添加LA的实验组。
1.6 酵母和聚球藻脂肪酸组成的GC-MS分析 1.6.1 总脂的提取及脂肪酸甲酯化采用改良的Bligh-Dyer脂类提取法[20-21]抽提对照组、转基因聚球藻和转基因酵母的总脂。具体步骤如下:自对照组和转基因组中,分别取相同细胞数量的细胞系,经液氮速冻及真空冷冻干燥;每个样品中加入1.5 mL氯仿、0.6 mL无菌水、1 mL酸洗玻璃珠后涡旋振荡30 min,以5 000 r/min的转速离心10 min;残渣使用氯仿、甲醇、水(体积比为1∶ 2∶ 0.8)溶液抽提2次后,收集所有有机相加入1/2体积的灭菌水充分混匀;同样离心收集下层有机相[聚球藻的样品中含有大量叶绿素,应使用CNWBOND Carbon-GCB固相萃取小柱(CNW,德国)去除总脂中的叶绿素]至酯化瓶,氮气吹干后备用。
在上述获得的总脂中加入1 mL的4%硫酸甲醇(体积比为4∶ 96)溶液,用N2充满酯化瓶后迅速封口,置于80 ℃水浴1 h以甲酯化反应;待样品瓶冷却后加入1 mL的0.9%氯化钠溶液和1 mL正己烷,以5 500 r/min的转速离心10 min,收集上清液;上清液经0.45 μm的滤头过滤后,收集滤液至新的酯化瓶中,N2吹干后用500 μL的正己烷复溶;-20 ℃保存备用。
1.6.2 脂肪酸的GC-MS分析以脂肪酸甲酯混标溶液(Sigama)作为参考,采用7890-5975型GC-MS联用仪(Angilent公司)对转基因酵母和转基因聚球藻的脂肪酸组成进行定性和定量分析[22]。GC色谱柱为HP-5MS 5% phenyl-ethylsiloxane型毛细管柱(30 m×250 μm×0.25 μm);柱箱运行程序为50 ℃保持1 min,以10 ℃/min升到150 ℃保持1 min,然后再以4 ℃/min升到250 ℃保持3 min。采用自动进样器上样,上样量为1 μL,分流比为50∶ 1。氦气为载气体,流速1 mL/min。MS采集参数选用EMV模式,跟踪检测的离子能为70 eV。参照质谱存储的数据库NIST08 MS进行脂肪酸组分的鉴定。使用GC-MS数据分析软件,通过面积归一化法计算各种脂肪酸的百分含量,转化效率为新产物的量与剩余外源底物的量和新产物的量之和的比值。结果均以3个反应的平均值±标准差来表示。使用SPSS 22.0进行差异显著性分析,若P < 0.05,则差异显著。
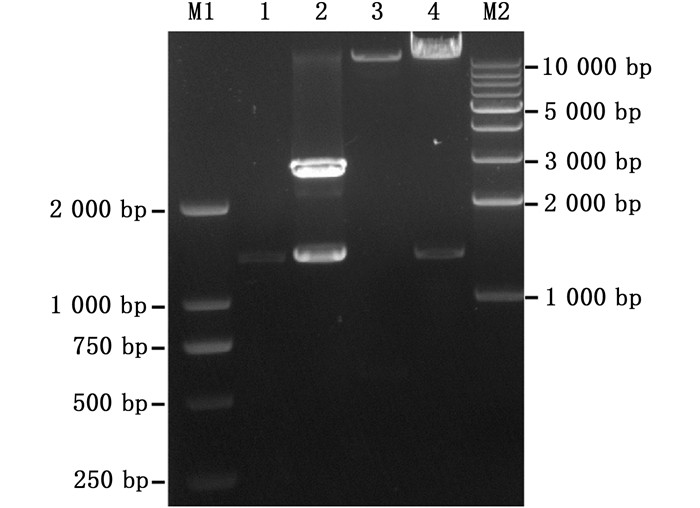
2 结果 2.1 双元表达载体pC-Δ15 FAD的构建使用TRIzol试剂法抽提缺刻缘绿藻总RNA,然后利用RT-PCR试剂盒合成cDNA第一链。根据缺刻缘绿藻Δ15 FAD基因的开放阅读框(ORF)序列(GenBank登录号:EU658930)以及载体pMD19-T和pCAMBIA1300的多克隆位点序列,设计1对携带限制性内切酶Eco R Ⅰ和Xba Ⅰ识别位点的特异性引物Δ15 FAD -F和Δ15 FAD -R,以合成的cDNA第一链为模板进行PCR反应。扩增产物(图 1泳道1)被连接至克隆质粒pMD19-T上以构建pMD19T-Δ15 FAD。经序列分析可知目的基因的大小为1 311 bp,除了限制性内切酶识别位点的序列外,其余序列与在GenBank中注册的该基因ORF序列完全一致。
|
1. Δ15 FAD基因ORF的扩增产物;2.克隆质粒pMD19T-Δ15FAD经EcoR Ⅰ和Xba Ⅰ的双酶切产物;3.质粒pCAMBIA1300的双酶切产物;4.重组双元表达载体pC-Δ15 FAD的双酶切产物;M1.DL2000的DNA分子量标准;M2.1 kb DNA ladder的分子量标准。 1.The amplified product of Δ15 FAD ORF; 2. The double-digested product of the construct pMD19T-Δ15 FAD using EcoR Ⅰ and Xba Ⅰ; 3.The double-digested product of the empty plasmid pCAMBIA1300 with the same restriction enzymes as in Lane 2; 4.The double-digested product of the recombinant binary expression vector pC-Δ15 FAD with the same restriction enzymes as in Lane 2; M1.DL2000 DNA standard; M2.1 kb DNA ladder standard. 图 1 双元表达载体pC-Δ15 FAD构建过程中相关产物的电泳图 Fig. 1 Electrophoresis patterns of several products related to the construction of recombinant binary expression vector pC-Δ15 FAD |
使用限制性内切酶Eco R Ⅰ和Xba Ⅰ对载体pMD19T-Δ15 FAD和pCAMBIA1300分别进行双酶切反应(图 1泳道2和3),将目的片段用T4 DNA连接酶连接以构建双元表达载体pC-Δ15 FAD,然后转化大肠杆菌DH5α感受态细胞。挑取阳性克隆菌落并经PCR验证以及测序分析,确保目的基因及其插入方向的正确性。所构建的pC-Δ15 FAD经双酶切反应,其产物经电泳检测,结果(图 1泳道4)显示了2条产物带,其中一条分子量较小的与目的基因的大小一致(图 1泳道4对泳道1),另一条分子量较大的与载体pCAMBIA1300的双酶切产物一致(图 1泳道4对泳道3),从而表明已成功地构建携带缺刻缘绿藻Δ15 FAD基因ORF的双元表达载体pC-Δ15 FAD。
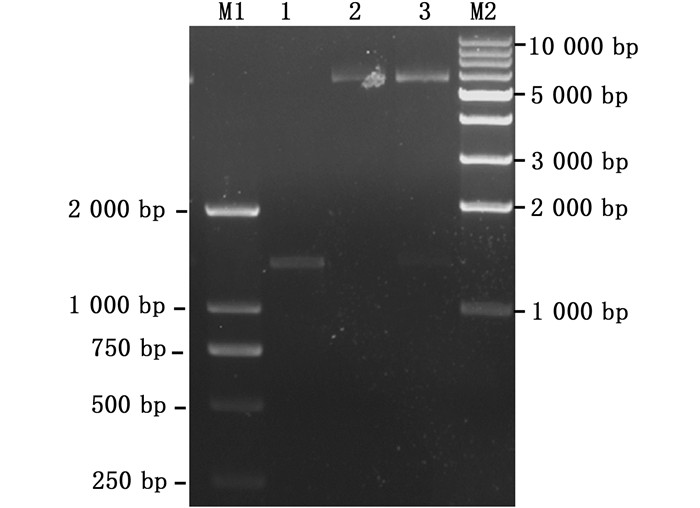
2.2 双元表达载体pY-Δ15 FAD的构建利用质粒提取试剂盒(天根)从李慧等[11]构建的转Δ15 FAD基因酿酒酵母以及实验室保存的含pYES2空载菌种中抽提质粒,得到质粒pYES2和pY-Δ15 FAD,使用限制性内切酶Eco R Ⅰ和Xba Ⅰ对pYES2空载和质粒pY-Δ15 FAD分别进行双酶切反应(图 2泳道2和3),泳道3中较小的条带与扩增得到的缺刻缘绿藻Δ15 FAD基因的ORF(图 2泳道1)大小一致,较大的条带与载体pYES2双酶切产物大小一致,从而表明我们已成功地得到携带缺刻缘绿藻Δ15 FAD基因ORF的双元表达载体pY-Δ15 FAD。
|
1. Δ15 FAD基因ORF的扩增产物;2.质粒pYES2的双酶切产物;3.重组双元表达载体pY-Δ15 FAD的双酶切产物;M1.DL2000的DNA分子量标准;M2.1 kb DNA ladder的分子量标准。 1.The amplified product of Δ15 FAD ORF; 2. The double-digested product of the empty plasmid pYES2 using EcoR Ⅰ and Xba I; 3.The double-digested product of the recombinant binary expression vector pY-Δ15 FAD with the same restriction enzymes as in Lane 2; M1. DL2000 DNA standard; M2.1 kb DNA ladder standard. 图 2 双元表达载体pY-Δ15 FAD构建过程中相关产物的电泳图 Fig. 2 Electrophoresis patterns of several products related to the construction of recombinant binary expression vector pY-Δ15 FAD |
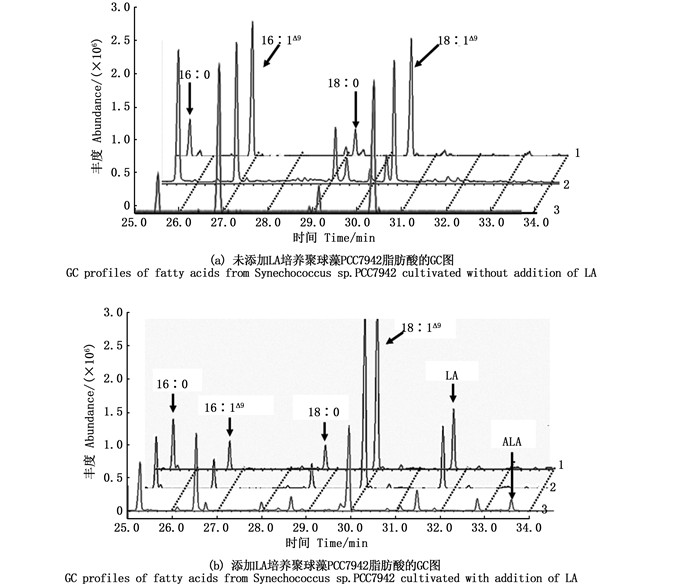
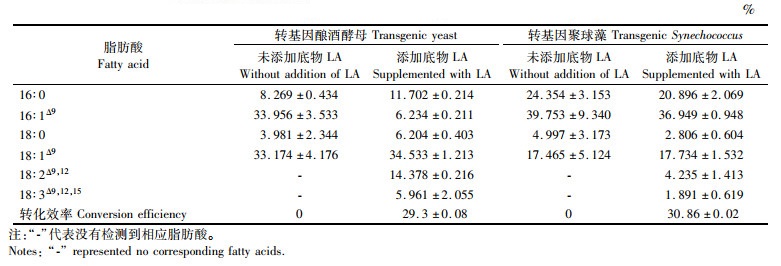
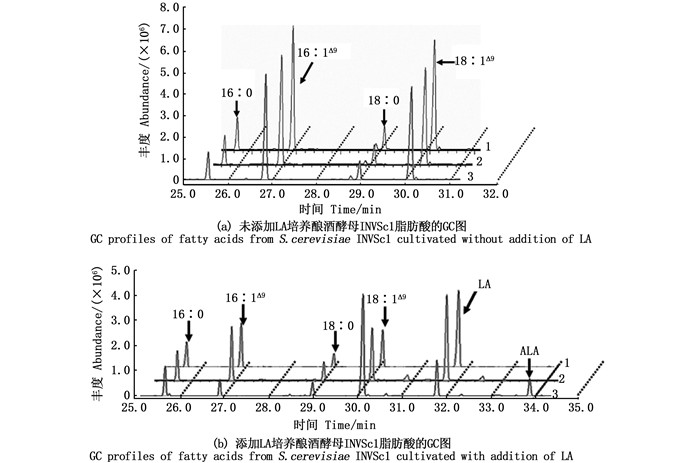
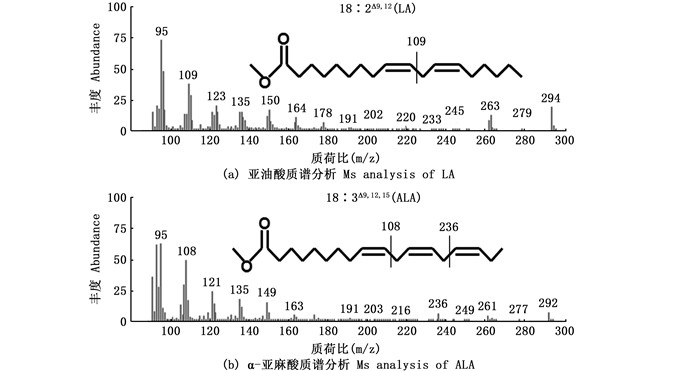
将2.2节构建的质粒pC-Δ15 FAD和pY-Δ15 FAD分别转化至聚球藻PCC7942和酿酒酵母INVSc1中,取相同细胞数的转基因聚球藻和转基因酵母,分别添加等量的LA底物进行培养;待二者生长至稳定期时,分别取含Δ15 FAD基因拷贝数相同的转基因酵母和转基因聚球藻,经液氮速冻后真空冷冻干燥,提取二者的总脂肪酸。脂肪酸甲酯的GC-MS分析结果(图 3和图 4)显示,以野生型和转空载体组为对照,在未添加底物LA时,聚球藻(图 3a)和酿酒酵母(图 4a)转基因组均无新的峰出现。添加底物LA后,与对照组相比,聚球藻(图 3b)和酿酒酵母(图 4b)转基因组均出现一个新的峰。通过对照标准脂肪酸甲酯的GC图谱及新产物的质谱图(图 5b),证实该物质为ALA。此外,添加底物LA后,聚球藻和酿酒酵母对照组和转基因组中均检测出LA(图 3b、图 4b、图 5a)。说明Δ15 FAD的基因产物能够在酿酒酵母和聚球藻的进入细胞的LA中Δ15碳位引入一个双键,从而产生可以检测到的ALA(表 1)。根据转基因细胞系各种脂肪酸的组分(表 1),计算可知,在转基因酵母和转基因聚球藻中,LA转化为ALA的效率分别为29.31%和30.86%;经统计分析,两者之间无显著差异(P>0.05)。
|
1. 野生型聚球藻;2. 转空载聚球藻;3. 转目的基因聚球藻。 1. The wild-type Synechococcus sp. PCC7942; 2. The transgenic Synechococcus sp. PCC7942 with plasmid of pCAMBIA1300; 3. The transgenic Synechococcus sp. PCC7942 with recombinant plasmid of pC-Δ15 FAD. 图 3 聚球藻PCC7942脂肪酸的GC图谱 Fig. 3 GC profiles of fatty acids from Synechococcus sp. PCC7942 |
|
表 1 转基因酵母和转基因聚球藻在添加外源LA培养后脂肪酸的组分 Tab.1 Fatty acid compositions of the transgenic Synechococcus and yeast under the culture supplemented with exogenous linoleic acid (LA) |
|
1.野生型酵母;2.转空载酵母;3.转目的基因酵母。 1. The wild-type yeast; 2. The transgenic yeast with plasmid of pYES2; 3. The transgenic yeast with recombinant plasmid of pY-Δ15 FAD. 图 4 酿酒酵母脂肪酸的GC图谱 Fig. 4 GC profiles of fatty acids from S. cerevisiae |
|
图 5 LA和ALA的MS图谱 Fig. 5 MS profiles of LA and ALA |
聚球藻PCC7942[23-25]和酿酒酵母[26-27]细胞的脂肪酸组成简单,这些脂肪酸主要包含棕榈酸(16∶ 0)、棕榈油酸(palmitoleic acid,16∶ 1Δ9)、硬脂酸(18∶ 0)和油酸(oleic acid,18∶ 1Δ9)。聚球藻PCC7942和酿酒酵母只含有单不饱和脂肪酸,因为它们均只有1个Δ9 FAD,尽管聚球藻的Δ9 FAD是在酰基酯sn-1和sn-2位上的脂肪酸经过脱氢反应引入第1个双键[1],而酿酒酵母的却和结合于CoA上的脂肪酸发生相同的作用[27-28]。本研究从非转基因的聚球藻PCC7942和酿酒酵母中也只检测到这4种主要脂肪酸(图 3、图 4、表 1),说明本研究的脂肪酸检测结果是可信的。在检测聚球藻的脂肪酸组成时,保留时间29 ~30 min,发现了3个小峰(图 3a),但经质谱分析,发现它们都是一些芳香族非脂肪酸的杂质峰;同样的情况也出现在添加外源LA培养的转基因聚球藻中(图 3b),但杂质峰的保留时间不同。
由于脂肪酸组成简单及其成熟的遗传转化系统,聚球藻PCC7942[12, 29]和酿酒酵母[14, 30]常被用于FAD的功能鉴定。本实验室也曾利用酿酒酵母分别对缺刻缘绿藻Δ9 FAD [31]、Δ6 FAD [32]及ω3 FAD [11]的基因功能进行了分析。本研究将缺刻缘绿藻Δ15 FAD基因的ORF首次转化至聚球藻中,获得转基因藻后若添加外源的LA来培养,自转基因的藻细胞中能检测到ALA(图 3a和3b),说明缺刻缘绿藻的Δ15 FAD也能在聚球藻PCC7942中把部分进入细胞的LA饱和成ALA。这与李慧等[11]在酿酒酵母中的研究结果完全一致,从而进一步明确了缺刻缘绿藻Δ15 FAD基因的功能。
本研究利用双元表达载体pCAMBIA1300将缺刻缘绿藻的Δ15 FAD基因转化至聚球藻PCC7942,这样,Δ15 FAD基因的ORF在pCAMBIA1300载体上CaMV35S启动子的作用下[33]整合至聚球藻的基因组中,因而能随着聚球藻的基因组被翻译和表达,从而发挥作用,而在酿酒酵母中的重组表达则使用质粒pYES2,它在酵母细胞中独立复制、翻译和表达[34],因此完全不同于聚球藻的遗传转化。但缺刻缘绿藻的Δ15 FAD无论在酿酒酵母还是在聚球藻中,均能将LA脱氢去饱和成ALA,且两者的转化效率(分别达到了29.31%和30.86%)无显著差异。结合缺刻缘绿藻Δ15 FAD属于膜结合去饱和酶(含4个跨膜区两次跨膜[8])且缺乏细胞色素b5功能域[35],以及酿酒酵母和聚球藻中都存在,这个无差异的转化效率预示着缺刻缘绿藻Δ15 FAD可能属于酰基酯FAD,即在酰基酯sn-1和sn-2位上的脂肪酸自羧基端的第15个碳位上进行去饱和反应。但排除不了缺刻缘绿藻Δ15 FAD在酿酒酵母和聚球藻中对与脂肪酸相结合的ACP或CoA不存在底物特异性的可能,不过,基于至今所报道的Δ15 FAD对底物的特异性[36]来分析,这种对底物没有偏好型的可能性非常小。因此,要想明确缺刻缘绿藻的Δ15 FAD一定是酰基酯的FAD,还需要先重组表达这个膜结合蛋白,并在体外添加酰基酯作为反应底物的直接实验证据来证明。
| [1] |
MURATA N, WADA H. Acyl-lipid desaturases and their importance in the tolerance and acclimatization to cold of cyanobacteria[J]. Biochemical Journal, 1995, 308(1): 1-8. DOI:10.1042/bj3080001 |
| [2] |
LOS D A, MURATA N. Structure and expression of fatty acid desaturases[J]. Biochimica et Biophysica Acta (BBA)-Lipids and Lipid Metabolism, 1998, 1394(1): 3-15. DOI:10.1016/S0005-2760(98)00091-5 |
| [3] |
TOCHER D R, LEAVER M J, HODGSON P A. Recent advances in the biochemistry and molecular biology of fatty acyl desaturases[J]. Progress in Lipid Research, 1998, 37(2/3): 73-117. |
| [4] |
HWANGBO K, AHN J W, LIM J M, et al. Overexpression of stearoyl-ACP desaturase enhances accumulations of oleic acid in the green alga Chlamydomonas reinhardtii[J]. Plant Biotechnology Reports, 2014, 8(2): 135-142. DOI:10.1007/s11816-013-0302-3 |
| [5] |
KAZAZ S, MIRAY R, BAUD S. Acyl-acyl carrier protein desaturases and plant biotic interactions[J]. Cells, 2021, 10(3): 674. DOI:10.3390/cells10030674 |
| [6] |
MACARTNEY A, MARESCA B, COSSINS A R. Acyl-CoA desaturases and the adaptive regulation of membrane lipid composition[J]. Temperature Adaptation of Biological Membranes, 1994, 14(7): 129-139. |
| [7] |
REISIGL H. Zur systematik und Ökologie alpiner bodenalgen[J]. Österreichische Botanische Zeitschrift, 1964, 111(4): 402-499. DOI:10.1007/BF01372910 |
| [8] |
李春阳, 杜道海, 于水燕, 等. 缺刻缘绿藻ω3脂肪酸去饱和酶基因的特性及在氮饥饿过程中相对转录量的分析[J]. 水产学报, 2010, 34(9): 1343-1353. LI C Y, DU D H, YU S Y, et al. Characterization of a ω3 fatty acid desaturase gene from Myrmecia incisa and its relative transcription during the stress course of nitrogen starvation[J]. Journal of Fisheries of China, 2010, 34(9): 1343-1353. |
| [9] |
罗梦柳, 桑敏, 张成武, 等. 氮、磷对缺刻缘绿藻生长、总脂及花生四烯酸积累的影响[J]. 天然产物研究与开发, 2010, 22(3): 378-382. LUO M L, SANG M, ZHANG C W, et al. Effects of nitrogen and phosphorus on the growth, total fatty acids and arachidonic acid production of Parietochloris incisa[J]. Natural Product Research and Development, 2010, 22(3): 378-382. |
| [10] |
童牧, 于水燕, 欧阳珑玲, 等. 氮饥饿与磷饥饿促使缺刻缘绿藻花生四烯酸含量增加的比较[J]. 水产学报, 2011, 35(5): 763-773. TONG M, YU S Y, OUYANG L L, et al. Comparison of increased arachidonic acid content in Myrmecia incisa cultured during the course of nitrogen or phosphorus starvation[J]. Journal of Fisheries of China, 2011, 35(5): 763-773. |
| [11] |
李慧, 欧阳珑玲, 周志刚. 缺刻缘绿藻ω3脂肪酸去饱和酶基因(ω3FAD )在酿酒酵母中的低温诱导表达[J]. 农业生物技术学报, 2012, 20(7): 735-744. LI H, OUYANG L L, ZHOU Z G. Low-temperature-induced expression of a ω3 fatty acid desaturase gene (ω3FAD ) from Myrmecia incisa in Saccharomyces cerevisiae[J]. Journal of Agricultural Biotechnology, 2012, 20(7): 735-744. |
| [12] |
SANTOS-MERINO M, GARCILLÁN-BARCIA M P, DE LA CRUZ F. Engineering the fatty acid synthesis pathway in Synechococcus elongatus PCC 7942 improves omega-3 fatty acid production[J]. Biotechnology for Biofuels, 2018, 11(1): 239. DOI:10.1186/s13068-018-1243-4 |
| [13] |
LOS D A, MURATA N. Membrane fluidity and its roles in the perception of environmental signals[J]. Biochimica et Biophysica Acta (BBA)-Biomembranes, 2004, 1666(1/2): 142-157. |
| [14] |
NIU B, GUO L, ZHAO M M, et al. Molecular cloning, characterization, and expression of an ω-3 fatty acid desaturase gene from Sapium sebiferum[J]. Journal of Bioscience and Bioengineering, 2008, 106(4): 375-380. DOI:10.1263/jbb.106.375 |
| [15] |
LIU W, SUN Z, CHEN C X, et al. Novel insights into type 2 diacylglycerol acyltransferases in microalga Myrmecia incisa[J]. Journal of Applied Phycology, 2021, 33(1): 25-35. DOI:10.1007/s10811-020-02071-x |
| [16] |
欧秀元. 多不饱和脂肪酸ARA和EPA合成途径在酿酒酵母中的重构[D]. 天津: 南开大学, 2011. OU X Y. Polyunsaturated fatty acids ARA and EPA biosynthetic pathway in Saccharomyces cerevisiae[D]. Tianjin: Nankai University, 2011. |
| [17] |
STANIER R Y, KUNISAWA R, MANDEL M, et al. Purification and properties of unicellular blue-green algae (Order Chroococcales)[J]. Bacteriological Reviews, 1971, 35(2): 171-205. DOI:10.1128/br.35.2.171-205.1971 |
| [18] |
SHESTAKOV S V, KHYEN N T. Evidence for genetic transformation in blue-green alga Anacystis nidulans[J]. Molecular and General Genetics, 1970, 107(4): 372-375. DOI:10.1007/BF00441199 |
| [19] |
余海霞, 罗聪, 徐趁, 等. 一种简单高效提取高质量转基因拟南芥和烟草DNA的方法[J]. 分子植物育种, 2016, 14(6): 1436-1440. YU H X, LUO C, XU C, et al. A simple and efficient method for high quality DNA extraction from transgenic Arabidopsis and tobacco[J]. Molecular Plant Breeding, 2016, 14(6): 1436-1440. |
| [20] |
BLIGH E G, DYER W J. A rapid method of total lipid extraction and purification[J]. Canadian Journal of Biochemistry and Physiology, 1959, 37(8): 911-917. DOI:10.1139/o59-099 |
| [21] |
魏东, 袁显渊, 向文洲. 微藻总脂含量快速测定的方法比较[J]. 现代食品科技, 2014, 30(7): 242-246. WEI D, YUAN X Y, XIANG W Z. Comparison of methods for rapid determination of total lipid content in microalgae[J]. Modern Food Science & Technology, 2014, 30(7): 242-246. |
| [22] |
MEYER A, KIRSCH H, DOMERGUE F, et al. Novel fatty acid elongases and their use for the reconstitution of docosahexaenoic acid biosynthesis[J]. Journal of Lipid Research, 2004, 45(10): 1899-1909. DOI:10.1194/jlr.M400181-JLR200 |
| [23] |
SATO N, MURATA N, MIURA Y, et al. Effect of growth temperature on lipid and fatty acid compositions in the blue-green algae, Anabaena variabilis and Anacystis nidulans[J]. Biochimica et Biophysica Acta (BBA)-Lipids and Lipid Metabolism, 1979, 572(1): 19-28. DOI:10.1016/0005-2760(79)90196-6 |
| [24] |
MURATA N, WADA H, GOMBOS Z. Modes of fatty acid desaturation in cyanobacteria[J]. Plant and Cell Physiology, 1992, 33(7): 933-941. |
| [25] |
LOS D A, MIRONOV K S. Modes of fatty acid desaturation in cyanobacteria: An update[J]. Life, 2015, 5(1): 554-567. DOI:10.3390/life5010554 |
| [26] |
HUNTER K, ROSE A H. Lipid composition of Saccharomyces cerevisiae as influenced by growth temperature[J]. Biochimica et Biophysica Acta (BBA)-Lipids and Lipid Metabolism, 1972, 260(4): 639-653. |
| [27] |
STUKEY J E, MCDONOUGH V M, MARTIN C E. The OLE1 gene of Saccharomyces cerevisiae encodes the Δ9 fatty acid desaturase and can be functionally replaced by the rat stearoyl-CoA desaturase gene[J]. Journal of Biological Chemistry, 1990, 265(33): 20144-20149. |
| [28] |
MCDONOUGH V M, STUKEY J E, MARTIN C E. Specificity of unsaturated fatty acid-regulated expression of the Saccharomyces cerevisiae OLE1 gene[J]. The Journal of Biological Chemistry, 1992, 267(9): 5931-5936. |
| [29] |
HITZ W D, CARLSON T J, BOOTH J R, et al. Cloning of a higher-plant plastid Δ-6 fatty acid desaturase cDNA and its expression in a cyanobacterium[J]. Plant Physiology, 1994, 105(2): 635-641. |
| [30] |
BEAUDOIN F, MICHAELSON L V, HEY S J, et al. Heterologous reconstitution in yeast of the polyunsaturated fatty acid biosynthetic pathway[J]. Proceedings of the National Academy of Sciences of the United States of America, 2000, 97(12): 6421-6426. |
| [31] |
XUE W B, LIU F, SUN Z, et al. A Δ-9 fatty acid desaturase gene in the microalga Myrmecia incisa Reisigl: cloning and functional analysis[J]. International Journal of Molecular Sciences, 2016, 17(7): 1143. |
| [32] |
ZHANG L, CAO H S, NING P, et al. Functional characterization of a Δ6 fatty acid desaturase gene and its 5'-upstream region cloned from the arachidonic acidrich microalga Myrmecia incisa Reisigl (Chlorophyta)[J]. Journal of Oceanology and Limnology, 2018, 36(6): 2308-2321. |
| [33] |
TAN X L, KONG F M, ZHANG L L, et al. Cloning and analysis of hemoglobin gene in cyanobacterium and transformation into Brassica napus[J]. Acta Agronomica Sinica, 2009, 35(1): 66-70. |
| [34] |
詹瑶, 曹高燚, 曹雪松, 等. 酿酒酵母起始密码子表达载体pYES2-ATG的构建及应用[J]. 分子植物育种, 2018, 16(23): 7683-7688. ZHAN Y, CAO G Y, CAO X S, et al. Construction and application of initiation codon expression vector pYES2-ATG of Saccharomyces cerevisiae[J]. Molecular Plant Breeding, 2018, 16(23): 7683-7688. |
| [35] |
刘凡, 李慧, 李春阳, 等. 缺刻缘绿藻FAD 基因的序列特征及其相对转录量对氮饥饿的响应[J]. 中国水产科学, 2012, 19(5): 729-740. LIU F, LI H, LI C Y, et al. Characterization of fatty acid desaturase (FAD) genes in Myrmecia incisa and the effect of nitrogen starvation on their transcription[J]. Journal of Fishery Sciences of China, 2012, 19(5): 729-740. |
| [36] |
WANG M X, CHEN H Q, GU Z N, et al. ω3 fatty acid desaturases from microorganisms: structure, function, evolution, and biotechnological use[J]. Applied Microbiology and Biotechnology, 2013, 97(24): 10255-10262. |
2. International Research Center for Marine Biosciences, Ministry of Science and Technology, Shanghai Ocean University, Shanghai 201306, China
 2022,
Vol. 31
2022,
Vol. 31


