2. 上海海洋大学 大洋渔业资源可持续开发教育部重点实验室, 上海 201306;
3. 国家远洋渔业工程技术研究中心, 上海 201306;
4. 远洋渔业协同创新中心, 上海 201306
斑马鱼(Danio rerio)隶属硬骨鱼纲(Osteichthyes)鲤形目(Cypriniformes)鲤科(Cyprinidae)短担尼鱼属(Danio),是一种原产于南亚地区的小型热带淡水鱼。自STREISINGER教授于20世纪70年代将斑马鱼作为实验对象进行遗传、发育等方面的研究[1]后,斑马鱼一直用于各方面的研究。斑马鱼体积小,饲养方便,且容易繁殖,发育快,相比于小鼠等哺乳类动物操作简单,且节约费用,这使得斑马鱼成为继小鼠后又一重要的模式生物[2]。此外,斑马鱼的应激调节系统、心血管功能系统的功能各方面都与人类高度相似。可见,斑马鱼作为模式生物,有其独特的优势[3-4]。
核糖体蛋白的经典功能是与核糖体RNA一起进行蛋白质的合成过程。但是,目前越来越多的研究发现,核糖体蛋白在其经典功能的基础上可能承担着核糖体以外的其他生物学功能[5-7]。生物体在遭受刺激的情况下,部分核糖体蛋白会出现形成核糖体以外的生物学功能,帮助机体恢复正常的生理活动来协助细胞适应应激环境[8]。例如,核糖体蛋白的多核糖体缔合在人类细胞中被低氧改变,低氧是肿瘤微环境的特征,缺氧影响人核糖体蛋白S12的多聚体分布和核糖体蛋白mRNA的选择性剪接[9]。研究[10]发现,斑马鱼基因组中编码核糖体蛋白的一些基因有着非常重要的功能。例如,利用CRISPR/Cas9技术成功编辑了斑马鱼rpl15基因,rpl15突变体产生了类似先天性纯红细胞再生障碍性贫血疾病的表型。低温诱导的斑马鱼rpl11表达量降低,导致P53表达量缓慢升高[11]。斑马鱼早期胚胎中,rpl5和prl11的缺陷将产生红细胞再生障碍性贫血患者症状,导致类似的血液生发障碍及胚胎的轻度畸形[12]。
microRNA(miRNA)可以通过调控其靶基因的表达水平从而参与细胞的各类进程,并参与许多关键的生理进程与病理过程,其作用非常重要[13]。已有研究[14]表明:一些核糖体基因的表达受到miRNA的调控。例如,miRNA-223-3p是调控缺血人结肠微血管内皮细胞(CMEC)增殖的核心miRNA,miRNA-223-3p可通过调节核糖体蛋白rps6kb1/HIF-1α信号通路,抑制缺血CMEC血管新生的迁移和增殖过程,从而降低血管新生能力。miR-455-3p通过靶向调控fabp4,从而抑制卵巢癌细胞增殖、迁移,有望成为卵巢癌的潜在治疗靶点[15]。另外,目前有很多研究表明,miRNA是对植物和动物中的环境胁迫做出响应的关键调节剂。通过调节基因表达,miRNA可以恢复或重建新的表达程序,从而增强细胞对压力的耐受性[16],而低氧环境则属于分环境胁迫中的重要一种[17]。本项目前期研究中,对低氧胁迫和常氧条件下斑马鱼鳃进行了小RNA组测序比较,结果发现,仅有2个miRNAs在低氧胁迫下的斑马鱼鳃中表达量显著下降。这两个显著低表达的miRNAs很可能调控着低氧胁迫下鳃中显著高表达的基因。
鱼类鳃器官与外界水体环境直接接触,最先感知水体溶氧变化[18],是绝大部分水生动物氧气交换的直接器官[19],本文选择斑马鱼作为实验对象,通过对低氧胁迫与常氧条件下斑马鱼鳃组织转录组测序分析,比较低氧胁迫与常氧条件斑马鱼鳃中核糖体蛋白家族基因的表达差异,希望为揭示斑马鱼的低氧适应机制提供新思路。
1 材料与方法 1.1 材料实验所用野生型的斑马鱼(WT)来自于大洋渔业资源可持续开发教育部重点实验室,饲养水体溶解氧质量浓度为6. 7 mg/L,养殖温度为28 ℃。每日8: 00、18: 00喂食丰年虫。
试验试剂包括Trizol试剂(吉泰生物公司),DEPC水(生物生工有限公司)、氯仿(24∶ 1)、异丙醇和无水乙醇。
实验器材包括移液器、各类枪头、剪刀、镊子、锡纸、EP管、研磨管、研磨棒、超净工作台、冰块(均购自上海生工生物有限公司)、离心机(德国Eppendorf有限公司)、旋涡仪和低氧驯化箱(长沙华晓电子科技有限公司定制)。
1.2 方法 1.2.1 转录组测序转录组测序样本为本实验室培养的多代斑马鱼,分别放置于2.0 mg/L与1.0 mg/L的低氧驯化箱中,进行为期两周的低氧胁迫,利用质量浓度6.7 mg/L的氧作为常氧对照组。低氧和常氧采用的斑马鱼样本为相同品系,且饲养条件等完全相同。
两周后,取出3种不同氧质量浓度条件下的斑马鱼并进行解剖,取出鳃组织。为保证RNA提取的质量,每个氧质量浓度下养殖15条斑马鱼,解剖这些斑马鱼的鳃,并分作两组重复。Trizol法提取的RNA进行电泳检测,这样共取得6个样本,分别为常氧下鳃组织G1、G2;1.0 mg/L氧质量浓度下鳃组织1.0G1、1.0G2;2.0 mg/L氧质量浓度下鳃组织2.0G1、2.0G2。以上实验步骤均选择在冰上进行。
1.2.2 转录组分析鳃组织低氧转录组数据使用本实验室已测除热休克蛋白基因[19]外均未发表的低氧数据和已发表的常氧数据[20],使用Python的相关包获取其clean数据,使用hisat2将其转换为bam格式,使用samtools将其排序后使用cufflinks软件进行差异基因分析。使用Rstudio软件以及其程序包clusterprofile,org.Dr.eg.db等R包进行GO富集的分析,使用ggplot2、pheatmap等绘图相关的R包进行图形绘制。
1.2.3 靶基因预测使用TargetScanFish(http://www.targetscan.org/fish_62/)和miRanda(http://www.microrna.org/microrna/home.do)两个网站同时进行miRNA的靶基因预测。已知生物体在面对环境变化时会通过改变蛋白或者调节mRNA的翻译以适应环境,本文对鳃进行低氧胁迫后对与蛋白的变化以及mRNA的翻译调节有关的表达显著的核糖体蛋白差异基因进行分析,使用在低氧胁迫下斑马鱼鳃中表达量显著下降的2条miRNAs(miR-455-3p和miR-125-b-5p)对核糖体蛋白差异的60个基因进行靶基因预测。
1.2.4 qRT-PCR验证在生工生物进行序列合成(表 1),每个样本、每个基因设置3个平行实验,配制好后放入qPCR仪进行检测,后将检测到的数据导出分析。

|
表 1 实时荧光定量PCR引物 Tab.1 Primers for qRT-PCR |
提取常氧、1.0 mg/L低氧质量浓度条件下的斑马鱼鳃组织蛋白,从每个样本提取30 μg的蛋白进行12% SDS-PAGE蛋白胶电泳。用孔径为0. 22 μm的PVDF膜(Millipore) 在300 mA下转膜70 min。封闭后分别用Anti-RPL11抗体(1∶ 1 000)和Anti-ACTIN抗体(1∶ 1 000) 孵育过夜。再用PBST洗涤3次(每次10 min),二抗孵育(1∶ 10 000),室温下静置1 h。用PBST洗涤3次,加入显影液,使用化学发光成像仪成像,检测蛋白的表达。
1.2.6 靶基因验证将性成熟的斑马鱼于前一夜进行交配,取其产的受精卵,使用显微注射技术将tol2-EGFP-rpl13和tol2-EGFP-rplp1质粒, 稀释质粒为终质量浓度100 ng/μL并与50 μmol/L miR-455-3p(实验组)、50 μmol/L NC(阴性对照组)共同注射至野生型斑马鱼Ⅰ细胞期受精卵中,空质粒(空白对照组)单独注射至受精卵中,24~48 h后拍照观察荧光强度变化。收集注射后的斑马鱼受精卵,用PBS洗涤3次,然后用RIPA缓冲液(Beyotime,中国)和蛋白酶抑制剂PMSF(Sigma-Aldrich,St.Louis,MO,USA)在冰上裂解30 min,随后放入4 ℃ 12 000 r/min离心10 min,将上清吸入新的1.5 mL EP管内,加入4X SDS Buffer,煮10 min后放入-20 ℃备用。
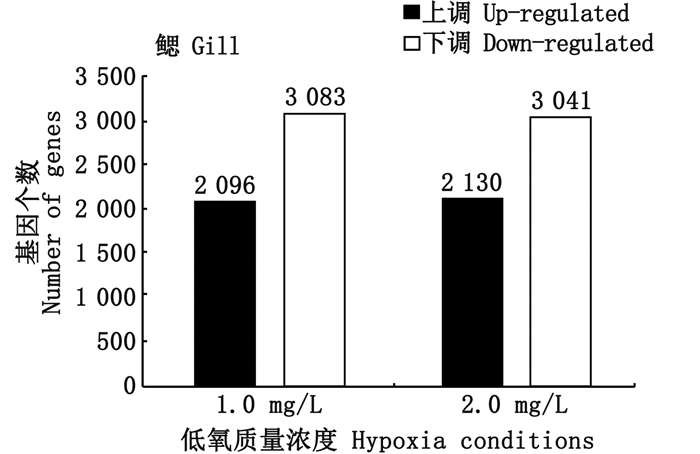
2 结果与分析 2.1 鳃组织转录组基因表达差异分析转录组分析结果显示,在当低氧质量浓度为1.0 mg/L时,发现5 179个基因表达量有显著变化,占表达基因总数的29.08%。2.0 mg/L氧质量浓度胁迫下斑马鱼鳃组织中,有5 171个显著差异表达的基因,占总表达基因数的29.04%。差异基因统计如图 1所示。
|
图 1 不同氧质量浓度下斑马鱼鳃中差异基因统计图 Fig. 1 Differential genes in gill tissue under normoxia and hypoxia conditions |
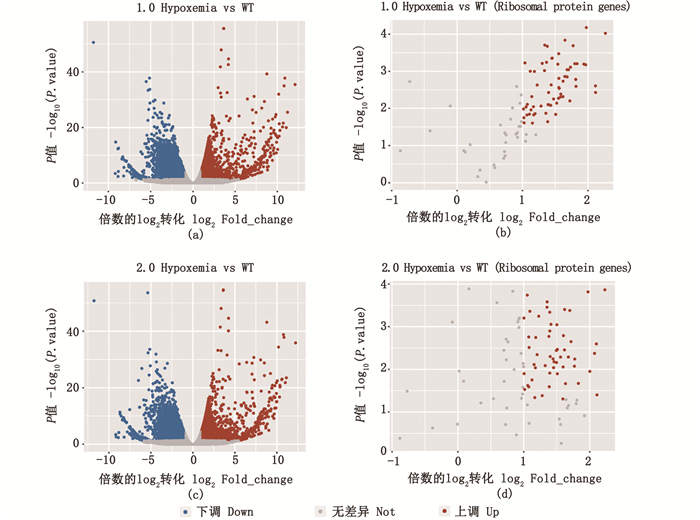
差异基因的火山图如图 2所示。图 2(a)和图 2(b)是1.0 mg/L低氧条件下,与常氧条件下鳃组织差异基因比较。图 2(c)和图 2(d)是2.0 mg/L低氧条件下,与常氧条件下鳃组织差异基因比较。图 2(b)和图 2(d)是两种低氧胁迫下核糖体蛋白基因表达差异变化比较。
|
横坐标代表基因不同样品中表达倍数变化,纵坐标代表基因表达量变化的统计学显著程度,图中的散点代表各个基因,灰色圆点表示无显著性差异的基因,红色圆点表示显著上调的差异基因,蓝色圆点表示显著下调的差异基因。(a) 1.0 mg/L低氧与常氧条件下斑马鱼鳃组织差异基因比较;(b) 1.0 mg/L低氧与常氧条件下斑马鱼鳃组织核糖体差异基因比较;(c) 2.0 mg/L低氧与常氧条件下斑马鱼鳃组织差异基因比较;(d) 2.0 mg/L低氧与常氧条件下斑马鱼鳃组织核糖体差异基因比较。 the abscissa represents change gene expression in different samples, ordinate represents the amount of gene expression changes of statistically significant level, the scatter in the graph represents each gene, gray dot said there was no significant difference of gene, red dot said rise significantly differences in gene, and blue dot said significantly lower genetic variations. (a) Comparison of differential genes in zebrafish gill tissue under 1.0 mg/L hypoxia and normoxia conditions; (b) Comparison of ribosome differential genes in zebrafish gill tissues under 1.0 mg/L hypoxia and normoxia conditions; (c) Comparison of differential genes in zebrafish gill tissue under 2.0 mg/L hypoxia and normoxia conditions; (d) Comparison of ribosome differential genes in zebrafish gill tissue under 2.0 mg/L hypoxia and normoxia conditions. 图 2 不同低氧质量浓度下斑马鱼鳃组织中差异基因的火山图 Fig. 2 Volcano Plot of differently expressed genes in gill at different oxygen mass concentrations |
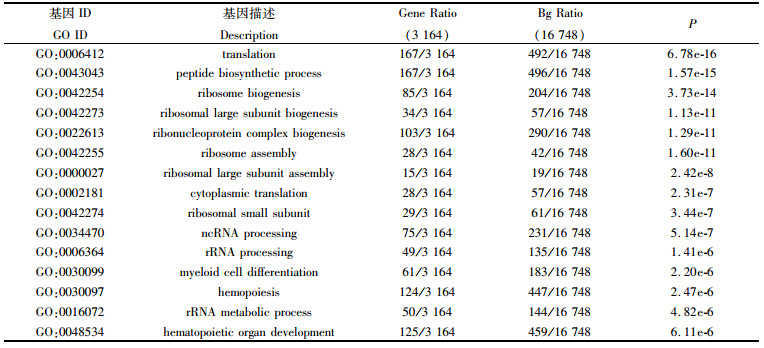
在两种低氧胁迫下,不同氧质量浓度下的差异基因的差别较小(图 1)。因此,选择1.0 mg/L氧质量浓度与常氧质量浓度下的鳃组织转录组数据来比较分析斑马鱼核糖体蛋白基因的变化情况。差异基因GO富集分析结果显示:在低氧胁迫下鳃中差异基因GO富集(生物过程)的前15条GO通路中,均包括核糖体蛋白基因。5条通路与核糖体蛋白组装合成相关,包括核糖体生物发生“ribosome biogenesis”,核糖体大亚基生物发生“ribosomal large subunit biogenesis”,核糖体组装“ribosome assembly”,核糖体大亚基组装“ribosomal large subunit assembly”,核糖体小亚基“ribosomal small subunit ”这5条通路(表 2)。
|
表 2 1.0 mg/L低氧胁迫下鳃中差异基因GO富集分布 Tab.2 Differential gene GO enrichment distribution in gills under 1.0 mg/L hypoxia stress |
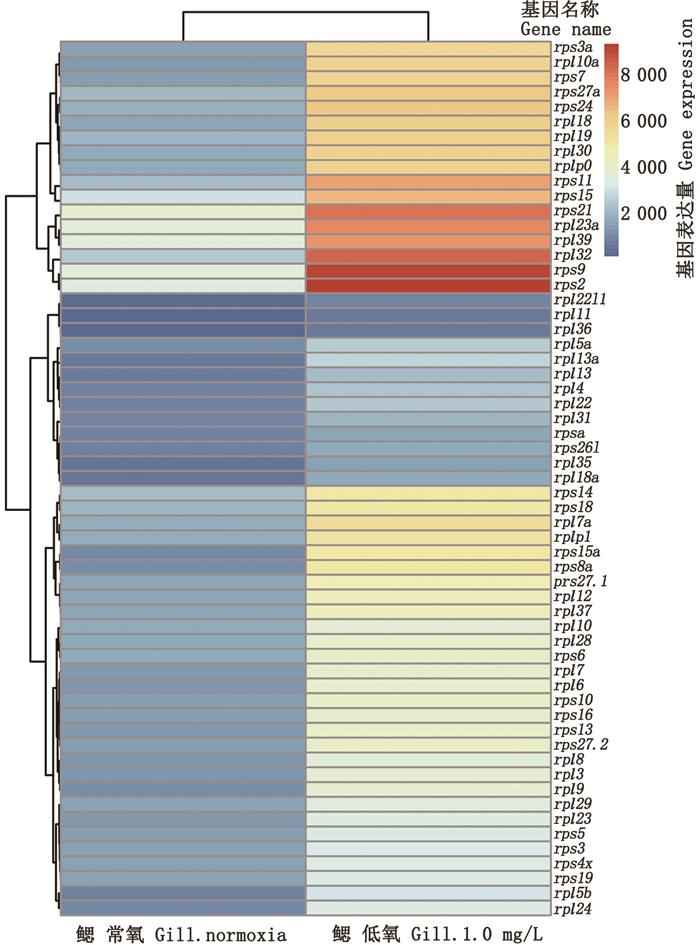
值得一提的是,在不同浓度的低氧胁迫下,发生显著改变的核糖体蛋白基因的表达量均为上调。在两个质量浓度的低氧胁迫下鳃中60个核糖体蛋白基因同时显著上调,其中,大亚基核糖体蛋白基因共有35个,小亚基核糖体蛋白基因有25个,见图 3。
|
图中的颜色代表了不同基因在低氧胁迫后的表达量,其中颜色由蓝到黄到红代表了表达量依次增加。 The colors in the figure represent the expression levels of different genes after hypoxia stress, where the colors from blue to yellow to red represent the sequential increase in the expression levels. 图 3 低氧胁迫下核糖体家族基因在鳃组织中差异表达分析 Fig. 3 Analysis of differential expression of ribosomal family genes in gill tissue under hypoxia stress |
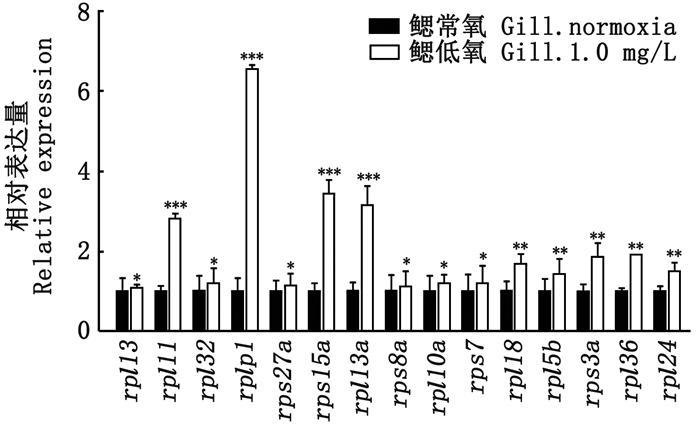
选择15个上述上调核糖体蛋白基因通过qRT-PCR进行验证,结果表明:在低氧条件下,15个核糖体蛋白基因的表达量均为上调(图 4)。
|
* 表示与对照组差异显著(P < 0. 05);**表示与对照组差异极显著(P < 0. 01);***表示与对照组差异极其显著(P < 0. 001)。 * means significant difference compared with the control (P < 0. 05); **means very significant difference compared with the control (P < 0. 01);***means extremely significant difference compared with the control (P < 0. 001). 图 4 低氧胁迫下核糖体家族基因在鳃组织中qRT-PCR差异表达分析 Fig. 4 Differential expression analysis of ribosome family genes in gill under hypoxia stress by qRT-PCR |
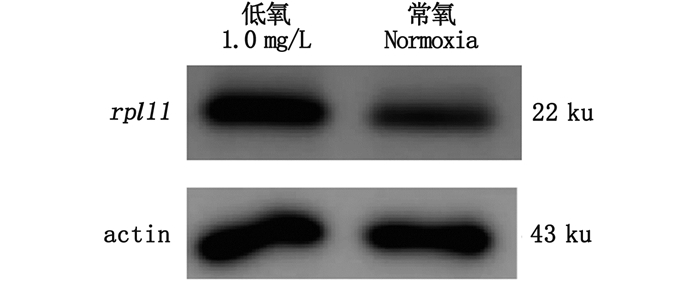
另外,利用购买到的抗体RPL11通过Western Blot进行验证,结果表明,在低氧条件下,rpl11蛋白的表达明显升高(图 5)。
|
图 5 低氧胁迫下核糖体家族基因rpl11在鳃组织中WB差异表达分析 Fig. 5 Differential expression analysis of ribosomal family gene rpl11 in gill tissues under hypoxia stress |
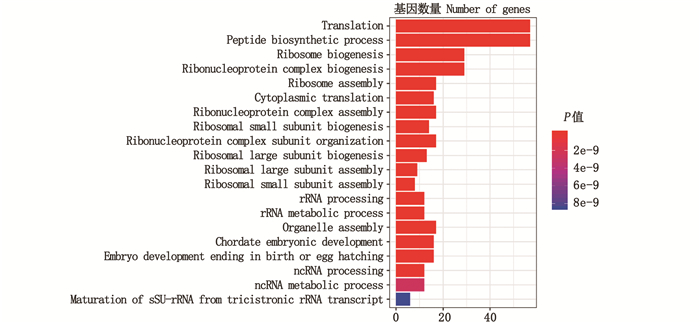
转录组结果表明,核糖体家族基因GO富集中,在“translation”中共发现了44个差异的核糖体蛋白基因在其上富集(图 6)。结合上文,认为在受低氧胁迫的情况下,生物体通过改变核糖体蛋白调节翻译来适应低氧环境。
|
图 6 鳃组织低氧差异核糖体蛋白基因GO富集 Fig. 6 Gill tissue hypoxic ribosomal protein gene GO enrichment |
生物信息学表明,改变的miRNA与预测的mRNA的表达呈负相关。在不同质量浓度的低氧胁迫下,发生显著改变的核糖体蛋白基因的表达量均为上调(图 3),推测这可能受到表达量下降的miRNA的调控。
因此,选择前期筛选出的在低氧条件下斑马鱼鳃中表达量显著下降的2个miRNAs,对60个核糖体蛋白基因进行靶基因预测。通过靶基因预测得知:miR-455-3p可以同时靶向rpl13和rplp1,其结合位点和目标匹配区域如表 3所示。

|
表 3 鳃中差异miRNA靶向核糖体蛋白基因靶点 Tab.3 Differential miRNA targeting ribosomal protein gene targets in the gills |
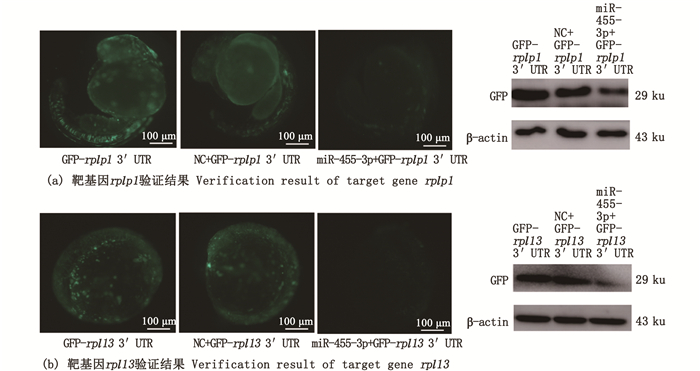
构建tol2-EGFP-rpl13和tol2-EGFP-rplp1质粒, 稀释质粒为终质量浓度100 ng/μL并与50 μmol/L miR-455-3p(实验组)、50 μmol/L NC(阴性对照组)共同注射至野生型斑马鱼Ⅰ细胞期受精卵中,空质粒(空白对照组)单独注射至受精卵中。24~48 h后拍照观察荧光强度变化(图 7),并且将卵收集,提取总蛋白进行Western blot,以检测其荧光蛋白的表达(图 7)。结果表明,miR-455-3p分别与rpl13和rplp1共同注射的荧光强度以及表达量显著低于对照组,进一步验证了miR-455-3p靶向作用于rpl13和rplp1。
|
图 7 斑马鱼显微注射检测GFP荧光表达 Fig. 7 Detection of the expression of GFP fluorescence |
对斑马鱼在不同低氧质量浓度(1.0 mg/L、2.0 mg/L)下进行为期两周的低氧胁迫,并取常氧(6.7 mg/L)作为对照。通过高通量测序测定在3种氧质量浓度下斑马鱼鳃组织的转录组,并分析相对于常氧,两个低氧质量浓度下鳃组织中的核糖体蛋白的变化。结果显示,在不同质量浓度的低氧胁迫下,发生显著改变的核糖体蛋白基因的表达量均为上调(图 3)。选择的15个核糖体蛋白基因qRT-PCR验证结果与转录组数据一致。通过GO富集分析可以看出,遗传信息处理过程富集的第一条通路为“translation”,在该条通路中共发现了44个差异的核糖体蛋白基因(图 6)。可以推测,在受低氧胁迫的情况下,生物体通过改变核糖体蛋白调节翻译来适应低氧环境。
值得一提的是:在鳃中表达量相对较高的差异核糖体蛋白基因中,发现有部分基因(如:rps3、rps27等)在应激状态下有其他生物学功能。rps3是在低氧胁迫下斑马鱼鳃中高表达的核糖体蛋白(图 3)。研究表明,在外界刺激造成DNA损伤后,rps3会过表达并参与修复DNA损伤[21]。与此同时,rps3也是一种蛋白依赖蛋白,能够调节纺锤体在有丝分裂过程中的运动并影响细胞周期的进程[22]。rps27也是在低氧胁迫下斑马鱼鳃中显著高表达的核糖体蛋白(图 3)。有研究[23]表明,机体在受到刺激并造成DNA损伤时会过表达rps27以响应DNA损伤。还有研究[24]表明,rps27a有着保护细胞正常形态的作用。
P53基因是一种重要的抑癌基因,在调节细胞增殖、凋亡和细胞周期中起关键作用,鼠微双蛋白(MDM2)皆可以负性调节P53抑癌基因,在应激条件下P53会被不同的基因激活或者稳定以保证细胞正常的凋亡,保持基因组的完整并清除衰老细胞, 而rpl23与rpl7在应激条件下可以与MDM2结合进而激活P53基因[25]。核糖体蛋白rpl22可以阻断P53-MDM2的通路以保护P53基因免被降解[26],同时也有报道[27]称rpl11可以结合并抑制MDM2的泛素连接酶,从而促进p53的稳定。
从差异基因的GO富集结果中可以看出,有大量的核糖体蛋白通过调节mRNA的翻译以面对低氧胁迫。结合核糖体蛋白在面对环境变化时具有其他生物学功能(如:修复受损RNA,控制细胞的不正常凋亡,调节细胞周期,维持细胞的正常形态等),可以推测,在低氧下核糖体蛋白基因的高表达将有助于适应低氧环境。
3.2 低氧胁迫下调控核糖体蛋白表达的miRNA生物体在面对环境的变化时会通过改变蛋白或者调节mRNA的翻译以适应环境。选择前期筛选出的在低氧条件下斑马鱼鳃中表达量显著下降的2个miRNAs,对60个核糖体蛋白基因进行靶基因预测。靶基因预测结果显示,miR-455-3p可以同时靶向rpl13和rplp1,并通过显微注射技术和蛋白免疫印迹技术进行靶基因验证,结果与预测相符。
有研究报道,核糖体蛋白基因rplp1对于登革热病毒和其他蚊媒黄病毒的复制是必要的。rplp1减轻了登革热病毒包膜编码序列中的核糖体悬浮,从而提高了蛋白质的稳定性。研究还发现,rplp1的缺失可以影响少数细胞mRNA核糖体密度。这表明rplp1在多通道跨膜蛋白的生物发生中发挥作用。另外,rplp1对核糖体的延伸具有重要的作用。rplp1可以通过提高共翻译折叠的效率来提高蛋白质稳定性[28]。可以预测,在低氧胁迫下的斑马鱼鳃中低表达的miR-455-3p通过靶向提高rplp1的表达,从而提高了低氧胁迫下蛋白质的稳定性。
另外,有研究报道,在单核细胞趋化蛋白中,核糖体基因rplp1的敲除降低了心肌细胞的增殖和分化,同时增加了成纤维细胞。在果蝇胚胎阶段中,心脏特异性rpl13的敲除,将导致“无心脏”表型[29]。可以推测,在低氧下斑马鱼鳃中低表达的miR-455-3p将通过靶向提高rpl13的表达,有可能增强了细胞的增殖以应对低氧胁迫。
总体而言,虽然目前关于鱼类鳃低氧应激相关的miRNA研究较少,但从这些miRNA在低氧条件下参与其他物种的作用可以推测,这些miRNA可能有着抑制细胞凋亡,增强器官的低氧耐受性,保护细胞免受缺氧带来的损伤等一系列功能。在低氧下斑马鱼鳃中低表达的miR-455-3p同时靶向两个显著上调的核糖体蛋白基因rpl13和rplp1,根据rpl13和rplp1已报道的功能,可以合理推测,miR-455-3p靶向提高rpl13和rplp1基因的表达,可以提升斑马鱼对低氧环境的适应性。
| [1] |
SARASAMMA S, VARIKKODAN M M, LIANG S T, et al. Zebrafish: A premier vertebrate model for biomedical research in Indian scenario[J]. Zebrafish, 2017, 14(6): 589-605. DOI:10.1089/zeb.2017.1447 |
| [2] |
刘昌盛, 穆宇, 杜久林. 斑马鱼在生命科学研究中的应用[J]. 生命科学, 2007, 19(4): 382-386. LIU C S, MU Y, DU J L. Application of the zebrafishin the research of life sciences[J]. Chinese Bulletin of Life Sciences, 2007, 19(4): 382-386. DOI:10.3969/j.issn.1004-0374.2007.04.006 |
| [3] |
SANTHAKUMAR K, JUDSON E C, ELKS P M, et al. A zebrafish model to study and therapeutically manipulate hypoxia signaling in tumorigenesis[J]. Cancer Research, 2012, 72(16): 4017-4027. DOI:10.1158/0008-5472.CAN-11-3148 |
| [4] |
张凡, 黄秋花, 陈赛娟, 等. 用斑马鱼模型研究低氧应激在造血和血液疾病中的作用[J]. 上海交通大学学报(医学版), 2016, 36(8): 1237-1241. ZHANG F, HUANG Q H, CHEN S J, et al. Utilization of the zebrafish model for studying the role of hypoxic stress in hematopoiesis and hematopoietic diseases[J]. Journal of Shanghai Jiaotong University(Medical Edition), 2016, 36(8): 1237-1241. DOI:10.3969/j.issn.1674-8115.2016.08.025 |
| [5] |
LIAN Z R, JIE L, LI L, et al. Human S15a expression is upregulated by hepatitis B virus X protein[J]. Molecular Carcinogenesis, 2004, 40(1): 34-46. DOI:10.1002/mc.20012 |
| [6] |
LAVOIE C, TAM R, CLARK M, et al. Suppression of a temperature-sensitive cdc33 mutation of yeast by a multicopy plasmid expressing a Drosophila ribosomal protein[J]. Journal of Biological Chemistry, 1994, 269(20): 14625-14630. DOI:10.1016/S0021-9258(17)36670-X |
| [7] |
KAWAGUCHI R, GIRKE T, BRAY E A, et al. Differential mRNA translation contributes to gene regulation under non-stress and dehydration stress conditions in Arabidopsis thaliana[J]. The Plant Journal, 2004, 38(5): 823-839. DOI:10.1111/j.1365-313X.2004.02090.x |
| [8] |
SAVADARP, BONHAM-SMITHP C. Differential transcript accumulation and subcellular localization of Arabidopsis ribosomal proteins[J]. Plant Science, 2014, 223: 134-145. DOI:10.1016/j.plantsci.2014.03.011 |
| [9] |
BRUMWELL A, FELL L, OBRESS L, et al. Hypoxia influences polysome distribution of human ribosomal protein S12 and alternative splicing of ribosomal protein mRNAs[J]. RNA, 2020, 26(3): 361-371. DOI:10.1261/rna.070318.119 |
| [10] |
彭涛, 周唯君, 刘含, 等. CRISPR/Cas9技术敲除斑马鱼rpl15基因对斑马鱼红系造血发育的影响[J]. 第三军医大学学报, 2021, 43(8): 683-691. PENG T, ZHOU W J, LIU H, et al. Effects of rpl15 gene knockout by CRISPR/Cas9 on zebrafisherythroid hematopoietic development[J]. Journal of Third Military Medical University, 2021, 43(8): 683-691. |
| [11] |
刘明丽, 杨文意, 王金凤, 等. 低温胁迫下鱼类鳃中RPL11/MDM2/P53信号通路相关基因及蛋白表达差异分析[J]. 大连海洋大学学报, 2021, 36(1): 51-56. LIU M L, YANG W Y, WANG J F, et al. Expression analysis of RPL11/MDM2/P53 pathway related gene and protein in gills of fish exposed to cold stress[J]. Journal of Dalian Ocean University, 2021, 36(1): 51-56. |
| [12] |
周杨. 斑马鱼RPL5和RPL11缺陷致使DBA病征的分子机制研究[D]. 武汉: 华中科技大学, 2014. ZHOU Y. Molecular mechanism research of hematopoietic Failure due RPL5 and RPLⅡ deficiency in a Zebrafish Model of diamond-blackfan Anemia[D]. Wuhan: Huazhong University of Science and Technology, 2014. |
| [13] |
REINHART B J, SLACK F J, BASSON M, et al. The 21-nucleotide let-7 RNA regulates developmental timing in Caenorhabditis elegans[J]. Nature, 2000, 403(6772): 901-906. DOI:10.1038/35002607 |
| [14] |
戴国华, 宋宪波, 马培泽, 等. 微小RNA-223-3p通过调节Rps6kb1/HIF-1α信号通路抑制缺血心肌微血管内皮细胞血管新生[J]. 中华心血管病杂志, 2014, 42(12): 1039-1047. DAI G H, SONG X B, MA P Z, et al. MicroRNA-223-3p inhibits the angiogenesis of ischemic myocardial microvascular endothelial cells via modulating Rps6kb1/HIF-1α signal pathway[J]. Chinese Journal of Cardiology, 2014, 42(12): 1039-1047. DOI:10.3760/cma.j.issn.0253-3758.2014.12.013 |
| [15] |
谢婷婷, 苏瑛, 吴利英, 等. miR-455-3p通过靶向调控转脂蛋白4抑制卵巢癌细胞SKOV-3的增殖、迁移及上皮间质转化[J]. 中国肿瘤生物治疗杂志, 2019, 26(3): 306-311. XIE T T, SU Y, WU L Y, et al. miR-455-3p inhibits proliferation, migration and epithelial-mesenchymal transition of ovarian cancer SKOV-3 cells by regulating translipoprotein 4[J]. Chinese Journal of Cancer Biotherapy, 2019, 26(3): 306-311. |
| [16] |
曾幼玲, 杨瑞瑞. 植物miRNA的生物学特性及在环境胁迫中的作用[J]. 中国农业科学, 2016, 49(19): 3671-3682. ZENG Y L, YANG R R. Biological characteristics of plant MicroRNAs and actions in environmental stresses[J]. Scientia Agricultura Sinica, 2016, 49(19): 3671-3682. DOI:10.3864/j.issn.0578-1752.2016.19.001 |
| [17] |
冉皓宇, 陈良标. 低温驯化对斑马鱼胚胎发育和mtDNA拷贝数的影响[J]. 生物学杂志, 2019, 36(5): 16-20. RAN H Y, CHEN L B. Effects of cold acclimation on the embryogenesis and mtDNA copy number in zebrafishembryos[J]. Journal of Biology, 2019, 36(5): 16-20. |
| [18] |
陈世喜, 王鹏飞, 区又君, 等. 急性和慢性低氧胁迫对卵形鲳鲹鳃器官的影响[J]. 南方水产科学, 2017, 13(1): 124-130. CHEN S X, WANG P F, OU Y J, et al. Acute and chronic hypoxia effect on gills of golden pompano (Trachinotu sovatus)[J]. South China Fisheries Science, 2017, 13(1): 124-130. |
| [19] |
狄治朝, 周涛, 许强华. 低氧胁迫与常氧条件下斑马鱼鳃中热休克蛋白基因家族的表达差异比较[J]. 大连海洋大学学报, 2018, 33(6): 690-695. DI Z C, ZHOU T, XU Q H. Expression comparisons of heat shock proteins gene in gills of zebrafish exposed to both normoxia and hypoxia[J]. Journal of Dalian Ocean University, 2018, 33(6): 690-695. |
| [20] |
HU P, LIU M L, LIU Y M, et al. Transcriptome comparison reveals a genetic network regulating the lower temperature limit in fish[J]. Scientific Reports, 2016, 6: 28952. DOI:10.1038/srep28952 |
| [21] |
YADAVILLI S, HEGDE V, DEUTSCH W A. Translocation of human ribosomal protein S3 to sites of DNA damage is dependant on ERK-mediated phosphorylation following genotoxic stress[J]. DNA Repair, 2007, 6(10): 1453-1462. DOI:10.1016/j.dnarep.2007.04.009 |
| [22] |
JANG C Y, KIM H D, ZHANG X H, et al. Ribosomal protein S3 localizes on the mitotic spindle and functions as a microtubule associated protein in mitosis[J]. Biochemical and Biophysical Research Communications, 2012, 429(1/2): 57-62. |
| [23] |
REVENKOVAE, MASSON J, KONCZ C, et al. Involvement of Arabidopsis thaliana ribosomal protein S27 in mRNA degradation triggered by genotoxic stress[J]. The EMBO Journal, 1999, 18(2): 490-499. |
| [24] |
叶嘉良, 陈健, 吕正兵, 等. 家蚕泛肽-核糖体蛋白S27a的表达及功能研究[J]. 蚕业科学, 2007, 33(3): 394-402. YE J L, CHEN J, LYU Z B, et al. Expression and functional research of BmUBRP S27a from silkworm, bombyxmori[J]. Sericulture Science, 2007, 33(3): 394-402. |
| [25] |
FARRAR J, FISHER R, O'BRIEN K, et al. Novel ribosomal and autosomal recessive non-ribosomal protein gene candidates in diamond Blackfan Anemia (DBA)[J]. Pediatric Blood & Cancer, 2014, 61(S1): S2-S3. |
| [26] |
BO C, FANG Z L, PENG L, et al. Cancer-mutated ribosome protein L22 (RPL22/eL22) suppresses cancer cell survival by blocking p53-MDM2 circuit[J]. Oncotarget, 2017, 8(53): 90651-90661. |
| [27] |
KAYAMAK, WATANABES, TAKAFUJI T, et al. GRWD1 negatively regulates p53 via the RPL11-MDM2 pathway and promotes tumorigenesis[J]. The EMBO Reports, 2017, 18(1): 123-137. |
| [28] |
CAMPOS R K, WIJERATNE H R S, SHAH P, et al. Ribosomal stalk proteins RPLP1 and RPLP2 promote biogenesis of flaviviral and cellular multi-pass transmembrane proteins[J]. Nucleic Acids Research, 2020, 48(17): 9872-9885. |
| [29] |
SCHROEDER A M, ALLAHYARI M, VOGLER G, et al. Model system identification of novel congenital heart disease gene candidates: focus on RPL13[J]. Human molecular genetics, 2019, 28(23): 3954-3969. |
2. Key Laboratory of Sustainable Exploitation of Oceanic Fisheries Resources, Ministry of Education, Shanghai Ocean University, Shanghai 201306, China;
3. National Distant-water Fisheries Engineering Research Center, Shanghai 201306, China;
4. Collaborative Innovation Center for Distant-water Fisheries, Shanghai 201306, China
 2022,
Vol. 31
2022,
Vol. 31


