2. 上海海洋大学 国家海洋生物科学国际联合研究中心, 上海 201306;
3. 上海海洋大学 水产种质资源发掘与利用教育部重点实验室, 上海 201306
体细胞通过TGF-β(transforming growth factor-β)信号途径与生殖细胞相互作用,促进性腺发育和配子成熟[1]。TGF-β家族在控制细胞增殖与性分化中起着重要的作用[2],并且与多囊卵巢综合征(polycystic ovarian syndrome,PCOS)密切相关[3]。gsdf属于TGF-β家族,受雄性决定因子dmy直接调控,参与启动生殖细胞的雄性分化通路[4]。胚胎发育早期(St.35,外周血循环开启期),gsdf在雌雄性腺中微弱表达,随着胚胎发育及性腺体细胞dmy的表达(St.36,心脏形成),gsdf mRNA表达量开始在雄性性腺中表达dmy的体细胞中增加,呈现出明显的雌雄差异[5];gsdf缺失可导致野生型XY雄性青鳉雌性化,形成XY巨大卵巢[4, 6-7],卵巢中含有大量的卵黄发生前卵母细胞,生育能力下降[7]。此外,在gsdf缺失的斑马鱼卵巢中,发现第Ⅲ期卵母细胞发育受阻,早期卵母细胞积累[8]。以上研究显示,gsdf对雄性和雌性性腺以及生殖细胞的发育均具有重要作用。前期蛋白组学分析比对青鳉gsdf+/+XX卵巢、gsdf+/+XY精巢以及gsdf-/-XY卵巢,发现gsdf+/+XY精巢和gsdf-/-XY卵巢的Tsn蛋白表达量明显高于gsdf+/+XX卵巢[9]。
TSN最初被鉴定为单链DNA结合蛋白,随后在体外被证明也可与RNA结合[10]。在哺乳动物中已发现,TSN蛋白家族参与调控细胞分裂和细胞增殖。它在多种生物体中表达,包括裂殖酵母(Schizosaccharomyces pombe)、两栖类(Amphibian)、昆虫(Insect)和哺乳动物(Mammalia)。该蛋白在精子和卵子发生过程中可进行不同水平的转录后调控,例如促进基因表达,维持基因稳定性,进行亚细胞定位等[11-13]。在小鼠中,Tsn缺失可导致2月龄雄性小鼠精巢小区域出现空泡,并且空泡会随着个体增长而增多,同时精子数目发生减少[11],表明tsn对雄性生殖细胞及精巢的发育具有重要影响。
为探究青鳉tsn在配子发生中的作用及tsn与gsdf之间的关系,利用免疫荧光技术分析tsn在gsdf+/+ XX卵巢和gsdf-/- XY卵巢中的差异表达情况。
1 材料与方法 1.1 实验动物在实验中用到的正常野生型青鳉HdrR品系和gsdf缺失型青鳉,人工喂养于26~28 ℃的循环系统中,光周期为光照期14 h、黑暗期10 h。gsdf缺失型青鳉采用锌指核酸酶(Zinc-finger nuclease,ZFN)基因编辑技术获得[4]。
1.2 实验方法 1.2.1 tsn序列分析与系统发育树构建从Ensembl数据库中查找该因子在无脊椎动物(果蝇,Drosophila melanogaster)、鱼类(青鳉;斑马鱼)、两栖类(爪蟾,Xenopus tropicalis)、高等脊椎动物(小鼠,Mus musculus;人,Homo sapiens)中编码的氨基酸序列;通过Vector NTI软件比对多物种的氨基酸序列,比较分析进化保守性;利用MEGA 7.0软件,以果蝇Trsn为外类群,选用参数邻接法构建系统发育树。
1.2.2 青鳉多个组织cDNA的获取分别取3条野生型雌性青鳉和3条野生型雄性青鳉的脑、卵巢、精巢、肝脏、头肾、肠、眼睛,将雌雄个体相应的组织混合,以减少个体间的差异。采用Trizol法(ThermoFisher,美国)提取RNA,用M-MLV Reverse Transcriptase(TaKaRa大连,中国)逆转录酶和RNA模板合成cDNA。
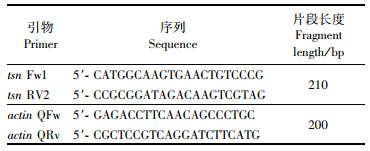
1.2.3 实时荧光定量PCR(Quantitative Real-time PCR,qPCR)以cDNA为模板,进行RT-PCR,检测cDNA和引物质量。然后通过SYBR Green Ⅰ (TaKaRa大连,中国)荧光染料法进行qPCR。qPCR的反应条件:95 ℃预变性30 s,95 ℃变性3 s,60 ℃退火30 s,72 ℃延伸2 min,循环数40。以青鳉肌动蛋白β-actin作为内参基因。引物见表 1。
|
表 1 实时荧光定量PCR分析的基因及引物 Tab.1 Genes and primers for qPCR analysis |
将组织用4%多聚甲醛固定液PFA(生工,中国)固定,置于摇床上(35 r/min,37 ℃)每15 min更换新鲜的4%PFA,更换3次后,4 ℃过夜;第2天用体积分数50%至100%乙醇(国药,中国)进行梯度脱水处理,4 ℃过夜;第3天用Lemosol(Wako,日本)进行2次组织通透处理后,浸蜡包埋。用组织切片仪(LeicaRM2265,德国)进行石蜡切片(厚度6 μm)。切片在42 ℃条件下过夜烘片,之后用二甲苯(生工,中国)脱蜡3次,每次20 min;用体积分数100%至50%乙醇进行梯度复水处理;0.1%Triton X-100现配现用,浸泡40 min,增强细胞通透性;5%羊血清(生工,中国)阻断封闭非特异抗原30 min后,敷特异性一抗(Abmart,中国)4 ℃过夜。第2天复温30 min,分别用1×PBS和1×PBST洗片去除未结合的游离一抗30 min,然后分别与鼠源和兔源二抗(MBL,中国)在室温下避光孵育,在此期间用TSATM-Plus TMR/Fluorescein System(PerkinElmer,德国)进行荧光信号增强放大染色,随后DAPI负染,用体积分数50%至100%乙醇梯度脱水处理后,加抗荧光淬灭封片剂(Sigma-Aldrich,美国)封片;共聚焦显微镜(Leica TCS SP8,德国)观察并拍摄图片。
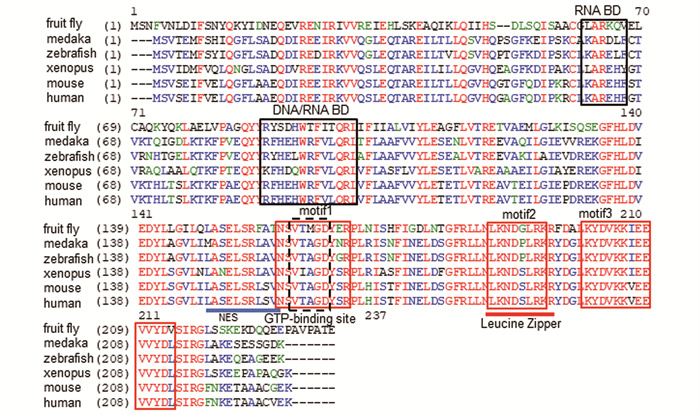
2 结果与分析 2.1 青鳉tsn的进化保守性青鳉tsn编码227个氨基酸,将其与果蝇、斑马鱼、爪蟾、小鼠和人的氨基酸序列进行比对发现,青鳉的氨基酸序列与哺乳类小鼠和人具有较高的相似性(78%),N端的RNA结合位点(RNA结合结构域,RNA BD),DNA/RNA结合位点(DNA/RNA结合结构域,DNA/RNA BD),C端的核输出信号(nuclear export signal,NES),与GTP结合域(GTP-binding site)关联的motif1,含有亮氨酸拉链结构(Leucine Zipper)的motif2,以及位于C末端的motif3,从无脊椎动物至高等脊椎动物高度保守(图 1)。
|
结构域RNA结合位点和DNA结合位点用黑色框标出;基序1,基序2和基序3用红色框标出;GTP结合位点用黑色虚线框标出;核输出信号用蓝色下划线标出;亮氨酸拉链结构用红色下划线标出。 RNA BD (RNA-binding site), DNA/RNA BD (DNA/RNA-binding site) are boxed in black; motif1, motif2, motif3 are boxed in red; GTP-binding site are boxed with dotted lines in black; NES (nuclear export-signal) (blue underlined); Leucine Zipper (red underlined). 图 1 青鳉与哺乳动物(人、鼠)、两栖类(爪蟾)以及无脊椎动物(果蝇)的氨基酸序列比对 Fig. 1 Amino acid alignment of the domains of mammal (human, mouse), amphibian(xenopus), fish (medaka, zebrafish) and invertebrate (fruit fly) |
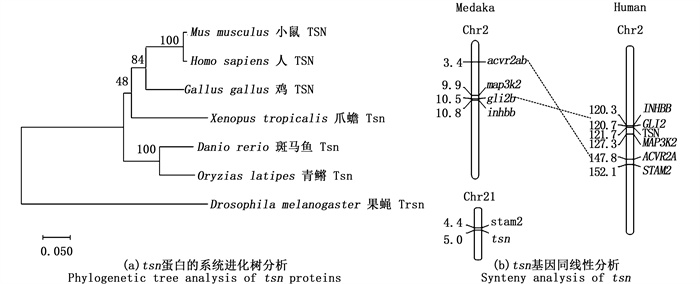
利用MEGA 7.0软件,选用参数邻接法以果蝇Trsn为外类群,对鱼类、两栖类、鸟类和哺乳类多物种的tsn进行系统发育树分析。结果显示:青鳉和斑马鱼等鱼类聚在硬骨鱼分支上,而哺乳类、鸟类和两栖类聚在另一个大的分支(图 2a)上。根据基因同线性(synteny)分析发现,tsn位于青鳉21号染色体,同人2号染色体的TSN相对应。人TSN附近的STAM2也在青鳉tsn附近能找到,但是INHBB和GLI2等紧密连锁基因却独立于青鳉tsn,在青鳉2号染色体上。值得注意的是,人TSN的连锁基因INHBB、GLI2、MAP3K2、ACVR2A与青鳉tsn连锁基因acvr2ab、map3k2、gli2b、inhbb在染色体上的排列方向正好相反。这些结果表明,青鳉2号染色体和人2号染色体的这一区域可能起源于一个共同祖先,并且在向高等哺乳动物的进化过程中发生了反转及TSN、STAM2等片段的插入。GLI2、INHBB和MAP3K2、ACVR2A都是生殖细胞发生发育重要关联因子[14-15],TSN的插入可能改变这些基因在生殖细胞性分化和发育过程的表达,影响其生理功能的发挥(图 2b)。
|
图 2 tsn分子序列和结构的保守性 Fig. 2 Evolutionary conservation of tsn across phyla |
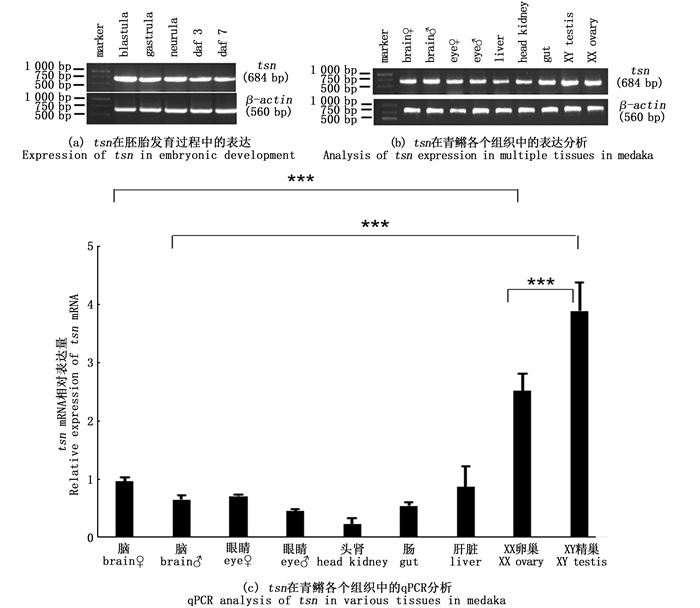
通过RT-PCR分析tsn mRNA在胚胎多个时期的表达,发现tsn mRNA在囊胚期、原肠胚期、神经胚期、受精后3 d(St.29:34体节期,dmy未表达)、受精后7 d(St.37:心包腔形成期,dmy表达)均有表达(图 3a)。同时,利用RT-PCR分析tsn mRNA在青鳉多个组织中的表达,结果显示, tsn mRNA在脑、眼睛、肝脏、头肾、肠、精巢、卵巢中广泛表达(图 3b)。以脑、眼睛、肝脏、头肾、肠、精巢、卵巢的cDNA为模板,对tsn mRNA在多个组织中的表达进行相对定量分析,发现tsn mRNA在精巢中表达量最高,并且tsn mRNA在精巢中的表达量极显著高于雄性脑及卵巢。此外,该结果也显示在卵巢中的表达量极显著高于雌性脑(P < 0.001),见图 3c。
|
daf 3.受精后3天;daf 7.受精后7天。星号表示tsn在青鳉精巢和脑中有显著性差异(*P < 0.05;**P < 0.01;***P < 0.001)。 daf 3.3 days after fertilization; daf7.7days after fertilization; The asterisks indicate significant differences among testis, ovary and brain(*P < 0.05; **P < 0.01;***P < 0.001). 图 3 tsn在多组织中的时空表达分析 Fig. 3 Temporal and spatial expression of tsn in multiple tissues |
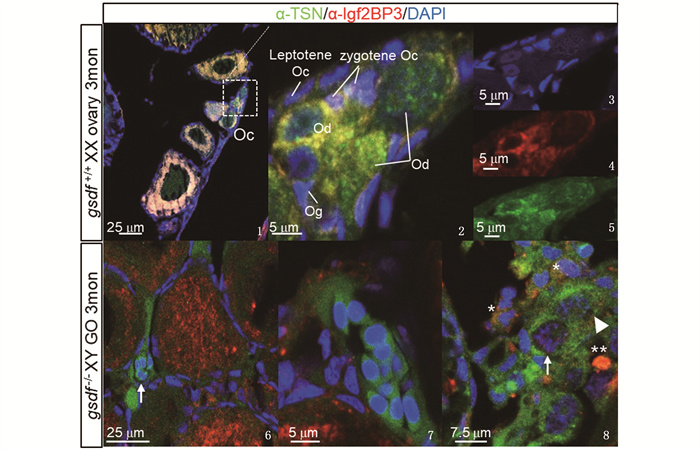
在gsdf+/+XX卵巢中,细线期卵母细胞的细胞核中有微弱Igf2BP3蛋白表达,偶线期卵母细胞(根据细胞形态学判断)的细胞核和细胞质中有大量抗Igf2BP3红色信号,Tsn仅在细胞质中表达,这使核周细胞质呈黄色,细胞核呈现红色(图版-2);随着卵母细胞减数分裂进行到双线期,核中只检测到抗Tsn绿色信号附着在双线期卵母细胞的染色体上(图版-2);Ⅰ期减数分裂末期,Tsn和Igf2BP3完全移出到细胞质中(图版-1)。
|
1. Tsn/Igf2BP3在gsdf+/+XX卵巢中的定位;2. 1的放大图;3-5. 2的单通道图像;6-8. Tsn/Igf2BP3在gsdf-/- XY卵巢中的定位;*. 初级卵母细胞;**. 死细胞残骸;Oc. 卵母细胞;Og. 卵原细胞;Od. 双线期卵母细胞;GO. 巨大卵巢;绿色. anti-Tsn;红色. anti-Igf2BP3;蓝色. DAPI。 1. Localization of Tsn/Igf2BP3 in gsdf+/+ XX ovaries; 2. magnified images of 1; 3-5. the single channels of 2; 6-8. Localization of Tsn/Igf2BP3 in gsdf-/- XY ovaries; *. primary oocyte; **. dead cell debris; Oc. oocyte; Og. oogonia; Od. diplotene oocyte; GO. giant ovary; Green. anti-Tsn; Red. anti-Igf2BP3; Blue. chromatin (DAPI). 图版 Tsn在gsdf+/+XX卵巢和gsdf-/- XY卵巢中的差异表达 Plate Expression of Tsn in gsdf+/+XX ovaries and gsdf-/- XY ovaries |
gsdf-/-XY型卵巢囊性生殖细胞的细胞质含有大量的抗Tsn(绿色)信号(图版-6白色箭头所示,7),即使这些生殖细胞进入减数分裂,Tsn信号也大多停留在细胞质中(图版-8白色箭头所示),少有进入细胞核(图版-8三角箭头所示);Igf2BP3在卵母细胞中大量表达(图版-6),同时还有一些Tsn和Igf2BP3共表达的初级卵母细胞(图版-8中*)以及抗Igf2BP3深染的死细胞残骸(图版-8中**)。
3 讨论本研究首次在青鳉上克隆了tsn,并对其结构进行分析,同时,在gsdf+/+XX卵巢和gsdf-/- XY的卵巢中对Igf2BP3和Tsn进行定位,针对青鳉Tsn的表达展开研究。
通过对tsn时空表达分析发现,tsn在青鳉性成熟期的多个组织中表达,与果蝇和小鼠tsn研究结果相一致:SUSEENDRANATHAN等[16]发现tsn在果蝇胚胎期,幼虫和成虫的各个组织中表达;CHENNATHUKUZHI等[11]也发现tsn在小鼠脑、头肾、肝脏、精巢中表达,提示了tsn在组织生长时发挥重要作用。此外,tsn在青鳉胚胎发育的多个时期也均有表达,表明tsn对胚胎发育同样具有重要功能。值得注意的是,tsn在精巢中的表达量显著高于卵巢,由此推测tsn在精巢发育过程中的作用机制不同于卵巢。目前,已有研究[11]提出在肝脏中Tsn可与microRNAs结合,但Tsn/microRNAs复合体的调节功能有待确定,因此Tsn在组织生长和胚胎发育中的具体调控机制仍需进一步深入探究。
基因的表达和在细胞内的定位,蛋白质翻译以及翻译后的修饰,对调控生殖细胞在早期胚胎发育过程中的增殖和性别分化十分重要。RNA结合蛋白(核糖核酸结合蛋白)参与转录后调控,与哺乳动物的生育能力有关,如IMPs(IGF-Ⅱ mRNA-binding proteins)在卵巢恶性生殖细胞肿瘤中大量表达。介导生殖细胞发育[17]。CHO等[18]发现,RNA结合蛋白TSN在粗线期生殖细胞的细胞核与Ⅰ期减数分裂末期的生殖细胞质中表达,本研究抗Tsn/抗Igf2BP3双色免疫荧光结果显示,Tsn蛋白产物穿梭于青鳉雌性生殖细胞的细胞质及细胞核中,与小鼠TSN的研究结果类似。氨基酸序列比对分析发现,Tsn的核输出信号以及亮氨酸拉链结构在青鳉中完全保守(图 1),提示了在青鳉雌雄生殖细胞发育过程中Tsn的核质间进出可能与靶转录物的阶段特异性输出和释放有关。小鼠TSN与TRAX(Translin-associated factor X)的相对比例影响二者在雄性生殖细胞中的核质分布[18],青鳉Trax同其他物种(鱼至哺乳动物)的氨基酸序列和功能域高度保守,Tsn/Trax蛋白复合体可能参与青鳉雌雄生殖细胞分化和发育过程,为进一步深入理解脊椎动物生殖细胞性分化的调控机制奠定了坚实的基础。
抗Tsn/抗Igf2BP3双色免疫荧光结果也显示,在gsdf+/+XX卵巢和gsdf-/-XY卵巢减数分裂不同时期的卵母细胞中,Tsn蛋白表达有明显差异。gsdf+/+XX卵母细胞的细胞核和细胞质中检测到大量的抗Tsn信号(图版-2),而gsdf-/-XY卵母细胞中,Tsn蛋白大量聚集在细胞质,只有少量附着在细胞核内(图版-8白色箭头所示);抗Igf2BP3信号在减数分裂早期(细线期,偶线期)卵母细胞的细胞核中,随着卵母细胞发育到双线期,该信号转移至细胞质。这表明Igf2BP3与Tsn蛋白质产物进出细胞核的动态变化,可能同生殖细胞减数分裂特定时期的染色体复制和亚细胞结构变化有关。
与此同时,根据抗Tsn/抗Igf2BP3双色免疫荧光结果发现,gsdf-/-XY卵巢中,Igf2BP3在早期生殖细胞的细胞质中与Tsn共同表达(图版-8中*),然而有一部分Tsn表达的囊性生殖细胞异常增殖,这部分囊性生殖细胞没有表达Igf2BP3(图版-6, 7)。本研究在早期发现的gsdf-/- XY卵巢囊性生殖细胞异常增殖的基础上[19],发现了Tsn的表达量以及进出细胞核的胞内动态变化同Gsdf信号相关联,并且Tsn在Gsdf缺失的异质化有丝分裂囊性增殖的生殖细胞中大量表达,提示了Tsn可能同Igf2BP3和/或其他RNA结合蛋白一起,参与RNA代谢并介导囊性生殖细胞的增殖和凋亡。而Tsn如何参与调控生殖细胞发育和性分化,最终产生精子或卵细胞的分子机制还有待研究。
综上所述,本研究以青鳉为模式生物发现了Tsn是潜在的雄性生殖细胞增殖的分子标志物,可能受dmy-gsdf信号直接或间接调控,参与生殖细胞有丝分裂和增殖,并介导生殖细胞从有丝分裂向减数分裂转换。青鳉Gsdf调控Tsn介导的生殖细胞增殖以及胞内动态变化为研究脊椎动物配子发生和性分化提供了线索。
| [1] |
YOUNG J C, WAKITANI S, LOVELAND K L. TGF-β superfamily signaling in testis formation and early male germline development[J]. Seminars in Cell & Developmental Biology, 2015, 45: 94-103. |
| [2] |
MORIKAWA M, DERYNCK R, MIYAZONO K. TGF-β and the TGF-β family: context-dependent roles in cell and tissue physiology[J]. Cold Spring Harbor Symposia on Quantitative Biology, 2016, 8(5): a021873. DOI:10.1101/cshperspect.a021873 |
| [3] |
RAJA-KHAN N, URBANEK M, RODGERS R J, et al. The role of TGF-β in polycystic ovary syndrome[J]. Reproductive Sciences, 2014, 21(1): 20-31. DOI:10.1177/1933719113485294 |
| [4] |
ZHANG X, GUAN G J, LI M Y, et al. Autosomal gsdf acts as a male sex initiator in the fish medaka[J]. Scientific Reports, 2016, 6(1): 19738. DOI:10.1038/srep19738 |
| [5] |
SHIBATA Y, PAUL-PRASANTH B, SUZUKI A, et al. Expression of gonadal soma derived factor (GSDF) is spatially and temporally correlated with early testicular differentiation in medaka[J]. Gene Expression Patterns, 2010, 10(6): 283-289. DOI:10.1016/j.gep.2010.06.005 |
| [6] |
IMAI T, SAINO K, MATSUDA M. Mutation of gonadal soma-derived factor induces medaka XY gonads to undergo ovarian development[J]. Biochemical and Biophysical Research Communications, 2015, 467(1): 109-114. DOI:10.1016/j.bbrc.2015.09.112 |
| [7] |
GUAN G J, SUN K Q, ZHANG X, et al. Developmental tracing of oocyte development in gonadal soma-derived factor deficiency medaka (Oryzias latipes) using a transgenic approach[J]. Mechanisms of Development, 2017, 143: 53-61. DOI:10.1016/j.mod.2016.12.006 |
| [8] |
YAN Y L, DESVIGNES T, BREMILLER R, et al. Gonadal soma controls ovarian follicle proliferation through Gsdf in zebrafish[J]. Developmental Dynamics, 2017, 246(11): 925-945. DOI:10.1002/dvdy.24579 |
| [9] |
ZHANG X T, CHANG Y Y, ZHAI W Y, et al. A potential role for the Gsdf-eEF1α complex in inhibiting germ cell proliferation: a protein-interaction analysis in medaka (Oryzias latipes) from a proteomics perspective[J]. Molecular and Cellular Proteomics, 2021, 20: 100023. DOI:10.1074/mcp.RA120.002306 |
| [10] |
ISHIDA R, OKADO H, SATO H, et al. A role for the octameric ring protein, Translin, in mitotic cell division[J]. FEBS Letters, 2002, 525(1/3): 105-110. |
| [11] |
CHENNATHUKUZHI V, STEIN J M, ABEL T, et al. Mice deficient for testis-brain RNA-binding protein exhibit a coordinate loss of TRAX, reduced fertility, altered gene expression in the brain, and behavioral changes[J]. Molecular and Cellular Biology, 2003, 23(18): 6419-6434. DOI:10.1128/MCB.23.18.6419-6434.2003 |
| [12] |
HAN J R, GU W, HECHT N B. Testis-brain RNA-binding protein, a testicular translational regulatory RNA-binding protein, is present in the brain and binds to the 3' untranslated regions of transported brain mRNAs[J]. Biology of Reproduction, 1995, 53(3): 707-717. DOI:10.1095/biolreprod53.3.707 |
| [13] |
HAN J R, YIU G K, HECHT N B. Testis/brain RNA-binding protein attaches translationally repressed and transported mRNAs to microtubules[J]. Proceedings of the National Academy of Sciences of the United States of America, 1995, 92(21): 9550-9554. DOI:10.1073/pnas.92.21.9550 |
| [14] |
M'BAYE M, HUA G H, KHAN H A, et al. RNAi-mediated knockdown of INHBB increases apoptosis and inhibits steroidogenesis in mouse granulosa cells[J]. Journal of Reproduction and Development, 2015, 61(5): 391-397. DOI:10.1262/jrd.2014-158 |
| [15] |
GAO Y, FANG X, VINCENT D F, et al. Disruption of postnatal folliculogenesis and development of ovarian tumor in a mouse model with aberrant transforming growth factor beta signaling[J]. Reproductive Biology and Endocrinology, 2017, 15(1): 94. DOI:10.1186/s12958-017-0312-z |
| [16] |
SUSEENDRANATHAN K, SENGUPTA K, RIKHY R, et al. Expression pattern of Drosophila translin and behavioral analyses of the mutant[J]. European Journal of Cell Biology, 2007, 86(3): 173-186. DOI:10.1016/j.ejcb.2006.11.005 |
| [17] |
HAMMER N A, HANSEN T V O, BYSKOV A G, et al. Expression of IGF-Ⅱ mRNA-binding proteins (IMPs) in gonads and testicular cancer[J]. Reproduction, 2005, 130(2): 203-212. DOI:10.1530/rep.1.00664 |
| [18] |
CHO Y S, CHENNATHUKUZHI V M, HANDEL M A, et al. The relative levels of translin-associated factor X (TRAX) and testis brain RNA-binding protein determine their nucleocytoplasmic distribution in male germ cells[J]. Journal of Biological Chemistry, 2004, 279(30): 31514-31523. DOI:10.1074/jbc.M401442200 |
| [19] |
WU X W, ZHANG Y Q, XU S M, et al. Loss of Gsdf leads to a dysregulation of Igf2BP3-mediated oocyte development in medaka[J]. General and Comparative Endocrinology, 2019, 277: 122-129. DOI:10.1016/j.ygcen.2019.04.001 |
2. International Research Center for Marine Biosciences, Ministry of Science and Technology, Shanghai Ocean University, Shanghai 201306, China;
3. Key Laboratory of Exploration and Utilization of Aquatic Genetic Resources, Ministry of Education, Shanghai Ocean University, Shanghai 201306, China
 2022,
Vol. 31
2022,
Vol. 31


