2. 中国水产科学研究院淡水渔业研究中心 农业农村部淡水渔业与种质资源利用重点实验室, 江苏 无锡 214081;
3. 安徽张林渔业有限公司, 安徽 铜陵 224151;
4. 铜陵市义安区水产管理站, 安徽 铜陵 244151
大口黑鲈(Micropterus salmoides),俗名加州鲈,起源于北美洲,自20世纪80年代引进中国以来,目前已经成为中国主要淡水养殖品种之一[1]。2019年中国淡水鲈(主要为大口黑鲈)养殖产量达47.78万t,其中,广东产量约占全国总产量59%,江苏和浙江约占22%[2]。大口黑鲈具有环境适应性强、生长速度快、养殖周期短、易捕捞、病害少等优点,另因其肉质鲜美、营养丰富而广受养殖者及消费者的欢迎[2]。但是,国内的大口黑鲈经过多年的养殖,出现了生长性能降低、性成熟提前等种质退化现象,这样严重制约了其养殖业的健康可持续发展。
近年来,在科研人员的努力下,大口黑鲈的遗传改良和新品种培育取得较大成就。大口黑鲈“优鲈1号”(品种登记号:GS-01-004-2010)是珠江水产研究所以国内4个养殖群体为基础种群,结合传统选育技术与分子生物学技术,经5代选育从而获得的大口黑鲈选育品种,该品种具有生长速度快、体型好等特点[3]。目前,大口黑鲈“优鲈1号”先后在广东、浙江、江苏、四川和湖南等省进行广泛推广。近年,在“优鲈1号”的基础上,基于群体交配组合和多代选育,又培育获得“优鲈3号”[4](品种登记号:GS-01-001—2018)。以上2个新品种的育成和推广大大提高了中国大口黑鲈养殖业的良种普及率。然而,随着大口黑鲈养殖面积的不断增长,养殖地域不断扩大,受限于大口黑鲈的成鱼怀卵量,现有新品种还难以完全解决优良苗种供求关系的紧张局面。此外,鱼类生长性能不仅受到遗传(群体或品种)因素影响,遗传和环境互作效应也不容忽视[5-6]。因此,基于现有新品种、养殖群体等优势种质,在不同地域开展的种质改良或新品种创制,无疑是维持中国大口黑鲈养殖业健康可持续的重要保障。
大口黑鲈有2个亚种: 一是北方亚种(M.salmoides salmoides),分布于美国的中东部、墨西哥东北部和加拿大的东南部;另外一个是佛罗里达亚种(M. salmoides floridanus),分布在美国的佛罗里达半岛南部[7]。过去一直认为2个亚种是同一种鱼,直至20世纪40年代BAILEY等[7]首次从形态学上对2亚种进行区分鉴定,发现2个亚种在肋骨数和侧线鳞上存在着明显差异[8-9]。此后又有许多学者通过同工酶技术[10-11]、分子标记手段[12-13]和线粒体[14-16]等有效手段辨别出这2个亚种。近缘杂交或群体交配设计是鱼类遗传育种的常规手段,目前国内在鲤(Cyprinus carpio)[17-18]、尼罗罗非鱼(Oreochromis niloticus)[19-20]、团头鲂(Megalobrama amblycephala)[21-22]和鳙(Hypophthalmichthys nobilis)[23]等重要经济鱼类的遗传育种研究中均有采用。大口黑鲈很早就开始了近缘杂交育种工作,WILLIAMSON等[24]和ZOLCZYNSKI等[25]对大口黑鲈2个亚种以及正反交F1的生长性状进行了试验,均发现北方亚种生长速度最快,其次为杂交种,最后为佛罗里达亚种。但KLEINSASSER等[26]和NEAL等[27]却发现杂交组合佛罗里达亚种(♀)×北方亚种(♂)生长速度最快,与前人的实验结果有所不同。为解决国内大口黑鲈群体遗传多样性下降的问题,周家辉等[28]利用2个大口黑鲈养殖群体开展了杂交实验,并对其子代的遗传和生长性能进行比较,发现杂交后代遗传多样性水平和生长性能均获得有效提高。基于美国引进的大口黑鲈原种群体和2个国内养殖群体,苏胜彦等[29]通过微卫星标记的研究发现国内养殖群体的遗传多样性水平有所下降。此外,养殖过程中还发现,大口黑鲈美国群体体表花纹清晰、生长速度快、适应性强,但不好驯养;国内养殖群体容易驯养,但目前国内养殖群体经历多代选育和养殖后,容易出现近交和种质退化现象。本研究以近年引进的美国群体和国内现有养殖群体开展完全双列杂交试验,使子代继承亲本优良性状,并对其生长性能等进行分析,以期为中国大口黑鲈养殖群体种质改良和新品种培育提供基础,提高大口黑鲈良种在国内的普及率。
1 材料与方法 1.1 实验鱼亲本大口黑鲈美国群体(US)是2016年从美国密苏里区域引入并在安徽张林渔业有限公司群体选育获得的第2代子代;国内养殖群体亲本(YZ)是2014年从湖州南浔继成水产养殖场引入并在安徽张林渔业有限公司繁殖、群体选育的第4代子代。2019年4月21日,基于2个群体开展完全双列杂交试验,从2个群体中分别挑选无病无伤、体质量为450~550 g的1龄鱼作为亲本,自然交配。每组所用亲本数量均为30尾,雌雄比例1∶ 1,在水泥池中自然产卵受精,繁殖获得USUS、USYZ、YZUS和YZYZ共4个交配组合的子代分别在小池暂养(鱼苗驯化为常规食性驯化)。养殖86 d后(3月龄),对4个组合的部分子代进行PIT电子标记并称重后进行同池养殖,各组子代的标记数量分别为USUS 660尾、USYZ 601尾、YZUS 614尾和YZYZ 560尾。
1.2 数据采集养殖361 d后(12月龄),通过拉网从池塘里随机捕获265尾具有PIT标记的识别个体,其中包含USUS 92尾、USYZ 64尾、YZUS 58尾和YZYZ 51尾,用电子天平称量体质量(精确度0.1 g),用量鱼板测量全长、体长、头长、体宽和体高等数据(精确度0.01 cm)。
1.3 计算公式实验结束后,用以下公式计算绝对增重率(AGR)、变异系数(CV)、肥满度(K)、超亲优势率(HB)和中亲杂种优势(HM)[30]:
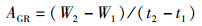 (1)
(1)
式中:AGR为绝对增重率,g/d;W1为t1(试验初始,d)时的体质量,g;W2为t2(试验结束,d)时的体质量,g。
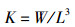 (2)
(2)
式中:K为肥满度,g/cm3;W为体质量,g;L为体长,cm。
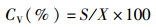 (3)
(3)
式中:CV为变异系数;S为某一性状的标准差;X为某一性状的平均值。
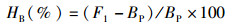 (4)
(4)
式中:HB为超亲优势率;F1为杂交子一代某一性状的平均值;BP为双亲中某一性状优良的亲本的平均值。
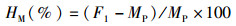 (5)
(5)
式中:HM为中亲杂种优势;F1为杂交子一代某一性状的平均值;MP为亲本某一性状的平均值。
1.4 数据分析用SPSS 11.5及Excel对试验数据进行整理,对生长性状指标进行方差分析、显著性检验(F检验)以及多重比较(Duncan氏法)分析,建立多元回归方程,并对主要生长性状进行表型相关(Pearson相关)分析、生长性状对体质量的通径分析和决定系数计算[31-32]。
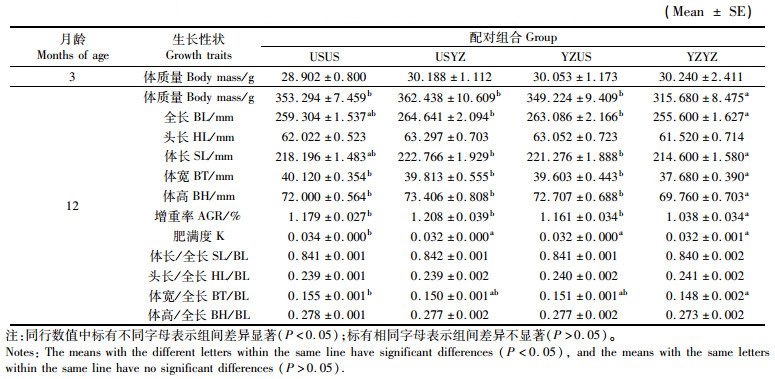
2 结果 2.1 生长性状的比较分析3月龄(从繁苗到标记)和12月龄,4个交配组合的子代生长数据见表 1。从表 1可见4个组合3月龄的生长性状差异不显著(P>0.05)。继续养殖275 d后,USYZ子代的平均体质量比USUS子代的平均体质量高2.59%,比YZYZ子代的平均体质量高14.81%,比YZUS子代的平均体质量高3.79%。
|
表 1 实验鱼生长性状比较分析 Tab.1 Comparative analysis of experimental fish growth traits |
12月龄,经比较,4个组合子代中USYZ生长最快。绝对增重率大小顺序为USYZ>USUS>YZUS>YZYZ;体长大小顺序为USYZ>YZUS>USUS>YZYZ;体高大小顺序为USYZ>YZUS>USUS>YZYZ。多重比较的结果表明:USYZ子代的体质量与YZYZ子代差异极显著(P<0.01),YZYZ子代的体质量与USUS子代差异显著(P<0.05);USYZ子代的绝对增重率与YZYZ子代差异极显著(P<0.01),USUS子代的绝对增重率与YZYZ子代差异显著(P<0.05);USYZ子代的体长与2个自繁组合(USUS和YZYZ)子代差异显著(P<0.05),YZUS子代的体长与YZYZ子代差异显著(P<0.05),其余差异不显著(P>0.05);USYZ子代的全长与2个自繁组合(USUS和YZYZ)子代差异显著(P<0.05),YZUS子代的全长与YZYZ子代差异显著(P<0.05),其余差异不显著(P>0.05);USYZ子代的体高与YZYZ子代差异极显著(P<0.01),YZUS子代的体高与YZYZ子代差异显著(P<0.05),其余差异不显著(P>0.05)。
4个交配组合子代的肥满度大小顺序:USUS>USYZ>YZUS>YZYZ。USUS子代的肥满度最高,与2个杂交组合子代(USYZ和YZUS)的差异均为极显著(P<0.01),与YZYZ子代的差异显著(P<0.05)。4个交配组合子代的体宽大小顺序:USUS>USYZ>YZUS>YZYZ,结果与肥满度一致。YZYZ子代体宽最小,与2个杂交组合子代的差异显著(P<0.05),与USUS子代的差异极显著(P<0.01)。
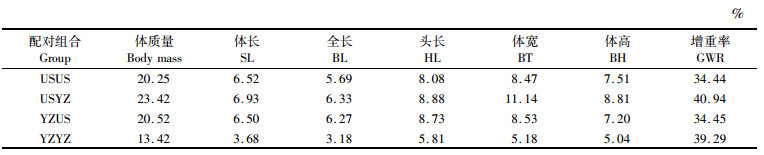
变异系数即生长离散的程度,变量值平均水平高,其离散程度的测度值越大,反之越小。从表 2可见,USYZ组合生长性状的变异系数在4个组合中均最大。YZUS组合生长性状的变异系数虽比USYZ组合小,但仍大于2个自繁组合(USUS和YZYZ)。
|
表 2 子代的生长性状变异系数 Tab.2 Coefficient of variation of growth traits of offspring |
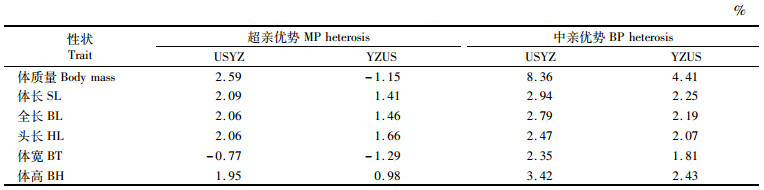
由表 3可见,2个杂交组合子代在各生长性状上均具有中亲优势(1.81%~8.36%), 其中: USYZ组合的子代在体质量、全长、体长、头长和体高上呈现超亲优势(1.95%~2.59%),YZUS组合的子代在全长、体长、头长和体高上呈现超亲优势(0.98%~1.66%);USYZ组合子代在各生长性能方面表现优于YZUS组合。
|
表 3 杂交组合子代生长性状的杂种优势 Tab.3 Super-parent heterosis rate of growth traits of hybrids |
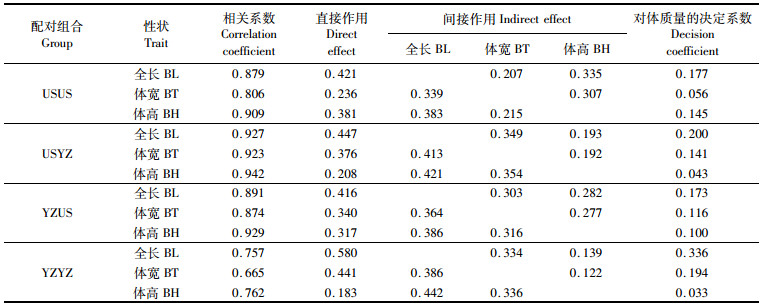
通径分析结果(表 4)显示,全长、体宽、体高对体质量的相关性均达到了显著性水平的正相关(P<0.05), 其中,全长对体质量的直接作用均大于其通过体高产生的间接作用,而体高对体质量的直接作用均小于其通过全长产生的间接作用,除YZYZ组合外,其余3个组合的体宽对体质量的直接作用均小于通过全长产生的间接作用。
|
表 4 3个形态性状对体质量的影响 Tab.4 Effect of three morphological traits on baby mass |
此外,在4个组别中,全长对体质量的决定系数始终大于体宽和体高的决定系数,对于USUS组合的子代体高对体质量的决定系数要高于体宽的决定系数,而其余3个组合中,体高对体质量的决定系数低于体宽对体质量的决定系数。
3 讨论根据试验结果,3月龄4个组合大口黑鲈子代的体质量并无显著差异,因此可排除各组合子代在前期小池暂养期间养殖环境等因素对其生长的影响。基于不同群体间的交配设计,是杂种优势的有效利用方法。本试验应用完全双列杂交技术得到的杂交子代具有超亲优势和中亲优势,且USYZ杂交组合相较2个亲本自繁组合(USUS和YZYZ)的生长速度分别快2.59%和14.81%,比YZUS杂交组合的生长速度快3.79%。王佳等[33]将黄金鲈(Perca flavescens)和伊犁鲈(P. schrenki)进行杂交,发现杂交F1生长比黄金鲈生长速度快33.91%。相对种间杂交试验中获得的杂种优势,本试验杂交子代表现出较小的生长优势,这可能由于国内群体和美国引进群体属于同一个亚种,亲缘关系较近。本试验杂交1代生长性状的变异系数均高于亲本群体的自繁子代,即遗传性状差异较大,这与张志新等[34]对白鲫(Carassius auratus)与散鳞镜鲤(C. carpio L.)的杂交实验中结果一致。在佟雪红等[35]对建鲤(C. carpio var. jian)和黄河鲤(C. carpio haematopterus)杂交的试验中杂交F1子代的变异系数也均高于亲本。同比周家辉等[28]对大口黑鲈北方亚种和“优鲈一号”的杂交试验中,其12月龄4个组合子代体长和体高的变异系数均高于本试验12月龄4个组合子代体长和体高的变异系数,这可能是2个试验养殖地点(分别在广州和安徽)、养殖环境和饲养方法等因素不同造成的。王佩佩等[36]对大口黑鲈3个杂交组合F1子代不同月龄的体质量分析发现,“优鲈3号”(♀)与佛罗里达亚种(♂)杂交子代的生长性能优于“优鲈3号”(♀)与北方亚种(♂)杂交子代。因此,可以考虑后续进一步引入佛罗里达亚种继续开展杂交试验,进一步提高大口黑鲈的生长性能。选育过程是长期的、连续的,本研究获得的杂交群体可通过多代的选育,从而筛选出生长性状稳定且优良的品系。正如董在杰[37]通过建鲤和黄河鲤进行双列杂交,经过5代的选育,筛选出生长快、长体形的优良个体即“福瑞鲤”,后又引入对低温具有较强适应能力的黑龙江野鲤(C. carpio amurensis),通过完全双列杂交建立自交和正反交家系构成选育基础群体,经过多代选育获得“福瑞鲤2号”等育种方案。此外,大口黑鲈与其他鱼类的杂交育种工作也有开展,如PARKER等[38]和李武威等[39]分别开展了大口黑鲈与蓝鳃太阳鱼(Lepomis mearchirus)杂交产生后代(杂交胚胎孵化率约为55%),但其子代是否继承太阳鱼耐低氧和适应高浊度环境的特性尚未可知,这在大口黑鲈后续选育工作中值得进一步探索。
通径分析可以将相关系数分解为性状对体质量的直接和间接作用,知晓各形态性状的重要性。基于通径分析结果,在后续选育过程中可以考虑通过便于测量的性状(体长、体高等)的间接选择来综合制定选育方案。在杨慧等[40]对3个红罗非鱼群体的形态差异分析我国台湾红罗非鱼和以色列红罗非鱼群体的体长、体厚、尾柄高是与体质量相关性较高的形态性状,体长、体高、体厚是影响马来西亚红罗非鱼群体体质量的重要性状。在鲈形目的鱼类中,胡彦波等[41]对花鲈(Lateolabrax maculatus)的研究表明,体宽对体质量的直接作用最大,头长、全长和尾柄高则主要通过体宽间接发挥作用。本研究发现,大口黑鲈全长、体宽、体高与体质量均呈极显著正相关,且全长对体质量的作用主要为直接作用,而体宽和体高对体质量的作用主要为间接作用,均主要通过全长间接影响体质量,与上述实验结果存在一定的差异,这可能与不同的鱼类适应环境的策略不同有关。在大口黑鲈的杂交研究中,何小燕等[42]发现体宽对体质量的直接作用远大于体长和眼间距,这一试验结果与本试验也存在较大差异,可能是由于大口黑鲈在不同生长阶段形态性状对体质量的影响效果不同,何小燕等选用的实验鱼为8月龄,而本试验选用的鱼为12月龄。正如李莉等[43]在对不同月龄大泷六线鱼(Hexagrammos otakii)研究中发现,其6月龄体长对体质量的影响最大,但18月龄全长对体质量的影响最大。在大口黑鲈体质量的相关研究中,王佩佩等[36]发现3个大口黑鲈杂交组合子代的平均体质量在不同月龄呈现出不同程度的显著性差异(P<0.05)。姜绪等[44]对5月龄大口黑鲈的形态性状与体质量的通径分析,结果与本试验一致,可见在大口黑鲈进行以体质量为主要目标的选育工作时,5月龄和12月龄的大口黑鲈都可以把全长作为主要选择性状,把体宽和体高作为辅助选择性状,从而提高选育的效率。本研究还发现,YZYZ组合子代体宽对体质量起到更大的决定作用,且不同组合子代的不同性状对体质量的决定系数存在差异,亦或组合间在体型方面可能存在差异。另外,4个组合子代在体宽/全长上具有极显著性差异(P<0.01),是否在其他体型指标具有更多差异,有待进一步研究,这也为后续继续选育提供了一个性状指标。
| [1] |
BAI J J, LUTZ-CARRILLO D J, QUAN Y C, et al. Taxonomic status and genetic diversity of cultured largemouth bass Micropterus salmoides in China[J]. Aquaculture, 2008, 278(1/4): 27-30. |
| [2] |
农业农村部渔业渔政管理局. 2020中国渔业统计年鉴[M]. 北京: 中国农业出版社, 2020. Fisheries Administration of Ministry of Agriculture and Rural Affairs. China fishery statistical yearbook 2020[M]. Beijing: China Agriculture Press, 2020. |
| [3] |
李胜杰, 白俊杰, 谢骏, 等. 大口黑鲈选育效果的初步分析[J]. 水产养殖, 2009, 30(10): 10-13. LI S J, BAI J J, XIE J, et al. Evaluation of selective breeding effect of largemouth bass (Micropterus salmoides) at third generation[J]. Journal of Aquaculture, 2009, 30(10): 10-13. DOI:10.3969/j.issn.1004-2091.2009.10.003 |
| [4] |
廖静. 加州鲈种苗的"两次升级"[J]. 海洋与渔业, 2019(12): 60-61. LIAO J. "Two upgrades" of California perch seedlings[J]. Ocean and Fishery, 2019(12): 60-61. DOI:10.3969/j.issn.1672-4046(s).2019.12.026 |
| [5] |
MOAV R, HULATA G, WOHLFARTH G. Genetic differences between the Chinese and European races of the common carp[J]. Heredity, 1975, 34(3): 323-340. DOI:10.1038/hdy.1975.42 |
| [6] |
TR  NG T Q, MULDER H A, VAN ARENDONK J A M, et al. Heritability and genotype by environment interaction estimates for harvest weight, growth rate, and shape of Nile tilapia (Oreochromis niloticus) grown in river cage and VAC in Vietnam[J]. Aquaculture, 2013, 384-387: 119-127. DOI:10.1016/j.aquaculture.2012.12.022 NG T Q, MULDER H A, VAN ARENDONK J A M, et al. Heritability and genotype by environment interaction estimates for harvest weight, growth rate, and shape of Nile tilapia (Oreochromis niloticus) grown in river cage and VAC in Vietnam[J]. Aquaculture, 2013, 384-387: 119-127. DOI:10.1016/j.aquaculture.2012.12.022 |
| [7] |
BAILEY R M, HUBBS C L. The black basses (Micropterus) of Florida with description of a new species[R]. University of Michigan Museum of Zoology Occasional Papers, 1949, 516: 1-40.
|
| [8] |
RICHARD H, EDITORS H C. Black bass biology and management[M]. Washington, DC: Sport Fishing Institute, 1975.
|
| [9] |
李仲辉, 杨太有. 大口黑鲈和尖吻鲈骨骼系统的比较研究[J]. 动物学报, 2001, 47(s1): 110-115. LI Z H, YANG T Y. Studies on osteology of Micropterus salmoides (Lacepede) and Lates calcarifer (Bloch)[J]. Acta Zoologica Sinica, 2001, 47(s1): 110-115. |
| [10] |
HINES S A, PHILIPP D P, CHILDERS W F, et al. Thermal kinetic differences between allelic isozymes of malate dehydrogenase (Mdh-B locus) of largemouth bass, Micropterus salmoides[J]. Biochemical Genetics, 1983, 21(11/12): 1143-1151. |
| [11] |
PHILIPP D P, CHILDERS W F, WHITT G S. A biochemical genetic evaluation of the northern and Florida subspecies of largemouth bass[J]. Transactions of the American Fisheries Society, 1983, 112(1): 1-20. DOI:10.1577/1548-8659(1983)112<1:ABGEOT>2.0.CO;2 |
| [12] |
WILLIAMS D J, KAZIANIS S, WALTER R B. Use of random amplified polymorphic DNA (RAPD) for identification of largemouth bass subspecies and their intergrades[J]. Transaction of the American Fisheries Society, 1998, 127(5): 825-832. DOI:10.1577/1548-8659(1998)127<0825:UORAPD>2.0.CO;2 |
| [13] |
LUTZ-CARRILLO D J, NICE C C, BONNER T H, et al. Admixture analysis of florida largemouth bass and northern largemouth bass using microsatellite loci[J]. Transactions of the American Fisheries Society, 2006, 135(3): 779-791. DOI:10.1577/T04-221.1 |
| [14] |
BREMER J R A, ZHANG L, BULAK J S, et al. A polymerase chain reaction-restriction fragment length polymorphism (PCR-RFLP) assay for the discrimination of mitochondrial DNA from the Florida and Northern subspecies of largemouth bass[J]. Transactions of the American Fisheries Society, 1998, 127(3): 507-511. DOI:10.1577/1548-8659(1998)127<0507:APCRNR>2.0.CO;2 |
| [15] |
李胜杰, 白俊杰, 叶星, 等. 基于线粒体D-loop区探讨我国养殖大口黑鲈的分类地位和遗传变异[J]. 海洋渔业, 2008, 30(4): 291-296. LI S J, BAI J J, YE X, et al. Approach on the taxonomic status and genetic variation of largemouth bass (Micropterus salmoides) cultured in China based on mitochondrial D-loop gene[J]. Marine Fisheries, 2008, 30(4): 291-296. DOI:10.3969/j.issn.1004-2490.2008.04.001 |
| [16] |
NEDBAL M A, PHILIPP D P. Differentiation of mitochondrial DNA in largemouth bass[J]. Transactions of the American Fisheries Society, 1994, 123(4): 460-468. DOI:10.1577/1548-8659(1994)123<0460:DOMDIL>2.3.CO;2 |
| [17] |
佟雪红, 董在杰, 缪为民, 等. 建鲤与黄河鲤的杂交优势研究及主要生长性状的通径分析[J]. 大连水产学院学报, 2007, 22(3): 159-163. TONG X H, DONG Z J, MIAO W M, et al. The heterosis of F1 hybrids (Jian carp×Huanghe carp) and path analysis of main growth traits[J]. Journal of Dalian Fisheries University, 2007, 22(3): 159-163. |
| [18] |
陈紫辉. 长鳍鲤(C. carpio var. longfin)、锦鲤(C. carpio var. koi)与正反交子代遗传差异分析[D]. 上海: 上海海洋大学, 2014. CHEN Z H. Genetic differentiation of long-fin carp (C. carpio var. longfin)×koi Carp (C. carpio var. koi) and their hybrids[D]. Shanghai: Shanghai Ocean University, 2014. |
| [19] |
李家乐, 李思发, 李勇, 等. 尼奥鱼[尼罗罗非鱼(♀)×奥利亚罗非鱼(♂)]同其亲本的形态和判别[J]. 水产学报, 1999, 23(3): 261-265. LI J L, LI S F, LI Y, et al. Morphology and discrimination of hybrid Oreochromis niloticus(♀)×Oreochromis aureus(♂) and their parents[J]. Journal of Fisheries of China, 1999, 23(3): 261-265. |
| [20] |
郭金涛, 赵金良, 甘远迪, 等. 尼罗罗非鱼(♀)×萨罗罗非鱼(♂)杂交后代F1、F2形态性状的遗传与变异[J]. 中国水产科学, 2014, 21(2): 275-282. GUO J T, ZHAO J L, GAN Y D, et al. Inheritance and variation of morphological traits in F1 and F2 hybrids of Oreochromis niloticus♀×Sarotherodon melanotheron ♂[J]. Journal of Fishery Sciences of China, 2014, 21(2): 275-282. |
| [21] |
谢刚, 叶星, 庞世勋, 等. 杂交鲂(广东鲂♀×团头鲂♂)及其亲本主要遗传性状的比较研究[J]. 湖北农学院学报, 2002, 22(4): 330-332. XIE G, YE X, PANG S X, et al. Comparative study on principal genetic characters of the first filial generation (Megalobrama hoffmanni♀×Megalobrama amblycephala ♂) and its parents[J]. Journal of Hubei Agricultural College, 2002, 22(4): 330-332. |
| [22] |
关文志, 郑国栋, 吴成宾, 等. 团头鲂与三角鲂或长春鳊杂交后代的生长及形态对比分析[J]. 中国水产科学, 2017, 24(1): 31-39. GUAN W Z, ZHENG G D, WU C B, et al. Comparative analysis of growth and morphological variations among Megalobrama amblycephala, M. terminalis, Parabramis pekinensis and their hybrids[J]. Journal of Fishery Sciences of China, 2017, 24(1): 31-39. |
| [23] |
朱文彬, 傅建军, 王兰梅, 等. 鳙30日龄生长性状的遗传参数[J]. 水产学报, 2020, 44(6): 883-893. ZHU W B, FU J J, WANG L M, et al. Genetic parameter analyses of growth traits at 30 days post-hatching in bighead carp (Hypophthalmichthy nobilis)[J]. Journal of Fisheries of China, 2020, 44(6): 883-893. |
| [24] |
WILLIAMSON J H, CARMICHAEL G J. An aquacultural evaluation of Florida, northern, and hybrid largemouth bass, Micropterus salmoides[J]. Aquaculture, 1990, 85(1/4): 247-257. |
| [25] |
ZOLCZYNSKI JR S J, DAVIES W D. Growth characteristics of the Northern and Florida subspecies of largemouth bass and their hybrid, and a comparison of catchability between the subspecies[J]. Transactions of the American Fisheries Society, 1976, 105(2): 240-243. DOI:10.1577/1548-8659(1976)105<240:GCOTNA>2.0.CO;2 |
| [26] |
KLEINSASSER L J, WILLIAMSON J H, WHITESIDE B G. Growth and catchability of Northern, Florida, and F, hybrid largemouth bass in Texas ponds[J]. North American Journal of Fisheries Management, 1990, 10(4): 462-468. DOI:10.1577/1548-8675(1990)010<0462:GACONF>2.3.CO;2 |
| [27] |
NEAL J W, NOBLE R L. Growth, survival, and site fidelity of Florida and intergrade largemouth bass stocked in a tropical reservoir[J]. North American Journal of Fisheries Management, 2002, 22(2): 528-536. DOI:10.1577/1548-8675(2002)022<0528:GSASFO>2.0.CO;2 |
| [28] |
周家辉, 李胜杰, 姜鹏, 等. 大口黑鲈北方亚种群体和"优鲈1号"群体及其正反杂交子代的遗传和生长性能比较[J]. 海洋渔业, 2020, 42(3): 324-331. ZHANG J H, LI S J, JIANG P, et al. Comparison analysis of genetic diversity and growth traits among "Youlu No.1" and their reciprocal hybrids of northern Micropterus salmoides[J]. Marine Fisheries, 2020, 42(3): 324-331. DOI:10.3969/j.issn.1004-2490.2020.03.008 |
| [29] |
苏胜彦, 张林兵, 李海洋, 等. 基于微卫星标记的大口黑鲈(Micropterus salmoides)原种和养殖群体遗传多样性和结构分析[J]. 浙江大学学报(农业与生命科学版), 2020, 46(6): 687-698. SU S Y, ZHANG L B, LI H Y, et al. Genetic diversity and structure analyses of largemouth bass (Micropterus salmoides) original and cultured populations based on microsatellite markers[J]. Journal of Zhejiang University (Agriculture & Life Sciences), 2020, 46(6): 687-698. |
| [30] |
殷名称. 鱼类生态学[M]. 北京: 中国农业出版社, 1993: 50-60. YIN M C. Fish ecology[M]. Beijing: China Agriculture Press, 1993: 50-60. |
| [31] |
李宁. 动物遗传学[M]. 北京: 中国农业出版社, 2003: 178. LI N. Animal genetics[M]. Beijing: China Agriculture Press, 2003: 178. |
| [32] |
顾万春. 统计遗传学[M]. 北京: 科学出版社, 2006: 320. GU W C. Statistical genetics[M]. Beijing: Science Press, 2006: 320. |
| [33] |
王佳, 刘青华, 施志仪. 黄金鲈与伊犁鲈杂交后代生长性能及杂交鲈性腺发育分析[J]. 淡水渔业, 2009, 39(5): 7-12. WANG J, LIU Q H, SHI Z Y. Analysis of growth and gonadal development in hybrids between Perca flavescens and Perca schrenki[J]. Freshwater Fisheries, 2009, 39(5): 7-12. |
| [34] |
张志新, 周大颜, 甘习军, 等. 白鲫与4种鲤杂交及其自交F1鱼苗的形态特征及生长[J]. 淡水渔业, 2019, 49(1): 81-86. ZHANG Z X, ZHOU D Y, GAN X J, et al. Comparison of morphological characteristics and growth in early stage of hybrid F1 generation among self-bred F1 Carassius cuvieri and several carp species of Cyprinus carpio[J]. Freshwater Fisheries, 2019, 49(1): 81-86. |
| [35] |
佟雪红, 袁新华, 董在杰, 等. 建鲤自交及与黄河鲤正反杂交子代的生长比较和通径分析[J]. 水产学报, 2008, 32(2): 182-189. TONG X H, YUAN X H, DONG Z J, et al. Growth comparison and path analysis of selfing of Jian carp and reciprocal crosses hybrids between Jian carp and Huanghe carp[J]. Journal of Fisheries of China, 2008, 32(2): 182-189. |
| [36] |
王佩佩, 周国勤, 陈树桥, 等. 大口黑鲈北方亚种、佛罗里达亚种及"优鲈3号"杂交F1子代生长性能及遗传多样性分析[J]. 海洋渔业, 2020, 42(4): 403-409. WANG P P, ZHOU G Q, CHEN S Q, et al. Analysis of growth trait comparison and genetic diversity of F1 progeny on cross species of southern largemouth bass, northern largemouth bass and "Youlu No.3"[J]. Marine Fisheries, 2020, 42(4): 403-409. |
| [37] |
董在杰. "福瑞鲤2号"新品种育种技术[J]. 科学养鱼, 2018, 4(4): 9-10. DONG Z J. Breeding technology of new variety "Furui Carp No.2"[J]. Scientific Fish Farming, 2018, 4: 9-10. |
| [38] |
PARKER H R, PHILIPP D P, WHITT G S. Gene regulatory divergence among species estimated by altered developmental patterns in interspecific hybrids[J]. Molecular Biology and Evolution, 1985, 2(3): 217-250. |
| [39] |
李武辉, 胡婕, 孙成飞, 等. 大口黑鲈(♀)×蓝鳃太阳鱼(♂)杂交F1的形态及遗传特征[J]. 水产学报, 2020, 44(8): 1225-1236. LI W H, HU J, SUN C F, et al. Morphological and genetic characteristics of hybrid F1 derived from largemouth bass (Micropterus salmoides) (♀)×bluegill (Lepomis mearchirus) (♂)[J]. Journal of Fisheries of China, 2020, 44(8): 1225-1236. |
| [40] |
杨慧, 朱文彬, 董在杰, 等. 3个红罗非鱼群体的形态差异分析[J]. 上海海洋大学学报, 2015, 24(5): 678-684. YANG H, ZHU W B, DONG Z J, et al. Morphological variation analysis of three populations of red tilapia[J]. Journal of Shanghai Ocean University, 2015, 24(5): 678-684. |
| [41] |
胡彦波, 温海深, 张美昭, 等. 花鲈形态性状对体质量的影响效果[J]. 中国海洋大学学报(自然科学版), 2018, 48(2): 38-48. HU Y B, WEN H S, ZHANG M Z, et al. Analysis of effects of morphological traits on body weight of spotted sea bass (Lateolabrax maculatus)[J]. Periodical of Ocean University of China, 2018, 48(2): 38-48. |
| [42] |
何小燕, 刘小林, 白俊杰, 等. 大口黑鲈形态性状对体重的影响效果分析[J]. 水产学报, 2009, 33(4): 597-603. HE X Y, LIU X L, BAI S J, et al. Mathematical analysis of effects of morphometric attribute on body weight of largemouth bass (Micropterus salmoides)[J]. Journal of Fisheries of China, 2009, 33(4): 597-603. |
| [43] |
李莉, 王雪, 菅玉霞, 等. 不同月龄大泷六线鱼形态性状与体质量的相关性及通径分析[J]. 上海海洋大学学报, 2019, 28(1): 58-66. LI L, WANG X, JIAN Y X, et al. Correlation and path analysis between morphological traits and body mass of Hexagrammos otakii at different months of age[J]. Journal of Shanghai Ocean University, 2019, 28(1): 58-66. |
| [44] |
姜绪, 林香青, 马惠, 等. 5月龄大口黑鲈形态性状与体重的相关及通径分析[J]. 山东农业科学, 2020, 52(5): 124-129. JIANG X, LIN X Q, MA H, et al. Correlation and path analysis on body weight and morphometric traits of 5-month-old Micropterus salmoides[J]. Shandong Agricultural Sciences, 2020, 52(5): 124-129. |
2. Key Laboratory of Freshwater Fisheries and Germplasm Resources Utilization, Ministry of Agriculture and Rural Affairs, Freshwater Fisheries Research Center, Chinese Academy of Fishery Sciences, Wuxi 214081, Jiangsu, China;
3. Zhanglin Fisheries Company, Tongling 224151, Anhui, China;
4. Fisheries Management Station of Yi'an District, Tongling 244151, Anhui, China
 2022,
Vol. 31
2022,
Vol. 31


