2. 青岛海洋科学与技术国家实验室海洋渔业科学与食物产出过程功能实验室, 山东 青岛 266237;
3. 农业农村部大洋渔业开发重点实验室, 上海 201306;
4. 国家远洋渔业工程技术研究中心, 上海 201306;
5. 大洋渔业资源可持续开发教育部重点实验室, 上海 201306
柔鱼(Ommastrephes bartramii)是大洋性鱿鱼类,主要分布在太平洋、印度洋、大西洋的热带和亚热带海域[1-3]。其资源量巨大,目前的商业性捕捞主要集中于北太平洋海域,是我国远洋鱿钓渔业的主要捕捞种类之一[4-5]。作为一种短生命周期(1年生)的鱿鱼种类,柔鱼的生活史较其他长生命周期种类更容易受到海洋环境变化及气候变化的影响[6-8]。已有大量研究[9-13]表明,海洋环境的变化会对柔鱼个体生长、栖息地分布产生很大影响,相应地造成渔场重心移动。同时,柔鱼资源量与厄尔尼诺/拉尼娜现象、产卵场适宜海表面温度范围、叶绿素适宜浓度范围、水温垂直结构以及亲潮和黑潮的变化有着密切的关系[9]。
耳石是头足类重要的硬组织之一,结构相对稳定,可用作种群鉴定[14]、年龄估算[15]以及生活史推算[16]等方面的研究材料。海洋环境变化不仅会对柔鱼的生长产生影响,也可能会对柔鱼耳石外部形态及其生长产生影响,但是目前尚不清楚影响程度如何,是否达到了统计学差异。为此,选择2012、2015和2016年3个年份的柔鱼样本,分析耳石外部形态及其生长差异,为北太平洋柔鱼渔业生物学研究提供基础。
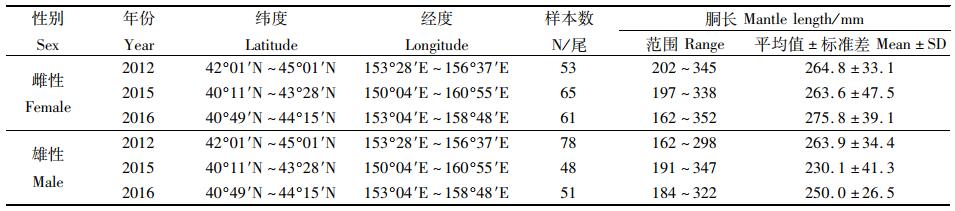
1 材料与方法 1.1 采样时间和范围选取2012、2015和2016年样本进行分析,分别代表不同环境条件年份,其中2012年为太平洋年代际振荡(pacific decadal oscillation, PDO)冷期拉尼娜年,2015年为PDO暖期厄尔尼诺年,2016年为PDO暖期拉尼娜年。样本主要采集于北太平洋海域,采样时间为7—10月。采集后的柔鱼样本直接在鱿钓船上冷冻,随后通过运输船运回实验室进行实验分析。样本采集时,按胴长大小随机选取样本,保证每年数据不少于100尾,3个年份累计取样356尾(表 1)。
|
表 1 不同海洋环境年北太平洋柔鱼样本基本信息 Tab.1 Basic information of O. bartramii samples in different marine environment years |
PDO指数(PDO indices, PDOI)是反映PDO强弱程度的指标,也是反映PDO相位的重要指标[17-18]。PDOI为正值时表示PDO暖期正相位,与此同时中太平洋海域海表面温度(sea surface temperature, SST)较低,美国西海岸SST较高;反之为PDO冷期负相位,表现为与PDO暖期相反的情况[17, 19]。根据大气和海洋联合研究所(Joint Institute for the Study of the Atmosphere and Ocean, http://research.jisao.washington.edu/pdo/)提供的PDOI可确定:2012年处于PDO冷期,2015和2016年处于PDO暖期。
厄尔尼诺和拉尼娜现象也是北太平洋海域主要气候事件之一,对北太平洋柔鱼生长有着很大的影响[10]。根据美国国家海洋和大气网站管理局(http://www.cpc.ncep.noaa.gov/products/analysis_monitoring/ensostuff/ensoyears.shtml)提供的厄尔尼诺和拉尼娜数据确定,2012和2016年为拉尼娜年,2015年为厄尔尼诺年。
对北太平洋柔鱼主要索饵场(35°N ~50°N和150°E ~175°E)海域海表面温度(SST)和叶绿素a(chlorophyll-a, Chl.a)质量浓度进行统计。数据来源于美国国家海洋和大气管理局网站(https://oceanwatch.pifsc.noaa.gov/erddap/griddap), 空间分辨率为0.05°×0.05°。
1.3 研究方法 1.3.1 生物学测定和耳石提取样本解冻后对其进行生物学测定,包括胴长(mantle length, ML)、体质量(body mass, BM)、性别和性腺成熟度。测量时,胴长精确至1 mm, 体质量精确至1 g。性腺成熟度的划分根据LIPINSKI等[20]的方法,根据性腺特征变化划分为Ⅰ~Ⅴ期,其中Ⅰ~Ⅱ期为未成熟个体,Ⅲ期及以上为成熟个体。从头部平衡囊内取出耳石,标号后放入含有质量分数为75%乙醇溶液的1.5 mL离心管内,以除去耳石表面附着的软膜和有机物质。
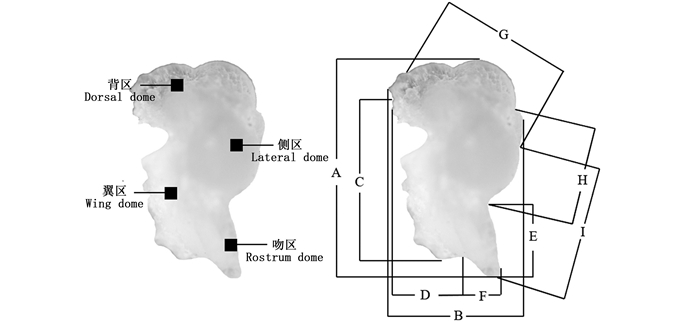
1.3.2 耳石外部形态测量将耳石从离心管内取出,凸面向上置于Nikon ZOOM645S体式显微镜×40倍下进行CCD拍照,然后利用Mshot专业图像分析软件,分别测量出耳石各形态参数值(图 1), 具体包括耳石总长(total statolith length, TSL)、最大宽度(maximum width, MW)、翼区长(wing length, WL)、翼区宽(wing width, WW)、吻区长(rostrum length, RL)、吻区宽(rostrum width, RW)、背侧区长(ventral dorsal dome length, DLL)、侧区长(lateral dome length, LDL)和吻侧区长(rostrum lateral dome length, RLL), 测量结果精确至1 μm。测量由两人分别进行,若两者测得结果误差超过5%则重新测量,最终取两者测量的平均值。
|
A.耳石总长;B.最大宽度;C.翼区长;D.翼区宽;E.吻区长;F.吻区宽;G.背侧区长;H.侧区长;I.吻侧区长。 A.TSL; B.MW; C.WL; D.WW; E.RL; F.RW; G.DLL; H.LDL; I.RLL. 图 1 柔鱼耳石各区和形态参数示意图 Fig. 1 Dome and morphometric parameters of O. bartramii's statolith |
统计分析不同性别和不同海洋环境年耳石形态特征值,并对形态参数数据进行主成分分析,得到表征耳石形态结构的主要参数。
利用不同生长模型(线性函数、幂函数、指数函数、对数函数)拟合主要形态参数与胴长之间的关系。利用赤池信息准则(akaike information criterion, AIC)[21-22], 选取AIC最小的模型为最适生长模型。
分析不同海洋环境年份耳石形态差异。为了消除个体差异和异速生长对耳石形态的影响,对耳石形态参数进行标准化,具体标准化过程参考文献[23]。然后对标准化后的数据进行单因素方差分析(ANOVA), 分析不同海洋环境年耳石形态参数的差异。
为了解环境因素对耳石形态的影响,分析不同海洋环境年索饵场SST和Chl.a质量浓度的月变化规律,并与标准化后的耳石形态参数进行对比分析。所有统计分析采用Excel、SPSS 24.0和R 4.0软件进行。
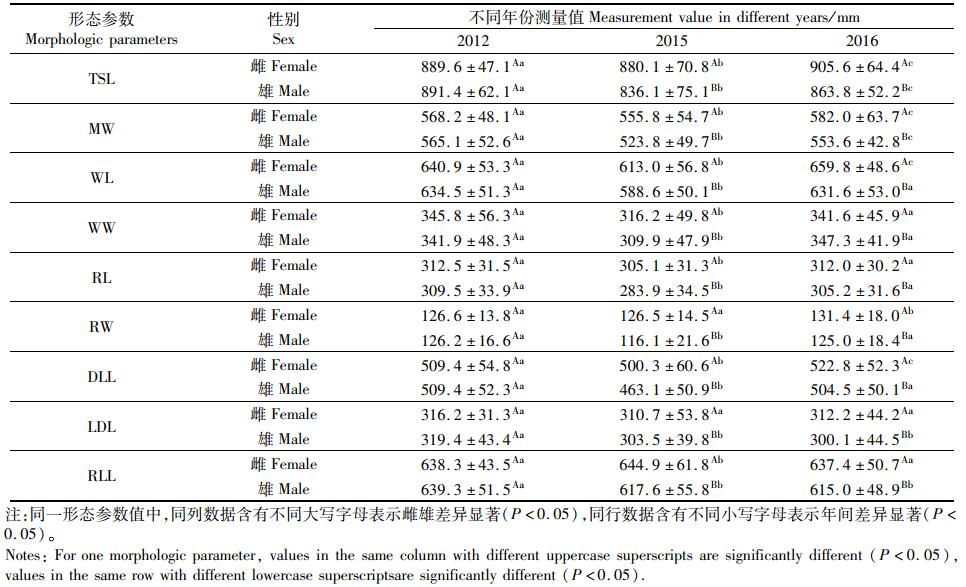
2 结果 2.1 耳石形态参数通过观察发现,柔鱼耳石具有明显的吻区、翼区、背区和侧区结构,其中翼区较大,吻区呈细长状,背侧区分界不明显。通过单因素方差分析发现,雌雄个体间各形态参数均存在显著差异(P < 0.05)。由表 2可知,不同海洋环境年、不同性别耳石形态各有其特征。其中:PDO冷期拉尼娜年(2012年)样本形态参数MW、WL、WW、RL和RW均为雌性个体较大,TSL、LDL和RLL均为雄性个体较大;PDO暖期厄尔尼诺年(2015年)雌性个体所有形态参数值均大于雄性个体;PDO暖期拉尼娜年(2016年)形态参数除WW外, 其他各个形态参数均为雌性个体大于雄性个体。
|
表 2 不同海洋环境年份北太平洋柔鱼9个形态参数平均值±标准差 Tab.2 Mean value and standard deviation of 9 morphologic parameters of O. bartramii's statolith in different marine environment years |
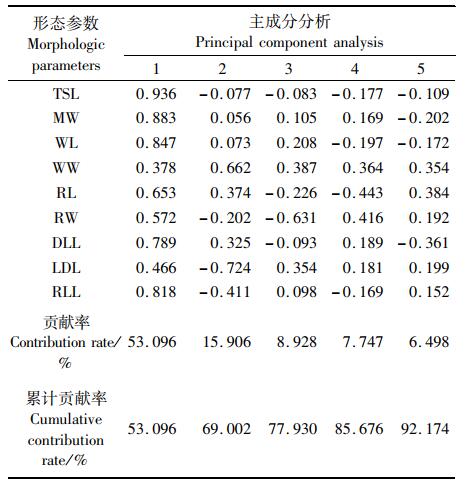
耳石9个形态参数的主成分分析结果显示(表 3), 第1~5个因子解释形态参数的贡献率分别为53.096 %、15.906%、8.928%、7.747%和6.498%, 累计贡献率约为92.174%。第1主成分中,除WW和LDL外,各形态参数负载系数均在0.5以上,其中TSL、WL和RLL的载荷系数最大,达到0.8以上,且均呈正相关;第2主成分中形态参数WW、LDL和RLL负载系数较大,均在0.4以上,第2主成分与WW呈正相关,与LDL、RLL呈负相关;第3主成分与RW呈较大的负相关,与WW和LDL呈较大的正相关;第4主成分中形态参数WW、RL和RW负载系数较大,均在0.3以上,其中第4主成分与WW和RW呈较大的正相关,与RL呈较大的负相关;第5主成分中形态参数WW、RL和DLL负载系数较大,均在0.3以上。
|
表 3 柔鱼耳石9个形态参数的5个主成分负荷值和贡献率 Tab.3 Loading values and contribution rates of five principal components for 9 morphologic parameters of O. bartramii's statolith |
根据主成分载荷,选取较大相关性的形态参数作为表征参数。因此,选取北太平洋柔鱼耳石长度参数TSL、WL、RLL和宽度参数MW、WW、RW等6个形态参数代替9个形态参数来描述耳石形态特征。
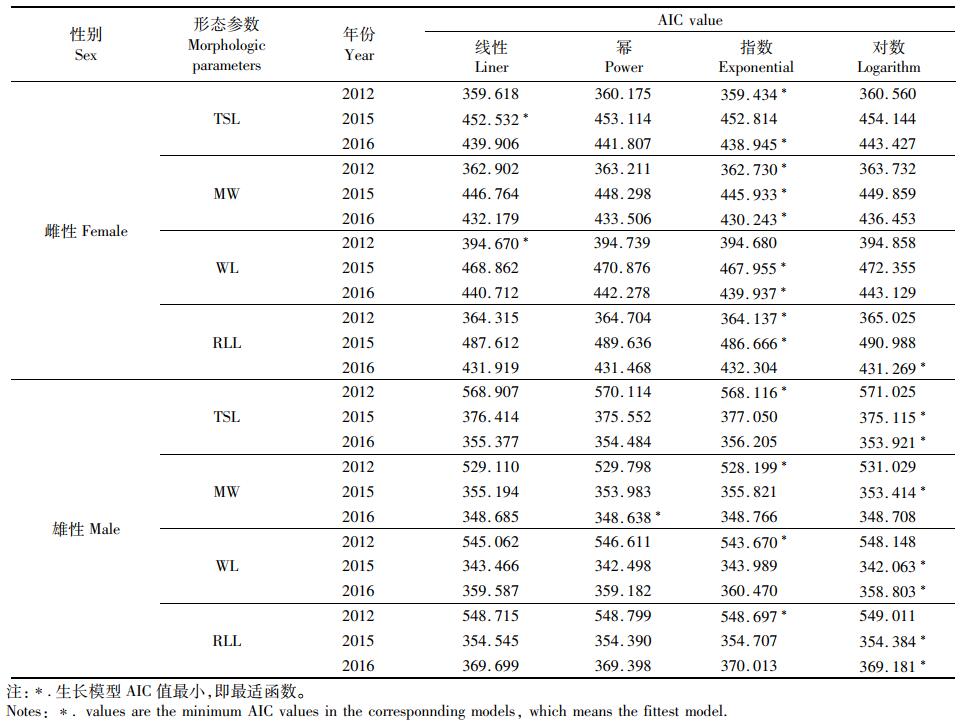
2.3 耳石生长 2.3.1 耳石绝对大小变化总体上,柔鱼耳石生长过程中,背区、吻区和翼区不断增大。大个体柔鱼的耳石比小个体柔鱼的耳石具有更明显的吻区和翼区。4种模型拟合结果显示:6个表征形态参数中,TSL、MW、WL和RLL与胴长之间相关性显著(P < 0.05), 而WW、RW与胴长之间相关性不显著(P > 0.05), 通过AIC值选择最适生长模型发现(表 4), PDO冷期拉尼娜年(2012年)除雌性耳石WL与胴长的关系最适函数为线性函数外,其余各个形态参数与胴长的关系最适函数均为指数函数;PDO暖期厄尔尼诺年(2015年)雌性耳石TSL与胴长的关系最适函数为线性函数,雌性耳石MW、WL和RLL与胴长的关系最适函数均为指数函数,雄性耳石4个主要形态参数与胴长的关系最适函数为对数函数;PDO暖期拉尼娜年(2016年)雌性耳石TSL、MW和WL与胴长关系最适函数为指数函数,雌性耳石RLL、雄性耳石TSL、WL和RLL与胴长关系最适函数为对数函数,雄性耳石TSL和WL与胴长的关系最适函数为幂函数,雄性耳石MW与胴长关系最适函数为幂函数(表 4)。
|
表 4 不同海洋环境年耳石形态参数与胴长关系的生长模型AIC检测结果 Tab.4 AIC values of different growth model of morphologic parameters and ML in different marine years |
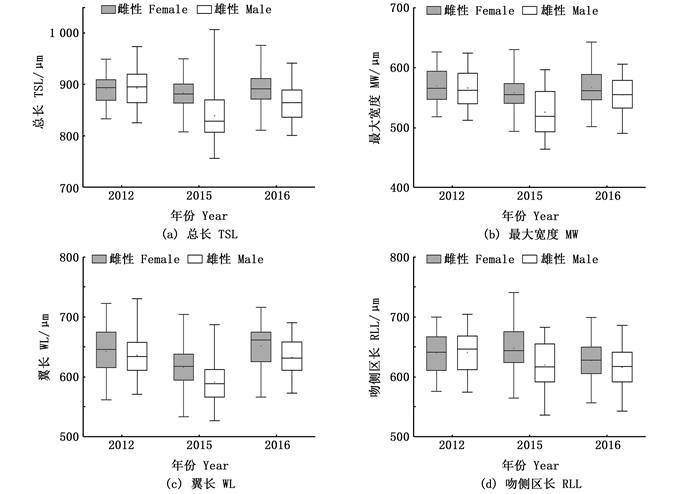
将TSL、MW、WL和RLL 4个表征形态参数进行标准化,对标准化后的4个形态参数进行比较,发现除雄性个体标准化后的RLL参数外,PDO冷期拉尼娜年(2012年)和PDO暖期拉尼娜年(2016年)4个标准化后的形态参数均不存在显著差异(P > 0.05), PDO暖期厄尔尼诺年(2015年)4个标准化后形态参数与PDO冷期拉尼娜年(2012年)和PDO暖期拉尼娜年(2016年)均存在显著差异。PDO冷期拉尼娜年(2012年)和PDO暖期拉尼娜年(2016年)雌性个体标准化后的TSL、MW和WL均大PDO暖期厄尔尼诺年(2015年)雌性个体,而PDO暖期厄尔尼诺年(2015年)雌性个体标准化后的RLL大于其他2年雌性个体(图 2)。PDO冷期拉尼娜年(2012年)和PDO暖期拉尼娜年(2016年)雄性个体标准化后的TLS、MW和WL也均大于PDO暖期厄尔尼诺年(2015年), 与雌性个体不同,雄性个体标准化后的RLL逐年减小(图 2)。
|
图 2 不同海洋环境年间个体的标准化后形态参数比较 Fig. 2 Comparison of standardized morphologic parameters of O. bartramii's statolith in different marine environment years |
耳石是头足类重要的硬组织之一,其生长与个体生长有着密切关系[24], 因此可以通过耳石形态来研究头足类个体的生长情况。研究发现,不同性别间耳石存在显著差异。不同海洋环境年雌性耳石各个形态参数均值均大于雄性耳石,说明同一群体雌性柔鱼耳石较雄性生长快。同时有学者认为,由于雌性柔鱼较雄性生长快,进而导致雌性柔鱼的耳石生长也相对较快[25-26], 这与本研究结果一致。马金等[24]认为,在同一环境中,雌性个体由于需要为性腺发育提供更多能量,个体生长缓慢导致雌雄个体耳石形成产生差异。头足类从幼体到成体的过程中,随着胴长增加,耳石外部形态变化逐渐减慢,有学者[27]认为可能与耳石调节头足类淋巴液流动和感知游泳加速度有关,头足类在幼体时期活动能力弱,需要更大的耳石感知较小的加速度,因此头足类耳石在幼体期间生长较快;但随着头足类个体发育,活动能力变强,对耳石感知加速度的需求降低,导致耳石相对于胴长的生长速度逐渐减小。
柔鱼耳石主要形态参数与胴长的生长关系也存在显著差异。马金等[24]研究发现,2007年柔鱼个体TSL、RL、WL与胴长呈幂函数关系,RW、WW与胴长没有显著的相关性,这与本研究结果稍有差异,这种最适生长关系的年间差异反映了不同海洋环境年耳石生长过程的差异性。综上所述,年际间柔鱼的生活史过程存在差异,这种差异直接或者间接影响其耳石各个部位的生长,两者的相互关系间接地反映了利用耳石形态特征进行柔鱼生长方面研究的可行性和科学性。
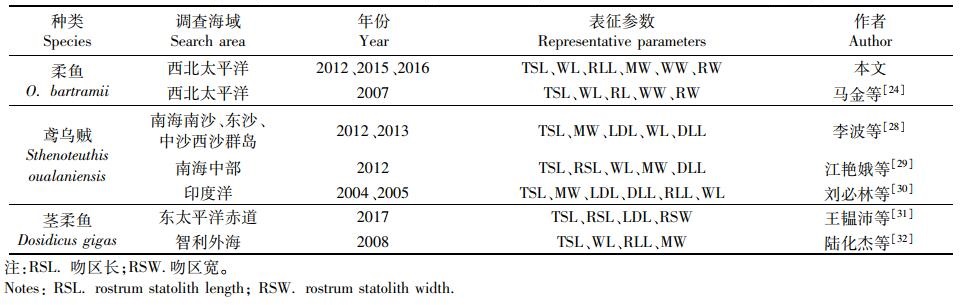
3.2 耳石表征参数差异本研究利用主成分分析筛选出TSL、WL、RLL、MW、WW、RW等作为西北太平洋柔鱼耳石形态特征的表征参数,其中,TSL、WL、RLL为长度表征参数,MW、WW、RW为宽度表征参数。马金等[24]以TSL、WL、RL、WW、RW等5个形态参数作为PDO冷期拉尼娜年(2007年)北太柔鱼的表征参数,与本研究不同,说明不同年份间头足类耳石形态特征有一定的差异性。同时,分布于不同海域的同种头足类耳石形态表征参数也存在差异性(表 5)。
|
表 5 不同头足类耳石形态特征的表征参数 Tab.5 Morphological characteristic representative parameters of statolith for Cephalopods |
环境对短生命周期生物的影响明显,尤其是北太平洋柔鱼等1年生头足类,极易受到周围环境变化的影响[2, 33]。因此,柔鱼耳石生长除受到个体生长的影响外,还受到外界环境影响[34]。通过分析标准化后的数据发现,PDO冷期拉尼娜年(2012年)与PDO暖期拉尼娜年(2016年)耳石形态参数间不存在显著差异,而PDO暖期厄尔尼诺年(2015年)与PDO暖期拉尼娜年(2016年)耳石形态参数存在显著差异,说明大尺度气候事件对柔鱼的影响不显著,而厄尔尼诺/拉尼娜事件会对柔鱼耳石形态造成影响。厄尔尼诺事件发生时,海水温度较低,海洋环境不利于柔鱼耳石的生长,使得该事件发生年份的柔鱼耳石偏小;与之相反,拉尼娜事件发生时,形成较为适宜的生存环境,使得柔鱼耳石生长较好,较厄尔尼诺年份大。方舟等[2]对不同海洋环境年的北太平洋柔鱼的角质颚形态研究发现,2016年(拉尼娜年)柔鱼角质颚明显大于2015年(厄尔尼诺年)柔鱼角质颚。这与本研究结果一致,说明拉尼娜事件会促进柔鱼的硬组织生长,而厄尔尼诺事件会抑制柔鱼的硬组织生长。
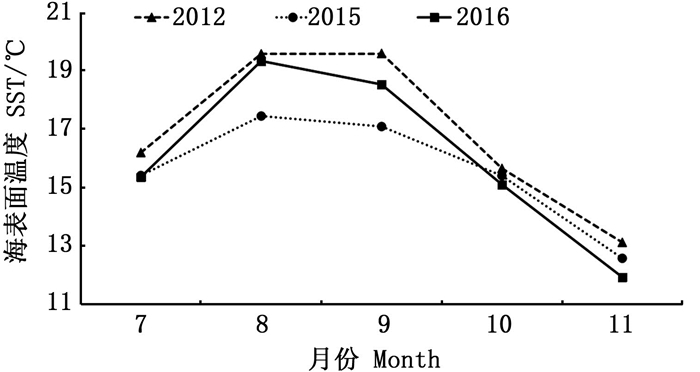
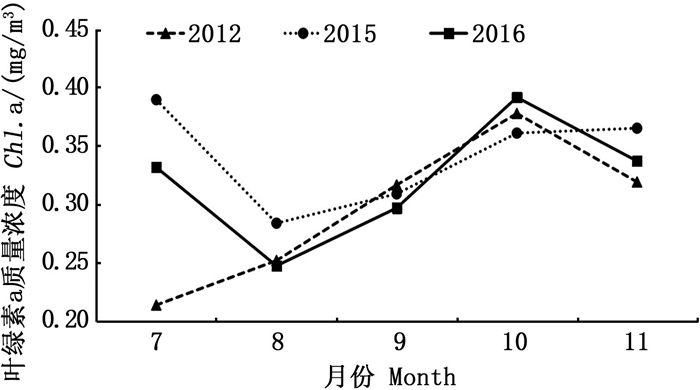
栖息环境和摄食情况是影响柔鱼资源量以及补充量的重要环境因子[13, 35-36], 且温度、盐度、溶解氧等环境因素也会对耳石的生长造成直接的影响[34]。已有研究[37]发现,柔鱼索饵场适宜的SST范围为17~22 ℃。本研究发现,同为拉尼娜年的2012和2016年7—9月索饵场环境较厄尔尼诺年(2015年)更为适宜,较高的SST对应较大的耳石,可以认为SST的变化会对耳石的生长造成影响(图 3)。同样栖息环境Chl. a适宜质量浓度为0.2~0.5 mg/m3[37], 3年的Chl. a质量浓度均分布在柔鱼适宜质量浓度范围内, 且8—9月Chl. a质量浓度差异不明显(图 4)。但2015年Chl. a质量浓度在7—8月发生骤降,这可能是导致该年耳石较小的原因之一。而同时期的2016年Chl. a质量浓度虽然在7—8月发生骤降,但其之后8—10月回升较大。2012年7—10月Chl. a质量浓度整体呈上升趋势,且在9月之后超过2015年。这也可以认为是2012年和2016年柔鱼耳石较大的原因之一。综上所述,SST和Chl. a质量浓度对耳石形态会产生较大的影响,7—9月的环境因素对该年度的影响较大。
|
图 3 不同海洋环境年索饵场平均SST的月变化趋势 Fig. 3 The monthly variation trend of SST on fishing ground in different marine environment years |
|
图 4 不同海洋环境年索饵场平均Chl. a质量浓度的月变化趋势 Fig. 4 The monthly variation trend of Chl. a on fishing groundindifferentmarine environment years |
本研究分析了不同性别和不同海洋环境年的柔鱼耳石形态差异,结合SST和Chl. a质量浓度的变化分析了不同海洋环境影响下耳石形态出现差异的可能原因。研究发现耳石的某些形态特征值与柔鱼个体大小之间关系显著,同时发现不同海洋环境影响下,这种关系存在显著的年间差异,因此推断耳石形态研究可用于基于个体生长等方面的研究。同时发现耳石形态与环境变化之间存在某种联系,但由于柔鱼个体所经历的具体生境变化尚未得知,因此不能建立耳石形态参数与环境因子之间的模型。因此,在将来的研究中,需要更为精确地分析环境如何影响耳石形态变化并建立海洋环境因子与耳石形态参数的模型,为柔鱼生物学研究提供更多基础资料。
| [1] |
陈新军, 刘必林, 王尧耕. 世界头足类[M]. 北京: 海洋出版社, 2009: 60-69. CHEN X J, LIU B L, WANG Y G. World cephalopod[M]. Beijing: China Ocean Press, 2009: 60-69. |
| [2] |
方舟, 陈新军, 瞿俊跃, 等. 北太平洋柔鱼角质颚形态及生长年间差异[J]. 上海海洋大学学报, 2020, 29(1): 109-120. FANG Z, CHEN X J, QU J Y, et al. Annual variation of beak morphology and growth models for neon flying squid (Ommastrephes bartramii) in north Pacific Ocean[J]. Journal of Shanghai Ocean University, 2020, 29(1): 109-120. |
| [3] |
余为, 陈新军, 易倩. 西北太平洋海洋净初级生产力与柔鱼资源量变动关系的研究[J]. 海洋学报, 2016, 38(2): 64-72. YU W, CHEN X J, YI Q. Relationship between spatio-temporal dynamics of neon flying squid Ommastrephes bartramii and net primary production in the northwest Pacific Ocean[J]. Haiyang Xuebao, 2016, 38(2): 64-72. DOI:10.3969/j.issn.0253-4193.2016.02.006 |
| [4] |
王尧耕, 陈新军. 世界大洋性经济柔鱼类资源及其渔业[M]. 北京: 海洋出版社, 2005: 152-153. WANG Y G, CHEN X J. The resource and fishery of World Oceanic economic squid[M]. Beijing: China Ocean Press, 2005: 152-153. |
| [5] |
陈新军. 世界头足类资源开发现状及我国远洋鱿钓渔业发展对策[J]. 上海海洋大学学报, 2019, 28(3): 321-330. CHEN X J. Development status of world cephalopod fisheries and suggestions for squid jigging fishery in China[J]. Journal of Shanghai Ocean University, 2019, 28(3): 321-330. |
| [6] |
BOWER J R, ICHII T. The red flying squid (Ommastrephes bartramii): a review of recent research and the fishery in Japan[J]. Fisheries Research, 2005, 76(1): 39-55. DOI:10.1016/j.fishres.2005.05.009 |
| [7] |
YU W, CHEN X J, YI Q, et al. Spatio-temporal distributions and habitat hotspots of the winter-spring cohort of neon flying squid Ommastrephes bartramii in relation to oceanographic conditions in the Northwest Pacific Ocean[J]. Fisheries Research, 2016, 175: 103-115. DOI:10.1016/j.fishres.2015.11.026 |
| [8] |
NISHIKAWA H, TOYODA T, MASUDA S, et al. Wind-induced stock variation of the neon flying squid (Ommastrephes bartramii) winter-spring cohort in the subtropical North Pacific Ocean[J]. Fisheries Oceanography, 2015, 24(3): 229-241. DOI:10.1111/fog.12106 |
| [9] |
YU W, CHEN X J, CHEN Y, et al. Effects of environmental variations on the abundance of western winter-spring cohort of neon flying squid (Ommastrephes bartramii) in the Northwest Pacific Ocean[J]. Acta Oceanologica Sinica, 2015, 34(8): 43-51. DOI:10.1007/s13131-015-0707-7 |
| [10] |
YU W, CHEN X J, YI Q, et al. Impacts of climatic and marine environmental variations on the spatial distribution of Ommastrephes bartramii in the Northwest Pacific Ocean[J]. Acta Oceanologica Sinica, 2016, 35(3): 108-116. DOI:10.1007/s13131-016-0821-1 |
| [11] |
YU W, CHEN X J, CHEN C S, et al. Impacts of oceanographic factors on interannual variability of the winter-spring cohort of neon flying squid abundance in the Northwest Pacific Ocean[J]. Acta Oceanologica Sinica, 2017, 36(10): 48-59. DOI:10.1007/s13131-017-1069-0 |
| [12] |
XU J, CHEN X J, CHEN Y, et al. The effect of sea surface temperature increase on the potential habitat of Ommastrephes bartramii in the Northwest Pacific Ocean[J]. Acta Oceanologica Sinica, 2016, 35(2): 109-116. DOI:10.1007/s13131-015-0782-9 |
| [13] |
ALABIA I D, SAITOH S I, MUGO R, et al. Seasonal potential fishing ground prediction of neon flying squid (Ommastrephes bartramii) in the western and central North Pacific[J]. Fisheries Oceanography, 2015, 24(2): 190-203. DOI:10.1111/fog.12102 |
| [14] |
DÍAZ-SANTANA-ITURRÍOS M, SALINAS-ZAVALA C A, GRANADOS-AMORES J. Description of the statolith shape of two sympatric ommastrephids in the Mexican Pacific obtained from geometric morphometrics as a tool for identification at the species level[J]. Marine Biodiversity, 2018, 48(3): 1667-1671. DOI:10.1007/s12526-017-0650-2 |
| [15] |
陈新军, 马金, 刘必林, 等. 基于耳石微结构的西北太平洋柔鱼群体结构、年龄与生长的研究[J]. 水产学报, 2011, 35(8): 1191-1198. CHEN X J, MA J, LIU B L, et al. Population structure, age and growth of neon flying squid (Ommastrephes bartramii) in the northwest PacificOcean based on statolith microstructure[J]. Journal of Fisheries of China, 2011, 35(8): 1191-1198. |
| [16] |
SAKAI M, BRUNETTI N, IVANOVIC M, et al. Interpretation of statolith microstructure in reared hatchling paralarvae of the squid Illex argentinus[J]. Marine and Freshwater Research, 2004, 55(4): 403-413. DOI:10.1071/MF03148 |
| [17] |
MANTUA N J, HARE S R. The pacific decadal oscillation[J]. Journal of Oceanography, 2002, 58(1): 35-44. DOI:10.1023/A:1015820616384 |
| [18] |
ZHANG Y, WALLACE J M, BATTISTI D S. ENSO-like interdecadal variability: 1900-93[J]. Journal of Climate, 1997, 10(5): 1004-1020. DOI:10.1175/1520-0442(1997)010<1004:ELIV>2.0.CO;2 |
| [19] |
YU W, CHEN X J, YI Q. Interannual and seasonal variability of winter-spring cohort of neon flying squid abundance in the Northwest Pacific Ocean during 1995-2011[J]. Journal of Ocean University of China, 2016, 15(3): 480-488. DOI:10.1007/s11802-016-2884-1 |
| [20] |
LIPÍNSKI M R, UNDERHILL L G. Sexual maturation in squid: quantum or continuum?[J]. South African Journal of Marine Science, 1995, 15(1): 207-223. DOI:10.2989/02577619509504844 |
| [21] |
CERRATOR M. Interpretable statistical tests for growth comparisons using parameters in the von bertalanffy equation[J]. Canadian Journal of Fisheries and Aquatic Sciences, 1990, 47(7): 1416-1426. DOI:10.1139/f90-160 |
| [22] |
韩青鹏, 陆化杰, 陈新军, 等. 南海北部海域中国枪乌贼角质颚的形态学分析[J]. 南方水产科学, 2017, 13(4): 122-130. HAN Q P, LU H J, CHEN X J, et al. Morphological analysis of beaks of Uroteuthis chinensis in the northern South China Sea[J]. South China Fisheries Science, 2017, 13(4): 122-130. DOI:10.3969/j.issn.2095-0780.2017.04.015 |
| [23] |
LLEONART J, SALAT J, TORRES G J. Removing allometric effects of body size in morphological analysis[J]. Journal of Theoretical Biology, 2000, 205(1): 85-93. DOI:10.1006/jtbi.2000.2043 |
| [24] |
马金, 陈新军, 刘必林, 等. 西北太平洋柔鱼耳石形态特征分析[J]. 中国海洋大学学报, 2009, 39(2): 215-220. MA J, CHEN X J, LIU B L, et al. Morphologic features of statolith for Ommastrephes bartramii in the northwest Pacific Ocean[J]. Periodical of Ocean University of China, 2009, 39(2): 215-220. |
| [25] |
BIGELOW K A. Age and growth of the oceanic squid Onychoteuthis borealijaponica in the North Pacific[J]. Fishery Bulletin, 1994, 92: 13-25. |
| [26] |
BRUNETTI N E, IVANOVIC M L, AUBONE A, et al. Reproductive biology of red squid (Ommastrephes bartramii) in the Southwest Atlantic[J]. Revista de Investigación y Desarrollo Pesquero, 2006, 18: 5-19. |
| [27] |
刘必林, 陈新军, 陆化杰, 等. 头足类耳石[M]. 北京: 科学出版社, 2011: 36-38. LIU B L, CHEN X J, LU H J, et al. Statolith of cephalopod[M]. Beijing: Science Press, 2011: 36-38. |
| [28] |
李波, 阳秀芬, 邱星宇, 等. 基于耳石形态特征的南海鸢乌贼群体判别分析[J]. 广东海洋大学学报, 2019, 39(2): 58-66. LI B, YANG X F, QIU X Y, et al. Discriminant analysis of purpleback flying squid (Sthenoeuthis oualaniensis) groups based on statolith morphology in the South China Sea[J]. Journal of Guangdong Ocean University, 2019, 39(2): 58-66. |
| [29] |
江艳娥, 陈作志, 林昭进, 等. 南海中部海域鸢乌贼耳石形态特征分析[J]. 南方水产科学, 2014, 10(4): 85-90. JIANG Y E, CHEN Z Z, LIN Z J, et al. Statolith morphology of purpleback flying squid Sthenoeuthis oualaniensis in the central South China Sea[J]. South China Fisheries Science, 2014, 10(4): 85-90. DOI:10.3969/j.issn.2095-0780.2014.04.014 |
| [30] |
刘必林, 陈新军, 钟俊生. 印度洋西北海域鸢乌贼耳石的形态特征分析[J]. 上海水产大学学报, 2008, 17(5): 604-609. LIU B L, CHEN X, J, ZHONG J S. Statolithmorphology of the purpleback flyings quid Sthenoeuthis oualaniensis in the northwest Indian Ocean[J]. Journal of Shanghai Fisheries University, 2008, 17(5): 604-609. |
| [31] |
王韫沛, 陈新军, 方舟, 等. 东太平洋赤道海域茎柔鱼耳石外部形态特征分析[J]. 海洋湖沼通报, 2019(6): 147-156. WANG Y P, CHEN X J, FANG Z, et al. Statolith morphology of jumbo flying squid (Dosidicus gigas) in waters near the Equator of Eastern Pacific Ocean[J]. Transactions of Oceanology and Limnology, 2019(6): 147-156. |
| [32] |
陆化杰, 陈新军, 刘必林. 智利外海茎柔鱼(Dosidicus gigas)耳石外部形态特征分析[J]. 海洋与湖沼, 2010, 41(2): 233-239. LU H J, CHEN X J, LIU B L. Statolith morphology of jumbo flying squid Dosidicus gigas in thehigh sea waters off Chile[J]. Oceanologia et Limnologia Sinica, 2010, 41(2): 233-239. |
| [33] |
吴梦瑶, 田思泉. 基于海表面温度SST的剩余产量模型评估太平洋褶柔鱼秋生群资源[J]. 上海海洋大学学报, 2019, 28(6): 933-942. WU M Y, TIAN S Q. Stock assessment for autumn cohort of Todarodes pacificus based on surplus yield model with sea surface temperature[J]. Journal of Shanghai Ocean University, 2019, 28(6): 933-942. |
| [34] |
马金, 陈新军, 刘必林, 等. 环境对头足类耳石微结构的影响研究进展[J]. 上海海洋大学学报, 2009, 18(5): 616-622. MA J, CHEN X J, LIU B L, et al. Review of the influence of environment factorson microstructure of statoliths of cephalopod[J]. Journal of Shanghai Ocean University, 2009, 18(5): 616-622. |
| [35] |
ALABIA I D, SAITOH S I, MUGO R, et al. Identifying pelagic habitat hotspots of neon flying squid in the temperate waters of the central North Pacific[J]. PLoS One, 2015, 10(11): e0142885. DOI:10.1371/journal.pone.0142885 |
| [36] |
温健, 陆鑫一, 陈新军, 等. 基于海表温度和光合有效辐射的西北太平洋柔鱼冬春生群体栖息地热点预测[J]. 上海海洋大学学报, 2019, 28(3): 456-463. WEN J, LU X Y, CHEN X J, et al. Predicting the habitat hot spots of winter-spring cohort of Ommastrephes bartramii in the northwest Pacific Ocean based on the sea surface temperature and photosynthetically active radiation[J]. Journal of Shanghai Ocean University, 2019, 28(3): 456-463. |
| [37] |
WANG J T, YU W, CHEN X J, et al. Detection of potential fishing zones for neon flying squid based on remote-sensing data in the Northwest Pacific Ocean using an artificial neural network[J]. International Journal of Remote Sensing, 2015, 36(13): 3317-3330. DOI:10.1080/01431161.2015.1042121 |
2. Laboratory for Marine Fisheries Science and Food Production Processes, Qingdao National Laboratory for Marine Science and Technology, Qingdao 266237, Shandong, China;
3. Key Laboratory of Oceanic Fisheries Exploration, Ministry of Agriculture and Rural Affairs, Shanghai 201306, China;
4. National Engineering Research Center for Oceanic Fisheries, Shanghai 201306, China;
5. Key Laboratory of Sustainable Exploitation of Oceanic Fisheries Resources, Ministry of Education, Shanghai 201306, China
 2021,
Vol. 30
2021,
Vol. 30


