2. 上海海洋大学 国家水生动物病原库, 上海 201306;
3. 上海海洋大学 农业农村部淡水水产种质资源重点实验室, 上海 201306
甲霜灵又称立达霉,是一种酰胺类农药,具有广谱高效的杀菌效果[1]。常用来防治番茄[2]、黄瓜[3]、马铃薯[4]、芥菜[5]、雪莲果等[6]果蔬中由霜霉菌、腐霉菌[7]等引发的病变。由于甲霜灵对于防治鱼类水霉病具有良好的效果且对靶动物安全, 常用作一种替代孔雀石绿的新型渔用药物以治疗水产动物的水霉病[8],并已获得四类新兽药证书[证号:(2017)新兽药证字18号]。随着甲霜灵的使用越来越广泛,其残留问题也日益凸显。有研究[9]认为,人淋巴细胞暴露于甲霜灵中将会发生变异。欧盟食品安全局[10]在2011年对葡萄、菠菜等果蔬以及猪、羊等反刍动物中甲霜灵的最大残留限量作了规定,但在水产品中相关规定尚未成形。
高效液相色谱[11-13]常用于检测蔬菜、水及土壤中甲霜灵的残留,高效液相色谱-质谱联用[14-16]也用于检测蔬果、鸽肉等食品中甲霜灵的残留,ADLNASAB等[17]、OLIVA等[18]则用气相色谱法对果汁及葡萄酒中的甲霜灵残留进行了检测。但这些检测方法需要依托实验平台的昂贵仪器及专业技术人员进行,具有局限性,且需花费较长时间,不利于在基层推广。因此急需一种新的,能够快速、现场检测水产品中甲霜灵残留的方法。目前,尚无针对甲霜灵在水产品中残留检测的免疫学检测方法作为初筛方法。
胶体金免疫层析(colloidal gold enhanced immunochromatography assay,GICA)作为当今最快速的新型检测技术之一,在三氯氰胺、环丙氨嗪[19]、氧氟沙星[20]等多种药物残留检测领域应用广泛。该技术不仅灵敏度高、操作简单,不需要特殊设备以及专业的检测人员,而且仅几分钟就能直接现场观察判断结果,非常适合用于初筛,作为液相色谱等复筛方法的补充。目前,尽管建立了基于高效液相色谱法的水产品中甲霜灵残留的复检方法,但快速初筛方法还是空白。
为了建立快速检测水产品中抗水霉药物甲霜灵残留的免疫学方法,本研究利用胶体金标记纯化的甲霜灵单克隆抗体作金垫,将甲霜灵-牛血清蛋白偶联物作为检测线(C线),羊抗鼠IgG作为质控线(T线),制备甲霜灵胶体金免疫层析试纸条,建立了一种快速、简便,可不依赖专业人员现场直接检测草鱼等水产品中甲霜灵残留的方法,为水产品质量监控提供技术支持。
1 材料与方法 1.1 实验材料甲霜灵单克隆抗体购买自法泰斯特(北京)技术有限公司;牛血清白蛋白(BSA)购自上海鼎国生物公司;羊抗鼠抗体IgG购自上海鼎国生物公司;硝酸纤维素膜、胶体金垫等购自Millipore公司。实验材料还包括德国Eppendorf公司台式离心机,PowerPac系列Bio-Rad电泳仪,Bio-Tek公司ELx800酶标仪,Agilent 1100液相色谱仪(包含紫外检测器、柱温箱、四元泵、自动进样器等),色谱柱:C18(4.6 mm×250 mm×5 μm)等。
1.2 实验方法 1.2.1 单克隆抗体的鉴定单克隆抗体亚型鉴定:采用间接ELISA法[21],用Invitrogen试剂盒测定甲霜灵单抗亚型。单克隆抗体的分子量及纯度鉴定:采用常规SDS-PAGE法测定单抗的分子量,鉴定抗体纯化效果[22]。单克隆抗体的亲和力鉴定:采用非竞争性酶免疫法ELISA测定单克隆抗体亲和力[23],绘制抗原抗体结合曲线并计算单抗抗体的亲和力常数值。单克隆抗体的灵敏度测定:利用方阵法筛选抗原抗体最佳反应质量浓度,配制不同质量浓度甲霜灵标准品,用直接竞争ELISA测定单抗对其抑制率。绘制抗体竞争抑制曲线,进行相关回归分析,计算单抗的IC50值。
1.2.2 胶体金试纸条的制备采用改进的柠檬酸钠还原法制备胶体金颗粒[24],参考龚云飞等[25]的方法标记甲霜灵单克隆抗体并完成试纸条的制备及组装。
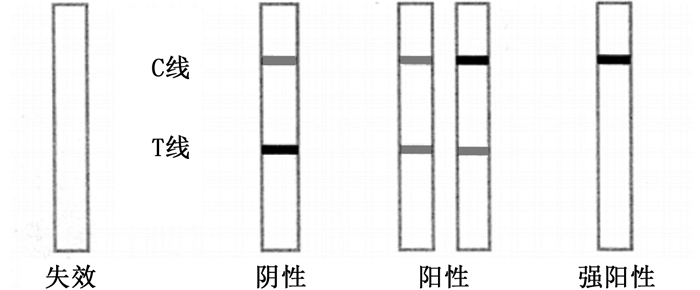
1.2.3 胶体金试纸条性质测定基于间接竞争ELISA理论,用水(含质量分数10%乙腈)配置甲霜灵标准液,使其质量浓度为50、10、5、1和0.1 mg/mL。分别取200 μL与微孔板上冻干的标记抗体反应1 min后,插入试纸条进行检测,室温下反应3~5 min,根据结果判断检测限。结果判断参考LIU等[26],如图 1所示:质控线(C)无条带时,试纸条失效或反应不完全;C线条带颜色深,检测线(T)无颜色时为强阳性结果;C线条带颜色比T浅时,为阴性结果;C线、T线条带颜色相同或者是C线颜色深于T线,则为阳性结果。
|
图 1 结果判读示意图 Fig. 1 Schematic diagram of the result interpretation |
分别配制10 mg/mL的恩诺沙星、磺胺甲恶唑、氟苯尼考、呋喃唑酮、吡喹酮、强力霉素、孔雀石绿和亚甲基蓝,用甲霜灵胶体金免疫层析试纸进行测定。
1.2.4 甲霜灵胶体金免疫层析试纸条在水产品检测中的应用准确称取搅碎的水产品肉糜5.00 g加入适量甲霜灵标准品溶液,使其添加剂量为10、6、2、1、0.2、0 mg/kg,每组样品设3个平行。分别加入15 mL磷酸缓冲液,高速匀浆5 min,转入离心管中以4 500 r/min离心15 min,过C18固相萃取小柱,洗脱液35 ℃氮气吹干,用1 mL V(乙腈):V(磷酸)=9:11缓冲液进行复溶,取200 μL用胶体金免疫层析试纸进行测定。
1.2.5 甲霜灵胶体金免疫层析试纸条结果与HPLC对比试验1.2.4节所余复溶液上机检测。液相条件:反相色谱柱C18柱(4.6 mm×250 mm×5 μm)或相当性能;流动相:V(乙腈):V(磷酸)=9:11;流速:1.0 mL/min;检测波长:210 nm;柱温:30 ℃;进样量:10 μL, 停止时间:15 min。
2 结果与分析 2.1 单克隆抗体的鉴定 2.1.1 单克隆抗体亚型鉴定利用Proteintech公司试剂盒,测定单克隆抗体亚型为IgG1,Kappa型,见表 1。

|
表 1 单克隆抗体亚型鉴定 Tab.1 Identification of monoclonal antibody subtypes |
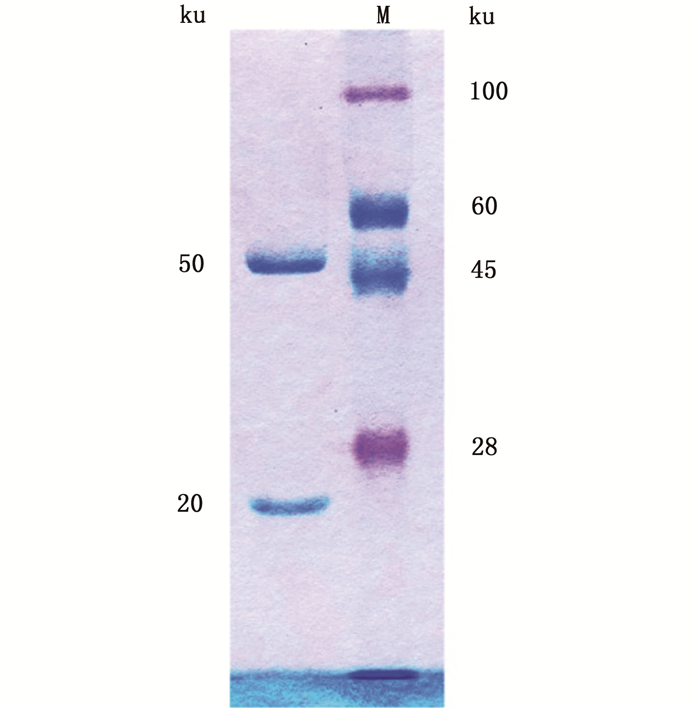
根据SDS-PAGE电泳结果(图 2),显示两条单一目的条带,重链50 ku,轻链20 ku,分子质量约为150 ku,无杂带,证明抗体纯化效果较好。
|
图 2 SDS电泳测定单克隆抗体纯度 Fig. 2 SDS electrophoresis determination of monoclonal antibody purity |
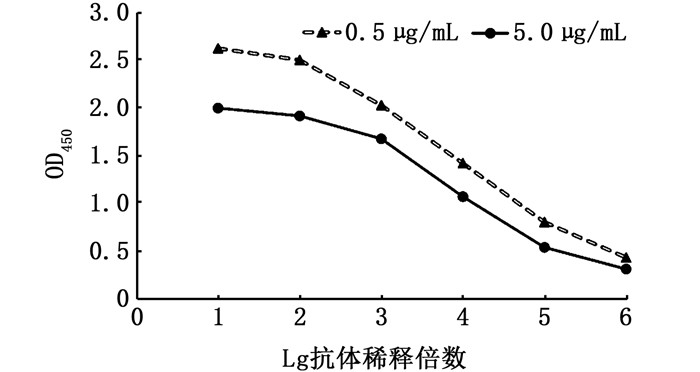
采用非竞争性酶免疫法ELISA测定单克隆抗体亲和力。将纯化的单抗按照100、1 000、10 000、100 000、1 000 000、10 000 000倍稀释成6个浓度,分别与0.5、5.0两个浓度的抗原包被的酶标板进行反应。以不同抗体浓度的对数值为横坐标,OD值为纵坐标绘制抗原抗体结合曲线,见图 3。根据公式分别计算出抗体的亲和力常数值为2.46×109 L/mol,说明甲霜灵单克隆抗体灵敏度高。
|
图 3 甲霜灵单克隆抗体亲和力常数测定 Fig. 3 Determination of the affinity constant of monoclonal antibody to metalaxyl |
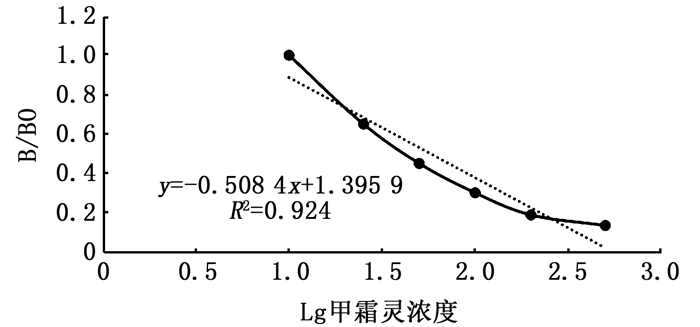
经过方阵试验的优化筛选,确定了抗原浓度为5.0 μg/mL是直接竞争ELISA测定最佳工作条件,竞争抑制曲线见图 4,曲线方程为y = -0.508 4x + 1.395 9,R2 = 0.924,IC50值为59.57 ng/mL,说明甲霜灵单克隆抗体特异性强。
|
图 4 甲霜灵抗体竞争抑制曲线 Fig. 4 Metalaxyl antibody competitive inhibition curve |
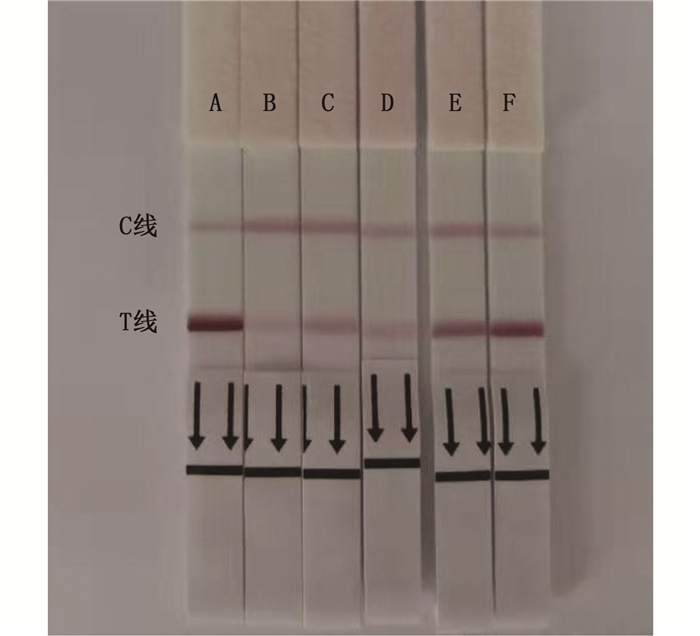
试纸条的检测结果如图 5所示,通过1.2.3节所述方法对试纸条的结果进行判定,在甲霜灵质量浓度为50 mg/mL时,试纸条上的T线条带颜色明显比C线浅,为阳性结果。随着样品质量浓度的下降,到浓度为5 mg/mL时,T线与C线条带颜色一致,1 mg/mL时T线条带颜色明显深于C线,为阴性结果,因此肉眼判定甲霜灵胶体金的最低检测限为5 mg/mL。
|
A.阴性对照; B. 50 mg/mL; C. 10 mg/mL; D. 5 mg/mL; E. 1 mg/mL; F. 0.1 mg/mL。 A. Negative control; B. 50 mg/mL; C. 10 mg/mL; D. 5 mg/mL; E. 1 mg/mL; F. 0.1 mg/mL. 图 5 胶体金试纸条检测限 Fig. 5 Colloidal gold test strip detection limit |
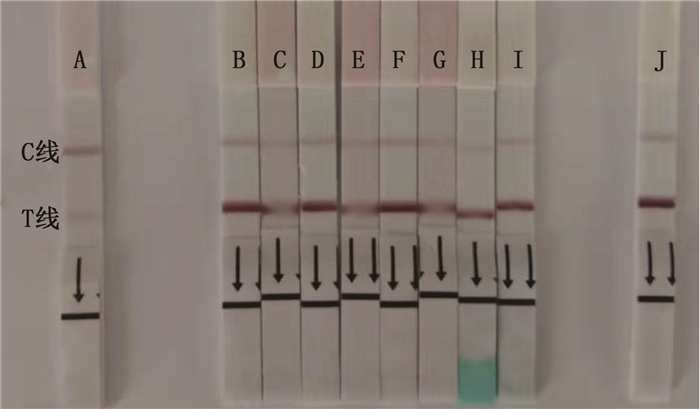
试纸条的特异性测定结果如图 6所示,甲霜灵胶体金试纸条检测恩诺沙星、磺胺甲恶唑、氟苯尼考、呋喃唑酮、吡喹酮、强力霉素、孔雀石绿和亚甲基蓝时结果均为阴性,即甲霜灵胶体金免疫层析试纸条与这些药物均不存在交叉反应,具有较好的特异性。
|
A.甲霜灵; B.恩诺沙星; C.磺胺甲恶唑; D.氟苯尼考; E.呋喃唑酮; F.吡喹酮; G.强力霉素; H.孔雀石绿; I.亚甲基蓝; J.阴性对照。 A. metalaxyl; B. enrofloxacin; C. sulfamethoxazole; D. florfenicol; E. furazolidone; F. praziquantel; G. doxycycline; H. malachite green; I. methylene blue; J. negative control. 图 6 胶体金试纸条特异性 Fig. 6 Colloidal gold test strip specificity |
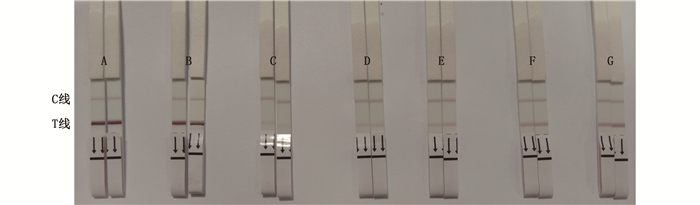
用胶体金试纸条对草鱼、凡纳滨对虾和花蛤3种水产品的添加样品进行检测,如图 7~9和表 2所示,结果表明:当花蛤样品添加量为1 mg/kg,草鱼、凡纳滨对虾样品添加量为2 mg/kg时,肉眼可见胶体金试纸条C线颜色深于T线,判定结果为阳性,即在花蛤样品中,甲霜灵胶体金试纸条的检测限为1mg/kg,在草鱼、凡纳滨对虾样品中检测限为2 mg/kg。
|
A.阴性对照; B. 0 mg/kg; C.10 mg/kg; D. 6 mg/kg; E. 2 mg/kg; F. 1 mg/kg; G. 0.2 mg/kg。 A. negative control; B. 0 mg/kg; C. 10 mg/kg; D. 6 mg/kg; E. 2 mg/kg; F. 1 mg/kg; G. 0.2 mg/kg. 图 7 草鱼肌肉样品检测限 Fig. 7 Grass carp muscle sample detection limit |

|
A.10 mg/kg; B. 6 mg/kg; C. 2 mg/kg; D. 1 mg/kg; E.0.2 mg/kg; F.0 mg/kg。 图 8 凡纳滨对虾肉样品检测限 Fig. 8 Detection limit of white shrimp samples |

|
A.10 mg/kg; B. 6 mg/kg; C.2 mg/kg; D.1 mg/kg; E. 0.2 mg/kg; F.0 mg/kg。 图 9 花蛤肉样品检测限 Fig. 9 Detection limit of calyx meat samples |
|
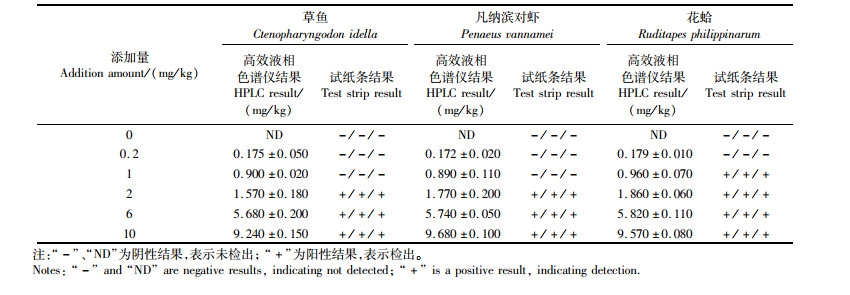
表 2 水产品样品中液相检测结果与试纸条检测结果(n=3) Tab.2 Liquid phase test results and test strip test results in aquatic product samples(n=3) |
分别用两种方法对添加不同质量浓度的水产品样品进行检测,结果如表 2,在草鱼、凡纳滨对虾、花蛤样品添加质量浓度为0 mg/kg时,HPLC与试纸条均未检出;在添加质量浓度为0.2 mg/kg时,HPLC可以检出,且平均回收率良好,均高于85%;在花蛤样品添加量不低于1 mg/kg,草鱼、凡纳滨对虾样品添加量不低于2 mg/kg时,HPLC与CGIA都能检出,且检出结果一致。
3 讨论甲霜灵广泛使用产生的污染将对动物、人类的健康造成威胁。YAO等[27]研究发现甲霜灵的对映体R-甲霜灵处理斑马鱼及其胚胎24 h的LC50分别为258.47 mg/L和237.67 mg/L,SAKR等[28]则认为低剂量的甲霜灵会影响斑马鱼(Danio rerio)胚胎的心脏正常发育。建立一种快速的、灵敏的检测方法应用于水产品检测,势在必行。近年来流行的胶体金免疫层析试纸条检测法无疑是最适选择。
3.1 甲霜灵单克隆抗体甲霜灵单克隆抗体为IgG1,Kappa型,重链50 ku,轻链2 ku,分子质量约为150 ku。抗体的亲和力直接反映抗原抗体的结合能力,亲和力常数是分析抗体性质的重要参数,同时也是抗体稳定性的重要指标[29]。亲和常数107~1012 L/mol为高亲和力,亲和常数105~106 L/mol为低亲和力[30]。本研究中甲霜灵单克隆抗体的亲和力常数为2.46×109 L/mol,属高亲和力的抗体,为建立甲霜灵残留的快速检测提供了必要的保证。IC50也是抗体性质的重要参数,IC50越小,则单克隆抗体特异性越强,表明抗体对检测抗原的特异性识别能力越强。本研究中甲霜灵单克隆抗体的IC50为59.57 ng/mL,特异性强。甲霜灵单克隆抗体灵敏度高、特异性强,可用于检测甲霜灵试纸条的制备。
3.2 甲霜灵胶体金免疫层析试纸条特异性半抗原末端的特征结构对特异性的影响最大[31],抗体的特异性越强,组装的试纸条发生交叉反应的机会越少。孔雀石绿[32]与亚甲基蓝[33]曾同样用于治疗水产养殖中的水霉病,后因安全问题被禁,而恩诺沙星、磺胺甲恶唑、氟苯尼考、呋喃唑酮、吡喹酮和强力霉素是我国水产养殖常用药物[33-39],故选择这8种药物以测定甲霜灵胶体金试纸条的特异性。甲霜灵为酰胺类药物,酰胺键是其主要特征结构;氟苯尼考为氯霉素类药物,二氯乙酰胺为其特征结构,丙二醇为主要抗菌活性结构;吡喹酮为一种吡嗪并异喹啉化合物;亚甲基蓝为一种中性pH时带阳离子电荷吩噻嗪盐;磺胺甲噁唑为磺胺类药物,磺基为其特征官能团,磺胺酰基对位上的游离氨基为抗菌活性部位;恩诺沙星为氟喹诺酮类药物,这类药物7位上的取代基团是影响抗体特异性的主要因素;呋喃唑酮为硝基呋喃类药物,硝基为其主要特征结构;强力霉素为四环素类药物,含有并四苯基本骨架,以及多个羟基、烯醇羟基及羰基;孔雀石绿则为一种三苯甲烷类化合物。由于药物结构的差异性,甲霜灵胶体金免疫层析试纸条与测定的8种药物无交叉反应,只能特异性地检测出甲霜灵残留。
3.3 甲霜灵胶体金免疫层析试纸条检测水产品肌肉组织中的残留草鱼等水产品组织成分复杂,富含蛋白质、脂肪和钾离子等[40],这些基底物质将干扰检测,降低检测灵敏度。合适的提取液是决定检测能否成功的首要因素,提取液的提取效果将直接影响检测结果。甲霜灵易溶于大多数有机溶剂、酸性溶液,如乙腈、甲醇、磷酸水、醋酸等,本研究对比乙腈与磷酸水的提取剂效果,确定磷酸水为最适提取剂。同时,利用固相萃取柱净化样品,分别采用正相萃取柱PSA和反相萃取柱C18对提取液进行净化,发现C18固相萃取柱净化效果更为明显,与江泽军等[1]检测水稻中甲霜灵残留时固相萃取柱选择结果一致。对于大多数水产品,该前处理步骤已经能够保证分析的完成。
基于合理的前处理方法,本研究建立的甲霜灵胶体金试纸条肉眼可见最低检测限为5 mg/mL;检测草鱼、凡纳滨对虾、花蛤3种水产品时,检测时间短,肉眼可见的检测限分别为2 mg/kg、2 mg/kg、1 mg/kg,与相应的HPLC检测结果对比,准确性较高。
本研究建立的方法操作简单,不需依托昂贵仪器以及专业操作人员且缩短了检测时间,适用于现场水产品样品中甲霜灵残留的快速筛查。但由于结果是通过肉眼直观判断,存在模糊判定以及个人视觉差异的情况,建议多设置重复组,并对检测结果阳性及肉眼判断有困难的样品进一步用HPLC进行复核, 以提高检测结果的准确性。
| [1] |
江泽军, 张鹏, 李永飞, 等. 分散固相萃取-高效液相色谱-串联质谱法测定水稻和土壤中的福美双与甲霜灵残留[J]. 农药学学报, 2015, 17(3): 313-320. JIANG Z J, ZHANG P, LI Y F, et al. Simultaneous determination of thiram and metalaxyl residues in rice and soil by dispersive solid phase extraction and high performance liquid chromatography-tandem mass spectrometry[J]. Chinese Journal of pesticide Science, 2015, 17(3): 313-320. DOI:10.3969/j.issn.1008-7303.2015.03.10 |
| [2] |
MALHAT F M. Persistence of metalaxyl residues on tomato fruit using high performance liquid chromatography and QuEChERS methodology[J]. Arabian Journal of Chemistry, 2017, 10(s1): S765-S768. |
| [3] |
WANG M Y, ZHANG Q, CONG L J, et al. Enantioselective degradation of metalaxyl in cucumber, cabbage, spinach and pakchoi[J]. Chemosphere, 2014, 95: 241-246. DOI:10.1016/j.chemosphere.2013.08.084 |
| [4] |
PORTER L D, HAMM P B, DAVID N L, et al. Metalaxyl-M-resistant Pythium species in potato production areas of the pacific northwest of the U.S.A.[J]. American Journal of Potato Research, 2009, 86(4): 315-326. DOI:10.1007/s12230-009-9085-z |
| [5] |
MEHTA N, SAHARAN G S, KATHPAL T S. Absorption and degradation of metalaxyl in mustard plant (Brassica juncea)[J]. Ecotoxicology and Environmental Safety, 1997, 37(2): 119-124. DOI:10.1006/eesa.1997.1533 |
| [6] |
黎其万, 刘宏程, 张玉荣, 等. 雪莲果中甲霜灵、异菌脲和除虫脲残留量的高效液相色谱测定方法[J]. 分析试验室, 2007, 26(12): 83-86. LI Q W, LIU H C, ZHANG Y R, et al. Determination of metalaxyl, iprodione and diflubenzuron residues in yacon by HPLC[J]. Chinese Journal of Analysis Laboratory, 2007, 26(12): 83-86. DOI:10.3969/j.issn.1000-0720.2007.12.021 |
| [7] |
WHITE D J, CHEN W D, SCHROEDER K L. Assessing the contribution of ethaboxam in seed treatment cocktails for the management of metalaxyl-resistant Pythium ultimum var. ultimum in Pacific Northwest spring wheat production[J]. Crop Protection, 2019, 115: 7-12. DOI:10.1016/j.cropro.2018.08.026 |
| [8] |
李浩然, 欧仁建, 邱军强, 等. 立达霉对七彩神仙鱼卵水霉病的防治效果[J]. 南方农业学报, 2015, 46(4): 697-701. LI H R, OU R J, QIU J Q, et al. Control effect of Ridomil on saprolegniasis infected Discus fish (Symphysodon aequifasciatus) zygotes[J]. Journal of Southern Agriculture, 2015, 46(4): 697-701. DOI:10.3969/j.issn.2095-1191.2015.4.697 |
| [9] |
DEMSIA G, VLASTOS D, GOUMENOU M, et al. Assessment of the genotoxicity of imidacloprid and metalaxyl in cultured human lymphocytes and rat bone-marrow[J]. Mutation Research/Genetic Toxicology and Environmental Mutagenesis, 2007, 634(1/2): 32-39. |
| [10] |
European Food Safety Authority. Review of the existing maximum residue levels (MRLs) for metalaxyl-M according to Article 12 of Regulation (EC) No 396/2005[J]. EFSA Journal, 2011, 9(12): 2494. DOI:10.2903/j.efsa.2011.2494 |
| [11] |
LIU X Y, YANG Y, CUI Y, et al. Dissipation and residue of metalaxyl and cymoxanil in pepper and soil[J]. Environmental Monitoring and Assessment, 2014, 186(8): 5307-5313. DOI:10.1007/s10661-014-3779-5 |
| [12] |
何书海, 李腾崖, 陈菲. 高效液相色谱法对环境样品中甲基托布津与甲霜灵残留的测定[J]. 分析测试学报, 2010, 29(2): 161-164, 170. HE S H, LI T Y, CHEN F. Residual determination of thiophanate-methyl and metalaxyl in environment by high performance liquid chromatography[J]. Journal of Instrumental Analysis, 2010, 29(2): 161-164, 170. DOI:10.3969/j.issn.1004-4957.2010.02.012 |
| [13] |
殷春杭, 朱国念, 钱允辉, 等. 蔬菜中甲霜灵残留量的HPLC分析[J]. 农药, 2006, 45(10): 686. YIN C H, ZHU G N, QIAN Y H, et al. HPLC determination metalaxyl residues in vegetable[J]. Agrochemicals, 2006, 45(10): 686. DOI:10.3969/j.issn.1006-0413.2006.10.013 |
| [14] |
王华, 彭小燕, 李继兰. 加速溶剂萃取结合GC-MS法测定葡萄酒中甲霜灵的残留[J]. 食品工业, 2008, 29(1): 71-74. WANG H, PENG X Y, LI J L. Determination of metalaxyl in wine by accelerate solvent extraction combination with gas chromatography/mass spectromety[J]. The Food Industry, 2008, 29(1): 71-74. |
| [15] |
徐娟, 陈捷, 林峰, 等. 液相色谱-串联质谱法测定八种食品中甲霜灵[J]. 食品科学, 2010, 31(4): 175-178. XU J, CHEN J, LIN F, et al. Liquid chromatography-tandem mass spectrometric determination of metalaxyl residue in animal-derived and plant-derived foods[J]. Food Science, 2010, 31(4): 175-178. |
| [16] |
黄超群, 谢文, 于卓然, 等. 液相色谱-串联质谱法测定果蔬中10种酰胺类农药的残留量[J]. 食品安全质量检测学报, 2015, 6(3): 886-892. HUANG C Q, XIE W, YU Z R, et al. Determination of 10 amide pesticides in fruits and vegetables by liquid chromatography-tandem mass spectrometry[J]. Journal of Food Safety & Quality, 2015, 6(3): 886-892. |
| [17] |
ADLNASAB L, EZODDIN M, SHABANIAN M, et al. Development of ferrofluid mediated CLDH@Fe3O4@Tanic acid-based supramolecular solvent:application in air-assisted dispersive micro solid phase extraction for preconcentration of diazinon and metalaxyl from various fruit juice samples[J]. Microchemical Journal, 2019, 146: 1-11. DOI:10.1016/j.microc.2018.12.020 |
| [18] |
OLIVA J, NAVARRO S, BARBA A, et al. Determination of chlorpyrifos, penconazole, fenarimol, vinclozolin and metalaxyl in grapes, must and wine by on-line microextraction and gas chromatography[J]. Journal of Chromatography A, 1999, 833(1): 43-51. DOI:10.1016/S0021-9673(98)00860-7 |
| [19] |
LE T, YAN P F, XU J, et al. A novel colloidal gold-based lateral flow immunoassay for rapid simultaneous detection of cyromazine and melamine in foods of animal origin[J]. Food Chemistry, 2013, 138(2/3): 1610-1615. |
| [20] |
BYZOVA N A, SMIRNOVA N I, ZHERDEV A V, et al. Rapid immunochromatographic assay for ofloxacin in animal original foodstuffs using native antisera labeled by colloidal gold[J]. Talanta, 2014, 119: 125-132. DOI:10.1016/j.talanta.2013.10.054 |
| [21] |
龙淼, 杨正涛, 张乃生, 等. 达氟沙星单克隆抗体的制备与鉴定[J]. 畜牧与兽医, 2008, 40(11): 73-75. LONG M, YANG Z T, ZHANG N S, et al. Preparation and identification of monoclonal antibodies to danofloxacin[J]. Animal Husbandry & Veterinary Medicine, 2008, 40(11): 73-75. |
| [22] |
郭尧君. 蛋白质电泳实验技术[M]. 北京: 科学出版社, 1999. GUO X J. Protein electrophoresis experiment technology[M]. Beijing: Science Press, 1999. |
| [23] |
胡鲲, 黄宣运, 姜有声, 等. 环丙沙星单克隆抗体的制备及其免疫学特性分析[J]. 中国免疫学杂志, 2010, 26(6): 538-543. HU K, HUANG X Y, JIANG Y S, et al. Generation of the monoclonal antibody against Ciprofloxacin and analysis for its immunological traits[J]. Chinese Journal of Immunology, 2010, 26(6): 538-543. |
| [24] |
高以明, 吴艳涛, 王寿利, 等. 检测莱克多巴胺胶体金免疫层析试验的建立[J]. 中国动物检疫, 2009, 26(12): 37-38, 42. GAO Y M, WU Y T, WANG S L, et al. Establishment of a colloidal gold immunochromatographic assay for detection of ractopamine[J]. Chinese Journal of Animal Health Inspection, 2009, 26(12): 37-38, 42. DOI:10.3969/j.issn.1005-944X.2009.12.017 |
| [25] |
龚云飞, 陈宗伦, 奚茜, 等. 三聚氰胺胶体金免疫层析试纸条的研制[J]. 生物工程学报, 2012, 28(7): 887-898. GONG Y F, CHEN Z L, XI X, et al. Colloidal gold immunochromatographic strip for rapid detection of melamine[J]. Chinese Journal of Biotechnology, 2012, 28(7): 887-898. |
| [26] |
LIU B, WA NG, L L, TONG B, et al. Development and comparison of immunochromatographic strips with three nanomaterial labels:colloidal gold, nanogold-polyaniline-nanogold microspheres (GPGs) and colloidal carbon for visual detection of salbutamol[J]. Biosensors and Bioelectronics, 2016, 85: 337-342. DOI:10.1016/j.bios.2016.05.032 |
| [27] |
YAO K, ZHU L, DUAN Z H, et al. Comparison of R-metalaxyl and rac-metalaxyl in acute, chronic, and sublethal effect on aquatic organisms:Daphnia magna, Scenedesmus quadricanda, and Danio rerio[J]. Environmental Toxicology, 2009, 24(2): 148-156. DOI:10.1002/tox.20415 |
| [28] |
SAKR S, LAMFON H, ESSAWY A. Ginger (Zingiber officinale) extract ameliorates metalaxyl fungicide induced nephrotoxicity in albino mice[J]. African Journal of Pharmacy and Pharmacology, 2011, 5(2): 104-112. |
| [29] |
万文徽. 单克隆抗体亲和常数的测定[J]. 单克隆抗体通讯, 1993, 9(2): 72-75. WAN W H. Detection of monoclonal antibody affinity constant[J]. Monoclonal Antibody Communications, 1993, 9(2): 72-75. DOI:10.3321/j.issn:1007-8738.1993.02.027 |
| [30] |
DELVES P J. Monoclonal antibodies:principles and practice[J]. Journal of the Royal Society of Medicine, 1985, 78(12): 1072. |
| [31] |
李俊锁, 邱月明, 王超. 兽药残留分析[M]. 上海: 上海科学技术出版社, 2002: 258-261. LI J S, QIU Y M, WANG C. Analysis of veterinary drug residues[M]. Shanghai: Shanghai Science and Technology Press, 2002: 258-261. |
| [32] |
冯雷, 孙文通, 李波, 等. 水产品中残留孔雀石绿和无色孔雀石绿液质联用分析方法研究[J]. 食品科学, 2009, 30(4): 193-196. FENG L, SUN W T, LI B, et al. HPLC-MS analysis of malachite green and leucomalachite green residues in aquatic products[J]. Food Science, 2009, 30(4): 193-196. DOI:10.3321/j.issn:1002-6630.2009.04.040 |
| [33] |
LYU X M, YANG X L, XIE X Y, et al. Comparative transcriptome analysis of Anguilla japonica livers following exposure to methylene blue[J]. Aquaculture Research, 2018, 49(3): 1232-1241. DOI:10.1111/are.13576 |
| [34] |
张德云, 匡维华, 郑映钦. 恩诺沙星在日本鳗鲡体内残留消除规律研究[J]. 水产科学, 2007, 26(4): 210-213. ZHANG D Y, KUANG W H, ZHENG Y Q. Studies on elimination of enrofloxacin residues and its metabolites in eel tissues[J]. Fisheries Science, 2007, 26(4): 210-213. DOI:10.3969/j.issn.1003-1111.2007.04.007 |
| [35] |
艾晓辉, 刘长征, 周运涛. 不同水温和给药方式下磺胺甲噁唑在草鱼体内的药动学研究[J]. 水生生物学报, 2005, 29(2): 210-214. AI X H, LIU C Z, ZHOU Y T. A study on pharmacokinetic of sulphamethoxazole in grass carp at different temperatures and administration regimes[J]. Acta Hydrobiologica Sinica, 2005, 29(2): 210-214. DOI:10.3321/j.issn:1000-3207.2005.02.020 |
| [36] |
林茂, 王雪虹, 姚志贤. 氟苯尼考在两种鳗鲡体内残留及消除规律的研究[J]. 集美大学学报(自然科学版), 2011, 16(2): 92-96. LIN M, WANG X H, YAO Z X. Residue and elimination of florfenicol in eels Anguilla japonica and A. anguilla[J]. Journal of Jimei University (Natural Science), 2011, 16(2): 92-96. DOI:10.3969/j.issn.1007-7405.2011.02.003 |
| [37] |
徐维海, 林黎明, 朱校斌, 等. HPLC/MS法对呋喃唑酮及其代谢物AOZ在罗非鱼体内残留研究[J]. 上海水产大学学报, 2005, 14(1): 35-39. XU W H, LIN L M, ZHU X B, et al. The research of residues of furazolidone and its metabolite in tilapias by HPLC/MS[J]. Journal of Shanghai Fisheries University, 2005, 14(1): 35-39. |
| [38] |
沈晓盛, 于慧娟, 蔡友琼, 等. 高效液相色谱法测定水产品中残留的吡喹酮[J]. 色谱, 2007, 25(6): 861-863. SHEN X S, YU H J, CAI Y Q, et al. Determination of praziquantel residue in aquatic products using high performance liquid chromatography[J]. Chinese Journal of Chromatography, 2007, 25(6): 861-863. DOI:10.3321/j.issn:1000-8713.2007.06.015 |
| [39] |
戴佳傲, 韦芬, 鲍宝龙, 等. 杀鲑气单胞菌杀藻作用的初步研究[J]. 上海海洋大学学报, 2020, 29(3): 439-446. DAI J A, WEI F, BAO B L, et al. Preliminary study on algaecide function of chitinase from Aeromonas salmonicida[J]. Journal of Shanghai Ocean University, 2020, 29(3): 439-446. |
| [40] |
罗峰. 水产品中强力霉素抗生素的快速测定[J]. 光谱实验室, 2008, 25(1): 268-271. LUO F. Rapid determination of doxycycline antibiotic in fisheries[J]. Chinese Journal of Spectroscopy Laboratory, 2008, 25(1): 268-271. DOI:10.3969/j.issn.1004-8138.2008.01.083 |
2. National Pathogen Collection Center for Aquatic Animals, Shanghai Ocean University, Shanghai 201306, China;
3. Key Laboratory of Freshwater Aquatic Genetic Resources, Ministry of Agriculture and Rural Affairs, Shanghai Ocean University, Shanghai 201306, China
 2021,
Vol. 30
2021,
Vol. 30


