2. 农业农村部水产品贮藏保鲜质量安全风险评估实验室, 上海 201306;
3. 上海水产品加工及贮藏工程技术研究中心, 上海 201306;
4. 上海海洋大学 食品热加工工程技术研究中心, 上海 201306
副溶血弧菌(Vibrio parahaemolyticus,Vp)是一种常见的嗜盐性革兰氏阴性菌,广泛分布于近海水域及海底沉积物中[1],是我国海产品中最为常见的病原菌之一[2-3]。食用被该菌污染的水产品,可引起恶心、呕吐、腹泻等肠胃炎反应,严重的可能引发败血症甚至导致死亡[4]。近年来,副溶血弧菌还被证实是对虾肝胰腺坏死综合征的主要诱因[5],严重危害对虾的质量安全,制约着对虾养殖业的可持续发展。
副溶血弧菌全基因组序列显示,该菌存在两种Ⅵ型分泌系统(type Ⅵ secretion system, T6SS):位于1号染色体上的T6SS1和位于2号染色体上的T6SS2[6]。T6SS是近年来新发现的一种蛋白转运系统,与细菌的毒力和环境适应能力密切相关[7-9]。近期研究发现T6SS可帮助霍乱弧菌在种内和种间竞争中发挥优势[10-11],并且有研究[12]表明副溶血弧菌的T6SS1与其生态位的竞争相关。然而,关于副溶血弧菌Ⅵ型分泌系统对其种内竞争的影响,研究尚属空白。
本研究针对这一空白,首先对85株副溶血弧菌的T6SS相关基因的携带情况进行了分析,并选取T6SS1+与T6SS1-的副溶血弧菌菌株进行混合培养,探究其种内竞争情况,同时运用qPCR技术分析混合培养后T6SS相关基因的表达情况,以期探究副溶血弧菌T6SS对其种内竞争的影响,为副溶血弧菌T6SS功能的进一步揭示提供科学的参考。
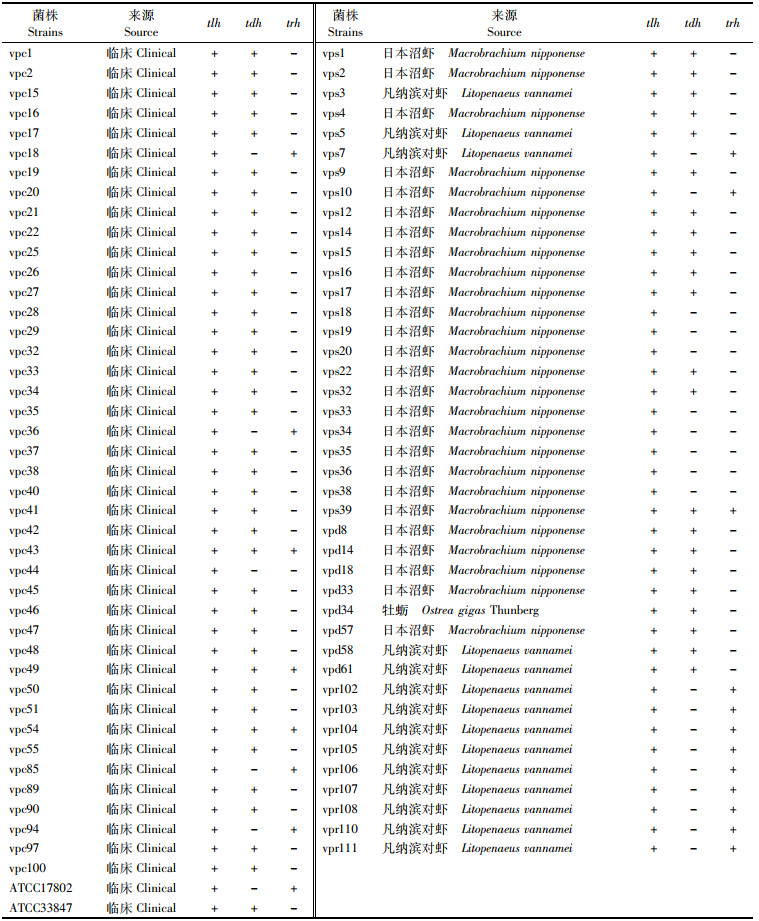
1 材料与方法 1.1 菌株来源选取本实验室分离自环境的41株菌株,其中3株(vps3、vps5、vps7)来自于中国科学院微生物研究所(Institute of Microbiology,Chinese Academy of Sciences,IMCAS),1株(vps39)来自于美国疾病预防控制中心(Centers for Disease Control and Prevention,CDC),其余37株均来自于上海市各水产市场的水产品中。其中tdh+基因型(tdh+/trh+和tdh+/trh-)菌株22株,tdh-基因型(tdh-/trh+和tdh-/trh-)菌株19株。44株临床分离株,其中42株来自于肠道门诊腹泻患者肛拭子样本,2株为标准菌株ATCC17802、ATCC33847由本实验室保存。其中tdh+基因型(tdh+/trh+和tdh+/trh-)菌株38株,tdh-基因型(tdh-/trh+和tdh-/trh-)菌株6株,所有菌株均为tlh阳性(种特异性基因)。基本信息如表 1所示。
|
表 1 85株副溶血弧菌的基本信息 Tab.1 The information of 85 V. parahaemolyticus isolates |
硫代硫酸盐-柠檬酸盐-胆盐蔗糖琼脂培养基(Thiosulfate citrate bile salts sucrose agar culture medium,TCBS)、蛋白胨大豆琼脂培养基(Tryptic soy broth, TSB)和蛋白胨购自北京陆桥科技有限公司;DNA Marker购自宝生物工程(大连)有限公司,PCR Mix、琼脂糖和细菌基因组DNA提取试剂盒均购自北京天根生化科技有限公司,动物总RNA快速提取试剂盒(Trizol-离心柱型)、反转录试剂盒和荧光定量试剂盒购于TaKaRa公司。以上试剂均在有效期内使用。
1.3 菌种活化及菌液制备将副溶血弧菌菌株从-80 ℃保存的甘油管中取出,划线接种于TCBS平板,37 ℃倒置培养12~16 h,挑取合适单菌落于10 mL TSB试管中(3% NaCl),37 ℃、200 r/min摇床培养8~10 h,连续活化2次,作为DNA提取菌液备用。
1.4 副溶血弧菌基因组DNA的提取按照细菌基因组DNA提取试剂盒说明书对85株副溶血弧菌基因组DNA进行提取,将提取的DNA储藏于-20 ℃的冰箱中备用。
1.5 PCR引物与扩增条件引物设计:tlh,tdh,trh引物序列参考文献[13]合成。其他引物参考副溶血弧菌RIMD 2210633 (GenBank登录号: BA000032)基因序列,使用Primer 5.0软件设计,委托生工生物工程(上海)股份有限公司合成。序列信息见表 2。PCR扩增条件:25 μL体系,95 ℃,4 min;94 ℃,1 min;退火30 s,退火温度见表 2;72 ℃,1 000 bp/min;30个循环;72 ℃延伸10 min。PCR产物用1.5%琼脂糖凝胶电泳进行验证,阳性对照由生工生物工程(上海)有限公司测序验证,所有实验均独立重复2次。

|
表 2 引物序列信息 Tab.2 Information of primer sequences |
由于同种菌株之间的检测需要不同的目标基因,所以选取tdh和trh基因为目标引物和探针。每组选取1个tdh菌株与1个trh菌株进行混合培养,其中:tdh+菌株为vps2、vpc16、vps16(T6SS1+)和vpd18(T6SS1-);trh+菌株为vps7(T6SS1+),vpr108、vpr111和vpc18(T6SS1-)。
菌株活化2次,离心取沉淀,用蛋白胨水(Peptone water, PW,0.85% NaCl,0.1%蛋白胨)进行稀释,将OD600值调整至0.6左右,保证接种量一致。将其分为8组,第1组:vps2(T6SS1+)和vpr108(T6SS1-);第2组:vpc16(T6SS1+)和vpr108(T6SS1-);第3组:vps7(T6SS1+)和vpd18(T6SS1-);第4组:vps7(T6SS1+)和vps16(T6SS1+);第5组:vpc16(T6SS1+)和vpc18(T6SS1-);第6组:vps2(T6SS1+)和vpr111(T6SS1-);第7组,vpd18(T6SS1-)和vpr108(T6SS1-);第8组,vps7(T6SS1+)和vpc16(T6SS1+)。按0.1%接种量将两株菌接种到同一10 mL TSB试管中,置于37 ℃摇床培养8 h后,取1 mL菌液按上述方法提取DNA,用于qPCR反应。
1.6.2 荧光定量PCR(qPCR)菌液活化2次,确定其OD600值后,用PW进行10倍梯度稀释,取合适浓度涂布于TCBS平板上,37 ℃过夜培养计数。同时取1 mL菌液进行DNA提取,-20 ℃冰箱保存备用。将平板涂布结果为109 CFU/mL的副溶血弧菌菌悬液进行10倍梯度稀释,获得终浓度为10~109 CFU/mL的菌液,分别取1 mL提取DNA后进行qPCR反应,输出相应的循环阈值(Ct值)作为标准曲线y轴。同时将菌液稀释涂布于TCBS培养基,计数结果作为x轴(log10CFU/mL),构建该反应的标准曲线,并计算曲线的斜率(slope),利用公式E=10-1/slope-1计算反应的扩增效率[14]。
选择副溶血弧菌tdh基因和trh基因作为荧光定量PCR的扩增靶基因,其中Taq Man探针分别标记为CY5和FAM作为荧光基团。本实验所使用的Taq Man探针以及相关引物根据参考文献[15]由上海英潍捷基公司合成。荧光定量PCR的反应体系为20 μL,包括10×PCR缓冲液2 μL,Mg2+缓冲液(50 μmol/μL) 1.2 μL,dNTPs Mix(10 μmol/μL)0.5 μL,正反向引物(10 μmol/μL)各0.5 μL,DNA模板1 μL,Taq酶0.2 μL,探针(10 μmol/μL)0.2 μL及ddH2O 13.9 μL。qPCR反应参数为:95 ℃预变性1 min;共40个循环,每个循环95 ℃,5 s;59 ℃,45 s。在延伸阶段收集荧光信号,反应结束后,对获得的信号数据进行处理。
1.7 T6SS相关基因表达量的检测荧光定量PCR的反应体系(20 μL):TB Green Premix Ex Taq Ⅱ 10 μL,PCR Primer-F 0.8 μL (10 μmol/μL),PCR Primer-R 0.8 μL (10 μmol/μL),ROX Reference Dye 0.4 μL, cDNA模板2 μL及ddH2O 6 μL。PCR反应参数为:95 ℃预变性30 s;40个循环中,每个循环均95 ℃ 15 s,60 ℃ 60 s。
将16S rRNA基因定为副溶血弧菌的内参基因,其上下游引物5′端到3′端分别为gacacggtccagactcctac/ggtgcttcttctgtcgctaac[16],参考副溶血弧菌RIMD 2210633 (GenBank登录号: BA000032)基因序列,使用Primer 5.0软件将T6SS相关蛋白基因作为靶基因设计引物,委托生工生物工程(上海)股份有限公司合成。引物序列及基因功能信息见表 3。

|
表 3 反转录荧光定量PCR反应引物序列信息 Tab.3 Information of qPCR primer sequences |
使用SPSS 19.0软件对数据进行单因素方差分析(ANOVA),检验水平为P < 0.05时为差异显著,具有统计学意义。
2 结果与分析 2.1 T6SS基因携带情况分析选取T6SS1结构蛋白VipA1和T6SS2结构蛋白VipA2基因,以及4个T6SS1相关基因vp13885、vp1390、vp1393、vp1415 [17]进行检测。结果发现,在85株副溶血弧菌中,有62株携带T6SS1结构基因vipA1,其中临床分离株中有41株,占全部临床分离株的93.2%,而环境分离株中有21株,占全部环境分离株的51.2%,临床分离株中的而T6SS2结构基因vipA2在所有的副溶血弧菌中广泛存在。
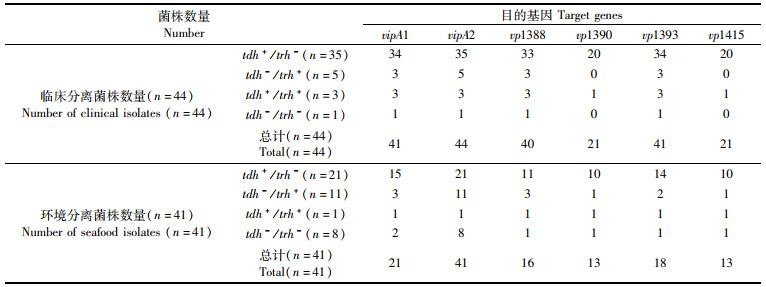
所检测的4个T6SS1相关基因vp1388、vp1390、vp1393、vp1415在85株所测副溶血弧菌中只有34株为全部阳性,其余53株中均至少缺少1个T6SS1相关基因,并且这其中环境分离株的缺失程度明显大于临床分离株,说明T6SS1基因簇在不同来源副溶血弧菌中存在一定的差异性,检测结果见表 4。
|
表 4 临床与环境分离株T6SS相关基因携带情况 Tab.4 Distribution of T6SS related genes for all 85 V. parahaemolyticus isolates from clinical and seafood sources |
以溶血素基因为依据,所检测的60株tdh+菌株(tdh+/trh+和tdh+/trh-)中,32株含有全部的T6SS基因,占53.3%;25株tdh-菌株(tdh-/trh+和tdh-/trh-)中只有2株含有全部的T6SS基因,占8.0%(2/25),tdh菌株更倾向于含有完整的T6SS基因簇。以tdh+和tdh-为分组,T6SS1相关基因携带情况有显著性差异,P < 0.05,具有统计学意义,tdh+菌株比tdh-菌株携带更多的T6SS1相关基因,未发现trh基因与T6SS1有何相关性。
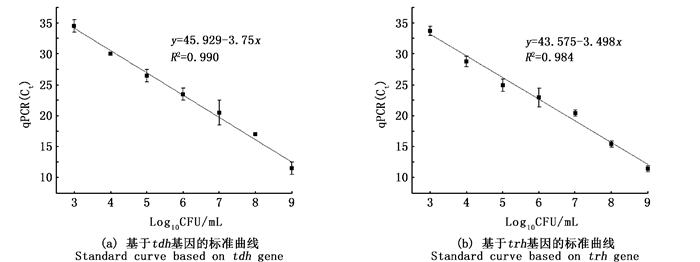
2.2 副溶血弧菌混合培养中的数量变化以已知菌数量的DNA建立标准曲线,标定Ct值与菌落数的关系。以tdh基因做标准曲线获得方程为y=45.929-3.75x,R2=0.990;以trh基因建立标准曲线方程为y=43.575-3.498x,R2=0.984;其扩增效率E在80%~120%之间,表明该方程能够较好地描述Ct值与菌落数的线性关系。见图 1。
|
图 1 副溶血弧菌qPCR定量标准曲线 Fig. 1 Standard curves of qPCR for V. parahaemolyticus |
选取8株菌株,两两混合培养8 h,测定各菌株数量,其中:vps2、vpc16、vps16为T6SS1+菌株,vpd18为T6SS1-菌株,但4株菌都携带tdh基因,且不含trh基因,因此将tdh基因作为该菌株的标志基因进行细菌数量检测;菌株vps7为T6SS1+菌株,vpr108、vpr111、vpc18为T6SS1-菌株,4株菌都携带trh基因,且不含tdh基因,因此将trh基因作为标志基因进行细菌数量检测。
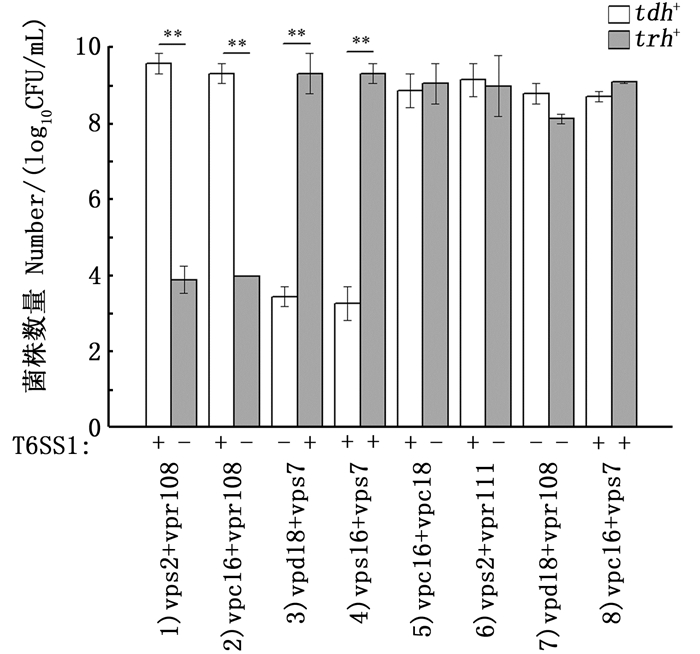
每组以相同接种量进行混合培养8 h后,用qPCR进行数量统计。由图 2可知:8组中有4组出现数量上的明显差异,携带T6SS1的菌株vps2、vpc16以及vps7在特殊组别中呈现出了明显的种内竞争力(组1、2、3、4),1、2组中vps2和vpc16为优势菌株,3、4组中vps7为优势菌株,并且优势菌株数量范围在9.31~9.58 log10 CFU/mL,劣势菌只有3.27~3.98 log10 CFU/mL,统计学分析显示两菌株之间数量差异极显著,P < 0.01。而第5、6、7、8组在混合培养时,各菌株数量并未出现类似前4组的明显差异,其菌数量范围均在8.12~9.14 log10 CFU/mL之间,差异不显著,P>0.05。这一结果表明,在混合培养条件下,大部分携带T6SS1的副溶血弧菌存在明显的种内竞争优势,但并非所有的T6SS1+菌株都对T6SS1-菌株有明显抑制作用。T6SS1+菌株对T6SS1+菌株之间也可能存在竞争作用,vps7(T6SS1+)可以抑制vps16(T6SS1+),但是vps7和vpc16(T6SS1+)混合培养后其数量差异不大。在T6SS1-菌株中并未发现具有竞争优势的菌株,当vpd18(T6SS1-)与vpr108混合培养,其数量差异不大,无显著性差异,P>0.05。
|
*表示差异显著,**表示差异极显著 *means P < 0.05, ** means P < 0.01 图 2 混合培养条件下不同副溶血弧菌的数量变化 Fig. 2 A competition assay of different V. parahaemolyticus at a 1: 1 concentration |
提取培养8 h后的副溶血弧菌RNA,以单独培养时副溶血弧菌的基因表达量为参照,通过qPCR相对定量法(ΔΔCt),观察T6SS相关基因(OmpA、VgrG、Hcp、VipB)表达变化。OmpA为T6SS的跨膜蛋白,介导分泌蛋白的跨膜转运,VgrG为T6SS1的转位蛋白,介导效应物的转移;Hcp为T6SS的转位蛋白,同时也是T6SS的结构蛋白,构成T6SS注射器结构,VipB是T6SS的结构蛋白。
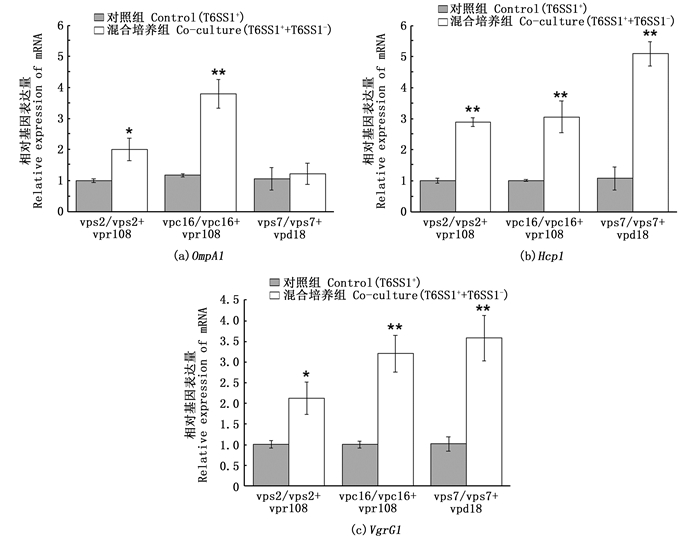
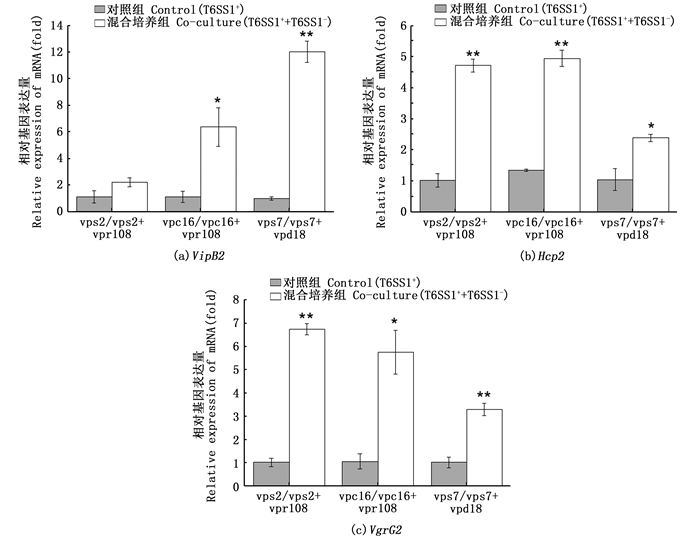
较单一培养的菌株,混合培养8 h后的副溶血弧菌T6SS1相关基因OmpA1、Hcp1、VgrG1的表达量均有明显的上调,结果如图 3所示。图 4呈现了混合培养中副溶血弧菌T6SS2相关基因VipB2、Hcp2、VgrG2的表达情况,结果显示这些基因的表达量在混合培养条件下也都明显上调。导致这一现象的原因可能是,在混合培养的条件下,副溶血弧菌可通过增强自身T6SS1和T6SS2相关基因的表达,以应对其在混合培养中的种内竞争。
|
*表示差异显著,**表示差异极显著 *means P < 0.05, ** means P < 0.01 图 3 混合培养后不同组副溶血弧菌T6SS1相关基因表达水平 Fig. 3 T6SS1 genes expression of qPCR analysis in V. parahaemolyticus |
|
*表示差异显著,**表示差异极显著 *means P < 0.05, ** means P < 0.01 图 4 混合培养后不同组副溶血弧菌T6SS2相关基因表达水平 Fig. 4 T6SS2 genes expression of qPCR analysis in V. parahaemolyticus |
对85株副溶血弧菌的基因检测发现,大约90%的临床分离株携带T6SS1基因,而在环境分离菌株中,只有约一半的菌株携带部分所检测的T6SS1基因。针对T6SS1的主要结构蛋白进行调查,发现在副溶血弧菌临床分离株中的T6SS1基因存在比例要远远高于环境分离株,而T6SS2存在于所有的副溶血弧菌中。这一结果大致与之前的报道[17]一致,比例上的差异可能跟细菌的分类不同(按血清型分类或按分离来源分类)有关,也有可能与不同地区分离的细菌背景不同有关。
T6SS是近年来新发现的与细菌致病力和适应性密切相关的分泌系统,费氏弧菌可依赖Ⅵ型分泌系统杀死非致病菌株,从而进行种内竞争[18]。在霍乱弧菌中T6SS介导抗菌作用和种内竞争[19-20],副溶血弧菌的基因组结构与霍乱弧菌的基因结构相似,因此,我们推测副溶血弧菌的T6SS在功能上可能与霍乱弧菌相似,与种内竞争相关[12, 21]。本研究通过混合接种的方式,进一步证实了该观点:部分T6SS1+的副溶血弧菌存在明显的种内竞争优势,混合接种条件下能够特异性地明显抑制其他同种菌株的生长繁殖。
在本实验条件下,有一部分T6SS1+的菌株可与T6SS1-菌株兼容共生,例如vpc16和vpc18,vps2和vpr111,并且在T6SS1+与T6SS1+菌株的混合培养组中,有1组出现了数量上的差异(vps16和vps7),1组兼容共存(vps7和vpc16)。造成这一现象的原因可能是,这些菌株的T6SS1相关基因存在不同程度的突变或缺失,导致其种内竞争力不能很好地展现。针对研究结果,提出这样的推测:(1)副溶血弧菌针对的是一种细菌成分,这种成分在某些菌株中是不存在的,或者对某些菌株种类来说不是必需的,这可能和T6SS1相关基因存在不同程度的突变或缺失有关;(2)部分菌株能抑制T6SS1活性;(3)一些菌株对T6SS1的毒性具有抵抗力,例如霍乱弧菌和费氏弧菌的T6SS可以选择性的抑制同种菌株[12, 18]。
进一步分析T6SS1相关基因的表达情况,结果显示在混合培养之后,其相关基因表达量均上调,这证实了混合培养确实激活了T6SS1的表达。并且,研究表明T6SS2在混合培养后的基因相对表达量也显著上调,这是否说明T6SS2也参与混合培养下的种内竞争?本研究初步探究了副溶血弧菌Ⅵ型分泌系统对其种内竞争的影响,表明T6SS1的存在可明显地提升副溶血弧菌在混合培养中的生长能力,是其进行种内竞争的主要工具之一。但是在自然环境中,副溶血弧菌的种内竞争现象可能不只由T6SS1单一因素介导,可能是由于多种基因共同作用的结果,其作用机理还有待进一步研究。
| [1] |
LETCHUMANAN V, CHAN K G, LEE L H. Vibrio para-haemolyticus:a review on the pathogenesis, prevalence, and advance molecular identification techniques[J]. Frontiers in Microbiology, 2014, 5: 705. DOI:10.3389/fmicb.2014.00705 |
| [2] |
TSAI S E, JONG K J, TEY Y H, et al. Molecular characterization of clinical and environmental Vibrio parahaemolyticus isolates in Taiwan[J]. International Journal of Food Microbiology, 2013, 165(1): 18-26. |
| [3] |
毛雪丹, 胡俊峰, 刘秀梅. 用文献综述法估计我国食源性副溶血性弧菌病发病率[J]. 中华疾病控制杂志, 2013, 17(3): 265-267. MAO X D, HU J F, LIU X M. Study on incidence of foodborne disease caused by Vibrio parahaemolyticus by literature review method[J]. Chinese Journal of Disease Control & Prevention, 2013, 17(3): 265-267. |
| [4] |
WANG R Z, FANG S, WU D L, et al. Screening for a single-chain variable-fragment antibody that can effectively neutralize the cytotoxicity of the Vibrio parahaemolyticus thermolabile hemolysin[J]. Applied and Environmental Microbiology, 2012, 78(14): 4967-4975. DOI:10.1128/AEM.00435-12 |
| [5] |
LI P, KINCH L N, RAY A, et al. Acute hepatopancreatic necrosis disease-causing Vibrio parahaemolyticus strains maintain an antibacterial type Ⅵ secretion system with versatile effector repertoires[J]. Applied and Environmental Microbiology, 2017, 83(13): e00737-17. DOI:10.1128/AEM.00737-17 |
| [6] |
BOYD E F, COHEN A L V, NAUGHTON L M, et al. Molecular analysis of the emergence of pandemic Vibrio parahaemolyticus[J]. BMC Microbiology, 2008, 8(1): 110. DOI:10.1186/1471-2180-8-110 |
| [7] |
HACHANI A, WOOD T E, FILLOUX A. Type Ⅵ secretion and anti-host effectors[J]. Current Opinion in Microbiology, 2016, 29: 81-93. DOI:10.1016/j.mib.2015.11.006 |
| [8] |
RINGEL P D, HU D, BASLER M. The role of type Ⅵ secretion system effectors in target cell lysis and subsequent horizontal gene transfer[J]. Cell Reports, 2017, 21(13): 3927-3940. DOI:10.1016/j.celrep.2017.12.020 |
| [9] |
WANG J F, ZHOU Z H, HE F, et al. The role of the type Ⅵ secretion system vgrG gene in the virulence and antimicrobial resistance of Acinetobacter baumannii ATCC 19606[J]. PLoS One, 2018, 13(2): e0192288. DOI:10.1371/journal.pone.0192288 |
| [10] |
UNTERWEGER D, KITAOKA M, MIYATA S T, et al. Constitutive type Ⅵ secretion system expression gives Vibrio cholerae intra- and interspecific competitive advantages[J]. PLoS One, 2012, 7(10): e48320. DOI:10.1371/journal.pone.0048320 |
| [11] |
UNTERWEGER D, MIYATA S T, BACHMANN V, et al. The Vibrio cholerae type Ⅵ secretion system employs diverse effector modules for intraspecific competition[J]. Nature Communications, 2014, 5(1): 3549. DOI:10.1038/ncomms4549 |
| [12] |
SALOMON D, GONZALEZ H, UPDEGRAFF B L, et al. Vibrio parahaemolyticus type Ⅵ secretion system 1 is activated in marine conditions to target bacteria, and is differentially regulated from system 2[J]. PLoS One, 2013, 8(4): e61086. DOI:10.1371/journal.pone.0061086 |
| [13] |
WEST C K G, KLEIN S L, LOVELL C R. High frequency of virulence factor genes tdh, trh, and tlh in Vibrio parahaemolyticus strains isolated from a pristine estuary[J]. Applied and Environmental Microbiology, 2013, 79(7): 2247-2252. DOI:10.1128/AEM.03792-12 |
| [14] |
牛犇, 穆丽丽, 张昭寰, 等. 低温条件下即食虾中单增李斯特菌与副溶血性弧菌共存分子预测模型的建立[J]. 食品科学, 2018, 39(23): 1-6. NIU B, MU L L, ZHANG Z H, et al. Development of predictive models based on qPCR for the growth of Listeria monocytogenes and Vibrio parahaemolyticus coexisting on cooked shrimps stored at low temperatures[J]. Food Science, 2018, 39(23): 1-6. DOI:10.7506/spkx1002-6630-201823001 |
| [15] |
NIU B, MU L L, XIAO L L, et al. Reduction of infection risk mediated by co-culturing Vibrio parahaemolyticus and Listeria monocytogenes in refrigerated cooked shrimp[J]. Journal of the Science of Food and Agriculture, 2018, 98(12): 4454-4461. DOI:10.1002/jsfa.8969 |
| [16] |
WANG L, LING Y, JIANG H W, et al. AphA is required for biofilm formation, motility, and virulence in pandemic Vibrio parahaemolyticus[J]. International Journal of Food Microbiology, 2013, 160(3): 245-251. DOI:10.1016/j.ijfoodmicro.2012.11.004 |
| [17] |
柴旭锋, 齐家伟, 赵莉, 等. 副溶血弧菌在鱼鳞表面形成生物被膜的动态过程及酸性电解水对其清除效果[J]. 上海海洋大学学报, 2019, 28(5): 792-800. CHAI X F, QI J W, ZHAO L, et al. Eradication effect of acidic electrolyzed water on Vibrio parahemolyticus biofilm formed on fish scale surface[J]. Journal of Shanghai Ocean University, 2019, 28(5): 792-800. |
| [18] |
SPEARE L, CECERE A G, GUCKES K R, et al. Bacterial symbionts use a type Ⅵ secretion system to eliminate competitors in their natural host[J]. Proceedings of the National Academy of Sciences of the United States of America, 2018, 115(36): E8528-E8537. DOI:10.1073/pnas.1808302115 |
| [19] |
SALOMON D, KINCH L N, TRUDGIAN D C, et al. Marker for type Ⅵ secretion system effectors[J]. Proceedings of the National Academy of Sciences of the United States of America, 2014, 111(25): 9271-9276. DOI:10.1073/pnas.1406110111 |
| [20] |
RAY A, SCHWARTZ N, DE SOUZA SANTOS M, et al. Type Ⅵ secretion system MIX-effectors carry both antibacterial and anti-eukaryotic activities[J]. EMBO Reports, 2017, 18(11): 1978-1990. DOI:10.15252/embr.201744226 |
| [21] |
JIANG N, TANG L, XIE R Q, et al. Vibrio parahaemolyticus RhsP represents a widespread group of pro-effectors for type Ⅵ secretion systems[J]. Nature Communications, 2018, 9(1): 3899. DOI:10.1038/s41467-018-06201-5 |
2. Laboratory of Quality and Safety Risk Assessment for Aquatic Product on Storage and Preservation, Ministry of Agriculture and Rural Affairs, Shanghai 201306, China;
3. Shanghai Engineering Research Center of Aquatic Product Processing & Preservation, Shanghai 201306, China;
4. Engineering Research Center of Food Thermal-Processing Technology, Shanghai Ocean University, Shanghai 201306, China
 2020,
Vol. 29
2020,
Vol. 29


