宽体金线蛭(Whitmania pigra Whitman),俗称蚂蟥,是水蛭药材的主流品种,中医认为其干制品入药具有破血、通经、逐瘀的功效[1],临床上广泛用于人类心脑血管疾病的治疗[2],具有很高的药用价值。近年来,市场对宽体金线蛭的需求不断增大,其在药材市场价格持续走高。然而,由于环境污染、水质恶化、农药化肥滥用等因素,宽体金线蛭生存环境不断遭受破坏,加之人工捕获过度,宽体金线蛭野生资源正日益衰减。为满足市场需要,各地广泛开展宽体金线蛭养殖业。目前,对于宽体金线蛭的研究主要集中于分类鉴定、抗凝血活性物质的分离、药用机理和人工繁育等方面[3-6],关于宽体金线蛭系统发育及遗传分化的研究虽有报道[7-10],但有关宽体金线蛭种质资源状况方面的研究尚未得到充分开展,仅见姜爱兰等[11]选用RAPD标记研究了黑龙江宾县、湖北大悟县及江苏兴化等5个宽体金线蛭群体的遗传多样性及种质资源现状。江苏省是我国宽体金线蛭养殖大省,苏州、泰州、扬州作为江苏省宽体金线蛭养殖中野生青年苗的主要来源地,研究其种质资源现状意义重大,但尚未见到关于该地理区域宽体金线蛭野生群体种质资源方面的研究报道。
线粒体DNA(mitochondrial DNA, mtDNA)具有结构简单、母性遗传、进化速度快且不发生重组等特点,作为一种良好的分子标记,已被广泛用于群体遗传学和系统发育关系研究[12-14]。其中,细胞色素b (Cytochrome b,Cytb)基因进化速度适中,易于扩增和测序,且作为蛋白编码基因其结构和功能已被探明,是研究动物遗传变异的良好标记,因此在动物种群遗传、系统发育等研究中得到广泛应用[15-18]。
利用线粒体Cytb基因序列作为分子标记,对江苏省苏州张家港、泰州海陵、扬州高邮3个野生宽体金线蛭地理群体的遗传多样性进行研究,以期对该区域宽体金线蛭种质资源现状进行评估,从而为宽体金线蛭资源的保护利用及种质改良提供基础资料及科学依据。
1 材料与方法 1.1 实验材料2017年8―11月于苏州张家港、泰州海陵、扬州高邮3个地区分别采集宽体金线蛭野生样本26尾、26尾、25尾,平均体质量10 g以上,样本采集后用95%乙醇固定,4 ℃保存备用。
1.2 实验方法 1.2.1 基因组DNA的提取每个宽体金线蛭样本取肌肉组织约30 mg,采用北京艾德莱生物公司海洋动物基因组DNA快速提取试剂盒提取基因组DNA,用1%琼脂糖凝胶电泳进行检测,-20 ℃保存备用。
1.2.2 目的片段的PCR扩增和测序根据GenBank报道的宽体金线蛭线粒体全序列(序列号:EU304459.1)中的Cytb基因设计引物对宽体金线蛭线粒体Cytb基因全序列进行扩增,引物序列F:5'-CATTGTTGTGAAGTTAGT-3',R:5'-TTGAAGGGTTATAGTTTA-3'。PCR扩增体系25 μL(Mix:12.5 μL,F:0.5 μL,R:0.5 μL,ddH2O:9.5 μL;DNA模板:2 μL)。PCR扩增程序:94 ℃预变性3 min;30个循环(94 ℃变性35 s、41 ℃退火30 s、72 ℃延伸95 s),最后72 ℃延伸10 min。扩增产物用1.5%琼脂糖凝胶电泳进行检测后送往生工生物工程(上海)股份有限公司进行测序。
1.3 数据分析所得序列用BioEdit[19]软件进行序列编辑、比对,并进行人工校正。采用DnaSP 5.0[20]软件计算变异位点数、简约信息位点数、单倍型数。用Arlequin 3.11[21]软件计算序列碱基组成、平均核苷酸差异数、单倍型多样性和核苷酸多样性,采用分子方差分析(AMOVA)进行群体的遗传分化分析,计算Tajima’s D[22]值和Fu’s Fs[23]值,用于中性检验,并进行核苷酸不配对分布检测,进行种群动态分析。用Mega 5[24]软件基于Kimura 2-Parameter模型计算两两群体间的遗传距离,选用以邻接法(Neighbor-Joining)构建宽体金线蛭单倍型系统发育树。
2 结果与分析 2.1 宽体金线蛭Cytb基因序列组成分析共获得77个宽体金线蛭线粒体Cytb基因全序列,Cytb基因全长为1 146 bp,无碱基的插入和缺失。样本的A、G、T、C的平均含量分别为27.57%、15.77%、43.49%、13.17%。其中,A+T含量(71.06%)远高于G+C含量(28.94%),Cytb基因的碱基组成具有较大的偏倚性,T的含量显著高于其他3种碱基的含量。
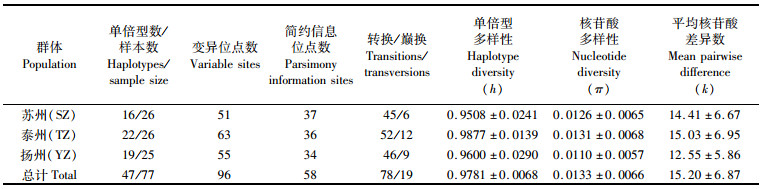
2.2 宽体金线蛭Cytb基因序列遗传多样性分析共检测到96个多态位点,其中有58个简约信息位点,78处转换,19处巅换。3个群体中变异位点最多的是泰州海陵群体(63个),而3个群体的简约信息位点数相差不大,分别为37(苏州张家港)、36(泰州海陵)、34(扬州高邮), 见表 1。在77个样本中,共获得47个单倍型,共享单倍型数1个(Hap 6),推测Hap 6可能是这3个群体宽体金线蛭的起源。泰州群体与扬州群体共享1个单倍型,泰州群体与苏州群体共享3个单倍型,苏州群体与扬州群体共享7个单倍型。泰州海陵群体拥有的单倍型数目最多(22个),苏州张家港群体最少(16个)。在47个单倍型中,有38个为单个群体独享单倍型,占比80.85%。其中,泰州海陵群体19个(Hap 17~35),扬州高邮群体12个(Hap 36~47),苏州张家港群体7个。在所有单倍型中出现频率最高的是Hap 2(7次)和Hap 9(6次),说明这两种单倍型可能是在宽体金线蛭长期进化过程中形成的较为稳定的优势基因型。
|
表 1 宽体金线蛭3个野生群体线粒体Cytb基因序列的遗传多样性参数 Tab.1 Genetic diversity parameters of mtDNA Cytb in 3 populations of W. pigra |
3个群体的总单倍型多样性、总核苷酸多样性、平均核苷酸差异数分别为0.978 1、0.013 3、15.20,其中泰州海陵群体的单倍型多样性(0.987 7)、核苷酸多样性(0.013 1)及平均核苷酸差异数(15.03)均高于其他两个群体,苏州张家港群体的单倍型多样性(0.950 8)最低,扬州高邮群体的核苷酸多样性(0.011 0)及平均核苷酸差异数(12.55)均最低。
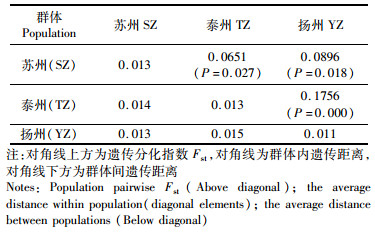
2.3 宽体金线蛭群体遗传结构分析由表 2可知,宽体金线蛭群体间遗传距离为0.013~0.015,其中,泰州海陵群体和扬州高邮群体之间的遗传距离最大(0.015),苏州张家港群体和扬州高邮群体间的遗传距离最小(0.013)。在3个地理群体中,扬州高邮群体的群内遗传距离最小(0.011),苏州张家港和泰州海陵群体的群内遗传距离均为0.013。宽体金线蛭3个群体间的遗传分化指数Fst范围为0.065 1~0.175 6,且差异显著(P < 0.05),说明宽体金线蛭3个地理群体之间均存在遗传分化。其中,泰州海陵群体与扬州高邮群体之间的遗传分化指数最高,为0.175 6,且差异极显著(P < 0.01),表明两群体间遗传分化极为显著。AMOVA分析结果显示,宽体金线蛭群体间和群体内的遗传变异分别占总变异的11.13%和88.87%,且分化指数Fst为0.111 3,差异显著(P < 0.05),说明宽体金线蛭遗传变异主要来自群体内。
|
表 2 宽体金线蛭群体内、群体间遗传距离及遗传分化Fst Tab.2 Genetic distance within and between 3 populations and population pairwise |
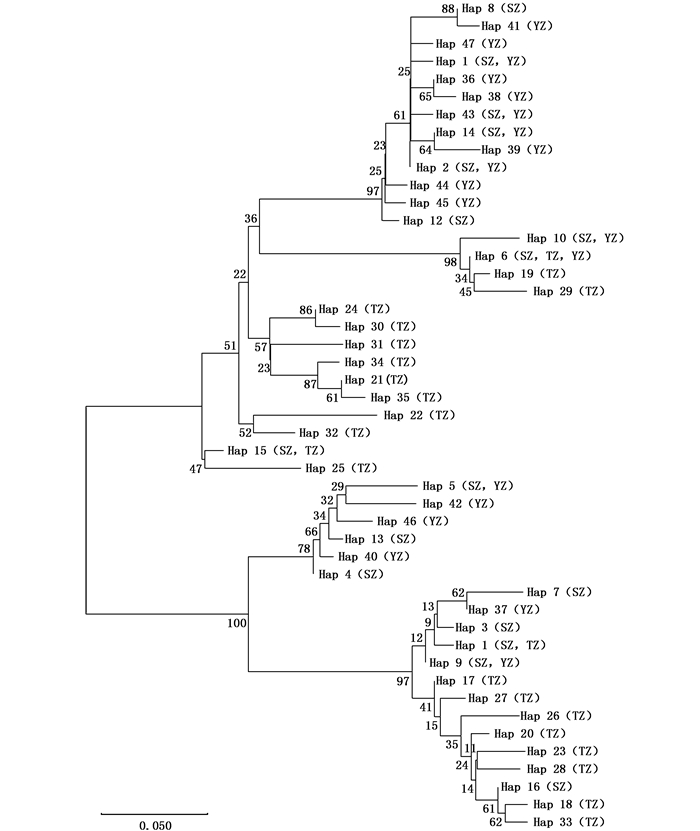
基于Kimura 2-Parameter模型以邻接法(Neighbor-Joining)构建宽体金线蛭3个群体Cytb基因单倍型系统发育树(图 1),检验次数设置为1 000次。由图 1可见,3个群体的单倍型相互混杂在一起,广泛分布于单倍型邻接关系树上,大部分节点分支支持率较低(< 50%),没有发现明显的地理分隔格局和谱系结构。
|
SZ.苏州群体;TZ.泰州群体;YZ.扬州群体 SZ.Suzhou population; TZ.Taizhou population; YZ.Yangzhou population 图 1 宽体金线蛭线粒体Cytb基因单倍型NJ系统树 Fig. 1 Neighbor-Joining tree based on mtDNA Cytb haplotypes of W.pigra |
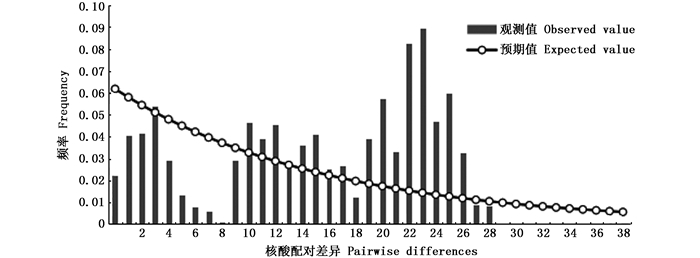
对宽体金线蛭3个野生群体进行中性检验和核苷酸不配对分布分析的结果显示,总体Tajima’s D值为-0.749 0(P>0.10),Fu’s Fs值为-13.633 7(P < 0.05)。分别对每个地理群体进行中性检验,其中,苏州张家港群体和扬州高邮群体的Tajima’s D和Fu’s Fs值均无显著差异(P>0.05)。泰州海陵群体的Fu’s Fs(-5.680 2)为显著负值(P < 0.05),Tajima’s D值为-0.344 9,但差异不显著(P>0.05)。宽体金线蛭单倍型核苷酸不配对分布出现多个峰(图 2),且观测值与期望值偏离较明显。综合分析表明,3个宽体金线蛭野生群体总体大小保持相对稳定,没有发生明显的种群扩张。
|
图 2 宽体金线蛭线粒体Cytb单倍型核苷酸不配对分布图 Fig. 2 Mismatch distribution analysis of mtDNA Cytb sequence of W.pigra |
遗传多样性是生命进化的基础,与物种繁衍、疾病抵抗以及适应生活环境息息相关,遗传多样性的降低会导致物种适应环境变化的能力下降[25],研究物种的遗传多样性对于评估物种资源现状、制定野生种群保护策略以及进行养殖种群种质的遗传改良等方面具有重要意义[26]。群体的单倍型多样性(h)及核苷酸多样性(π)是评价群体遗传多样性水平的重要指标[27-28],其值越大表示群体多态程度越高。根据GRANT等[29]关于线粒体DNA序列遗传变异的理论,单倍型多样度(h)与核苷酸多样度(π)的组合分为4种类型:高h(>0.5)与高π(>0.005);高h(>0.5)与低π(< 0.005);低h(< 0.5)与低π(< 0.005);低h(< 0.5)与高π(>0.005)。3个宽体金线蛭群体的单倍型多样性位于0.950 8~0.987 7之间,核苷酸多样性位于0.011 0~0.013 1之间,符合高h和高π的模式,表明泰州海陵、扬州高邮及苏州张家港3个不同地理群体的宽体金线蛭群体遗传变异水平均较高,对环境变化和自然选择的适应能力较强,野生宽体金线蛭资源整体处于较好的状态。其中,泰州海陵群体的单倍型多样性及核苷酸多样性在3个群体中均最高,这表明,与其他两个地理群体相比,泰州海陵群体呈现出更高的遗传多样性,苏州张家港群体和扬州高邮群体遗传多样性相对较小。熊良伟等[30]收集泰州海陵、苏州张家港、扬州高邮等地的野生宽体金线蛭进行养殖实验,发现泰州海陵地区宽体金线蛭养殖成活率及增重倍数均高于苏州张家港及扬州高邮地区,显示出更高的环境适应能力,其推测这种差异的出现可能与不同地区宽体金线蛭的遗传差异有关,在一定程度上印证了这一观点。
3.2 群体间遗传结构分析种群内的遗传漂变和种群间的基因交流决定了生物种群的遗传分化[31],而地理隔离会阻碍群体间的基因交流,是造成遗传分化的重要因素[32-33],同时不同地理区域的生境差异和自然选择作用也会对遗传结构差异造成显著影响[34-35]。宽体金线蛭群体内的遗传变异率显著高于群体间,遗传变异主要来自于群体内部,与刘飞[9]对宽体金线蛭以RAPD、ISSR、SARP为分子标记的研究结果一致。遗传分化指数Fst可作为衡量群体间遗传分化程度的指标,当遗传分化指数Fst为0~0.05时表明遗传分化程度较低,Fst为0.05~0.15表明分化程度中等,Fst为0.15~0.25代表分化程度高,大于0.25时表明分化程度极大[36]。根据此理论,宽体金线蛭3个群体间均存在一定的遗传分化,其中,苏州张家港群体与泰州海陵群体和扬州高邮群体之间均存在中等程度的遗传分化,泰州海陵群体与扬州高邮群体之间高度分化。LIU等[8]利用微卫星标记对江苏省建湖、大丰、句容、溧阳和南京等7个地区宽体金线蛭群体遗传结构进行研究,同样发现江苏省不同地区宽体金线蛭群体间遗传分化较大。姜爱兰等[11]研究表明不同地区宽体金线蛭群体间遗传距离的差异与实际地理距离具有一定的相关性。根据SLAYKIN[37]提出的观点,群体遗传分化与空间地理距离呈正向关系,即群体间地理位置越近,基因交流越频繁,遗传分化程度越小。泰州海陵群体与扬州高邮群体间的地理距离最近,但遗传分化程度却最高,推测可能是由于宽体金线蛭自身迁移能力有限,影响了群体间的基因交流,且遗传结构的变化需要一个漫长的过程[38-39]。这与底栖海洋鱼类由于移动能力较差,阻碍不同地理群体间的基因交流而易于产生遗传分化相类似[40]。因此,推测地理隔离可能宽体金线蛭不同群体间遗传分化的产生中了发挥了重要作用。3个宽体金线蛭群体间虽存在一定程度的遗传分化,但并未形成明显的地理谱系结构,说明群体间仍进行了一定的基因交流,这可能是不同地理区域的生境差异、自然选择以及人类活动等综合作用的结果。近年来,宽体金线蛭人工养殖产业迅速发展,可能也在一定程度上加强了不同地区宽体金线蛭苗种之间的基因交流。
综上,苏州张家港、泰州海陵、扬州高邮3个野生宽体金线蛭地理群体的遗传变异丰富,遗传多样性总体处于较高水平,野生种质资源处于较好的状态,说明虽然野生宽体金线蛭资源总量锐减,但可能尚未对遗传多样性造成重大影响,建议尽早制定有效的保护策略,以恢复资源量。相较于苏州、扬州群体,泰州群体显示出更高的遗传多样性水平,种质资源较好,因此,建议及时有效加强对苏州张家港和扬州高邮宽体金线蛭群体的管理和保护,促进其资源的可持续发展。
| [1] |
杨潼. 中国动物志[M]. 北京: 科学出版社, 1996: 139-145. YANG T. Fauna sinica[M]. Beijing: Science Press, 1996: 139-145. |
| [2] |
周乐, 赵文静, 常惟智. 水蛭的药理作用及临床应用研究进展[J]. 中医药信息, 2012, 29(1): 132-133. ZHOU L, ZHAO W J, CHANG W Z. Advances in pharmacological effects and clinical application of leech[J]. Information on Traditional Chinese Medicine, 2012, 29(1): 132-133. DOI:10.3969/j.issn.1002-2406.2012.01.056 |
| [3] |
刘英奎.基于数值分类学及分子系统学的宽体金线蛭和光润金线蛭分类研究[D].西安: 陕西师范大学, 2011. LIU Y K. Taxonomic research of Whitmania pigra and Whitmania laevis based on cluster analysis and molecular phylogenetic analysis[D]. Xi'an: Shaanxi Normal University, 2011. |
| [4] |
凃乾, 刘义梅, 陈科力, 等. 宽体金线蛭抗凝血有效成分分离研究[J]. 时珍国医国药, 2016, 27(5): 1086-1088. TU Q, LIU Y M, CHEN K L, et al. Study on separation of anticoagulant active components from Whitmania pigra[J]. Lishizhen Medicine and Materia Medica Research, 2016, 27(5): 1086-1088. |
| [5] |
李战福, 罗莉, 李伟龙, 等. 宽体金线蛭人工养殖技术研究进展[J]. 中国渔业质量与标准, 2018, 8(2): 36-41. LI Z F, LUO L, LI W L, et al. Research progress on artificial breeding technology of Whitmania pigra[J]. Chinese Fishery Quality and Standards, 2018, 8(2): 36-41. DOI:10.3969/j.issn.2095-1833.2018.02.005 |
| [6] |
熊良伟, 王帅兵, 王建国, 等. 宽体金线蛭繁殖性能及蛭苗生长特征研究[J]. 上海海洋大学学报, 2016, 25(3): 374-380. XIONG L W, WANG S B, WANG J G, et al. Study on reproductive ability and growth traits of the Whitmania pigra Whitman[J]. Journal of Shanghai Ocean University, 2016, 25(3): 374-380. |
| [7] |
徐云玲, 聂晶, 肖凌. 6种水蛭的COⅠ、12S rRNA和16S rRNA基因及分子进化分析[J]. 生物学杂志, 2013, 30(6): 10-13. XU Y L, NIE J, XIAO L. Molecular evolution analysis of COⅠ, 12S rRNA and 16S rRNA gene in six species of leech[J]. Journal of Biology, 2013, 30(6): 10-13. |
| [8] |
LIU F, SHI H Z, GUO Q S, et al. Isolation and characterization of microsatellite loci for the analysis of genetic diversity in Whitmania pigra[J]. Biochemical Systematics and Ecology, 2013, 51: 207-214. DOI:10.1016/j.bse.2013.08.030 |
| [9] |
刘飞.蚂蟥生长繁殖习性及其遗传多样性分子标记研究[D].南京: 南京农业大学, 2008. LIU F. Study on propagation habits of Whitmania pigra Whitman and its genetic diversity by molecular marker[D]. Nanjing: Nanjing Agricultural University, 2008. |
| [10] |
LIU F, GUO Q S, SHI H Z, et al. Genetic diversity and phylogenetic relationships among and within populations of Whitmania pigra and Hirudo nipponica based on ISSR and SRAP markers[J]. Biochemical Systematics and Ecology, 2013, 51: 215-223. DOI:10.1016/j.bse.2013.08.020 |
| [11] |
姜爱兰, 王信海, 丁辰龙, 等. 宽体金线蛭5个地理群体遗传多样性的RAPD分析及生长指标的比较研究[J]. 江西农业学报, 2018, 30(10): 7-12. JIANG A L, WANG X H, DING C L, et al. Genetic diversity of five geographical populations of Whitmania pigra revealed by RAPD analysis and their growth index comparison[J]. Acta Agriculturae Jiangxi, 2018, 30(10): 7-12. |
| [12] |
倪守胜, 杨钰, 柳淑芳, 等. 基于线粒体Cytb基因的虾夷扇贝群体遗传结构分析[J]. 中国水产科学, 2017, 24(3): 432-439. NI S S, YANG Y, LIU S F, et al. Population-genetics analysis of the Japanese scallop Patinopecten yessoensis based on mitochondrial Cytb gene[J]. Journal of Fishery Sciences of China, 2017, 24(3): 432-439. |
| [13] |
郭立, 李隽, 王忠锁, 等. 基于四个线粒体基因片段的银鱼科鱼类系统发育[J]. 水生生物学报, 2011, 35(3): 449-459. GUO L, LI J, WANG Z S, et al. Phylogenetic relationships of noodle-fishes (Osmeriformes:Salangidae) based on four mitochondrial genes[J]. Acta Hydrobiologica Sinica, 2011, 35(3): 449-459. |
| [14] |
LIU Z J, CORDES J F. DNA marker technologies and their applications in aquaculture genetics[J]. Aquaculture, 2004, 238(1/4): 1-37. |
| [15] |
肖武汉, 张亚平. 鱼类线粒体DNA的遗传与进化[J]. 水生生物学报, 2000, 24(4): 384-391. XIAO W H, ZHANG Y P. Genetics and evolution of mitochondrial DNA in fish[J]. Acta Hydrobiologica Sinica, 2000, 24(4): 384-391. DOI:10.3321/j.issn:1000-3207.2000.04.014 |
| [16] |
徐丹丹, 黄燕, 曾庆, 等. 基于mtDNACytb基因序列的我国不同水系野生鲇种群遗传多样性与种群历史分析[J]. 水产学报, 2017, 41(10): 1489-1499. XU D D, HUANG Y, ZENG Q, et al. Genetic diversity and population history among geographic populations of Silurus asotus in different water systems in China based on mtDNA Cytb gene sequences[J]. Journal of Fisheries of China, 2017, 41(10): 1489-1499. |
| [17] |
王剑平, 朱鹏飞, 王健, 等. 基于线粒体Cyt b基因序列的洞庭湖河蚬遗传多样性分析[J]. 水生态学杂志, 2018, 39(5): 89-94. WANG J P, ZHU P F, WANG J, et al. Genetic diversity analysis of Corbicula fluminea in Dongting Lake based on the Mitochondrial Cyt b gene[J]. Journal of Hydroecology, 2018, 39(5): 89-94. |
| [18] |
曾凡荣, 王军, 周孔霖, 等. 基于线粒体Cytb基因探讨我国日本囊对虾4个地理群体的遗传结构及种群分化[J]. 厦门大学学报(自然科学版), 2010, 49(5): 701-706. ZENG F R, WANG J, ZHOU K L, et al. Genetic structure and population differentiation in four wild populations of Marsupenaeus japonicus based on cytochrome b gene segment sequence of mitochondrial DNA[J]. Journal of Xiamen University (Natural Science), 2010, 49(5): 701-706. |
| [19] |
ELKINS K M. Analysis of deoxyribonucleic acid (DNA) sequence data using BioEdit[M]//ELKINS K M. Forensic DNA Biology. Waltham, MA: Academic Press, 2013: 129-132.
|
| [20] |
LIBRADO P, ROZAS J. DnaSP v5:a software for comprehensive analysis of DNA polymorphism data[J]. Bioinformatics, 2009, 25(11): 1451-1452. DOI:10.1093/bioinformatics/btp187 |
| [21] |
EXCOFFIER L, LAVAL G, SCHNEIDER S. Arlequin (version 3.0):an integrated software package for population genetics data analysis[J]. Evolutionary Bioinformatics, 2005, 1: 47-50. |
| [22] |
TAJIMA F. Statistical method for testing the neutral mutation hypothesis by DNA polymorphism[J]. Genetics, 1989, 123(3): 585-595. |
| [23] |
FU Y X. Statistical tests of neutrality of mutations against population growth, hitchhiking and background selection[J]. Genetics, 1997, 147(2): 915-925. |
| [24] |
TAMURA K, PETERSON D, PETERSON N, et al. MEGA5:molecular evolutionary genetics analysis using maximum likelihood, evolutionary distance, and maximum parsimony methods[J]. Molecular Biology and Evolution, 2011, 28(10): 2731-2739. DOI:10.1093/molbev/msr121 |
| [25] |
施立明. 遗传多样性及其保存[J]. 生物科学信息, 1990, 2(4): 159-164. SHI L M. Genetic diversity and its conservation[J]. Bioscience Communication, 1990, 2(4): 159-164. |
| [26] |
单斌斌, 宋娜, 刘淑德, 等. 基于线粒体COⅠ基因序列的金乌贼群体遗传学研究[J]. 中国海洋大学学报, 2017, 47(5): 50-56. SHAN B B, SONG N, LIU S D, et al. Genetic variation of different Sepia esculenta populations in China coastal waters based on mitochondrial COⅠ gene analysis[J]. Periodical of Ocean University of China, 2017, 47(5): 050-056. |
| [27] |
潘建飞, 史兆国, 成述儒, 等. 甘肃主要马群体遗传多样性及系统发育研究[J]. 农业生物技术学报, 2014, 22(2): 210-218. PAN J F, SHI Z G, CHENG S R, et al. The study of genetic diversity and phylogenetic evolution in indigenous horses (Equus caballus) of Gansu[J]. Journal of Agricultural Biotechnology, 2014, 22(2): 210-218. DOI:10.3969/j.issn.1674-7968.2014.02.010 |
| [28] |
谢少林, 吕子君, 周爱国, 等. 基于线粒体Cytb和COⅠ基因对珠江、海南和红河长臀鮠群体遗传结构分析[J]. 生态科学, 2016, 35(3): 65-72. XIE S L, LV Z J, ZHOU A G, et al. Population genetic structure of C. multiradiatus, C. bouderius and C. henrici on the mitochondrial Cytb and COⅠ sequence[J]. Ecological Science, 2016, 35(3): 65-72. |
| [29] |
GRANT W S, BOWEN B W. Shallow population histories in deep evolutionary lineages of marine fishes:insights from sardines and anchovies and lessons for conservation[J]. Journal of Heredity, 1998, 89(5): 415-426. DOI:10.1093/jhered/89.5.415 |
| [30] |
熊良伟, 王建国, 岳丽佳, 等. 江苏省不同地区宽体金线蛭青年苗养殖性能研究[J]. 时珍国医国药, 2019, 30(2): 456-458. XIONG L W, WANG J G, YUE L J, et al. Study on breeding performance of leech seedlings of Whitmania pigra in different areas of Jiangsu Province[J]. Lishizhen Medicine and Materia Medica Research, 2019, 30(2): 456-458. |
| [31] |
刘飞, 郭巧生, 史红专, 等. 蚂蟥和水蛭种间遗传变异和系统关系的ITS序列分析[J]. 中国中药杂志, 2011, 36(4): 414-419. LIU F, GUO Q S, SHI H Z, et al. Analysis of genetic differentiation and phylogenetic relationship between Whitmania pigra and Hirudo nipponia based on ITS sequence[J]. China Journal of Chinese Materia Medica, 2011, 36(4): 414-419. |
| [32] |
DE WOLF H, VERHAGEN R, BACKELJAU T. Large scale population structure and gene flow in the planktonic developing periwinkle, Littorina striata, in Macaronesia (Mollusca:Gastropoda)[J]. Journal of Experimental Marine Biology and Ecology, 2000, 246(1): 69-83. DOI:10.1016/S0022-0981(99)00177-X |
| [33] |
曲若竹, 侯林, 吕红丽, 等. 群体遗传结构中的基因流[J]. 遗传, 2004, 26(3): 377-382. QU R Z, HOU L, LÜ H L, et al. The gene flow of population genetic structure[J]. Hereditas (Beijing), 2004, 26(3): 377-382. DOI:10.3321/j.issn:0253-9772.2004.03.022 |
| [34] |
ANDERSON C I H, RODHOUSE P G. Life cycles, oceanography and variability:ommastrephid squid in variable oceanographic environments[J]. Fisheries Research, 2001, 54(1): 133-143. |
| [35] |
高天翔, 毕潇潇, 赵林林, 等. 基于线粒体Cytb基因全序列的松江鲈群体遗传结构分析[J]. 水生生物学报, 2013, 37(2): 199-207. GAO T X, BI X X, ZHAO L L, et al. Population genetic structure of roughskin sculpin Trachidermus fasciatus based on the mitochondrial Cytb sequence[J]. Acta Hydrobiologica Sinica, 2013, 37(2): 199-207. |
| [36] |
WRIGHT S. The genetical structure of populations[J]. Annals of Eugenics, 1949, 15(1): 323-354. DOI:10.1111/j.1469-1809.1949.tb02451.x |
| [37] |
SLATKIN M. Gene flow and the geographic structure of natural populations[J]. Science, 1987, 236(4803): 787-792. DOI:10.1126/science.3576198 |
| [38] |
杨天燕, 孟玮, 海萨, 等. 基于线粒体Cytb序列对新疆额尔齐斯河贝加尔雅罗鱼遗传结构的分析[J]. 动物学杂志, 2017, 52(2): 304-313. YANG T Y, MENG W, HAI S, et al. Population genetic structure of siberian dace (Leuciscus leuciscus baicalensis) in irtysh river China based on the Cytb gene sequences[J]. Chinese Journal of Zoology, 2017, 52(2): 304-313. |
| [39] |
刘梦侠, 王丽娟, 孔令怡, 等. 荣成湾孔鳐群体线粒体DNA cytb部分序列的遗传多样性分析[J]. 海洋科学, 2012, 36(10): 85-91. LIU M X, WANG L J, KONG L Y, et al. Genetic diversity analysis of partial sequences of mtDNA cytb in Raja porosa stock of the Rongcheng bay[J]. Marine Sciences, 2012, 36(10): 85-91. |
| [40] |
李玉龙, 刘修泽, 于旭光, 等. 基于线粒体COⅠ基因和控制区序列的辽宁沿海弯棘斜棘䲗群体遗传多样性和遗传结构分析[J]. 水生生物学报, 2017, 41(3): 581-588. LI Y L, LIU X Z, YU X G, et al. Population genetic structure and diversity analysis of Repomucenus curvicornis in the Liaoning coast based on DNA sequences of the mitochondrial COⅠ gene and control region[J]. Acta Hydrobiologica Sinica, 2017, 41(3): 581-588. |
 2020,
Vol. 29
2020,
Vol. 29


