2. 上海海洋大学 农业部淡水水产种质资源重点实验室, 上海 201306;
3. 上海海洋大学 水产动物遗传育种中心上海市协同创新中心, 上海 201306;
4. 中国地质科学院矿产资源研究所 国土资源部盐湖资源与环境重点实验室, 北京 100037
我国拥有一千多个盐湖,面积可达4.1万km2,主要分布在我国西部和东北部[1]。其中西藏高原是世界上海拔最高面积最大的盐湖区[2],西藏盐湖对于各类资源开发利用、生物多样性的保护以及全球气温变化的监控来说都至关重要。国内外学者早期对西藏矿产资源颇有研究,后期对其蕴藏的生物资源也越来越重视,一些喜盐生物体具有很大的经济价值和科学价值,比如螺旋藻属(Spirulina sp.)、杜氏藻属(Dunaliella sp.)、褶皱臂尾轮虫(Brachionus plicatilis)、卤虫(Artemia sp.)和蒙古裸腹溞(Monia mongolica)等。目前,对于西藏盐湖的浮游植物种类鉴定、群落结构组成以及盐度对群落结构的影响等方面的研究均有一定进展。
多格错仁盐湖面积488 km2,位于西藏北羌塘盆地中北部,由于多格错仁处于那曲地区的藏北无人区,自然环境恶劣,交通、生活和研究条件不便,前几年对多格错仁地质构造[3-5]、盐泉[6-7]、卤水[8]和锂、钾矿物质[9]的研究较多,但对多格错仁盐湖生物资源的研究几乎为空白。为此,本文对西藏多格错仁盐湖进行采样分析,通过对表、底层浮游植物群落结构对比、水平方向上的变化趋势,探究其空间分布的规律,为多格错仁盐湖的研究和资源开发提供生物学基础。
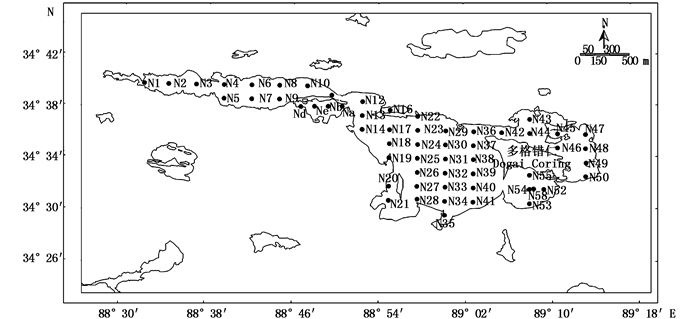
1 材料与方法 1.1 采样点设置本文研究区域为北羌塘盆地中北部的多格错仁盐湖,海拔超过4 800 m。于2009年4月27日到5月6日随中国地质科学院矿产资源研究所对西藏多格错仁盐湖进行生物调查研究,共确定58个站点,经度范围为88°31′58″~89°13′26″E,纬度范围为34°29′28″~34°39′37″N(图 1)。本次站点设置较为规律,除了个别处于湖边角的采样点外,在每个经度、每个纬度上均设置两个及以上的站点。
|
图 1 多格错仁盐湖采样站点分布图
Fig. 1 Map of sampling sites in the Dogai Coring Salt Lake
|
水深和盐度环境因子的数据分别用Hondex声纳测深仪和HQd系列便携式仪表测量得到。
采样方法参照《湖泊生态系统观测方法》[10]。采集定性样品时,用25号浮游生物网(网目64 μm)在水面下作“∞”字形来回移动,大约5~10 min,样品收集于60 mL的标本瓶,立即加入4%甲醛溶液固定。
用5 L柱状采水器采集定量样品。在表层采10 L水后放置于水桶中, 取1 L水样装在标本瓶中,加入4%甲醛溶液固定,底层也用上述方法取样,带回室内将采集回来的样品分别倒入室内沉淀器中,并加入15 mL鲁哥氏液沉淀48 h,浓缩至50 mL于血清瓶保存。
定性及定量样品用光学显微镜(Olympus CX21,10×40倍)鉴种,取0.1 mL滴入浮游植物计数框内,用盖玻片封口放置在显微镜下观察计数,单个样品重复计数两次取平均值(两次计数结果相对偏差小于±15%)[11]。
种类鉴定主要依据朱浩然[12]、魏印心[13]、齐雨藻等[14]、施之新[15]、胡鸿钧和魏印心等[16]、CANTER-LUND和LUND等[17]对藻类特征描述。
浮游植物生物量的计算方法为根据每种浮游植物的近似几何图形在显微镜成像系统下用软件(TSView 6.0)进行测量,按相应的几何公式计算浮游植物的细胞体积,换算成浮游植物生物量鲜质量(设浮游植物密度为1),对优势种随机测量30~50个细胞取平均值[18]。
1.3 数据处理与分析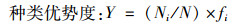 (1)
(1)
式中:Ni为第i种的个体数;N为所有种类的总个体数;fi为第i种的出现频率。Y > 0.02为优势种[19]。
Shannon-Wiener物种多样性指数:
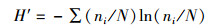 (2)
(2)
 (3)
(3)
 (4)
(4)
式中:N为样品中所有种类的总个体数; S为样品中种类总数; ni为第i种物种个体数[20-22]。
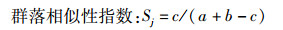 (5)
(5)
式中:a代表一个地方的物种总数;b代表另外一个地方的物种总数;c为两地区共有物种总和。当Sj值为0~0.25时,为极不相似;当Sj值为0.25~0.50时,为中等不相似;当Sj值为0.50~0.75时,为中等相似;当Sj值为0.75~1.00时,为极相似。
采用SPSS 18.0对数据进行统计及聚类分析。
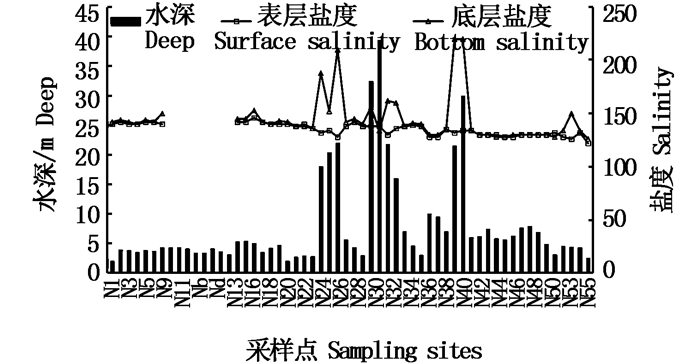
2 结果与分析 2.1 盐湖盐度和水深盐湖平均水深为7.8 m,处于湖中心的N30站点最深,为39.4 m;处于湖西部边缘的N1以及处于湖中心西边缘的N19最浅,均为2.0 m(图 2)。
|
图 2 多格错仁盐湖水深和表、底层盐度的水平分布
Fig. 2 Horizontal distribution of water depth and salinity in Dogai Coring Salt Lake
|
盐湖表层平均盐度为135,底层为145,底层略高于表层,表、底层有显著性差异(P<0.05)。表层盐度最高的站点是N14,位于湖中心西边缘,为146;底层最高的是N39和N40,位于湖中心,均为220。表层和底层盐度最低的站点均为N58,位于湖东部边缘,盐度分别为122、126。总体上看,表、底层盐度分布类似,均为湖中心盐度比湖两侧高。从图 2可以看出,底层部分站点盐度远远高于平均值,且均是深度较深的采样点。Spearman相关性分析得知,水深和底层盐度不存在统计学意义上的相关关系(R=0.189,P>0.05)。
2.2 种类组成 2.2.1 种类数多格错仁盐湖共鉴定出浮游植物231种及变种,隶属于4门72属。其中蓝藻门(Cyanophyta)17属39种,硅藻门(Bacillariophyta)32属164种,裸藻门(Euglenophyta)4属6种和绿藻门(Chlorophyta)19属27种。硅藻门种类最多,占总种类数的71.0%;其次是蓝藻门和绿藻门,分别占14.7%和11.7%;裸藻门最少,占2.6%。表层浮游植物种数为121种,底层为189种,都以硅藻门为主,占各自种类总数百分比均超过60%,蓝藻门和绿藻门次之,裸藻门最少(图 3)。表层、底层浮游植物种类的Jaccard相似性指数Sj为0.37,中等不相似。其中表、底层硅藻门种类数差异较大,底层比表层多63种。除了绿藻门种类比表层少之外,蓝藻门和裸藻门种类均比表层多,但差异均不大。

|
图 3 多格错仁盐湖表、底层浮游植物种类组成对比
Fig. 3 Comparison of species number of phytoplankton between surface and bottom water in Dogai Coring Salt Lake
|
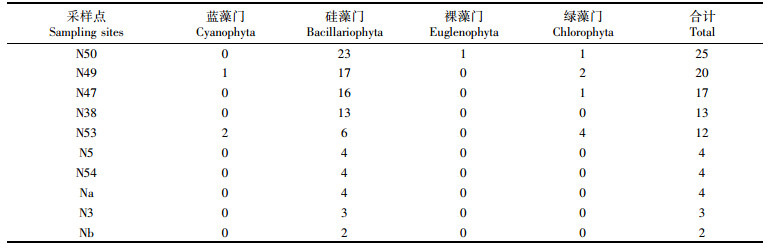
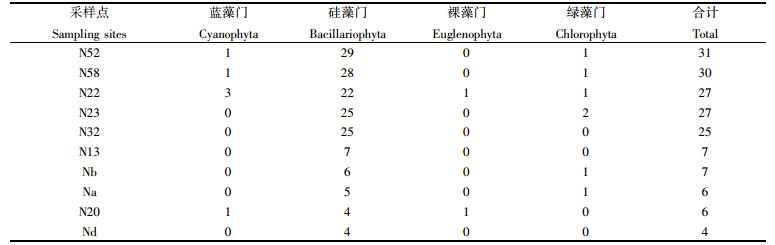
表层浮游植物种类数排前5的站点为N50、N49、N47、N38及N53,大部分位于盐湖东部,其中种类最多的是站点N50,为25种,占总种类的20.7%;种类数排倒数前5的站点为N5、N54、Na、N3及Nb,大部分位于盐湖西部,种类最少的是站点Nb,为2种,占总种类数的1.7%(表 1)。同表层分布情况相同,种类数最多的站点大多处于盐湖东部,最少的大多处于盐湖西部,且种类最多的是站点N52,为31种,占总种类的16.4%;种类最少的是站点Nd,为4种,占总数的2.1%(表 2)。可见,多格错仁盐湖表、底层水浮游植物种类的分布呈东部多,西部少的趋势。
|
表 1 多格错仁盐湖表层具有较多和较少浮游植物种类数的站点 Tab.1 The sampling stations with the most and least species number of phytoplankton for the surface water of the Lake Dogaicoring |
|
表 2 多格错仁盐湖底层具有较多和较少浮游植物种类数的站点 Tab.2 The sampling stations with the most and least species number of phytoplankton for the bottom water of the Lake Dogaicoring |
表、底层浮游植物优势种组成差异不大,均属硅藻门。菱形藻未定种(Nitzschia sp.)和舟形藻未定种(Navicula sp.)在盐湖表层占优势,优势度分别为0.35和0.25。这两种硅藻在底层4种优势种中均出现,且优势度排前两位,分别为0.25、0.17。底层优势种中其余2种为菱板藻未定种(Hantzschia sp.)和两尖菱板藻(H. amphioxys)。
表层浮游植物常见种有两尖菱板藻、菱板藻未定属、小椿藻未定种(Characium sp.)、脆杆藻属未定种(Fragilaria sp.)、桥弯藻属未定种(Cymbella sp.)、针杆藻属未定种(Synedra sp.)、两尖菱板藻线形变种(H. amphioxys var. linearis)、谷皮菱形藻(N. palea)、普通等片藻线形变种(Diatoma vulgare var.)、异极藻属未定种(Gomphonema sp.)、小球藻(Chlorella vulgaris)和双壁藻属未定种(Diploneis sp.)。底层浮游植物常见种有桥弯藻属未定种、谷皮菱形藻、脆杆藻属未定种、针杆藻属未定种、两尖菱板藻线形变种、囊裸藻属未定种(Trachelomonas sp.)、两尖菱板藻小头端变种(H. amphioxys var. capitellata)和异极藻属未定种。
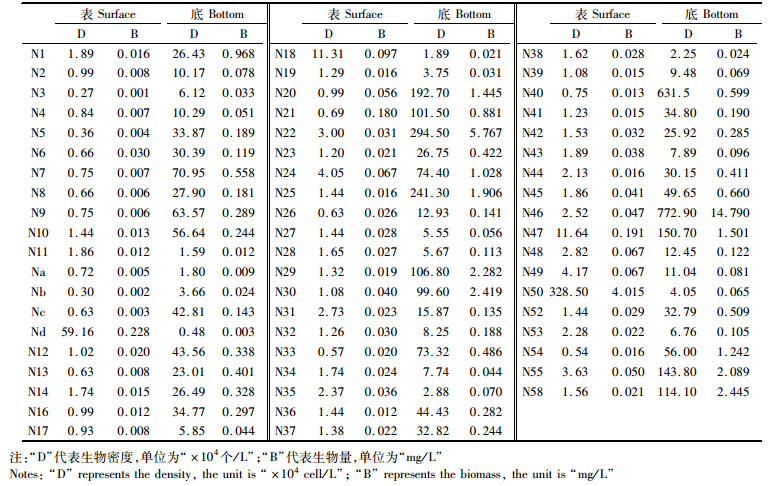
2.3 浮游植物的生物密度与生物量 2.3.1 表、底层浮游植物现存量的对比表层浮游植物平均生物密度为8.44×104个/ L,平均生物量为0.102 1 mg/L;底层平均生物密度为68.43×104个/L,生物量为0.819 8 mg/L。表、底层生物密度和生物量均有显著性差异(P<0.05)。现存量最高点与盐度最高点趋同,N50、N46均位于盐湖右边缘,它们分别为表层生物密度(328.50×104个/L)、生物量(4.014 6 mg/L)以及底层生物密度(772.93×104个/L)、生物量(14.793 1 mg/L)值最高的站点。同样,N3、Nd位于盐湖最左端,生物密度和生物量分别为0.27×104个/L、0.000 9 mg/L以及0.48×104个/L和0.002 8 mg/L,它们是值最低的站点(表 3)。
|
表 3 多格错仁盐湖表、底层浮游植物生物密度和生物量 Tab.3 Density and biomass of phytoplankton in surface and bottom water of Lake Dogaicoring |
Spearman相关性分析表明,表层生物密度(R=-0.447,P>0.05)和表层生物量(R=-0.336,P>0.05)与表层盐度无显著相关关系;底层生物密度(R=-0.017,P>0.05)和底层生物量(R=-0.043,P>0.05)与底层盐度均无显著相关关系。
2.4 多样性指数多格错仁盐湖表层水浮游植物Shannon-Wiener多样性指数(H′)均值为1.51±0.33,高于底层(1.46±0.40);表层Margalef丰富度指数(D)为0.74±0.30,低于底层(1.04±0.45);表层Pielous均匀度指数(J)为0.76±0.15,高于表层(0.57±0.15)。
从平均值看来,盐湖表层水体浮游植物种类数少于底层,但3种多样性指数皆大于底层。西藏多格错仁处于藏北无人区,没有人类活动造成的污染,且西藏以牧业为主,更没有工业污染源,一般以多样性H′、丰富度D、均匀度J为基础的水体环境质量评价标准[23-26]可能并不适合于评价多格错仁盐湖的水质。根据其3种物种多样性指数(H′均值范围为1.46~1.51、D均值范围为0.74~1.04、J均值范围为0.57~0.76)判断该湖浮游植物物种多样性不高。
2.5 聚类分析将表、底层浮游植物依据生物密度、生物量、多样性指数、均匀度指数和丰富度指数分别进行聚类分析。表层浮游植物可分为三大类(图6a),Nd、N50、N18、N47、N24、N55、N22、N49、N48、N46、N53、N45、N20、N35、N43、N31、N42、N44为一类,大部分处于盐湖东部;Nb单独为一类,剩下的自为一类。从地理分布上来看,特点显著地为以N11为结点的西部为一类,Nb为一类,以N42为结点的东部为一类。
底层浮游植物结构较表层相对单一,仅分为两大类(图6b),Nd单独为一类,剩下的自为一类。在除Nd之外的这一大类中又可以分为两类,N11、N18、N35、N38、Na分为一类,其他52个站点为一类,没有显著规律,底层各个站点之间的差异并不大。
3 讨论 3.1 浮游植物群落结构多格错仁盐湖浮游植物的优势种均属于硅藻门,硅藻门在种类总数的占比均超过79%。照湖泊藻类属性类型的划分原则:当硅藻生物量占比超过60%、生物密度占比超过20%时,为硅藻型湖泊;当硅藻生物量占比超过60%,但生物密度占比小于20%时,或者当生物量占比在50%和60%之间、生物密度占比超过20%且有除硅藻门外明显次要优势藻门类时,该湖泊被定义为硅藻过渡型湖泊;其余湖泊按照浮游植物不同门类生物量、生物密度的比例划分为蓝藻型湖泊、绿藻型湖泊等。本湖硅藻门生物密度比例大于20%,生物量比例大于60%,且基于本实验室对西藏那曲地区12个盐湖的研究[27],发现其中8个盐湖为硅藻型湖泊,占比66.67%,多格错仁盐湖也为硅藻型湖泊。

|
图 4 多格错仁盐湖表、底层浮游植物聚类分析
Fig. 4 Clustering analysis of phytoplankton in surface and bottom of the Dogai Coring Salt Lake
|
多格错仁盐湖的水深和盐度呈中心高,两边低的趋势,盐湖西部的深度略低于东部,但西部底层水的盐度均值略高于东部。从浮游植物种类数空间分布、生物密度以及生物量这3个方面来看,均出现盐湖西部少,东部多的现象,生物密度、生物量与盐度呈负相关。SUI等[28]对松嫩平原25个盐湖的研究表明,浮游植物生物密度、物种丰富度和物种多样性随盐度的增高而降低。但对多格错仁盐湖进行相关性分析可知盐度与浮游植物现存量不存在显著相关关系,且袁显春等[29]对西藏阿里地区盐湖浮游生物研究表明,浮游生物物种多样度随盐度升高而降低,在0.31~300.71 g/L的盐度范围内,并不存在相关关系。赵文等[30]发现,盐度为8~138 g/L的范围内,浮游植物的生物密度、生物量随盐度升高而减小,但负相关关系不显著。
3.2 表、底层浮游植物群落结构对比从表层至底层的垂直分布上来看,浮游植物的种类、生物密度以及生物量是逐渐递增的,而且底层浮游植物群落结构的各项指标比表层高很多。杨东方等[31]研究表明光照、水温和营养盐三个理化因子中,对浮游植物生长影响最大的是光照条件,其次是水温。对于浮游植物而言,它本身的生长繁殖仅需要少量的光照,在贫营养湖中,阳光通过清澈透明的水层可以直射底层,使整个湖的表、底层水都能进行光合作用,强大光照的水体表层反而抑制浮游植物光合作用[32-33],其次浮游植物适应水温变化是通过改变细胞分裂速率[34],单位叶绿素生产力[35-36]的方式来实现的。不同种类的浮游植物适应的水温条件也不同[37],而硅藻是一种喜冷性物种,多数比较适合在较冷的水体环境中生存[38],且对于高盐高碱的水体环境耐受性也很高[39]。另外,硅藻是一种常在河流、湖泊底部的附着藻,西藏盐湖底层的浮游植物可能包括从基质脱离出来的底栖藻类。
| [1] |
柯为. 盐湖生物资源的研发[J]. 生物工程学报, 2008, 24(2): 261. KE W. Salt Lake biological resources research and development[J]. Chinese Journal of Biotechnology, 2008, 24(2): 261. |
| [2] |
唐渊, 于升松, 刘青. 西藏盐湖水化学特征的初步研究[J]. 盐湖科技资料, 1981(s1): 22-34. TANG Y, YU S S, LIU Q. Preliminary study on water chemistry characteristics of salt lake in Tibet[J]. Journal of Salt Lake Research, 1981(s1): 22-34. |
| [3] |
牛新生, 刘喜方, 陈文西.西藏多格错仁地区钙华系统的发现及其沉积特征[C]//第一届全国青年地质大会论文集.福州: 中国地质学会, 2013: 1128-1129. NIU X S, LIU X F, CHEN W X. Discovery of travertine system and its sedimentary characteristics in Dogai Coring, Tibet[C]//National Youth Geological Congress. Fuzhou: Geological Society of China, 2013: 1128-1129. |
| [4] |
吴珍汉, 江万, NELSOND, 等. 藏北多格错仁红层及孢粉组合特征[J]. 现代地质, 2002, 16(3): 225-230. WU Z H, JIANG W, NELSON D, et al. Strata and spores association of Dogai Coring redbeds of North Tibetan Plateau[J]. Geoscience, 2002, 16(3): 225-230. DOI:10.3969/j.issn.1000-8527.2002.03.001 |
| [5] |
牛新生, 刘喜方, 陈文西. 西藏多格错仁南岸钙华地球化学特征与钾盐地质意义[J]. 沉积学报, 2013, 31(6): 1031-1040. NIU X S, LIU X F, CHEN W X. Travertine in South Bank of Dogai Coring, Tibet: geochemical characteristics and potash geological significance[J]. Acta Sedimentologica Sinica, 2013, 31(6): 1031-1040. |
| [6] |
牛新生, 陈文西, 刘喜方. 羌塘盆地多格错仁地区盐泉地球化学特征及成钾预测[J]. 现代地质, 2013, 27(3): 621-628. NIU X S, CHEN W X, LIU X F. Geochemial characteristics on salt springs and potash perspective in Dogai Coring Area of Qiangtang Basin[J]. Geoscience, 2013, 27(3): 621-628. DOI:10.3969/j.issn.1000-8527.2013.03.013 |
| [7] |
牛新生, 刘喜方, 陈文西. 西藏北羌塘盆地多格错仁地区盐泉水化学特征及其物质来源[J]. 地质学报, 2014, 88(6): 1003-1010. NIU X S, LIU X F, CHEN W X. Hydrochemical characteristic and origin for salt springs water in Dogai Coring Area of North Qiangtang Basin, Tibet[J]. Acta Geologica Sinica, 2014, 88(6): 1003-1010. |
| [8] |
乌志明, 郑绵平, 刘喜方, 等. 多格错仁盐湖卤水冷冻、日晒两步法浓缩制卤研究[J]. 无机化学学报, 2012, 28(5): 995-1000. WU Z M, ZHENG M P, LIU X F, et al. Concentration of brines from the Dogai Coring Lake, Northern Tibet, by using the two-step process: freezing and solar evaporation[J]. Chinese Journal of Inorganic Chemistry, 2012, 28(5): 995-1000. |
| [9] |
商斌.西藏多格错仁盐湖大型锂、钾矿床成矿物质来源[D].北京: 中国地质大学(北京), 2013. SHANG B. Sources of ore-forming materials of the Li and K deposits in the Dogai Coring Salt Lake, Qinghai-Tibet Plateau[D]. Beijing: China University of Geosciences (Beijing), 2013. http://cdmd.cnki.com.cn/Article/CDMD-11415-1015506056.htm |
| [10] |
黄祥飞. 湖泊生态调查观测与分析[M]. 北京: 中国标准出版社, 2000. HUANG X F. Survey, observation and analysis of lake ecology[M]. Beijing: China Standard Press, 2000. |
| [11] |
ANDERSEN R A. Freshwater algae, their microscopic world explored[J]. Phycologia, 1996, 35(4): 372-373. |
| [12] |
朱浩然. 中国淡水藻志, 第七卷, 色球藻纲[M]. 北京: 科学出版社, 1991. ZHU H R. The freshwater algae of China, Volume 7, Chroococcophyceae[M]. Beijing: Science Press, 1991. |
| [13] |
魏印心. 中国淡水藻志, 第七卷第1册, 双星藻目 中带鼓藻科 鼓藻目鼓藻科[M]. 北京: 科学出版社, 2003. WEI Y X. Flora algarum sinicarum aquae dulcis, Volume 7, Volume 1, Zygnematales Mesotaniaceae, Desmidiales Desmidiaceae[M]. Beijing: Science Press, 2003. |
| [14] |
齐雨藻, 李家英, 谢淑琦. 中国淡水藻志, 第十卷, 硅藻门, 羽纹纲[M]. 北京: 科学出版社, 2004. QI Y Z, LI J Y, XIE S Q. Flora algarum sinicarum aquae dulcis, Volume 10, Bacillariophyta, Pennatae[M]. Beijing: Science Press, 2004. |
| [15] |
施之新. 中国淡水藻志, 第十二卷, 硅藻门, 异极藻科[M]. 北京: 科学出版社, 2004. SHI Z X. Flora algarum sinicarum aquae dulcis, Volume 12, Bacillariophyta, Gomphonemaceae[M]. Beijing: Science Press, 2004. |
| [16] |
胡鸿钧, 魏印心. 中国淡水藻类——系统、分类及生态[M]. 北京: 科学出版社, 2006. HU H J, WEI Y X. The freshwater algae of China-systematics, taxonomy and ecology[M]. Beijing: Science Press, 2006. |
| [17] |
CANTER-LUND H, LUND J W G. Freshwater algae-their microscopic world explored[M]. Bristol: Biopress Ltd, 1995.
|
| [18] |
XIA Y C, KUANG Q J. Study on the phytoplankton in a large reservoir[J]. Chinese Journal of Oceanology and Limnology, 1992, 10(4): 359-370. DOI:10.1007/BF02843837 |
| [19] |
王云龙, 袁骐, 沈新强. 长江口及邻近水域春季浮游植物的生态特征[J]. 中国水产科学, 2005, 12(3): 300-306. WANG Y L, YUAN Q, SHEN X Q. Ecological character of phytoplankton in spring in the Yangtze River estuary and adjacent waters[J]. Journal of Fishery Sciences of China, 2005, 12(3): 300-306. DOI:10.3321/j.issn:1005-8737.2005.03.011 |
| [20] |
TSIRTSIS G, KARYDIS M. Evaluation of phytoplankton community indices for detecting eutrophic trends in the marine environment[J]. Environmental Monitoring and Assessment, 1998, 50(3): 255-269. DOI:10.1023/A:1005883015373 |
| [21] |
ANDERSEN R A. Diversity of eukaryotic algae[J]. Biodiversity & Conservation, 1992, 1(4): 267-292. |
| [22] |
BROADY P A. Diversity, distribution and dispersal of Antarctic terrestrial algae[J]. Biodiversity & Conservation, 1996, 5(11): 1307-1335. |
| [23] |
刘书宇, 马放, 张建祺. 景观水体富营养化模拟过程中藻类演替及多样性指数研究[J]. 环境科学学报, 2007, 27(2): 337-341. LIU S Y, MA F, ZHANG J Q. Studies on biodiversities in eutrophication process of landscaping water body in northern China[J]. Acta Scientiae Circumstantiae, 2007, 27(2): 337-341. DOI:10.3321/j.issn:0253-2468.2007.02.026 |
| [24] |
闫纪业, 冯树丹, 韩媛媛, 等. 塘-湿地生态复合处理系统的硅藻生物指数评价[J]. 沈阳师范大学学报(自然科学版), 2009, 27(1): 114-118. YAN J Y, FENG S D, HAN Y Y, et al. Diatom biology index appraisal in pond-wetland combined eco-system[J]. Journal of Shenyang Normal University (Natural Science), 2009, 27(1): 114-118. DOI:10.3969/j.issn.1673-5862.2009.01.031 |
| [25] |
张景平, 黄小平, 江志坚, 等. 珠江口海域污染的水质综合污染指数和生物多样性指数评价[J]. 热带海洋学报, 2010, 29(1): 69-76. ZHANG J P, HUANG X P, JIANG Z J, et al. Assessment of the Pearl River Estuary pollution by water comprehensive pollution index and biodiversity index[J]. Journal of Tropical Oceanography, 2010, 29(1): 69-76. DOI:10.3969/j.issn.1009-5470.2010.01.011 |
| [26] |
李仁全, 王明书, 孙敏, 等. 赤城湖指示藻类的组成及物种多样性指数分析[J]. 安徽农业科学, 2009, 37(2): 773-776, 782. LI R Q, WANG M S, SUN M, et al. Analysis of constitution features and species diversity index of indicator algae in Chicheng Lake[J]. Journal of Anhui Agricultural Sciences, 2009, 37(2): 773-776, 782. DOI:10.3969/j.issn.0517-6611.2009.02.132 |
| [27] |
陈立婧, 杨菲, 吴淑贤, 等. 西藏那曲地区盐湖浮游植物群落结构的特征[J]. 上海海洋大学学报, 2013, 22(4): 577-585. CHEN L J, YANG F, WU S X, et al. Characteristics of community structures of phytoplankton in the salt lakes in Naqu region, Tibet[J]. Journal of Shanghai Ocean University, 2013, 22(4): 577-585. |
| [28] |
SUI F Y, ZANG S Y, FAN Y W, et al. Effects of different saline-alkaline conditions on the characteristics of phytoplankton communities in the Lakes of Songnen Plain, China[J]. PLoS One, 2016, 11(10): e0164734. DOI:10.1371/journal.pone.0164734 |
| [29] |
袁显春, 郑绵平, 赵文, 等. 西藏阿里地区盐湖浮游生物生态调查[J]. 地质学报, 2007, 81(12): 1754-1763. YUAN X C, ZHENG M P, ZHAO W, et al. Plankton and ecology investigation of some saline lakes in Ali Region, Tibet[J]. Acta Geologica Sinica, 2007, 81(12): 1754-1763. DOI:10.3321/j.issn:0001-5717.2007.12.018 |
| [30] |
赵文. 中国北方内陆盐水的浮游植物[J]. 大连水产学院学报, 1992, 7(2/3): 49-64. ZHAO W. A study on the phytoplankton from inland saline waters in northern China[J]. Journal of Dalian Fisheries University, 1992, 7(2/3): 49-64. |
| [31] |
杨东方, 陈生涛, 胡均, 等. 光照、水温和营养盐对浮游植物生长重要影响大小的顺序[J]. 海洋环境科学, 2007, 26(3): 201-207. YANG D F, CHEN S T, HU J, et al. Magnitude order of the effect of light, water temperature and nutrients on phytoplankton growth[J]. Marine Environmental Science, 2007, 26(3): 201-207. DOI:10.3969/j.issn.1007-6336.2007.03.001 |
| [32] |
福迪.藻类学[M].罗迪安, 译.上海: 上海科学技术出版社, 1980. FOTT B. Algaeology[M]. LUO D A, trans. Shanghai: Shanghai Science and Technology Press, 1980. |
| [33] |
MAUCHA R. Die photosynthese des phytoplanktons vom gesichtspunkte der quantenlehre[J]. Hydrobiologia, 1948, 1(1/4): 45-62. |
| [34] |
EPPLEY R W. Temperature and phytoplankton growth in the sea[J]. Fishery Bulletin, 1972, 70(4): 1063-1085. |
| [35] |
TALLING J F. The relative growth rates of three plankton diatoms in relation to underwater radiation and temperature[J]. Annals of Botany, 1955, 19(3): 329-341. DOI:10.1093/oxfordjournals.aob.a083432 |
| [36] |
JACKSON D F. Algae, man and the environment[M]. Syracuse: Syracuse University Press, 1968.
|
| [37] |
BRAARUD T. Cultivation of marine organisms as a means of understanding environmental influences on populations[C]//SEARS M. Oceanography. Washington DC: American Association for Advancement of Science Publication, 1961: 271-298.
|
| [38] |
MORAIS P, CHÍCHARO M A, BARBOSA A. Phytoplankton dynamics in a coastal saline lake (SE-Portugal)[J]. Acta Oecologica, 2003, 24(s1): S87-S96. |
| [39] |
BLINN D W. Diatom community structure along physico-chemical gradients in Saline Lakes[J]. Ecology, 1993, 74(4): 1246-1263. DOI:10.2307/1940494 |
2. Key Laboratory ofFreshwater Aquatic Grenetic Resources, Ministry ofAgriculture, Shanghai Ocean University, Shanghai 201306, China;
3. Shanghai Collaborative Innovation for Aquatic Animal Genetics and Breeding, Shanghai Ocean University, Shanghai 201306, China;
4. Key Laboratory of Saline Lake Resources and Environments, Institute of Mineral Resources, CAGS MLR, Beijing 100037, China
 2018,
Vol. 27
2018,
Vol. 27


