2. 上海海洋大学 港航生态安全研究中心, 上海 201306
压载水系指在船舶航行过程中,控制船舶纵倾、横倾、吃水、稳定或应力而在船上加装的水及其悬浮物[1]。随着国际贸易的日益发展,全球商船队的不断扩大,船舶吨位的增大,据统计,全球船舶每年携带的压载水约有100亿吨[2]。压载舱作为船舶的特殊舱室,仅用来存放压载水,压载舱内黑暗、密闭、还可能含有有毒物质,给生存于其中的生物带来不利影响,一些生物因无法忍受压载舱的恶劣环境而死亡[3],海洋微生物的耐受能力强,因此在压载舱这种恶劣的环境下依然有大量的微生物存活。其中船舶携带的致病微生物,如衣原体、沙门氏菌、铜绿假单胞菌、立克次氏体、霉菌、霍乱弧菌、肺炎克雷伯氏菌等均在压载水中检出[4-7]。目前对于船舶压载水浮游动植物的相关研究已有很多[8-12],国内外对船舶压载水微生物的研究在逐渐受到重视,研究内容也在逐渐增多,王琪利用神经网络对船舶压载水微生物数量进行预测[13],傅志超对在船舶压载水公约要求下的压载水中的微生物进行了检测[14],冯云霄等对船舶携带压载水微生物情况进行了调查[15],李小洪对船舶压载水致病微生物入侵风险进行了分析[16]。已有文献提出处理有害的船舶压载水微生物的方法包括:从烷基化萘醌中提取有效杀菌分子[17],使用嗜盐抗生素生产者,来自海洋无脊椎动物的嗜盐菌细菌和使用移动基因组(宿主特异性噬菌体/病毒)抑制致病微生物的生长[18]等。目前很少有文献从公海交换压载水的角度对微生物多样性进行分析。本文对公海进行换水的压载水微生物与在近岸换水的压载水微生物多样性进行比较分析,研究船舶压载水微生物群落多样性,不仅可以预防微生物的入侵,保护海洋生态环境,同时还可以防控病原微生物的传播,控制海洋生物疾病和保护人类健康。
1 材料与方法 1.1 样品采集2015年春季(4月),采集4艘入境国际船舶压载水样品,编号为A1-A4(表 1)。现场使用YSI85-25便携式水质分析仪测定压载水样品的水化信息(水温、盐度、溶解氧和pH)并记录,用重氮-偶氮法、次溴酸钠氧化法、锌镉还原法和磷姆蓝分光光度法分别测定亚硝酸盐、氨氮、硝酸盐和磷酸盐。用灭菌过的蓝口玻璃瓶采集压载水样品,放置于冰盒中,在2 h内低温运送回上海海洋大学船舶压载水检测实验室。

|
表 1 船舶压载水样品信息 Tab.1 Ships ballast water sample information |
采集回实验室的样品立即进行处理:取1 L压载水,用3 μm和0.22 μm事先灭菌处理的微孔滤膜进行两级过滤,弃去3 μm微孔滤膜,0.22 μm微孔滤膜上截留的微生物即压载水样本中的微生物; 使用灭菌手术镊子,将0.22 μm滤膜转移到1.5 mL离心管中,对各个样品进行编号后,立即放入-80 ℃冰箱中冷冻4 h; 4 h后取出离心管,使用灭菌手术镊子和剪刀,将0.22 μm滤膜剪碎转移到1.5 mL灭菌离心管中; 使用3SDNA分离提取试剂盒(上海博彩生物技术有限公司)对微生物的DNA进行提取。
1.2.2 细菌16S rDNA扩增16S rDNA采用引物515F(5′-GTGCCAGC MGCCGCGG-3′)和907R(5′-CCGTCAATTCMTTT RAGTTT-3′),扩增细菌16S rRNA的V4和V5可变区序列。PCR反应体系20.0 μL:dNTP(2.5 mmol/L)2.0 μL,ddH2O 9.6 μL, Fast Pfu Polymerase 0.4 μL,5×FastPfu Buffer 4.0 μL,模板(20 ng/μL)2.00 μL,引物R(5 μmol/L)1.00 μL,引物F(5 μmol/L)1.00 μL。PCR反应程序:98 ℃预变性5 min; 98 ℃变性30 s,50 ℃退火30 s,72 ℃延伸45 s,27个循环; 72 ℃延伸5 min。PCR产物用2%琼脂糖凝胶电泳进行检测,扩增出目的条带后进行后续实验。
1.2.3 Illumina的Miseq平台测序利用Illumina公司的Miseq PE300平台进行测序得到的原始数据后对有效序列进行处理,其中优质序列84 316条,其中序列长度在401~ 420 bp的占99.11%,优质序列将用于后续生物信息分析。较高的总序列数和较高的优质序列比例表明,样本OTU可以有效表征样本中微生物种群。
2 结果 2.1 物种组成统计分析发现压载黄海远岸、南海远岸、东海远岸和香港(南海近岸)4个域海水的压载水样品细菌序列信息归类于27门、61纲、138目、249科、481属和836种。其中黄海远岸的压载水样检测到的物种数最多,达到564种;东海远岸的压载水样物种数最少,只有406种。南海远岸的压载水样检测到的物种数和南海近岸香港海域的压载水样微生物物种数差异不大,分别为433种和442种,香港海域压载水样检测到的物种比南海远岸压载水样少一个门类,为黏胶球形菌门(Lentisphaerae)。将各海域船舶压载水样品细菌群落以门为单元进行元素集合重叠分析(图 2),共有的门类有17种分别占70.83%、70.83%、89.47%和73.91%,所占比例较高,说明各海域压载水细菌群落结构总体相似。共有门类分别是变形菌门(Proteobacteria)、拟杆菌门(Bacteroidetes)、蓝细菌门(Cyanobacteria)、放线菌门(Actinobacteria)、厚壁菌门(Firmicutes),Marinimicrobia_SAR406_clade_、浮霉菌门(Planctomycetes)、疣微菌门(Verrucomicrobia)、芽单胞菌门(Gemmatimonadetes)、绿弯菌门(Chloroflexi)、PAUC34f、SBR1093、Nitrospinae、Gracilibacteria、衣原体(Chlamydiae)和硝化螺旋菌门(Nitrospirae),还有一种OTU序列在进行BLAST比对后没有得到确切的分类学信息。黄海远岸压载水样品独有门为Saccharibacteria;南海远岸压载水样品独有的物种为螺旋体门(Spirochaetes);东海远岸和香港压载水样中无独有的门类;Gracilibacteria这一门只在远岸压载水样品中出现,在香港海域压载水样品中没有检测到。
|
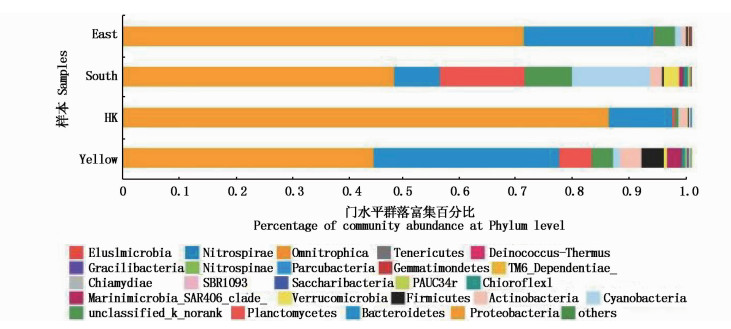
图 1 门水平上各样本物种组成
Fig. 1 Sample species composition at phylum level
|
|
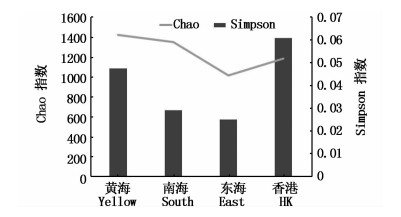
图 2 细菌群落多样性指数图
Fig. 2 Bacterial community diversity index
|
高通量测序检测到各海域压载水样品物种在门水平上的分类组成(图 1)。检测到东海远岸和香港海域压载水样品的变形菌门(Proteobacteria)比例分别为70.65%和85.52%,显著高于黄海远岸的11.21%和南海远岸的47.74%。检测到黄海远岸和东海远岸压载水样品中的拟杆菌门(Bacteroidetes)比例分别为32.64%和22.72%,显著高于南海远岸的8.00%和香港的11.21%。南海远岸压载水样品检测到的浮霉菌门(Planctomycetes 14.94%)和蓝细菌门(Cyanobacteria 13.74%)占比相对于其他海域压载水样品要高很多。其他海域占比情况分别是黄海:浮霉菌门(Planctomycetes) 5.74%和蓝细菌门(Cyanobacteria) 1.17%,东海:浮霉菌门(Planctomycetes) 0.15%和蓝细菌门(Cyanobacteria) 1.13%,香港:浮霉菌门(Planctomycetes) 0.44%和蓝细菌门(Cyanobacteria) 0.22%。
2.2 优势类群各海域压载水样中细菌优势亚群为γ-变形菌纲和α-变形菌纲,其中α-变形菌纲中有大量无法确定分类位置的序列, 包括一些优势属,表明海域存在大量未被认知的细菌类群物种。γ-变形菌纲比例大于α-变形菌纲,是目前所知的细菌中种类最多的一纲,其中假交替单胞菌属(Pseudoalteromonas)为γ-变形菌纲中绝对优势属,分布于各海域压载水样中。各海域压载水样品的优势组成相似,但各组所占比例差异较大。其中黄海远岸压载水样品优势类群为拟杆菌门中的Salinimicrobium 28.22%、γ-变形菌假交替单胞菌属5.91%和浮霉状菌属(Planctomyces) 5.26%;南海远岸压载水样品优势类群为浮霉状菌属14.89%、原绿球藻属12.82%和γ-变形菌假交替单胞菌属8.63%;东海远岸压载水样品优势类群为α变形菌淀杆菌属(Amylibacter 14.49%)、γ-变形菌假交替单胞菌属11.28%和拟杆菌门中Cryomorphaceae 10.67%;香港海域(南海近岸)压载水样品优势类群为γ变形菌假交替单胞菌属37.42%、典型海洋γ变形细菌Idiomarina 17.75%。其中南海远岸压载水样优势属浮霉状菌属占比14.89%、原绿球藻属占比12.82%,比其他海域压载水样检测出的浮霉状菌属、原绿球藻属比例要高很多,这和门水平分类结果相对应。
2.3 多样性指数图黄海远岸海域压载水样品细菌丰度最高(图 2),东海远岸海域压载水样品细菌丰度最低,物种丰度趋势为黄海>南海>香港>东海;南海近岸海域压载水样品细菌群落多样性最低,东海远岸海域压载水样品细菌群落多样性最高。物种多样性趋势为东海>南海>黄海>香港。即黄海远岸压载水细菌丰度最高,但多样性低;东海远岸压载水细菌丰度最低但物种多样性最高。
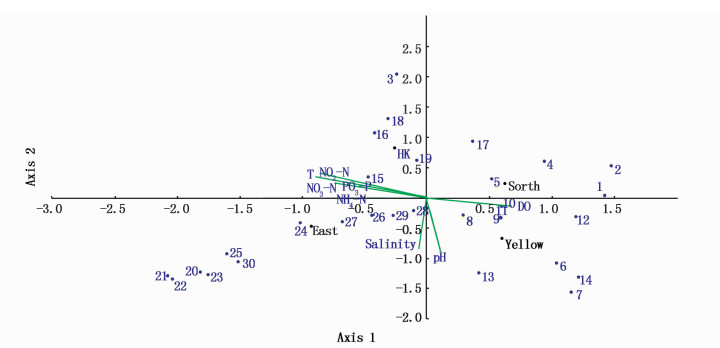
2.4 群落多样性与环境因子相关性分析结合同时期环境因子,对各海域压载水细菌群落与环境因子数据进行典范对应分析(图 3),不同数字代表不同属的物种。其中选取4个海域样点8项环境因子和相对丰度排序前30的物种进行典范对应分析。排序图中,前两个排序轴的特征值分别是0.419和0.345,结果显示各环境因子对物种的分布均有不同程度的影响,8个环境因子中溶解氧含量与第一排序轴成最大正相关0.684,温度与第一排序轴成最大负相关-0.926,营养因子与第一序轴成较强的负相关性,盐度(-0.062)和pH(0.114)与第一排序轴相关性较弱。黄海远岸压载水样点及其优势属Salinimicrobium(NO.7)同水化因子溶解氧、pH呈正相关性,温度、营养盐呈负相关性;南海远岸压载水样点及其优势属浮霉状菌属(NO.1 Planctomyces)、原绿球藻属(NO.2 Prochlorococcus)同溶解氧呈正相关性,温度、营养盐呈负相关性;东海远岸压载水样及其优势属α变形菌淀杆菌属(NO.22 Amylibacter)同温度、营养盐、盐度呈正相关性,溶解氧、pH呈负相关性;香港压载水样及其优势属γ变形细菌NO.18 Idiomarina同温度、营养盐呈正相关性,盐度、pH呈负相关性。在各海域广泛分布的假交替单胞菌属(NO.16 Pseudoalteromonas)同温度、营养盐有一定的正相关性,同盐度、pH有较强的负相关性。NO.13弧菌属同pH、盐度、溶解氧有较强的正相关性,与温度、营养盐呈负相关性; 在各海域压载水样中分布比较广泛的盐单胞菌(NO.8 Halomonas)同溶解氧、pH、盐度呈正相关性,与营养盐、温度有较强的负相关性。
|
图 3 样点-物种-环境因子典范对应分析(属水平)
Fig. 3 Samples-Species-factors canonical correspondence at genus level
1.Planctomyces; 2. Prochlorococcus; 3.Aureimarina; 4.Pseudohongiella5.Candidatus_Actinomarina; 6.Acinetobacter; 7.Salinimicrobium; 8.Halomonas; 9. Pseudomonas; 10. norank_f_Surface_2; 11.unclassified_k_norank; 12.norank_f_Rhodospirillaceae; 13.Vibrio; 14.norank_p_Marinimicrobia_SAR406_clade; 15. NS5_marine_group; 16.Pseudoalteromonas; 17.unclassified_f_Rhodobacteraceae; 18.Idiomarina; 19.Alteromonas; 20. norank_f_ZD0405; 21.Fluviicola; 22.Amylibacter; 23. SAR92_clade; 24.Sulfitobacter; 25.norank_f_Cryomorphaceae; 26.Cobetia; 27.unclassified_f_Surface_1; 28.unclassified_f_Flavobacteriaceae; 29.norank_f_Surface_1; 30. norank_f_SAR86_clade |
统计分析发现压载黄海远岸、南海远岸、东海远岸、香港(南海近岸)4个海域海水的压载水样品细菌序列信息归类于27门、61纲、138目、249科、481属和836种。不同海域的压载水样品细菌群落组成基本一致,共有门为17门,占比总门类62.96%,变形菌门占绝对优势地位,黄海海域物种丰度最高,东海物种丰度最低,这与海洋微生物群落结构的研究结果相一致[19-21]。各海域有自己独有的物种分布[22]。说明独特的压载舱环境虽然对物种有一定的选择作用,但以海水作为本底的压载水细菌群落结构同海洋细菌群落结构具有一致性[23]。
香港海域压载水样品细菌相较于公海换水的压载水样品,群落多样性和丰富度都比较低,且由于离岸较近易受人类活动影响,营养盐含量较高,细菌分布同温度、营养盐有很大的相关性。而生活在公海海域的微生物活动范围较广,离岸较远,受人类活动影响较小,水体营养元素干扰较少[24]。因此,远岸压载水细菌多样性更高,且在压载舱这种密闭、不透光的环境可以存活得更久,丰度相对也较高。
各海域压载水样中处绝对优势的假交替单胞菌属(Pseudoalteromonas)同温度、营养盐有一定的正相关性,同盐度、pH有较强的负相关性。假交替单胞菌属(Pseudoalteromonas)具有很强的生存能力和重要的生态学作用,对于研究压载水细菌具有一定的指导作用,值得进一步研究。JING等[25]发现在南海深水层中存在大量的假交替单胞菌属, 其细菌能分泌多种胞外活性物质, 有助于获取营养和竞争生存空间等, 具有重要的生态学作用。
南海远岸特有的优势属浮霉状菌属(Planctomyces)、原绿球藻属(Prochlorococcus)丰度相较于其他海域压载水样中要高很多,这可能是由于南海复杂的水文条件和独特的地理环境所致[26]。另外从细菌群落的典范对应分析结果中可以看出浮霉状菌属(Planctomyces)、原绿球藻属(Prochlorococcus)与溶解氧有很强的正相关性,溶解氧对于绿球藻的生长起关键作用[26]。浮霉菌主要为兼性厌氧菌, 利用糖类作为主要碳源; 其他为严格厌氧自养菌。浮霉菌细胞内存在大量的硫酸酯酶, 这种酶能够将磺胺杂多糖进行最初的降解, 从而参与分解杂多糖的过程, 在碳循环中发挥重要作用[27],压载舱中厌氧、较差的水质环境皆有利于浮霉菌的生长。
盐单胞菌属为革兰氏阴性菌,是一类中度嗜盐菌,盐单胞菌属的生长对盐度依赖大,对营养盐含量要求低[28-30]。这与本文的研究结果盐单胞菌属Halomonas同溶解氧、pH、盐度呈正相关性,与营养盐、温度有较强的负相关性相一致。在此次调查中,各海域压载水样中压载水均检测出盐单胞菌属,具有很好的生存能力,在水温较低且盐度较高的春季,其他异养细菌生长受到温度和营养盐限制,生存状态不佳,但盐单胞菌适应了相对较高的盐度环境,生存优势明显[31]。
各海域交换的压载水微生物多样性在很大程度上决定于当地的海洋微生物及其环境,不同的海域生活有特定的微生物,在一定程度上可考虑作为海域指示微生物。虽然压载水微生物数目相对于海洋微生物有所减少,但存活下来的微生物更应值得我们重视。压载水微生物生存机制比较复杂,不仅仅在水体中生活,一些则是寄生于体型相对较大的浮游动植物或是一些污损生物,且较差的水质环境容易滋养一些致病细菌,寄生于浮游动植物的细菌更容易在排海后传播开来。因此,十分有必要加强压载水置换管理以及致病微生物的防控措施。
| [1] |
IMO. International convention for the control and management of ships' ballast water and sediments[S]. London: International Maritime Organization, 2004.
|
| [2] |
TAMELANDER J, RIDDERING L, HAAG F, et al. Guidelines for Development of a National Ballast Water Management Strategy[R]. London, IMO, 2010. https://www.researchgate.net/publication/242473360_Guidelines_for_Development_of_a_National_Ballast_Water_Management_Strategy
|
| [3] |
刘洪波. 微波技术处理船舶压载水沉积物的研究[D]. 大连: 大连海事大学, 2009. LIU H B. Study on the treatment of ballast sediments with microwave technology[D]. Dalian: Dalian Maritime University, 2009. http://cdmd.cnki.com.cn/article/cdmd-10151-2009107337.htm |
| [4] |
EMAMI K, ASKARI V, ULLRICH M, et al. Characte-rization of bacteria in ballast water using MALDI-TOF mass spectrometry[J]. PLoS One, 2012, 7(6): e38515. DOI:10.1371/journal.pone.0038515 |
| [5] |
BURKHOLDER J M, HALLEGRAEFF G M, MELIA G, et al. Phytoplankton and bacterial assemblages in ballast water of U.S. military ships as a function of port of origin, voyage time, and ocean exchange practices[J]. Harmful Algae, 2007, 6(4): 486-518. DOI:10.1016/j.hal.2006.11.006 |
| [6] |
ALTUG G, GURUN S, CARDAK M, et al. The occurrence of pathogenic bacteria in some ships' ballast water incoming from various marine regions to the Sea of Marmara, Turkey[J]. Marine Environmental Research, 2012, 81: 35-42. DOI:10.1016/j.marenvres.2012.08.005 |
| [7] |
REVILLA-CASTELLANOS V J, GUERRERO A, GOMEZ-GIL B, et al. Pathogenic Vibrio parahaemolyticus isolated from biofouling on commercial vessels and harbor structures[J]. Biofouling, 2015, 31(3): 275-282. DOI:10.1080/08927014.2015.1038526 |
| [8] |
WU H, CHEN C, WANG Q, et al. The biological content of ballast water in China:A review[J]. Aquaculture & Fisheries, 2017, 2(6): 241-246. |
| [9] |
宫恩昊, 王钰婷, 刘艳, 等. 上海港船舶压载水浮游植物组成及生态因子的相关性[J]. 海洋湖沼通报, 2015(4): 161-167. GONG E H, WANG Y T, LIU Y, et al. Correlation of phytoplankton composition and ecological factors of ballast water in Shanghai Port[J]. Journal of Oceanology and Limnology, 2015(4): 161-167. |
| [10] |
刘亮, 王琼, 袁林, 等. 光催化与纯紫外工艺对船舶压载水微藻的处理效果比较[J]. 生物学杂志, 2014, 31(3): 29-32, 42. LIU L, WANG Q, YUAN L, et al. Comparison of the effects of photocatalysis and pure UV on the treatment of marine microalgae in ballast water[J]. Journal of Biology, 2014, 31(3): 29-32, 42. |
| [11] |
刘艳, 吴惠仙, 薛俊增. 海洋外来物种入侵生态学研究[J]. 生物安全学报, 2013, 22(1): 8-16. LIU Y, WU H X, XUE J Z. Invasion ecology of exotic species in the ocean[J]. Acta Biosafety Sinica, 2013, 22(1): 8-16. |
| [12] |
薛俊增, 刘艳, 王金辉, 等. 洋山深水港入境船舶压载水浮游动物种类组成分析[J]. 海洋学报(中文版), 2011, 33(1): 138-145. XUE J Z, LIU Y, WANG J H, et al. Analysis of species composition of ballast water in the entry ship of the Yangshan deep-water port[J]. Journal of the Chinese Society of Oceanography, 2011, 33(01): 138-145. |
| [13] |
王琪, 乔红宇. 基于GA-BP神经网络的船舶压载水微生物数量预测[J]. 江苏科技大学学报(自然科学版), 2016, 30(6): 529-537. WANG Q, QIAO H Y. Prediction of ballast water for the microbial indicators based on genetic algorithm and artificial neural network[J]. Journal of Jiangsu University of Science and Technology (Natural Science Edition), 2016, 30(6): 529-537. |
| [14] |
傅志超. 船舶压载水公约要求下的压载水中微生物的检测分析[J]. 中国水运, 2011, 11(8): 85-87. FU Z C. Detection and analysis of microorganisms in ballast water under ship ballast water convention requirements[J]. China Water Transport, 2011, 11(8): 85-87. |
| [15] |
冯云霄, 张乐, 方振东, 等. 秦皇岛口岸入境船舶压载水中微生物携带情况调查[J]. 环境科学导刊, 2011, 30(2): 58-61. FENG Y X, ZHANG L, FANG Z D, et al. Investigation of microbe taken by ballast water of entry ships in Qinhuangdao port[J]. Environmental Science Survey, 2011, 30(2): 58-61. |
| [16] |
李小洪, 刘文正, 杨燕秋, 等. 船舶压载水致病微生物入侵风险分析[C]//2012深圳市预防医学会学术研讨会论文汇编. 深圳: 深圳市预防医学会, 2012: 10. LI X H, LIU W Z, YANG Y Q, et al. Risk analysis of pathogenic microorganism invasion of ship ballast water[C]//2012 Shenzhen Preventive Medicine Society Symposium Compilation. Shenzhen: Shenzhen Preventive Medicine Association, 2012: 10. |
| [17] |
FAIMALI M, GARAVENTA F, CHELOSSI E, et al. A new photodegradable molecule as a low impact ballast water biocide:efficacy screening on marine organisms from different trophic levels[J]. Marine Biology, 2006, 149(1): 7-16. DOI:10.1007/s00227-005-0207-y |
| [18] |
REKADWAD B, KHOBRAGADE C. Microbial biofouling: a possible solution to treat harmful microorganisms in ship ballast water[M]//KALIA V C, KUMAR P. Microbial Applications Vol. 1. Cham: Springer, 201.
|
| [19] |
董逸. 我国黄、东海典型海域微生物群落结构及其与环境变化的关系[D]. 青岛: 中国科学院研究生院(海洋研究所), 2013. DONG Y. Microbial community structure and its relationship with environmental variations in typical areas of the Yellow Sea and East China Sea[D]. Qingdao: Graduate University of Chinese Academy of Sciences (Institute of Oceanography), 2013. http://cdmd.cnki.com.cn/Article/CDMD-80068-1013300024.htm |
| [20] |
刘敏. 我国黄、东海典型生态过程中的微生物群落结构[D]. 青岛: 中国科学院研究生院(海洋研究所), 2011. LIU M. Microbial community structure in specific ecological processes in the Yellow Sea and East China Sea, China[D]. Qingdao: Graduate University of Chinese Academy of Sciences (Institute of Oceanography), 2011. http://cdmd.cnki.com.cn/Article/CDMD-80068-1011093950.htm |
| [21] |
丁昌玲. 黄海、东海和南海海域蓝藻生物量及其时空分布[D]. 青岛: 中国海洋大学, 2009. DING C L. The abundance, the spatial and temporal distributions of cyanobacteria in the Yellow Sea, the East China Sea and the South China Sea[D]. Qingdao: Ocean University of China, 2009. http://cdmd.cnki.com.cn/Article/CDMD-10423-2009172796.htm |
| [22] |
孙佳. 大西洋、太平洋和印度洋微生物数量、生物量、多样性及其生态特征[D]. 厦门: 国家海洋局第三海洋研究所, 2008. SUN J. Numbers, biomass, biodiversity and ecological characteristics of microorganisms in Atlantic, pacific and Indian oceans[D]. Xiamen: Third Institute of Oceanography, State Oceanic Administration, 2008. http://cdmd.cnki.com.cn/Article/CDMD-85303-2008148749.htm |
| [23] |
肖南燕. 洋山港海域与船舶压载水及沉积物细菌多样性比较[D]. 上海: 上海海洋大学, 2016. XIAO N Y. Comparison of bacterial community diversity in Yangshan port, ship ballast water and sediment[D]. Shanghai: Shanghai Ocean University, 2016. http://cdmd.cnki.com.cn/Article/CDMD-10264-1016912417.htm |
| [24] |
卢婧雯, 张心齐, 杜丽丽, 等. 中国东海及南海近海4采样点海水可培养细菌的多样性研究[J]. 浙江大学学报(理学版), 2012, 39(4): 443-449. LU J W, ZHANG X Q, DU L L, et al. Bacterial isolation and diversity analysis of four seawater sampling sites of the East China Sea and the South China Sea[J]. Journal of Zhejiang University (Science Edition), 2012, 39(4): 443-449. |
| [25] |
JING H M, XIA X M, SUZUKI K, et al. Vertical profiles of bacteria in the tropical and subarctic oceans revealed by pyrosequencing[J]. PLoS One, 2013, 8(11): e79423. DOI:10.1371/journal.pone.0079423 |
| [26] |
黄冰心, 丁兰平. 中国海洋蓝藻门新分类系统[J]. 广西科学, 2014, 21(6): 580-586. HUANG B X, DING L P. The catalogue of marine canyobacteria of China[J]. Guangxi Sciences, 2014, 21(6): 580-586. |
| [27] |
GLÖCKNER F O, KUBE M, BAUER M, et al. Complete genome sequence of the marine planctomycete Pirellula sp. strain 1[J]. Proceedings of the National Academy of Sciences of the United States of America, 2003, 100(14): 8298-8303. DOI:10.1073/pnas.1431443100 |
| [28] |
VREELAND R H, LITCHFIELD C D, MARTIN E L, et al. Halomonas elongata, a new genus and species of extremely salt-tolerant bacteria[J]. International Journal of Systematic Bacteriology, 1980, 30(2): 485-495. DOI:10.1099/00207713-30-2-485 |
| [29] |
WHITMAN W B, GOODFELLOW M, KÄMPFER P, et al. Bergey's manual of systematic bacteriology[M]. 2nd ed. New York: Springer, 2012.
|
| [30] |
张甲耀, 夏盛林, 邱克明, 等. 潜流型人工湿地污水处理系统氮去除及氮转化细菌的研究[J]. 环境科学学报, 1999, 19(3): 323-327. ZHANG J Y, XIA S L, QIU K M, et al. Nitrogen removal by a subsurface flow constructed wetlands wastewater treatment system and nitrogen-transformation bacteria[J]. Acta Scientiae Circumstantiae, 1999, 19(3): 323-327. |
| [31] |
薛俊增, 肖南燕, 王琼, 等. 洋山港海域细菌群落多样性的季节变化[J]. 生态学报, 2016, 36(23): 7758-7767. XUE J Z, XIAO N Y, WANG Q, et al. Seasonal variation of bacterial community diversity in Yangshan port[J]. Acta Ecologica Sinica, 2016, 36(23): 7758-7767. |
2. Centre for Research on the Ecological Security of Ports and Shipping, Shanghai 201306, China
 2018,
Vol. 27
2018,
Vol. 27


