2. 农业部鱼类营养与环境生态研究中心, 上海 201306;
3. 水产动物遗传育种中心上海市协同创新中心, 上海 201306
随着全球水产养殖规模和产量的增加,鱼粉的供应不足已成为制约水产饲料工业发展的重要因素[1],降低鱼粉的使用量,增加植物蛋白源的使用量,是今后水产饲料发展的必然趋势。然而,植物蛋白中赖氨酸、蛋氨酸等必需氨基酸缺乏和其较低的消化率,是制约其大规模在水产饲料中使用的重要因素[2]。因此,可从补充必需氨基酸和添加酶制剂入手,提高植物蛋白的营养价值。
TESHIMA等[3]发现,饲料中添加晶体精氨酸盐酸盐对日本囊对虾(Penaeus japonicus)的生长无显著改善作用,在斑节对虾(Penaeus monodon)和凡纳滨对虾上也有类似报道[4];饲料中添加微囊氨基酸,较添加晶体氨基酸显著提高日本囊对虾的生长性能和饲料利用率[5]。微囊氨基酸在水中的溶失率低[4, 6-7],微囊氨基酸与蛋白态氨基酸的吸收较晶体氨基酸更为同步[8-9],故在对虾饲料中,微囊氨基酸的作用效果优于晶体氨基酸。
在低鱼粉颗粒饲料中添加蛋白酶,可提高异育银鲫对营养物质的消化率和沉积率,改善鱼体生长性能[10]。在虹鳟(Oncorhynchus mykiss)[11-12]、青鱼(Mylopharyngodon piceus)[13]、鲤(Cyprinus carpio)[14]饲料中添加蛋白酶,均改善了鱼体生长性能。LI等[15]研究发现,在低鱼粉凡纳滨对虾饲料中添加蛋白酶,可显著改善对虾生长,提高对虾肝胰腺蛋白酶活性。
尽管已有一些关于氨基酸、蛋白酶在水产动物中应用的报道,但将二者结合起来的研究尚未见报道。本试验以凡纳滨对虾为研究对象,以豆粕等蛋白代替基础饲料(含20%鱼粉)中5%鱼粉,单独或联合添加微囊氨基酸、蛋白酶,考察对虾体生长性能、饲料利用和消化酶的影响,为氨基酸和蛋白酶在对虾饲料中的合理应用提供依据,以降低对虾饲料中的鱼粉水平。
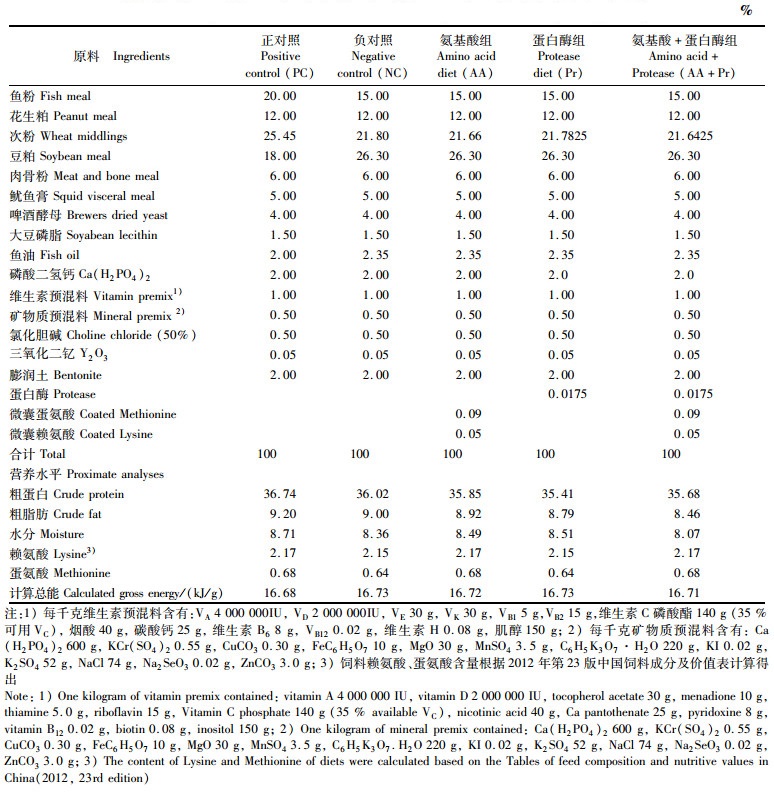
1 材料与方法 1.1 试验设计与试验饲料设计鱼粉含量20%的正对照组、鱼粉含量15%的负对照组(用豆粕等蛋白替代鱼粉)、在负对照饲料中分别添加微囊赖氨酸、蛋氨酸(简称氨基酸组),使之达到与正对照一致的水平, 添加175 mg/kg蛋白酶(蛋白酶组),及同时添加微囊赖氨酸、蛋氨酸和175 mg/kg蛋白酶(氨基酸+蛋白酶组),配制成5组等氮等能的饲料。饲料原料粉碎后过60目筛,按饲料配方(表 1)混合均匀,各饲料中添加500 mg/kg Y2O3作为外源指示剂。用单螺杆挤压机制成直径为1.2 mm的沉性颗粒饲料(制粒温度为85 ℃±5 ℃),于95 ℃烘箱内后熟化20 min,风干至水分含量低于10%,密封保存备用。
|
表 1 试验饲料组成和营养水平(风干基础) Tab.1 Composition and nutrient levels of the experimental diets (air dry basis) |
微囊赖氨酸、蛋氨酸由广东海纳川药业股份有限公司提供,有效含量分别为50%、39%。蛋白酶商品名为AG175,由加拿大JEFO动物营养公司提供,为细菌发酵产生的碱性丝氨酸蛋白酶,具有较高的耐温性,经制粒和后熟化后有79.3%和67.5%的保留率[16]。
1.2 试验虾及饲养管理凡纳滨对虾虾苗购自江苏南通某育苗基地,在水泥池中进行前期暂养,投喂商品饲料(苏州通威特种饲料有限公司生产,商品名:虾肝强,规格:20 kg,粗蛋白含量≥40%)。正式试验前24 h停止投饵,挑选个体大小均匀的健康对虾1 000尾(初始体质量约为2.96 g),随机分配到20口网箱(1.0 m×1.0 m×1.2 m),每口网箱50尾,试验共设置5个处理,每个处理4个重复(网箱)。养殖期间,每日投喂量为虾体质量的3%~8%(前期投喂高,后期低),分4次投喂(6:00、12:00、17:00和23:00),早晚投喂量占总量的70%。根据对虾的进食情况和天气情况及时调整具体投喂量,使各网箱投饲量基本一致,并确保饲料在投喂后2 h内被采食完;昼夜充气,采用虹吸法吸走池底残饵及粪便,每周吸污一次,吸污后换水1/3。试验期间,水温22~30 ℃、盐度0.5~1.0、溶氧≥5.6 mg/L,pH 7.8~8.5,氨氮≤0.2 mg/L,亚硝酸盐≤0.1 mg/L。饲养试验共持续42 d。养殖试验于上海海洋大学滨海特种养殖场进行。
1.3 粪便收集试验开始3周后,每次投喂后2 h,用镊子取食台上包膜完整的粪便于离心管中,-20 ℃冰箱中保存,待收集足量粪便样品后,105 ℃干燥、密封存放于-20 ℃冰箱中,用于营养物质消化率分析。
1.4 样品采集养殖试验开始时,随机选取60尾对虾于-20 ℃冰箱中保存,其中10尾虾合并为一个样本,用于初始样体成分分析。试验结束前24 h停止投喂。每个网箱随机挑选4尾虾,保存于-20 ℃冰箱中,用于全虾体成分分析;每网箱另取9尾虾(3尾合为一个样本)取其肝胰脏,-20 ℃冻存,测定相关消化酶活性;每网箱再选取10尾虾,用1 mL注射器从围心腔中取血淋巴液,3 000 r/min离心10 min后取上清液于-80 ℃保存备用,以测定相关生化指标。
1.5 测定指标与方法 1.5.1 生长性能试验结束前24 h停止投喂。每个网箱进行称重并记录尾数,计算存活率(SR)、增重率(WGR)、饲料系数(FCR)、蛋白质效率(PER)、蛋白质沉积率(PRR)和脂肪沉积率(LRR):
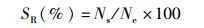 (1)
(1)
式中:Ns为虾收获尾数;Ne为虾投放尾数。
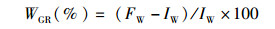 (2)
(2)
式中:FW为末均质量(g);IW为初均质量(g)。
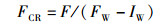 (3)
(3)
式中:F为投喂量。
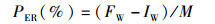 (4)
(4)
式中:M为摄食蛋白量。
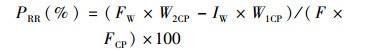 (5)
(5)
式中:W2CP为末全虾粗蛋白含量(%);W1CP为初全虾粗蛋白含量(%);F为投喂量(g);FCP为饲料粗蛋白含量(%)。
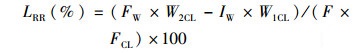 (6)
(6)
式中:W2CL为末全虾粗脂肪含量;W1CL为初全虾粗脂肪含量;FCL为饲料粗脂肪含量。
1.5.2 饲料、粪便、全虾组成和钇元素含量对虾及饲料样品常规分析采用国际标准方法。水分含量通过烘箱在105 ℃下烘干至恒重测定;粗蛋白质含量采用自动凯氏定氮仪(2300-Auto-analyzer,Foss Tecator,Sweden)测定;粗脂肪含量采用氯仿甲醇法测定;粗灰分含量是在550 ℃马福炉中灼烧12 h后测得。饲料和粪便中钇元素的分析采用等离子体原子发射光谱法(ICP)(Vista MPX,Varian,Alo Alto,California,America)。在此基础上,分别计算干物质和蛋白质表观消化率(ADDM,ADCP),如下:
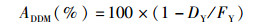 (7)
(7)
式中:DY为饲料钇含量(%);FY为粪便钇含量(%)。
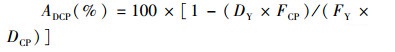 (8)
(8)
式中:FCP为粪便粗蛋白含量(%);DCP为饲料粗蛋白含量(%)。
1.5.3 肝胰脏消化酶活性将肝胰脏样品从-20 ℃冰箱中取出,4 ℃解冻,匀浆,3 000 r/min离心15 min,取上清测定消化酶活性。蛋白酶活力的测定采用福林酚法。蛋白酶单位定义(U/mg):1 mg组织蛋白在40 ℃、pH 9.8条件下,1 min水解酪素产生1 μg酪氨酸定义为一个酶活力单位。脂肪酶活力的测定采用南京建成试剂盒。脂肪酶单位定义(U/g):在37 ℃条件下,每克组织蛋白在本反应体系中与底物反应1 min,每消耗1 μmol底物为一个酶活力单位。淀粉酶活力的测定采用南京建成试剂盒。淀粉酶单位定义(U/g):每克组织蛋白在37 ℃与底物作用30 min,水解10 mg淀粉定义为1个淀粉酶活力单位。酶液蛋白质浓度采用考马斯亮兰法测定(试剂购于南京建成生物研究所)。
1.6 数据处理数据处理与分析采用SPSS 17.0分析软件进行ANOVA单因子方差分析和Duncan’s多重检验, 以P < 0.05作为差异显著性判断标准。
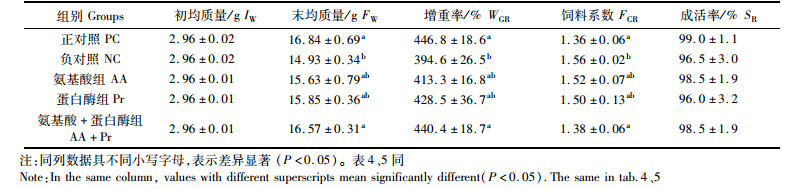
2 结果 2.1 生长性能由表 2可见,正对照组具有最高增重率和最低饲料系数,而低鱼粉饲料(负对照组)增重率最低,饲料系数最高(P < 0.05)。在低鱼粉饲料中添加微囊氨基酸或蛋白酶后,有提高增重率和降低饲料系数的趋势(P>0.05),且接近正对照组的水平(P>0.05);在低鱼粉饲料中同时添加微囊氨基酸和蛋白酶后,较负对照组虾体增重率提高11.5%,饲料系数降低0.18(P < 0.05),达到和正对照组一致的水平。各试验组在养殖过程中的成活率均大于95%,且无显著差异(P>0.05)。
|
表 2 饲料中添加氨基酸和蛋白酶对凡纳滨对虾生长性能的影响 Tab.2 Effects of coated amino acids and protease supplementation in low fish meal diets on growth performance of white shrimp |
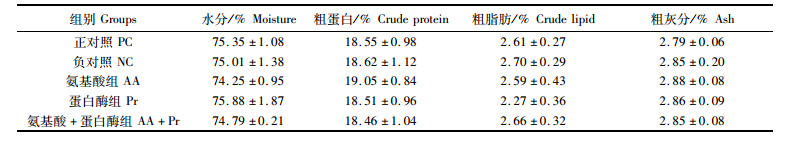
由表 3可见,各试验组全虾水分、粗蛋白、粗脂肪、粗灰分均无显著差异(P>0.05)。
|
表 3 饲料中添加氨基酸和蛋白酶对凡纳滨对虾体组成的影响 Tab.3 Effects of coated amino acids and protease supplementation in low fish meal diets on whole-body composition of white shrimp |
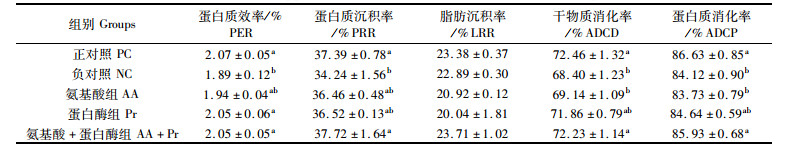
由表 4可见,低鱼粉组的蛋白质效率、蛋白质沉积率、干物质消化率和蛋白质消化率较正对照组显著降低(P < 0.05);与低鱼粉组相比,添加氨基酸,有提高蛋白质沉积率和干物质消化率趋势(P>0.05);添加蛋白酶,显著提高了蛋白质效率(P < 0.05),有提高蛋白质沉积率、干物质消化率和蛋白质消化率趋势(P>0.05);在低鱼粉饲料中添加氨基酸+蛋白酶后,蛋白质效率、蛋白质沉积率、干物质和蛋白质消化率均较低鱼粉组显著提高(P < 0.05),并达到与正对照组基本一致的水平。各组在脂肪沉积率上无显著差异(P>0.05)。
|
表 4 饲料中添加氨基酸和蛋白酶对营养物质表观消化率的影响 Tab.4 Effects of coated amino acids and protease supplementation in low fish meal diets on apparent digestibility of nutrients of white shrimp |
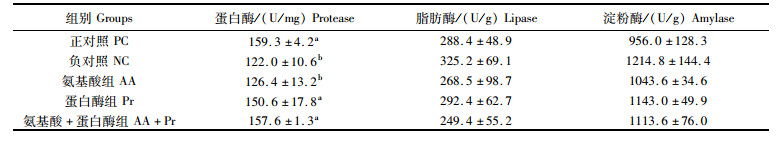
由表 5可见,在低鱼粉饲料中添加蛋白酶,或氨基酸+蛋白酶后,肝胰腺蛋白酶活性较低鱼粉组显著升高(P < 0.05),但单独添加氨基酸对肝胰腺蛋白酶活性无显著影响(P>0.05)。各试验组在肝胰腺脂肪酶、淀粉酶活性上无显著差异(P>0.05)。
|
表 5 饲料中添加氨基酸和蛋白酶对凡纳滨对虾肝胰腺消化酶的影响 Tab.5 Effects of coated amino acids and protease supplementation in low fish meal diets on activities of digestive enzymes in hepatopancreas of white shrimp |
本试验中,低鱼粉组(15%鱼粉)的凡纳滨对虾增重率较正对照组(20%鱼粉)下降11.7%,饲料系数升高0.20(P < 0.05, 表 2),主要原因与豆粕等蛋白代替5%鱼粉后,导致饲料蛋氨酸等必需氨基酸含量的下降(表 1)和营养物质消化率的下降(表 4)有关,也可能与胆固醇等的下降有关[16]。本试验从补充必需氨基酸和蛋白酶两个方面来改善低鱼粉饲料的利用性。
在对虾饲料中补充晶体氨基酸,大多数研究认为对于生长和饲料利用没有显著改善[3, 5, 17-18],其主要原因是晶体氨基酸与蛋白态氨基酸吸收不同步[8, 19]和晶体氨基酸在水中的溶失率较高[4, 6],故在对虾饲料补充氨基酸,通常采用微囊或包膜等缓释剂型。LIM[4]在饲料中添加包膜L-精氨酸饲养初始体质量0.95 g的斑节对虾8周,显著提高了增重率,降低了饲料系数,而添加晶体氨基酸对生长并未起到改善作用。在日本囊对虾[5]、凡纳滨对虾、罗氏沼虾(Macrobrachium rosenbergii)[20]的研究中,饲料中补充微囊氨基酸均显著提高了虾体生长性能。本试验在低鱼粉饲料中补充微囊蛋氨酸、赖氨酸后,改善了虾体生长性能,但未达到显著效果,可能与饲料挤压生产过程对微囊材料的破坏和氨基酸的损失有关。此外,在补充了赖氨酸、蛋氨酸后,可能还存在其他限制性氨基酸,影响了饲料效果的发挥;本实验中,氨基酸的添加,并没有改善干物质、蛋白质消化率(表 4),肝胰腺蛋白酶活性也没有提高(表 5),这意味着该组饲料的可消化养分含量依然低于正常鱼粉饲料(正对照组),故氨基酸组对虾体生产性能的改善不显著。
在水产饲料中添加蛋白酶,大多数研究认为对于生长和营养物质利用均有显著改善[1, 21-22]。在饲料制作过程中,蛋白酶能够对饲料蛋白起到一定水解作用[21],可弥补内源蛋白酶的不足,降解难以消化的大分子蛋白,降解饲料中的部分抗营养因子[22]和改善肠道组织结构[23]。LI等[15]在低鱼粉饲料中添加175 mg/kg蛋白酶饲喂凡纳滨对虾幼虾(3.3 g)56 d,提高增重率11.3%、降低饲料系数0.12(P < 0.05),肝胰腺蛋白酶活性也显著提高。在罗非鱼(Oreochromis spp.)[24]、虹鳟[1]、异育银鲫(Carassius auratus gibelio)[10]等的研究中,也有类似报道。LI等[15]在鱼粉含量为3%的罗非鱼颗粒饲料中添加蛋白酶,显著提高了饲料干物质和粗蛋白消化率,但在鱼粉含量9%的颗粒饲料中添加蛋白酶,则对消化率无显著影响。本试验在低鱼粉饲料中补充蛋白酶后,在数值上提高了虾体增重率和饲料干物质、粗蛋白表观消化率,显著提高了肝胰腺蛋白酶活性,达到和正对照组基本一致的水平(P>0.05)。饲料酶制剂作用的发挥,通常与饲料的原料组成和营养水平有关,也与动物种类和生长阶段,以及养殖环境等有关。
本试验中,在低鱼粉饲料中的单独补充微囊氨基酸和蛋白酶,虽在数值上改善了凡纳滨对虾生长性能,但均未达显著水平。将二者同时补充后,凡纳滨对虾增重率提高11.6%,饲料系数降低0.18(P < 0.05),虾体生长性能得到显著改善。石泽[10]在低鱼粉颗粒饲料中补充微囊赖氨酸、蛋氨酸的基础上添加175 mg/kg蛋白酶饲喂初始体质量为(35.0±0.2) g的异育银鲫,显著提高了营养物质利用率、改善了鱼体生长性能。酶制剂和氨基酸的合用,既提高了营养物消化率,也平衡了饲料氨基酸组成,这是在增加植物蛋白用量,降低鱼粉水平后,值得推荐的一种营养策略。
在本研究条件下,在鱼粉含量为15%的凡纳滨对虾饲料中单独补充500 mg/kg微囊赖氨酸、900 mg/kg微囊蛋氨酸,或175 mg/kg蛋白酶,对虾体生长性能和饲料利用无显著影响,但同时补充500 mg/kg微囊赖氨酸、900 mg/kg微囊蛋氨酸和175 mg/kg蛋白酶,可显著提高营养物质利用率,改善凡纳滨对虾生长性能。
| [1] | DREW M D, RACZ V J, GAUTHIER R, et al. Effect of adding protease to coextruded flax:pea or canola:pea products on nutrient digestibility and growth performance on rainbow trout (Oncorhynchus mykiss)[J]. Animal Feed Science and Technology, 2005, 119(1/2): 117–128. |
| [2] | HERNÁNDEZ C, SARMIENTO-PARDO J, GONZÁLEZ-RODRÍGUEZ B, et al. Replacement of fish meal with co-extruded wet tuna viscera and corn meal in diets for white shrimp (Litopenaeus vannamei Boone)[J]. Aquaculture Research, 2004, 35(12): 1153–1157. DOI:10.1111/are.2004.35.issue-12 |
| [3] | TESHIMA S, ISHIKAWA M, SHAH ALAM M, et al. Supplemental effects and metabolic fate of crystalline arginine in juvenile shrimp Marsupenaeus japonicus[J]. Comparative Biochemistry and Physiology Part B:Biochemistry and Molecular Biology, 2004, 137(2): 209–217. DOI:10.1016/j.cbpc.2003.11.005 |
| [4] | LIM C. Effect of dietary pH on amino acid utilization by shrimp (Penaeus vannamei)[J]. Aquaculture, 1993, 114(3/4): 293–303. |
| [5] | ALAM M S, TESHIMA S, KOSHIO S, et al. Effects of supplementation of coated crystalline amino acids on growth performance and body composition of juvenile kuruma shrimp Marsupenaeus japonicus[J]. Aquaculture Nutrition, 2004, 10(5): 309–316. DOI:10.1111/anu.2004.10.issue-5 |
| [6] | YÚFERA M, KOLKOVSKI S, FERNÁ NDEZ-DⅡAZ C, et al. Free amino acid leaching from a protein-walled microencapsulated diet for fish larvae[J]. Aquaculture, 2002, 214(1/4): 273–287. |
| [7] | LÓPEZ-ALVARADO J, LANGDON C J, TESHIMA S I, et al. Effects of coating and encapsulation of crystalline amino acids on leaching in larval feeds[J]. Aquaculture, 1994, 122(4): 335–346. DOI:10.1016/0044-8486(94)90342-5 |
| [8] | RØNNESTAD I, CONCEIÇÃO L E, ARAGÃO C, et al. Free amino acids are absorbed faster and assimilated more efficiently than protein in postlarval Senegal sole (Solea senegalensis)[J]. The Journal of Nutrition, 2000, 130(11): 2809–2812. |
| [9] | COWEY C B, WALTON M J. Studies on the uptake of (14C) amino acids derived from both dietary (14C) protein and dietary (14C) amino acids by rainbow trout, Salmo gairdneri Richardson[J]. Journal of Fish Biology, 1988, 33(2): 293–305. DOI:10.1111/jfb.1988.33.issue-2 |
| [10] |
石泽. 蛋白酶、有机酸对异育银鲫(Carassius auratus gibelio)和建鲤(Cyprinus carpio var. Jian)生长、营养物质利用率的影响[D]. 上海: 上海海洋大学, 2016.
SHI Z. Effects of dietary protease and organic acids on growth and nutrient utilization of gibel carp, Carassius auratus gibelio and Jian carp, Cyprinus carpio var. Jian[D]. Shanghai:Shanghai Ocean University, 2016. http://cdmd.cnki.com.cn/Article/CDMD-10264-1016912294.htm |
| [11] | DALSGAARD J, VERLHAC V, HJERMITSLEV N H, et al. Effects of exogenous enzymes on apparent nutrient digestibility in rainbow trout (Oncorhynchus mykiss) fed diets with high inclusion of plant-based protein[J]. Animal Feed Science and Technology, 2012, 171(2/4): 181–191. |
| [12] | DENSTADLI V, HILLESTAD M, VERLHAC V, et al. Enzyme pretreatment of fibrous ingredients for carnivorous fish:Effects on nutrient utilisation and technical feed quality in rainbow trout (Oncurhynchus mykiss)[J]. Aquaculture, 2011, 319(3/4): 391–397. |
| [13] |
陈建明, 叶金云, 许尧兴, 等. 饲料中添加中性蛋白酶对青鱼生长、消化及鱼体组成的影响[J].
水生生物学报, 2009, 33(4): 726–731.
CHEN J M, YE J Y, XU Y X, et al. Effect of adding neutral protease to diets on growth performance, digestion, and body composition of fingerling black carp (Mylopharyngodon piceus)[J]. Acta Hydrobiologica Sinica, 2009, 33(4): 726–731. |
| [14] |
刘鼎云, 冷向军, 卢永红, 等. 饲料中添加蛋白酶Aquagrow对鲤生长和蛋白质消化酶活性的影响[J].
淡水渔业, 2007, 37(5): 50–52.
LIU D Y, LENG X J, LU Y H, et al. Effects of adding protease (Aquagrow) in diet on growth and digestive protease activities of common carp[J]. Freshwater Fisheries, 2007, 37(5): 50–52. |
| [15] | LI X Q, CHAI X Q, LIU D Y, et al. Effects of temperature and feed processing on protease activity and dietary protease on growths of white shrimp, Litopenaeus vannamei, and tilapia, Oreochromis niloticus×O. aureus[J]. Aquaculture Nutrition, 2016, 22(6): 1283–1292. DOI:10.1111/anu.2016.22.issue-6 |
| [16] |
王鑫磊, 李航, 黄旭雄, 等. 饲料中胆固醇含量对淡水养殖凡纳滨对虾生长性能、抗弧菌和抗亚硝态氮胁迫能力的影响[J].
动物营养学报, 2016, 28(8): 2639–2649.
WANG X L, LI H, HUANG X X, et al. Effects of dietary cholesterol content on growth performance, vibrio and nitrite nitrogen stress resistant abilities of Litopenaeus vannamei Cultured in Freshwater[J]. Chinese Journal of Animal Nutrition, 2016, 28(8): 2639–2649. |
| [17] | LUO L, WANG J, PAN Q, et al. Apparent digestibility coefficient of poultry by-product meal (PBM) in diets of Penaeus monodon (Fabricius) and Litopenaeus vannamei (Boone), and replacement of fishmeal with PBM in diets of P. monodon[J]. Aquaculture Research, 2012, 43(8): 1223–1231. DOI:10.1111/are.2012.43.issue-8 |
| [18] | BAUER W, PRENTICE-HERNANDEZ C, TESSER M B, et al. Substitution of fishmeal with microbial floc meal and soy protein concentrate in diets for the pacific white shrimp Litopenaeus vannamei[J]. Aquaculture, 2012, 342-343(1): 112–116. |
| [19] |
麦康森. 放射性同位素标记法测定虾类饵料的消化率[J].
饲料研究, 1988: 13–15.
MAI K S. Determination of digestibility of shrimp diet by radioisotope marker[J]. Feed Research, 1988: 13–15. |
| [20] |
牛化欣. 微胶囊氨基酸制备及其在饲料加工和虾养殖中的效果研究[D]. 无锡: 江南大学, 2011.
NIU H X. Preparation of microencapsulated amino acids and its evaluation in feed proceesing and shrimp culture[D]. Wuxi:Jiangnan University, 2011. http://cdmd.cnki.com.cn/Article/CDMD-10295-1011209597.htm |
| [21] |
宋红利, 董晓慧, 谭北平, 等. 蛋白酶和有机酸盐对凡纳滨对虾生长性能、免疫酶和消化酶的影响[J].
广东饲料, 2016, 25(4): 29–34.
SONG H L, DONG X H, TAN B P, et al. Effects of dietary protease and organic acids on growth performence, immunoenzyme and digestive enzyme activity of white shrimp[J]. Guangdong Feed, 2016, 25(4): 29–34. |
| [22] | CAINE W R, VERSTEGEN M W A, SAUER W C, et al. Effect of protease treatment of soybean meal on content of total soluble matter and crude protein and level of soybean trypsin inhibitors[J]. Animal Feed Science and Technology, 1998, 71(1/2): 177–183. |
| [23] |
姚建国. 外源酶对家禽内源消化酶活性及饲料氨基酸消化率影响的研究[D]. 南京: 南京农业大学, 2001.
YAO J G. Influence of exogenous enzymes on endogenous digestive enzyme activity and feed amino acid digestibility of poultry[D]. Nanjing:Nanjing Agricultural University, 2001. http://cdmd.cnki.com.cn/Article/CDMD-10307-2001012888.htm |
| [24] | LIN S M, MAI K S, TAN B P. Effects of exogenous enzyme supplementation in diets on growth and feed utilization in tilapia, Oreochromis niloticus x O. aureus[J]. Aquaculture Research, 2007, 38(15): 1645–1653. DOI:10.1111/are.2007.38.issue-15 |
2. Centre for Research on Environmental Ecology and Fish Nutrition(CREEFN) of the Ministry of Agriculture, Shanghai Ocean University, Shanghai 201306, China;
3. Shanghai Collaborative Innovation for Aquatic Animal Genetics and Breeding, Shanghai Ocean University, Shanghai 201306, China
 2017,
Vol. 26
2017,
Vol. 26


