2. 上海海洋大学 水域环境生态上海高校工程研究中心, 上海 201306
随着社会经济快速发展,工农业废水排放量增大,江河湖库中氮磷含量越来越高,水体富营养化问题日渐严重[1-3]。水环境治理中最需要解决也是最难解决的是总氮削减与控制,特别是湖泊和河流总氮的控制对改善水质至关重要[4]。生态浮床作为河道水质改善的一种有效手段,具有可操作性强、运行成本低、易维护、生态风险小、景观效果好等优势,得到了广泛的研究和应用[5-7]。目前研究表明异养反硝化作用是治理污水最彻底且效果最好的方法[8],但需添加足够有机碳源如甲醇、乙醇、葡萄糖等充当电子供体才能充分发挥反硝化脱氮作用[9-10]。在多数自然水体中,一般生态浮床因缺乏足够碳源抑制反硝化细菌的生长,从而影响脱氮效果。因此本文对生态浮床进行了改良,且在前期试验中,验证了该工艺具有较好的脱氮效果。同时针对以往浮床植物研究多集中于种类筛选、组合以及不同季节处理效果[11-16],本文研究了组合型生态浮床不同介质组合情况对水体净化贡献率及动力学特征,分析浮床周年运行规律,从而为湖泊、水库、河流等的富营养化控制和水质改善提供理论依据和技术支撑。
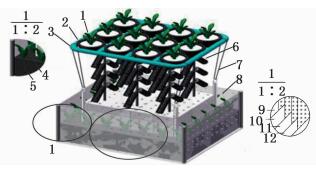
1 材料与方法 1.1 浮床系统主要介质构建组合型生态浮床工艺由3部分组成 (图 1),上层:挺水植物美人蕉 (Canna indica L.);中层:生物挂膜基质与生物碳源;下层:填料沉箱与沉水植物。
|
图 1 立体组合型生态浮床
Fig. 1 A three-dimensional modular ecological floating bed
1.挺水植物;2.篮子;3.浮床;4.沉水植物;5.淤泥;6.微生物生长介质;7.尼龙绳;8.沉箱;9.稻草调料仓;10.煤渣调料仓;11.玉米芯调料仓;12.活性沸石调料仓 1.Emerged plant; 2.Basket; 3.Floating bed; 4. submerged plants; 5.Sludge; 6.The media of microbial propagation; 7.nylon rope; 8.Caisson; 9.The bin of straw; 10.The bin of coal; 11.The bin of corncob; 12.The bin of natural zeolite |
上层:由直径12 mm的PVC塑料管构建浮床支架,面积约600 mm×500 mm,于浮床上塑料篮内种植挺水植物美人蕉 (Canna indica L.) 幼苗[株高 (13.57±0.55) cm,鲜重 (8.94±1.52) g/株,每丛6株]。中层:生物挂膜基质由高分子纤维绳和纤维网片组成,新型生物碳源为9束玉米芯[整根,约 (26.54±1.51) g]上下排列悬挂于高分子纤维绳上,每束4组玉米芯,每组2个,用以形成高效生物膜净化区。下层:填料沉箱采用多孔有机玻璃,沉箱700(长) mm×600(宽) mm×420(高) mm,填料仓为400 mm (长)×125 mm (宽)×420 mm (高)。填料沉箱外围沉水植物槽宽100 mm,槽底覆150 mm厚底泥,沉水植物为苦草[Vallisneria natans (Lour.) Hara,共22株,(6.24±0.38) g/株,长度方向6株,宽度5株]。下层4个填料沉箱内分别放置玉米芯 (整根,0.6 kg/包),煤渣2.2 kg/包,稻草0.17 kg/包,活化沸石4.2 kg/包,各4包 (尺寸10 mm×10 mm)。其中玉米芯、煤渣、稻草购于上海浦东新区泥城农作物中心,沸石购于上海泰坦科技股份有限公司,填料沉箱距实验池底60 mm。
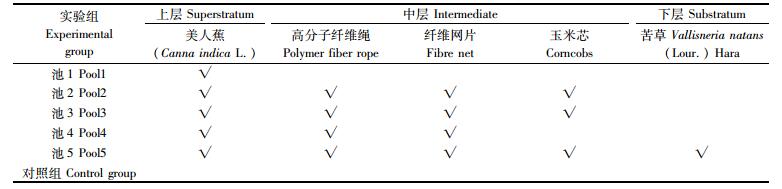
1.2 实验设计实验于2014年1月—12月在上海海洋大学科技园中试基地温室内进行,室内温度维持在15~20 ℃之间。受试水体采自上海奉贤奉城工业园区受污的海淀河[TN (16.10±0.27) mg/L,NH4+-N (7.97±0.05) mg/L,pH (8.27±0.22)]。实验池为880 mm (长)×880 mm (宽)×900 mm (深),冬季采用加热棒 (500 kW,每池2根) 控制水温在20 ℃左右;自然光照;水流采用微型曝气器缓慢释放气泡。共设6个实验池,其中1个对照组 (表 1)。将组合型生态浮床系统按实验设计放入6个实验池 (表 1)。为补充因取样及蒸发损耗水体,每周日及采样后用虹吸法添加受试水体至原始水位高度。
|
表 1 实验水池主要布置状况 Tab.1 The main condition of experimental ponds |
水样采自距浮床边200 mm,水面下200 mm处。采用国家标准方法[17]对其TN、NH4+-N进行测定,氨氮 (NH4+-N):纳氏试剂比色法 (GB 7479—87);总氮 (TN):碱性过硫酸钾消解紫外分光光度法 (GB 11894—89),所用仪器均为T6新世纪紫外可见分光光度计 (北京普析通用仪器有限责任公司)。每月12日早8:00取样,24 h小时内检测分析,实验从2014年1月12日开始,历时12个月。
1.4 数据处理与分析实验所得数据为“算术平均值±标准差”(Mean±SD),用单因素方差分析 (One-way ANOVA),选用LSR多重比较法比较均值之间的差异显著性,显著性水平为P < 0.10,采用Excel 2003制图,利用PASW Statistics18.0、origin 8.0软件进行数据分析。
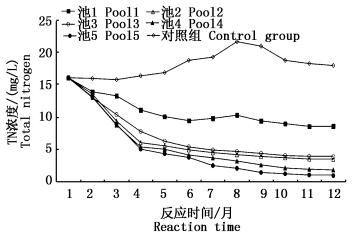
2 结果与分析 2.1 水体TN浓度的变化由图 2可知,受试水体起始总氮为 (16.10±0.27) mg/L, 前4个月各实验组总氮下降幅度较大,其中池5下降幅度最大,降至 (5.04±0.16) mg/L,中期后各组下降幅度逐步趋于稳定。由图 3发现,各实验组间梯度变化明显,因此该工艺中不同介质对总氮削减贡献度不同。池1和池2 TN浓度变化呈显著性差异,可见中层介质对水体TN削减效果明显。池3、池4较池5,TN浓度变化在前3个月内差异性不显著 (P > 0.10),4月以后三者的下降幅度呈显著性差异 (P < 0.10),说明浮床中层以玉米芯和人工纤维棉丝为载体附着的生物膜对水体有很好的净化能力。7月至8月,对照组水体TN浓度显著上升 (P < 0.10),9月后缓慢下降并稳定,且稳定后浓度高于实验初始时TN浓度。这与夏季因高温蓝藻和浮游生物生物量增加有关。
|
图 2 总氮 (TN) 质量浓度变化
Fig. 2 The changes of TN during experiment period
|
|
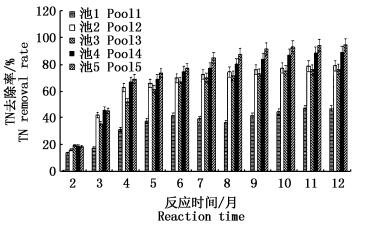
图 3 实验组总氮 (TN) 去除率
Fig. 3 Comparison of TN removal rate
|
由图 3可知,该工艺对水体总氮去除动力学分3个阶段:初期阶段 (<31 d),各实验组对水体TN去除效率较低;反应阶段 (31~120 d),不同实验组对水体TN去除率随反应时间延长而显著增加 (P < 0.10);稳定阶段 (120~334 d),随着反应时间延长,各实验组对水体TN的去除率增加不显著 (P > 0.10)。由单一挺水植物组成的浮床脱氮能力最差。池3、池4与池5相比可知,中层仅单一玉米芯或高分子纤维膜组脱氮效果不及二者均具备组。上、中、下组合浮床比上、中层组合浮床对TN去除能力强。池1与池2相比得出中层对TN去除贡献率为37.63%±2.2%,其中纤维组合贡献率为8.07%±1.31%,玉米芯贡献率为20.12%±0.91%;池2和池5相比可知TN去除过程中下层的贡献率为23.82%±1.8%,而上层对水体TN去除的贡献度在本次实验组无法直接获得,根据各实验组的数据推测上层的贡献率约为15.61%±1.2%。由此可知中层在水体TN的去除过程中贡献率最大,即中层微生物介质在脱氮过程中作用最大。
表 2可知各实验组削减指数模型的拟合度较高,说明TN浓度随时间的延长较初期阶段降低显著 (P < 0.10),随时间增加降低到一定浓度,并保持稳定状态。而对照组TN浓度先升高,再缓慢下降至一稍高浓度,并保持稳定。

|
表 2 总氮 (TN) 削减模型 Tab.2 Models of TN reduction |
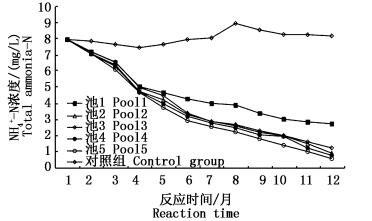
由图 4可知,受试水体NH4+-N起始浓度为 (7.97±0.05) mg/L,11个月后NH4+-N浓度明显下降,其中池5去除率高达93.0%±0.34%,效果最佳,这与浮床中、下层微生物介质所富集的菌群有较大关系。实验初期各实验组NH4+-N浓度下降幅度差异性不显著 (P>0.10) 的主导原因是挺水植物根系微生物群将水体中NH4+-N转化为自身生长所需物质。中后期NH4+-N的变化趋于平稳,且与对照组差异明显 (P < 0.10),说明浮床结构对NH4+-N有较好的去除效果。初期阶段各实验组间NH4+-N变化差异不大 (P>0.10),中后期实验组变化梯度明显大于对照组 (P < 0.10),可知浮床中、下层富集的硝化反硝化菌群对水体NH4+-N的去除具有一定作用。由池1知由单一美人蕉构建的浮床对水体氨氮也有一定去除效果,这与韩锡荣等[18]用美人蕉-陶粒基质组合式生态浮床工艺来削减水体中NH4+-N的效果相近。
|
图 4 氨氮 (NH4+-N) 质量浓度变化
Fig. 4 The changes of NH4+-N during experiment period
|
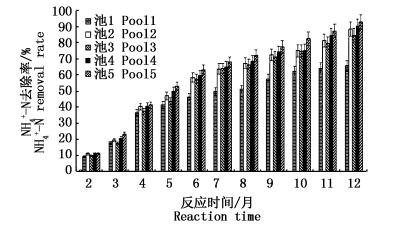
各实验组对水体NH4+-N的平均去除率达到80%±3.4%,去除效果较好。其中池5去除率最高,高达93.0%±1.6%(图 5)。实验组浮床对水体NH4+-N的去除动力学过程分为3个阶段:第一阶段 (<31 d),各实验组对水体NH4+-N去除率不明显 (P >0.10);第二阶段 (31~90 d),各实验组对水体NH4+-N去除率随反应时间延长表现出显著性差异(P < 0.10);第三阶段 (90~334 d),各实验组对水体NH4+-N去除率随着反应时间延长而缓慢增加。由各实验组曲线表明单一挺水植物组成的浮床水体NH4+-N的削减能力最差。池2、池3、池4相比可知,中层仅单一玉米芯或高分子纤维膜组去除NH4+-N的效果低于二者均具备组(P < 0.10)。各实验组相比可知,上、中、下组合浮床比上、中层组合浮床对NH4+-N的削减能力强。由池1、池2和池5对比可知组合浮床中层在削减水体NH4+-N的过程中贡献率最大,为40.75%±3.2%,其中由池3、4、5可知,纤维组合贡献率为10.56%±1.31%,玉米芯贡献率为25.24%±2.17%,其次为下层,贡献率是31.42%±2.4%,池1和池2对比可知上层贡献率为13.73%±1.4%。
|
图 5 实验组氨氮 (NH4+-N) 去除率
Fig. 5 Comparison of NH4+-N removal rate
|
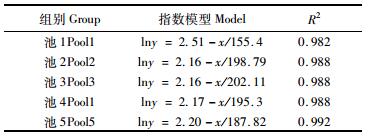
各实验组衰减指数模型的拟合度较高,说明NH4+-N浓度随时间的延长呈衰减指数曲线。即实验初期水体NH4+-N的浓度下降较快 (P < 0.10),到达某一浓度时,下降幅度变的较为缓慢 (P>0.10),直至一较低浓度并保持稳定 (表 3)。
|
表 3 氨氮 (NH4+-N) 削减模型 Tab.3 Models of NH4+-N reduction |
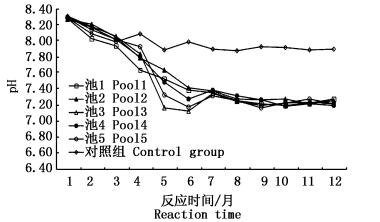
水体pH由实验初期的8.27±0.22下降到7.21±0.14后稳定于此。由于pH变化会导致微环境系统变化,进而影响脱氮细菌的活性,导致去除效率降低 (图 6)。当pH>8时,NH3的蒸发作用占主导,从而会影响氮等营养物质的去除,在酸性和中性条件下,植物根区附近的亚硝化细菌和硝化细菌活动增强,其中硝化作用占主导地位。詹发萃等[19]研究指出,不同pH条件下,凤眼莲的微生物群落活性不同,除氮效率也不同。本实验在4月份时实验组水体的pH稳定在7.21±0.14,营造了较稳定的pH环境条件。可以推测本组合型生态浮床系统能改善和促进水体修复系统内硝化细菌及反硝化细菌等菌群的数量和群落结构的多样性,这与罗佳等[20]的实验结果相似。
|
图 6 pH的变化
Fig. 6 Variations of pH in different enclosures during the experiment
|
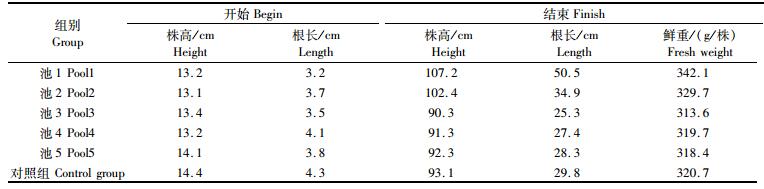
实验阶段挺水植物美人蕉生长状况良好 (表 4)。其中池1美人蕉的生长状况最好 (P < 0.10),即适宜范围内,株丛越多,美人蕉的长势也越好,说明植物的生物量越大,对氮磷的固定能力越强。池1美人蕉的根长最长,池2其次,说明浮床的中下层在一定程度上抑制了美人蕉根部的生长。
|
表 4 浮床挺水植物生长状况 Tab.4 Growth of emergent macrophytes |
诸多研究[21-23]表明选取具有茎状根、须根发达且适宜在潮湿及浅水区生长的美人蕉和根茎短粗、须根发达的多年生挺水宿根草本植物黄菖蒲为浮床植物具有较好的净水效果。本实验选择了盖度较大的美人蕉作为浮床植物,由图 2~5可知取得了较好的实验效果。生态浮床技术去污效果容易受季节和浮床植物量的限制,对于漂浮植物,其只利用了表层水体,对于深度较大的水体,其净化效率很难进一步提高[24-25]。本实验的组合型生态浮床具有上、中、下3层介质,尤其下层可调节入水深度能适应不同的水深,而且这样的组合结构能增强浮床的抗风浪性。组合型浮床的植物载体在劣V类水体中经过12个月的试验周期,试验结束时仍保持良好的状态,也说明本浮床的植物载体具有较高的抗腐蚀性。同时根据图 3和图 5水体的NH4+-N、TN去除率变化,可直观地反映各层之间协同综合作用的净水效果以及浮床各层的贡献率概况,上层为15.61%±1.2%,中层37.63%±2.2%,下层在23.82%±1.8%左右。池2、池5反映出下层沉箱外围的淤泥苦草与内围的填料仓在协同作用的情况下,能达到削减部分总氮的目的。池5除氮效果最好说明:通过上层挺水植物和中层玉米芯与人工纤维绳两者组合与下层沉箱部分立体组合式作用,能大幅削减TN,这表明浮床中层与下层相互结合,有利于构建同步硝化反硝化环境,有助微生物群落生存,增强水体净化能力。
3.2 植物与微生物协同脱氮机理由图 2和图 4 TN、NH4+-N的浓度变化可知,实验初期各实验组呈较大下降幅度,与空白对照组差别明显 (P < 0.10)。推测初始阶段脱氮主要依靠浮床上层挺水植物根系的吸收,可能有两方面的原因:一是植物本身根系比表面积大,在水中形成密集网,有助吸附水体大量悬浮物,并逐渐在根系表面形成生物膜。而膜中的微生物菌群又可通过吞噬和代谢水体中有机污染物转化为自身营养物质。二是植物根系分泌物对藻类生长具有杀伤力,可抑制藻类恶性繁殖。后期池1、池2、池3和池4的数据表明中层玉米芯与人工纤维膜脱氮效果显著 (P < 0.10),下层沉箱外围部分淤泥与苦草结合,加之沉箱内围填料仓的协同作用,也可有效脱氮,说明中下层共同营造的环境更有利于微生物生长,进而消解水体污染物。张志勇等[26]结果表明,在一定范围内随着氮浓度负荷增加,浮床对氮去除率亦增加。而本实验中,组合型生态浮床TN去除率高达94.2%±0.9%,NH4+-N去除率高达93.0%±3.4%,与实验初期受试水体水质较差有着较大关系。
3.3 水体生态系统的恢复性浮床经一年实验运行,水体pH由最初偏碱性8.27±0.22降至中性,并稳定在7.21±0.14左右。王端超等[27]结果表明,浮床区以硅藻门为主,对照区以绿藻门为主。生态浮床使得重富营养化水体中的绿藻数量在浮床区得到了控制,说明生态浮床对水体的富营养化具有抑制作用。本组合生态浮床在为微生物新陈代谢提供碳源的同时也为微生物的生长活动提供了场所,利于水体生态系统的构建。同时数据 (表 4) 显示挺水植物在试验阶段长势良好,表明该组合浮床对挺水植物生长无影响,对浅滩生态的恢复起到促进作用。
4 结论(1) 通过构建上、中、下组合形式的浮床,利用上层挺水植物根茎叶吸收、降解和富集污染物的基础上,中、下层填料巨大表面积更易于微生物的附着生长,便于形成生物膜,从而有效提高了水体生态修复效率。本组合型生态浮床不仅缩小占地面积且能适应范围更广的水深,同时节约了管理成本,利于生态型城市的建设,也为以城市河流水系和居住区人工水景为代表的水生生态系统的恢复和建设提供了依据。
(2) 本组合型生态浮床脱氮效果明显。经过12个月检测,本组合型生态浮床脱氮效果显著。其中浮床上层贡献率15.61%±1.2%,中层37.63%±2.2%,下层23.82%±1.8%,说明浮床系统中层介质对总氮与氨氮的降解能力占主导地位。实验组NH4+-N的平均去除率为93.0%±3.4%,而池5组去除效果最佳,TN去除率最高达94.2%±0.9%。由各实验组削减NH4+-N和TN的去除动力学曲线得出各削减模型均为不同程度的衰减指数曲线。
(3) 实验结束时,浮床内外的整体结构均处于较好状态,挺水植物的载体并未有被腐蚀的迹象,填料玉米芯也未腐烂。表明本组合型生态浮床能适应更长周期的运行。
(4) 本组合型生态浮床在河流、湖泊等自然水体中运行时浮床规格与排列密度以及外界环境温度、水流风浪、气候变化等因素对浮床净化效果影响等均有待深入研究。
| [1] | CHANGJ J, WUS Q, DAIY R, et al. Nitrogen removal fromnitrate-laden wastewater by integratedvertical-flow constructed wetlandsystems[J]. Ecological Engineering, 2013, 58: 192–201. DOI:10.1016/j.ecoleng.2013.06.039 |
| [2] | ZHAO F L, XI S, YANG X E, et al. Purifying eutrophic riverwaters with integrated floating island systems[J]. Ecological Engineering, 2012, 40: 53–60. DOI:10.1016/j.ecoleng.2011.12.012 |
| [3] | ZHUA H, YAN B X, XU Y Y, et al. Removal of nitrogen and COD in horizontal subsurface flow constructed wetlands under differentinfluent C/N ratios[J]. Ecological Engineering, 2014, 63: 58–63. DOI:10.1016/j.ecoleng.2013.12.018 |
| [4] |
王芳, 张汇文, 吴国华, 等. 生物质碳源组合型生态浮床系统脱氮效果研究[J].
环境工程学报, 2014, 8(8): 3099–3106.
WANG F, ZHANG H W, WU G H, et al. Study on nitrogen removal effect of biomass carbon release combined ecological floating bed system[J]. Chinese Journal of Environmental Engineering, 2014, 8(8): 3099–3106. |
| [5] | LI X N, SONG H L, LI W, et al. An integrated ecological floating-bed employing plant, freshwater clam and biofilm carrier for purification of eutrophic water[J]. Ecological Engineering, 2010, 36(4): 382–390. DOI:10.1016/j.ecoleng.2009.11.004 |
| [6] | HUANG L F, ZHUO J F, GUO W D, et al. Tracing organic matter removal in polluted coastal waters via floating bed phytoremediation[J]. Marine Pollution Bulletin, 2013, 71(1/2): 74–82. |
| [7] | SUN L P, LIU Y, JIN H. Nitrogen removal from polluted riverby enhanced floating bed grown canna[J]. Ecological Engineering, 2009, 35(1): 135–140. DOI:10.1016/j.ecoleng.2008.09.016 |
| [8] | PARK J B K, CRAGGS R J, SUKIAS J P S. Removal of nitrate and phosphorus from hydroponic wastewater using a hybrid denitrification filter (HDF)[J]. Bioresource Technology, 2009, 100(13): 3175–3179. DOI:10.1016/j.biortech.2009.01.036 |
| [9] | STRONG P J, MCDONALD B, GAPESD J. Enhancing denitrification using a carbon supplement generated from the wet oxidation of waste activated sludge[J]. Bioresource Technology, 2011, 102(9): 5533–5540. DOI:10.1016/j.biortech.2010.12.025 |
| [10] | HOCAOGLU S M, INSEL G, COKGOR E U, et al. Effect of sludge age on simultaneous nitrification and denitrification in membrane bioreactor[J]. Bioresource Technology, 2011, 102(12): 6665–6672. DOI:10.1016/j.biortech.2011.03.096 |
| [11] |
马立珊, 骆永明, 吴龙华, 等. 浮床香根草对富营养化水体氮磷去除动态及效率的初步研究[J].
土壤, 2000, 32(2): 99–101.
MA L S, LUO Y M, WU L H, et al. Dynamics and efficiency of nitrogen and phosphrous removal from eutrophicated water bodies by Vetiveria zizanioids(L.) Nash on floating-beds[J]. Soils, 2000, 32(2): 99–101. |
| [12] |
司友斌, 包军杰, 曹德菊, 等. 香根草对富营养化水体净化效果研究[J].
应用生态学报, 2003, 14(2): 277–279.
SI Y B, BAO J J, CAO D J, et al. Purification of eutrophicated water body by Vetiveria zizanioids[J]. Chinese Journal of Applied Ecology, 2003, 14(2): 277–279. |
| [13] |
李欲如, 操家顺. 冬季低温条件下浮床植物对富营养化水体的净化效果[J].
环境污染与防治, 2005, 27(7): 505–508.
LI Y R, CAO J S. Purification effects of floating bed plants on eutrophic water body under low temperature in winter[J]. Environmental Pollution & Control, 2005, 27(7): 505–508. |
| [14] |
付子轼, 邹国燕, 宋祥甫. 适应近郊污染河道治理工程的生态浮床植物筛选[J].
上海农业科技, 2007: 19–20.
FU Z S, ZOU G Y, SONG X F. Study on the filter of ecological floating bed plants to apply to suburban pollution river training works[J]. Shanghai Agricultural Science and Technology, 2007: 19–20. |
| [15] |
孙连鹏, 刘阳, 冯晨, 等. 不同季节浮床美人蕉对水体氮素等污染物的去除[J].
中山大学学报 (自然科学版), 2008, 47(2): 127–130.
SUN L P, LIU Y, FENG C, et al. Removal of Nitrogen from Water Bodies by Canna Floating Bed in Different Seasons[J]. Acta Scientiarum Naturalium Universitatis Sunyatseni, 2008, 47(2): 127–130. |
| [16] |
马庆, 孙从军, 高阳俊, 等. 滇池入湖河口生态浮床植物筛选研究[J].
生态科学, 2007, 26(6): 490–494.
MA Q, SUN C J, GAO Y J, et al. Study on the selecting the species of macrophytes for the ecological floating rafts in one of estuaries of DianchiLake[J]. Ecological Science, 2007, 26(6): 490–494. |
| [17] |
国家环保总局. 水和废水监测分析方法[M]. 4版. 北京: 中国环境科学出版社, 2002.
SE PA. Water and wastewater monitoring and analysis methods[M]. 4th ed. Beijing: China Environmental Science Press, 2002. |
| [18] |
韩锡荣, 黄浩, 周大众, 等. 低温条件下组合式生态浮床系统净化微污染水体的特性研究[J].
节水灌溉, 2015: 76–81.
HAN X R, HUANG H, ZHOU D Z, et al. Performances of an integrated ecological floating bed for purification of micro-polluted waters under low temperature condition[J]. Water Saving Irrigation, 2015: 76–81. |
| [19] |
詹发萃, 邓家齐, 夏宜琤, 等. 凤眼莲根区异养细菌的群落特征与异养活性的研究[J].
水生生物学报, 1993, 17(2): 150–156.
ZHAN F C, DENG J Q, XIA Y C, et al. Studies on community characteristics and heterotrophic activity of heterotrophic bacteria from root-zone of water hyacinth[J]. Acta Hydrobiologica Sinica, 1993, 17(2): 150–156. |
| [20] |
罗佳, 韩士群, 严少华, 等. 生态浮床对巢湖双桥河口水体细菌群落结构的影响[J].
南京农业大学学报, 2013, 36(2): 91–96.
LUO J, HAN S Q, YAN S H, et al. Effect of the ecological floating bed on the bacterial community in the Shuangqiao estuary of Chaohu Lake[J]. Journal of Nanjing Agricultural University, 2013, 36(2): 91–96. |
| [21] |
孙远奎. 生态浮床技术净化城市景观水体的试验研究[D]. 济南: 山东建筑大学, 2010.
SUN Y K. Study on the scenic water purification by ecological floating bed[D]. Jinan:Shandong Jianzhu University, 2010. |
| [22] |
郑剑锋. 临江河回水区富营养化预测及生态浮床治理技术研究[D]. 重庆: 重庆大学, 2010.
ZHENG J F. Study on eutrophication forecasting in Linjiang River backwater region and ecological floating bed technology[D]. Chongqing:Chongqing University, 2010. |
| [23] |
解岳. 城市富营养化景观水体的植物修复机理及现场试验研究[D]. 西安: 西安建筑科技大学, 2011.
XIE Y. Study on field experiment and mechanism of eutrophic landscape water restoration using plants[D]. Xi'an:Xi'an University of Architecture and Technology, 2011. |
| [24] | BROWNING K, GREENWAY M. Nutrient removal and plant biomass in a subsurface flow constructed wetland in Brisbane, Australia[J]. Water Science and Technology, 2003, 48(5): 183–189. |
| [25] | LANGERGRABER G. The role of plant uptake on the removal of organic matter and nutrients in subsurface flow constructed wetlands:a simulation study[J]. Water Science and Technology, 2005, 51(9): 213–223. |
| [26] |
张志勇, 刘海琴, 严少华, 等. 水葫芦去除不同富营养化水体中氮、磷能力的比较[J].
江苏农业学报, 2009, 25(5): 1039–1046.
ZHANG Z Y, LIU HQ, YAN S H, et al. Comparison of the removal ability of nitrogen and phosphorous by water hyacinth (Eichhornia crassipes) in differently eutrophic water[J]. Jiangsu Journal of Agricultural Sciences, 2009, 25(5): 1039–1046. |
| [27] |
王端超, 何淑琼, 王娟, 等. 冬季生态浮床对浮游藻类数量及生物多样性的影响[J].
环境工程学报, 2014, 8(9): 3785–3790.
WANG D C, HE S Q, WANG J, et al. Influence of ecological floating bed on density and biodiversity of planktonic algae in winter[J]. Chinese Journal of Environmental Engineering, 2014, 8(9): 3785–3790. |
2. Engineering Research Center for Water Environment Ecology in Shanghai, Shanghai Ocean University, Shanghai 201306, China
 2017,
Vol. 26
2017,
Vol. 26


