2. 中国水产科学研究院南海水产研究所, 广东 广州 510300;
3. 中国水产学会, 北京 100122;
4. 农业部南海渔业资源环境科学观测试验站, 广东 广州 510300;
5. 中国海监威海市文登区大队, 山东 威海 264400
为了恢复天然水域渔业资源种群数量,近年来沿海地区大规模开展了渔业资源增殖放流活动,花尾胡椒鲷(Plectorhinchus cinctu)逐渐成为主要放流鱼种之一。对花尾胡椒鲷进行标记跟踪等行为研究,是确定增殖放流数量与选取海域的当务之急。从技术手段来看,增殖放流标记方式有数字条码标记、体外标签、声频/无线电组合追踪标记等[1],前两种标记方式需要通过鱼类回捕来回收标志,第三种可分为电磁波生物遥测和超声波生物遥测[2]。由于电磁波在水中传播衰减系数较高,因此电磁波接收测量装置需要设置在水面以上,同时要求被跟踪生物体周期性浮出水面,发射电磁波进而对其遥测,适用对象主要以海洋哺乳类动物(海豚、鲸)和鳍足类(海豹、海狮)为主[3, 4]。而声波在水中传播衰减较小,超声波生物遥测法可将声波接收器设置于水中,因此更加适应海洋生物的动态跟踪。目前,国外使用该方法先后跟踪研究了鲑鳟科鱼类[5, 6]、大西洋鳕(Gadus morhua)[7, 8]、西鲱(Clupea sprattus)[9, 10, 11]、金枪鱼(Thunnus thynnus)[12, 13, 14, 15]、红方头鱼[16, 17, 18]及鲨鱼[19]的洄游、产卵与栖息等行为习性,国内实际观测仅有长江水产所危起伟[20]等人对中华鲟洄游进行过跟踪调查。现阶段采用的超声波标志体积大,常限于应用在体型较大的鱼类,利用小型超声波标志跟踪研究体型较小鱼类仍未见报道。
1 材料与方法 1.1 样品鱼选取本实验于2014年11月5-9日在中国水产科学研究院南海水产研究所深圳基地实验池( 70 m×70 m×4 m )内进行,实验池内平均表层水温25.5 ℃,平均盐度28.55,实验样品花尾胡椒鲷选取游动较为活跃的个体,以减小携带标志后对鱼体的影响。实验中花尾胡椒鲷体长为33.5 cm,体质量为970 g。
1.2 超声波标志跟踪发射-接收系统超声波标志测量系统主要由发射器(超声波标志)和接收装置组成。
本研究使用日本FUSION有限公司FPX-1030-60P50型编码标志,发射频率62.5 kHz,声源级155 dB re1μPa;标志外壳使用透明耐压亚克力管,外观尺寸直径10 mm,长35 mm,空气中重量4.5 g,水中重量1.8 g。使用31bit M序列伪随机编码对发射声波进行相位调制后发射传送,标志发射周期性脉冲信号,可以对32个标志进行编码。发射周期可调,对于1 s的设定值,标志可以连续工作时间为4 d(10 s间隔可以工作40 d);标志自身带有压力传感器,压力信号可以通过改变发射脉冲的内部间隔(标志一次发射两个脉冲)来实现,通过测量脉冲信号的内部间隔换算推定深度。
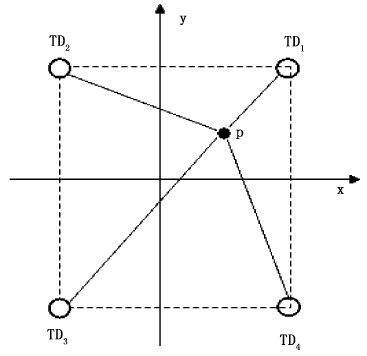
标志接收使用日本FUSION有限公司4通道FRX-4002型接收装置,该装置通过25 m电缆(可延长)连接4个接收器,可以同时跟踪32个编码标志,跟踪最大距离1 000 m左右。接收装置通过USB与电脑及存储装置连接,进行4通道接收标志信号的控制显示和数据收录。超声波位置测量系统示意图如图1所示。
|
图1 位置测量系统 TD1-TD4为声波接收器,P点为跟踪的标志。the TD1 - TD4 for acoustic receiver,point P as a sign of the trace. Fig.1 Positioning system |
声速是水平位置计算中必不可少的参数,因此要对实验池的声速进行测量。声速采用CTD探测后由温度、盐度、深度数据计算得出。由于实验池面积较小,水深为4 m,CTD升降沉放在实验池中心位置进行,并由实验员手动操作,测量声速为1 527.95 m/s。
1.4 标志放流跟踪方法实验中,将接收装置的4个接收换能器固定在实验池四周,4个接收器放置成正方形,接收器放在水下1 m处。标志携带方式有背鳍挂置和手术埋置两种,本实验采用手术将标志埋藏于花尾胡椒鲷腹部,用磁铁开关打开标志,设置声波脉冲发射周期为5 s。手术在麻醉条件下快速完成,减少对鱼类自身的损伤。最后将手术后的花尾胡椒鲷在实验池中放养,通过4个接收器接收并保存超声波标志的发射信号。
1.5 测位计算方法测位方法由垂直测位和水平测位两部分组成。
垂直坐标的测位方法中,由于标志自身带有压力传感器,压力信号可以通过标志发射信号的内部时间间隔来改变,进而测算深度数据。深度D(单位m)计算公式为:

水平坐标的测位方法中,根据长基线测位法(接收器之间的距离要远大于声波的波长),使用标志发出声波到达各个接收器之间的时间差来进行计算。如图1所示,假设标志P点的坐标为P(xp,yp),接收器的坐标为TDj(xj,yj)(j=1-4),标志P点到达接收器TD2、TD3和TD4的时间与到TD1的时间差为:
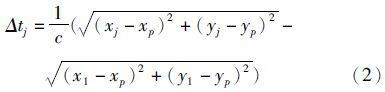
在实际测量中,标志的推测点P1的坐标为P1(xp1,yp1),P1到达接受器TD2、TD3和TD4的时间与到达TD1的时间差为:
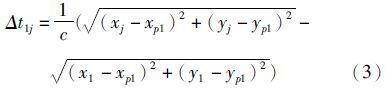
由于实际测量时超声波标志具有一定深度,因此Δt1j是斜距离时间差,而Δtj是Δt1j在xy平面上的投影。所以可以使用最小二乘法来计算推定P1(xp1,yp1)。具体的方法是先给出Δtj和Δt1j的差值满足小于等于给定值δ条件,

然后使用牛顿-高斯方法进行回归计算,解出x
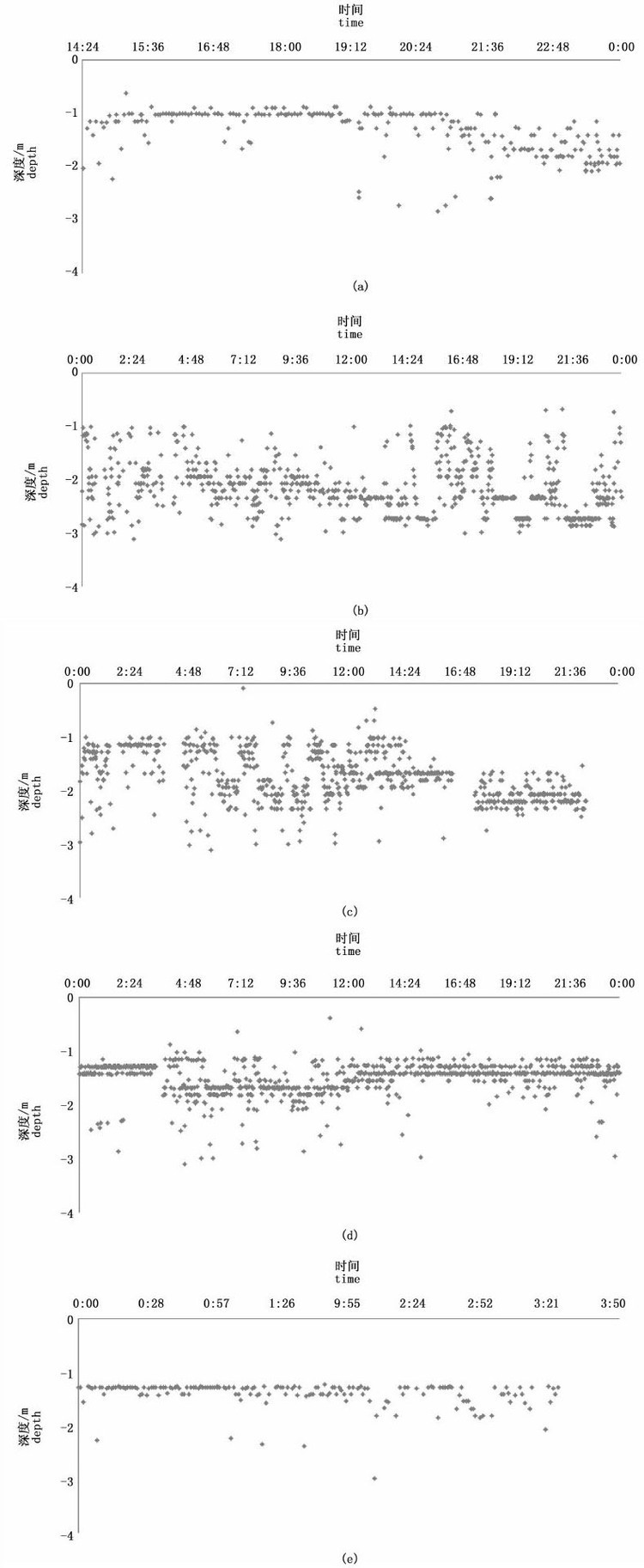
花尾胡椒鲷深度接收数据由2014年11月5日14:20起至11月9日3:20为止,深度变化如图2所示,图2中(a)-(b)分别为11月5日-9日深度分布图。从5 d的整体趋势看,当花尾胡椒鲷放流后在前5个小时内一直在中上层水域,主要原因是花尾胡椒鲷刚刚经过麻醉与手术,身体机能未完全恢复以及处于新水域环境,因此未进行大范围上下游动。结合水平数据会发现,此过程中花尾胡椒鲷的水平游动也仅在几米范围内。随后的观察中花尾胡椒鲷在中层水域进行上下游动,具体分析如下。
|
图2 花尾胡椒鲷的垂直分布 Fig.2 Vertical distribution of Plectorhinchus cinctu |
在11月5日19:20至11月7日夜间,花尾胡椒鲷处于中间水层游动,上下变化幅度为2 m左右,此过程中游动无明显昼夜规律,但在3~4 h的上下大范围游动后会存在2~3 h的深度稳定游动。初步判断这一阶段是其身体机能恢复期,在适应新环境而大规模游动一段时间后身体需要休息。
11月7日夜间至11月9日3:00花尾胡椒鲷的活动范围为1~2.5 m,此时活动较有规律,主要是在1~2 m水层分层游动,上层集中于1.3 m,下层集中于1.8 m,出现时间为11月8日3:00后,持续到12:00后恢复到1.3 m水层;11月9日3:00后发现其游动深度又出现下降趋势,初步判断深度下降期间是需要摄食的结果,因此向较深水域游动并持续一段时间。
由于跟踪时间较短,花尾胡椒鲷的昼夜活动规律不是十分明显,但能看出花尾胡椒鲷具有分层游动规律,放流前期主要集中在中上水层游动,上下波动较大,波动范围有2 m,后期集中在中层游动,深度较稳定。
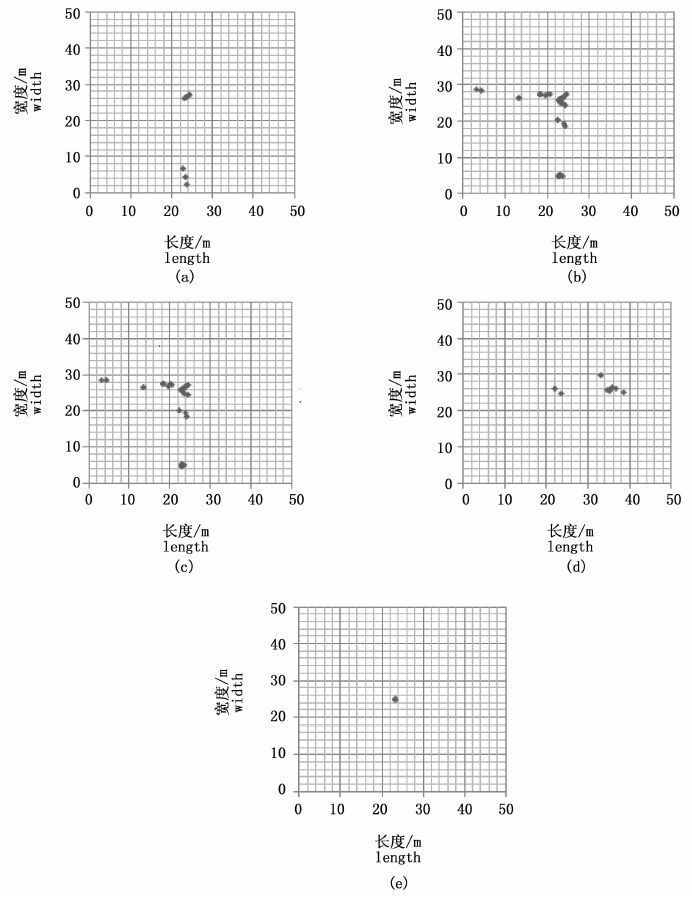
2.2 水平变动分析图3所示为花尾胡椒鲷连续5 d的水平位置分布。本文对水平分布数据进行简单分析,超声波标志发射信号同时被4个接收器接收,将这些接收信号处理后得出水平数据,然后根据实际实验池的大小去除偏差数据,最后剩余的为有效水平数据。实验中存在少量干扰信息,主要由接收器距离池壁较近,受多路径波的干扰引起。
|
图3 花尾胡椒鲷的水平分布 Fig.3 Horizontal distribution of Plectorhinchus cinctu |
图3(a)所示,靠近池壁处为花尾胡椒鲷放入实验池中的位置,可见花尾胡椒鲷由放流处渐渐游到实验池中间,随后在实验池中部小范围游动,主要是身体机能恢复阶段,与时间进行对照,花尾胡椒鲷在22:00左右又游到放流位置,且深度下降,初步判断是进行摄食。
图3(b)、(c)表明,花尾胡椒鲷分别以实验池中部为基准,向3个方向进行扩散游动,处于对新环境的探索中。同样与时间进行对照,夜间花尾胡椒鲷都会在放流初始位置附近游泳,深度下降,进行摄食。
图3(d)所示,花尾胡椒鲷垂直与水平数据在时间上不具有同时性,因此无法判断摄食深度下的水平位置,但仍可得出花尾胡椒鲷以中心位置为准向实验池边缘游动。图3-(e)为11月9日0:00到3:00花尾胡椒鲷的水平分布,由于时间较短,花尾胡椒鲷仍处于实验池中间位置,无法说明问题。结合所有垂直与水平数据得出,花尾胡椒鲷处于中间水层并且进行规律稳定的分层游动时,其水平位置都稳定分布于实验池中部。
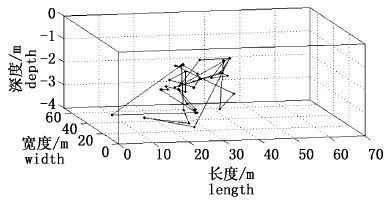
2.3 三维位置变化图4所示为花尾胡椒鲷连续5 d的三维位置变化图,由于已有深度与水平数据部分在时间上存在差异性,需要选择同一时间下水平与深度数据作为有效三维数据。另外,本次实验数据采用编程来选取4个直接波,由于水池中多路径波较多,手动选取效果会更好。如图4所示,花尾胡椒鲷运动轨迹仅限于实验池中部,基本不向池壁游动,主要活动范围为中间水层,且活动范围较小,摄食时由原始路线返回,深度降低。
|
图4 花尾胡椒鲷三维位置分布 Fig.4 Three-dimensional position distribution of Plectorhinchus cinctu |
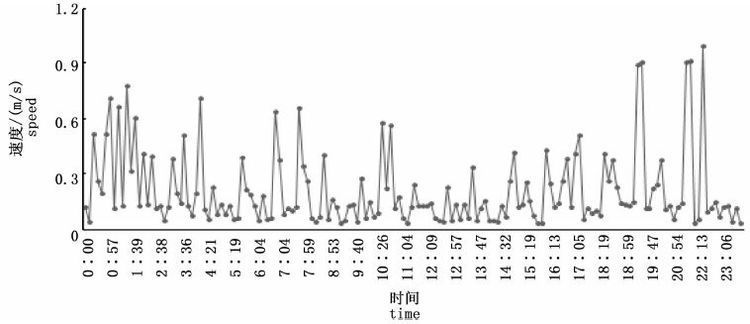
由连续5 d的垂直与水平数据得出,花尾胡椒鲷在11月8日活动规律性较明显,因此选取当日数据对其进行垂直方向的平均游泳速度计算分析,图5为花尾胡椒鲷一天内的平均游泳速度分布图。
|
图5 花尾胡椒鲷速度变化 Fig.5 Speed changing of Plectorhinchus cinctu |
图5表明,花尾胡椒鲷最大平均游泳速度在夜间出现为1 m/s,最小值为0.1 m/s左右,并均匀分布于全天中。除此,花尾胡椒鲷夜间平均速度明显高于白天,且变化波动较大,白天平均速度较低且变化较小。
综上可见,花尾胡椒鲷在夜间游回放流位置,并且深度降低进行摄食,同时游泳速度增大。
3 讨论本文在国内将超声波标志技术尝试性地应用到小型放流鱼类的跟踪研究中,从某种意义上取得了一定的成绩,结合日后跟踪研究,要考虑以下几点。
3.1 标志牌对花尾胡椒鲷正常生活的影响解决这一问题是超声波标志放流技术成功的前提条件。近年来,一些学者提出标记牌在空气中的重量不能超过标记生物体重的0.025倍[22, 23]。本实验中标志在空气中重4.5 g,是鱼体重量的0.005倍,因此标志对鱼体影响较少。有关研究表明,手术和标志对水生生物的身体及行为基本没有影响,例如RILLAHAN等在实验室中对大西洋鳕鱼[24, 25]进行标志植入,并观察其手术前后的行为差异,发现标志植入并未对大西洋鳕鱼的游泳及摄食行为造成影响。同时也有关于手术对鳙[26]影响的研究,其结果表明影响较小。但在本次实验中,分析前3天的数据,并无明显昼夜规律,初步判断是手术及新环境对花尾胡椒鲷产生影响,因此有专家提出对手术后的花尾胡椒鲷在水箱中暂养一段时间,待其恢复后放流,一般暂养时间为2~3 d。但是HART和SUMMERFELT[27]指出至少两种鱼在室外实施手术后立即放流到自然栖息环境中,要比手术后在水箱中暂养再放流的效果更好。对于本实验最好的改进方法是将花尾胡椒鲷在正常情况下在实验池中放养一段时间,在适应水池环境后手术并立即放回水池,进行跟踪观察。
3.2 接收系统对小型鱼类跟踪的影响选择合适的接收系统有助于达到较高的监测准确性,同时减少成本。本次实验所采用的接收系统为位置测量系统(Positioning system),通过长基线原理对携带标志鱼类进行跟踪,这种跟踪观测准确性较高,但观测范围有限,不适合大规模外海调查,因此对花尾胡椒鲷的放流跟踪具有局限性。目前国内对中华鲟的跟踪研究中使用舰载追踪系统,即将接收器和GPS放置在快艇上,通过快艇追踪定位,这种方法要求追踪鱼类个体较大。对于花尾胡椒鲷这种小型鱼类的外海放流研究,可以通过监测站或声呐浮标这两种接收系统[28, 29, 30]来实现,监测站费用高且位置受限,而声呐浮标位置选取自由。因此在未来的放流跟踪研究中可适当考虑应用声呐浮标系统以扩大跟踪范围,提高位置精度。
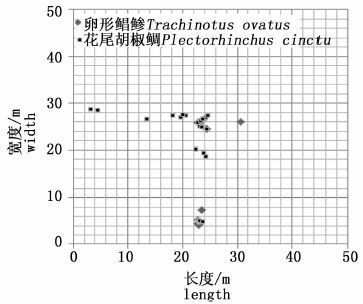
3.3 其他鱼类对花尾胡椒鲷生活的影响有研究表明,花尾胡椒鲷攻击性较强,善食弱小鱼类,也会与体形不相上下的鱼类争夺生存空间,不适合与其他鱼类在同一水域放养。为研究花尾胡椒鲷对其他鱼类在同一活动空间分布上的影响,实验池内同时跟踪了带有标志的卵形鲳鲹(Trachinotus ovatus),其体长为25.1 cm,体质量为587 g。取2014年11月6日花尾胡椒鲷与卵形鲳鲹的水平游动数据,分析得出其水平坐标分布图。如图6所示,两种鱼类在白天由中间水域向两个相反的方向游动,而在傍晚16:00-18:00又从两个方向游回最初放流位置,同时在放流位置底部游动,初步判断是摄食的原因。除此以外,花尾胡椒鲷与卵形鲳鲹在空间分布上具有相异性趋势,但具体规律仍需进一步研究。
|
图6 花尾胡椒鲷与卵形鲳鲹的水平分布 Fig.6 Horizontal distribution of Plectorhinchus cinctu and Trachinotus ovatus |
本文所研究的基于小型声学标记的花尾胡椒鲷的行为特点是:在适应水域环境后,花尾胡椒鲷主要集中在中上层游动且深度变化较小,具有以实验池中部向四周游动的规律,花尾胡椒鲷更适应于活动在实验池中部小范围水域,其夜间游泳速度明显高于白天。本次实验为后续将小型超声波标志应用到鱼体跟踪研究奠定了基础,同时在未来的跟踪研究中应尽量考虑到鱼体对放流环境及携带标志的适应性、放流海域与接收装置接收范围的对应性,及各放流鱼类共同跟踪的合理性,使跟踪效果达到最佳。
| [1] | 陈锦淘, 戴小杰. 鱼类标志放流技术的研究现状[J]. 上海水产大学学报, 2005, 14(4): 451-456. CHEN J T, DAI X J. Current status of fish tagging technology[J]. Journal of Shanghai Fisheries University, 2005, 14(4): 451-456. |
| [2] | 王成友, 危起伟, 杜浩, 等. 超声波遥测在水生动物生态学研究中的应用[J]. 生态学杂志, 2010, 29(11): 2286-2292. WANG C Y, WEI Q W, DU H, et al. Applications of ultrasonic telemetry in aquatic animal ecology: A review[J]. Chinese Journal of Ecology, 2010, 29(11): 2286-2292. |
| [3] | WELCH D W, MELNYCHUK M C, RECHISKY E R, et al. Freshwater and marine migration and survival of endangered Cultus Lake sockeye salmon (Oncorhynchus nerka) smolts using POST, a large-scale acoustic telemetry array[J]. Canadian Journal of Fisheries and Aquatic Sciences, 2009, 66(5): 736-750. |
| [4] | YOKOTA T, MITAMURA H, ARAI N, et al. Comparison of behavioral characteristics of hatchery-reared and wild red tilefish Branchiostegus japonicus released in Maizuru Bay by using acoustic biotelemetry[J]. Fisheries Science, 2006, 72(3): 520-529. |
| [5] | VOEGELI F A, LACROIX G L, ANDERSON J M, et al. Development of miniature pingers for tracking Atlantic salmon smolts at sea[J]. Hydrobiologia, 1998, 371-372: 35-46. |
| [6] | KAMIMURA H, MITSUNAGA Y. Temporal and spatial distributions of Biwa salmon Oncorhynchus masou subsp. by ultrasonic telemetry in Lake Biwa, Japan[J]. Fisheries Science, 2014, 80(5): 951-956. |
| [7] | WROBLEWSKI J S, NOLAN B G, ROSE G A, et al. Response of individual shoaling Atlantic cod to ocean currents on the northeast Newfoundland Shelf[J]. Fisheries Research, 2000, 45(1): 51-59. |
| [8] | RILLAHAN C, CHAMBERS M, HOWELL W H, et al. A self-contained system for observing and quantifying the behavior of Atlantic cod, Gadus morhua, in an offshore aquaculture cage[J]. Aquaculture, 2009, 293(1/2): 49-56. |
| [9] | KYNARD B, SUCIU R, HORGAN M. Migration and habitats of diadromous Danube River sturgeons in Romania: 1998-2000[J]. Journal of Applied Ichthyology, 2002, 18(4/6): 529-535. |
| [10] | PARSLEY M J, WRIGHT C D, VAN DER LEEUW B K, et al. White sturgeon (Acipenser transmontanus) passage at the Dallas Dam, Columbia River, USA[J]. Journal of Applied Ichthyology, 2007, 23(6): 627-635. |
| [11] | ACOLAS M L, ANRAS M L B, VERON V, et al. An assessment of the upstream migration and reproductive behaviour of allis shad (Alosa alosa L.) using acoustic tracking[J]. ICES Journal of Marine Science, 2004, 61(8): 1291-1304. |
| [12] | KLIMLEY A P, HOLLOWAY C F. School fidelity and homing synchronicity of yellowfin tuna, Thunnus albacares[J]. Marine Biology, 1999, 133(2): 307-317. |
| [13] | GUNN T, BLOCK B A. Advances in acoustic, archival and satellite tagging of tunas[M]//BLOCK A B, STEVEN E D. eds. Physiology, Ecology, and Evolution. California: Academic Press, 2011: 167-224. |
| [14] | HONDA K, HOBDAY A J, KAWABE R, et al. Age-dependent distribution of juvenile southern Bluefin tuna (Thunnus maccoyii) on the continental shelf off southwest Australia determined by acoustic monitoring[J]. Fisheries Oceanography, 2010, 19(2): 151-158. |
| [15] | 张平远. 日本将对印度洋金枪鱼资源继续探捕调查[J]. 水产科技情报, 2012, 39(2): 102-103. ZHANG P Y. Japan will continue to explore the resources of the Indian Ocean Tuna fishing survey[J]. Fisheries Science & Technology Information, 2012, 39(2): 102-103. |
| [16] | TAQUET M, DAGORN L, GIRARD J C, et al. Behavior of dolphinfish (Coryphaena hippurus) around drifting FADs as observed from automated acoustic receivers[J]. Aquatic Living Resources, 2007, 20(4): 323-330. |
| [17] | SULAK K J, RANDALL M T, EDWARDS R E, et al. Defining winter trophic habitat of juvenile Gulf Sturgeon in the Suwannee and Apalachicola rivermouth estuaries, acoustic telemetry investigations[J]. Journal of Applied Ichthyology, 2009, 25(5): 505-515. |
| [18] | MITAMURA H, ARAI N, MITASUNAGA Y, et al. Directed movements and diel burrow fidelity patterns of red tilefish Branchiostegus japonicus determined using ultrasonic telemetry[J]. Fisheries Science, 2005, 71(3): 491-498. |
| [19] | VOEGELI F A, SMALE M J, Webber D M, et al. Ultrasonic Telemetry, tracking and automated monitoring technology for sharks[J]. Environmental Biology of Fishes, 2001, 60(1/3): 267-281. |
| [20] | 危起伟, 杨德国, 柯福恩, 等. 长江中华鲟超声波遥测技术[J]. 水产学报, 1998, 22(3): 211-217. WEI Q W, YANG D G, KE F E, et al. Technique of ultrasonic telemetry for Chinese sturgeon, Acipenser sinensis, in Yangtze river[J]. Journal of Fisheries of China, 1998, 22(3): 211-217. |
| [21] | PARK J S, FURUSAWA M. Development of biotelemetry method combining SSBL and pinger synchronizing methods[J]. Nippon Suisan Gakkaishi, 2006, 72(6): 1082-1092. |
| [22] | GROTHUES T M. A review of acoustic telemetry technology and a perspective on its diversification relative to coastal tracking arrays[M]//NIELSEN J L, ARRIZABALAGA H, FRAGOSO N, et al. eds. Tagging and Tracking of Marine Animals with Electronic Devices. Netherlands: Springer, 2009, 9: 77-90. |
| [23] | GVLER N F, VBEYLI E D. Theory and applications of biotelemetry[J]. Journal of Medical Systems, 2002, 26(2): 159-178. |
| [24] | MIYAGI A, AMAKASU K, ABE K, et al. Change of source level of pinger due to implanting into fish[J]. Nippon Suisan Gakkaishi, 2011, 77(5): 791-798. |
| [25] | MCCOVEY B W Jr. Klamath river green sturgeon acoustic tagging and biotelemetry monitoring 2010[R]. Final Technical Report, Hoopa, CA, 2010: 1-15. |
| [26] | LUO H W, DUAN X B, LIU S P, et al. Effects of surgically implanted dummy ultrasonic transmitters on physiological response of bighead carp Hypophthalmichthys nobilis[J]. Fish Physiology and Biochemistry, 2014, 40(5): 1521-1532. |
| [27] | WOLTERS W, MASTERS A, VINCI B, et al. Design, loading, and water quality in recirculating systems for Atlantic Salmon (Salmo salar) at the USDA ARS National Cold Water Marine Aquaculture Center (Franklin, Maine)[J]. Aquacultural Engineering, 2009, 41(2): 60-70. |
| [28] | ZAGARS M, LKEJIMA K, ARAI N, et al. Migration patterns of juvenile Lutjanus argentimaculatus in a mangrove estuary in Trang province, Thailand, as revealed by ultrasonic telemetry[J]. Environmental Biology of Fishes, 2012, 94(2): 377-388. |
| [29] | KESSEL S T, COOKE S J, HEUPEL M R, et al. A review of detection range testing in aquatic passive acoustic telemetry studies[J]. Reviews in Fish Biology and Fisheries, 2014, 24(1): 199-218. |
| [30] | ARNOLD G, DEWAR H. Electronic tags in marine fisheries research: A 30-year perspective[M]//SIBERT J R, NIELSEN J L, eds. Electronic Tagging and Tracking in Marine Fisheries. Netherlands: Springer, 2001: 7-64. |
2. South China Sea Fisheries Research Institute, Chinese Academy of Fishery Sciences, Guangzhou 510300, Guangdong, China;
3. China Society of Fisheries, Beijing 100122, China;
4. KEK Field Scientific Experimental Station of South China Sea Fishery Resource and Environment, Ministry of Agriculture, Guangzhou 510300, Guangdong, China;
5. China Marine Surveillance, Weihai Wendeng District, Weihai 264400, Shandong, China
 2016, Vol. 25
2016, Vol. 25


