2. 上海海洋大学 水产与生命学院, 上海 201306;
3. 上海市奉贤区水产技术推广站, 上海 201499
凡纳滨对虾(Penaeus vannamei)因其对盐度广泛的适应性,而成为我国海淡水养殖的主要品种。但是,自20世纪90年代对虾白斑综合征病毒(white spot syndrome virus,WSSV)在该品种大规模流行以来[1],至今仍然时有暴发[2],并因其高致病性和高致死率,给对虾养殖产业带来巨大经济损失[3, 4]。对虾传染性皮下及造血器官坏死病毒(infectious hypodermal and hematopoietic necrosis virus,IHHNV)最早于1981年在凡纳滨对虾和蓝对虾(P. stylirostris)中发现[5],可导致凡纳滨对虾慢性矮小残缺综合征(runt-deformity syndrome,RDS),感染虾外观畸形、生长缓慢[6],因此,造成的经济损失亦很严重。
研究发现,近年来WSSV与IHHNV在国外对虾中的感染率依然很高,而且两者在对虾体内共存的现象亦很普遍[7],国内海南、山东、江苏以及台湾等地也有过共感染现象的报道[8, 9, 10, 11]。然而,迄今未见关于这两种病毒共感染后对对虾的组织损伤和对虾的免疫应答等的深入探究,而且这些IHHNV-WSSV共感染现象多发生在海水环境中,而我国内地多数地区已经实现了凡纳滨对虾的淡水养殖,为此,本研究于2014年对上海地区部分淡水养殖凡纳滨对虾进行了IHHNV-WSSV的共感染调查,并初步探究了两者共感染对对虾鳃丝组织和免疫酶活性的影响。
作为甲壳类动物,各种免疫相关酶在对虾的免疫应答中发挥了重要作用。超氧化物歧化酶(SOD)作为抗氧化系统的关键酶之一,可以平衡体内的氧自由基[12],在保护功能大分子不被破坏、增强机体免疫力等方面有着重要作用[13]。酸性磷酸酶(ACP)是巨噬细胞内溶酶体的重要组成部分,与吞噬作用密切相关,在破坏和消灭入侵病原、保护机体组织方面发挥着重要作用[14],本研究选取这两种免疫相关酶初步探究了IHHNV-WSSV共感染后对虾的免疫保护反应。
1 材料与方法 1.1 凡纳滨对虾感染率调查用凡纳滨对虾:2014年5-9月对上海地区两个凡纳滨对虾淡水养殖场(养殖场1和2)进行跟踪采集(≥10尾/次/池),并于对虾疾病暴发季节(7月),增加采集了另外4个养殖场(养殖场3-6),所有对虾样品均在采集后迅速用冰盒低温运回实验室待检。
感染用凡纳滨对虾:健康凡纳滨对虾[(5.5±0.5) g]为本单位海南研究基地购买SPF亲虾子一代在淡水环境下自行繁育而成。感染前,对虾分别在1 000 L玻纤桶中暂养3 d后用于实验。对虾暂养用水盐度约5,水温(28±0.5) ℃,pH 7.2~7.6;按对虾体质量的5%投喂颗粒饲料,每天投喂2次,24 h不间断充氧。
1.2 PCR检测取对虾头胸部肌肉约50 mg,按照产品说明书,用海洋动物组织基因组提取试剂盒(天根)提取总DNA。IHHNV和WSSV的套式PCR引物参考文献[15, 16, 17]合成(生工)。IHHNV和WSSV外引物扩增片段分别为648 bp和487 bp,内引物扩增片段分别为309 bp和316 bp。外引物的PCR扩增条件为:首先94 ℃预变性4 min,接着94 ℃变性30 s,52 ℃退火30 s,72 ℃延伸50 s循环30次,最后72 ℃延伸10 min。内引物的PCR扩增条件除了把退火温度提高到55 ℃外,其他条件与外引物相同。PCR产物用2%琼脂糖凝胶电泳并在凝胶成像系统观察。
1.3 人工感染用病毒液的制备IHHNV病毒液的制备参照TANG等[18]的方法稍作修改:IHHNV阳性对虾(本实验室于-80 ℃保存)去除头胸甲后取头胸部肌肉称重,用PBS(0.01 mol/L,pH 7.4,W∶V=1∶10)匀浆,8 000 r/min离心20 min ,上清液经0.22 μm滤膜过滤、分装,置于-80 ℃保存。
WSSV病毒保存液的制备和病毒感染液浓度的确定参考文献[2]进行,经过预实验,确定本次WSSV病毒感染液的浓度为病毒保存液作1×104倍稀释。
1.4 病毒的人工感染随机采集暂养的凡纳滨对虾进行PCR检测,结果表明,对虾均为IHHNV和WSSV阴性。接着,随机捞取300尾对虾,每尾对虾于第3腹节处肌肉注射IHHNV病毒保存液25 μL;同时,随机捞取300尾对虾注射等量的PBS(0.01 mol/L,pH 7.4)。感染对虾和PBS注射对虾分别暂养于1 000 L玻纤桶中(150只/桶),感染期间正常喂食、换水和充氧,水温(28±0.5) ℃。2周后,IHHNV感染组每桶取10尾虾的游泳足进行PCR和定量PCR检测,确认IHHNV感染成功,并且平均感染量约为每毫克组织1×104 拷贝。随后,IHHNV阳性对虾和PBS注射对虾用于WSSV感染实验。
WSSV攻毒实验分为4组,每组24尾对虾暂养于一个200 L玻纤桶中:IHHNV阳性对虾再感染WSSV实验组(IHHNV-WSSV)、PBS注射虾再感染WSSV实验组(WSSV)、IHHNV阳性对虾再注射PBS对照组(IHHNV)以及PBS注射虾再注射PBS对照组(control)。感染期间正常喂食、换水和充氧。本次实验重复3次。
1.5 死亡率观察WSSV感染后,每4 h观察一次,记录对虾发病和死亡情况,按时间节点计算各组累计死亡率。
1.6 病理分析感染实验观察终止即WSSV感染144 h后,分别采集IHHNV-WSSV组和WSSV组各3尾濒死对虾的鳃丝,用4%中性甲醛溶液固定,并经乙醇梯度脱水和石蜡包埋后制成厚度约5 μm的切片,H&E染色后,置于光镜下观察并拍照。
1.7 酶活检测重复前文1.1、1.3和1.4的过程,不同的是,WSSV感染液浓度的确定参考文献[2]方法并稍作调整,即“以感染7 d内对虾累计死亡率低于20%的最小稀释度作为病毒保存液的稀释度”。经过预实验确定WSSV感染浓度为病毒保存液作1×107倍稀释;感染组和对照组每组30尾对虾暂养于200 L玻纤桶中。WSSV感染后,以感染0、24、48、72、96、120和144 h为采样节点,每个节点每组采集3尾对虾,分别取肝胰腺和肌肉组织置于-80 ℃保存,用于SOD和ACP活性测定。SOD和ACP的酶活分析方法参考酶活检测试剂盒说明书(南京建成)进行。ACP定义为每克组织蛋白在37 ℃与基质作用30 min产生1 mg酚为1个金氏单位;SOD定义为在本反应体系中SOD抑制率达50%时所对应的酶量为一个SOD活力单位(U)。样品总蛋白采用考马斯亮蓝G-250比色法测定[19]。样品蛋白质含量计算公式为y=ax+b。
1.8 数据处理与分析应用SPSS 19.0统计软件对实验数据进行单因素方差分析(One-Way ANOVA),采用Duncan氏法比较组间差异,P<0.05为显著性差异水平,用Excel 2010绘制相关图表。
2 结果 2.1 IHHNV和WSSV感染率调查2014年5-9月,对上海地区两个淡水养殖场(养殖场1和2)凡纳滨对虾IHHNV和WSSV的感染率跟踪结果显示(表1):养殖场1和2的对虾WSSV和IHHNV的感染率均在31.5%以上,其中,养殖场1的IHHNV感染率高达40.8%,而养殖场2的WSSV感染率高达65.2%;IHHNV-WSSV共感染率在19.1%以上,最高的池塘可高达40%。但是,对比不同月份可见,感染率波动幅度较大。其中,养殖场1的部分跟踪池塘对虾于6月份暴发WSS,而养殖场2的部分跟踪池塘的两批对虾分别于7月和9月暴发WSS(两场暴发疾病池塘的WSSV感染率均为100%),也在一定程度上抬高了当批跟踪对虾的平均感染率。养殖场1的对虾于6月相继暴发WSS后,8-9月对重新放养的仔虾再次跟踪检测,新放养的对虾WSSV感染率和IHHNV-WSSV共感染率均较低(8.75%和6.3%),随着养殖时间的延长,到9月份时,两者的感染率都快速升高(37.7%和26.4%);IHHNV的感染率与WSSV没有完全的相关性,但是,大多数情况下,随着养殖时间的延长也呈现上升趋势。养殖场3-6的检测主要是基于疾病暴发季节对疾病的诊断(表2),因此,没有对IHHNV进行感染率检测。养殖场3和4的对虾样品均采自暴发疾病的池塘,对虾外观红体,在池边漫游,检测结果显示两个养殖场的样品全部表现为WSSV强阳性,证实对虾暴发WSS。我们对养殖场1、2和养殖场3、4暴发疾病池塘对虾的诊断结果表明,WSS是上海地区养殖凡纳滨对虾的主要疾病。
| 表1 淡水养殖凡纳滨对虾IHHNV和WSSV感染率调查 Tab.1 Investigation of IHHNV and WSSV in P. vannamei cultured in freshwater |
| 表2 发病季节(7月)上海地区部分淡水养殖凡纳滨对虾WSSV感染率 Tab.2 Prevalence of WSSV in clinically healthy and diseased P. vannamei cultured in freshwaterin Shanghai in July 2014 |
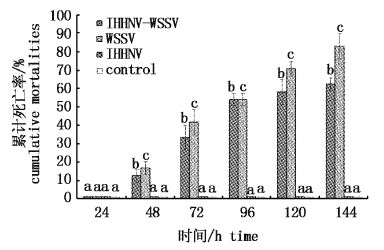
WSSV感染24 h以后,感染组对虾相继出现发病和死亡情况,临床表现为红体、停食、水面漫游和头胸甲内面白点,而IHHNV组和control组对虾未出现以上特征,也没有出现死亡现象。累计死亡率分析显示(图1),WSSV感染组和IHHNV-WSSV共感染组的对虾随着感染时间的延长累计死亡率都逐渐升高,而且WSSV组对虾的累计死亡率始终高于同期IHHNV-WSSV组。至WSSV感染后144 h实验终止时,WSSV组对虾的累计死亡率(83.3%±6.8%)约为IHHNV-WSSV组(62.5%±3.4 %)的1.3倍。
|
图1
WSSV感染后不同时间点每组凡纳滨对虾的累计死亡率
Fig.1
Time-course of cumulative mortalities of each group of P. vannamei post-infection with WSSV
不同小写字母代表同一时间点不同组活性差异显著(P<0.05)。 Different lowercase letters indicate significant difference among different groups in the same period (P<0.05). |
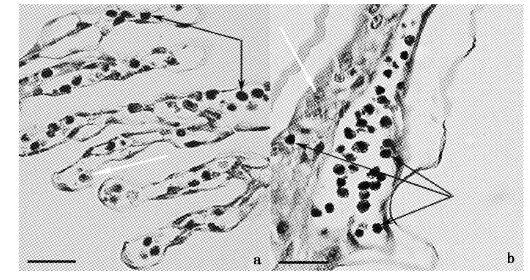
为了观察IHHNV-WSSV共感染和WSSV感染所致的组织损伤,WSSV感染144 h后,分别采集两组各3尾濒死对虾的鳃丝制成病理切片。如图2所示,无论是IHHNV-WSSV共感染组(图2a)还是WSSV组(图2b),所有濒死对虾的鳃丝内大量细胞(上皮细胞和血细胞等)呈现核肿大、染色质边聚以及蓝染的现象,符合WSSV大量复制的典型特征。两组濒死对虾鳃丝细胞的病变程度和病变细胞的数量没有显著差异。
|
图2
WSSV感染144 h后IHHNV-WSSV组和WSSV组濒死凡纳滨对虾的鳃丝病理变化
Fig.2
Histopathological changes in gills of moribund P. vannamei in the group of IHHNV-WSSV and WSSV and at 144h post-infection with WSSV
a. IHHNV-WSSV组对虾鳃丝; b. WSSV组对虾鳃丝。黑色箭头指向病毒感染的细胞,白色箭头指向正常细胞。标尺=20 μm。 a. Gills of P. vannamei in the group of IHHNV-WSSV; b. Gills of P. vannamei in the group of WSSV. The black arrows point to virus-infected cells,the white arrows point to normal cells. (H&E). Bar=20 μm. |
为了分析IHHNV-WSSV共感染对淡水养殖凡纳滨对虾免疫相关酶活性的影响,本研究在实施较低浓度WSSV感染实验后,分析了对虾肝胰腺和肌肉组织中SOD及ACP的活性变化。
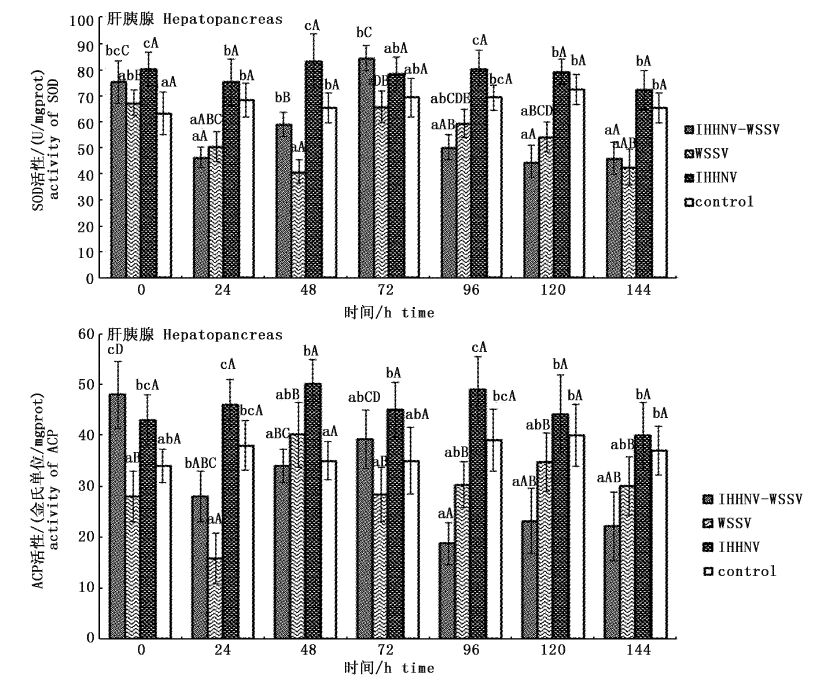
对肝胰腺SOD和ACP活性影响见图3,WSSV感染后,WSSV组和IHHNV-WSSV组对虾肝胰腺中SOD活性呈现先降后升的走势,在攻毒后24 h内迅速下降而显著低于同期IHHNV组和control组(P<0.05)。其中,WSSV组在24 h后仍然持续降低直至攻毒后48 h才开始逐渐升高,而IHHNV-WSSV组在24 h后即迅速升高,并在攻毒后72 h内与WSSV组同时到达最高值(P<0.05)。不同的是,IHHNV-WSSV组对虾SOD活性峰值高于同期对照组,而WSSV组对虾的峰值低于同期对照组。随后,两组对虾肝胰腺内SOD活性下降,并很快低于同期对照组(P<0.05);肝胰腺ACP的变化总体上与SOD类似,不同的是,WSSV组和IHHNV-WSSV组对虾肝胰腺内ACP活性均在感染24 h后开始上升,WSSV组上升迅速,于感染后48 h到达高峰,而IHHNV-WSSV组在感染72 h后才到达最高值,并且,两组的ACP活性都始终低于同期IHHNV组。同期对照组(IHHNV组和control组)对虾肝胰腺SOD和ACP虽然也出现小幅波动,但是差异均不显著(P>0.05)。
|
图3
WSSV感染后凡纳滨对虾肝胰腺中SOD和ACP的活性变化
Fig.3
Time-course of activities of SOD and ACP in the hepatopancreas of P. vannamei post-infection with WSSV
不同小写字母代表同一时间点不同组活性差异显著(P<0.05);不同大写字母代表同一组在不同时间点活性差异显著(P<0.05);下图同此。 Different lowercase letters indicate significant difference among different groups in the same period (P<0.05); different capital letters indicate significant difference among the different period in the same group (P<0. 05). The same case in the following figures. |
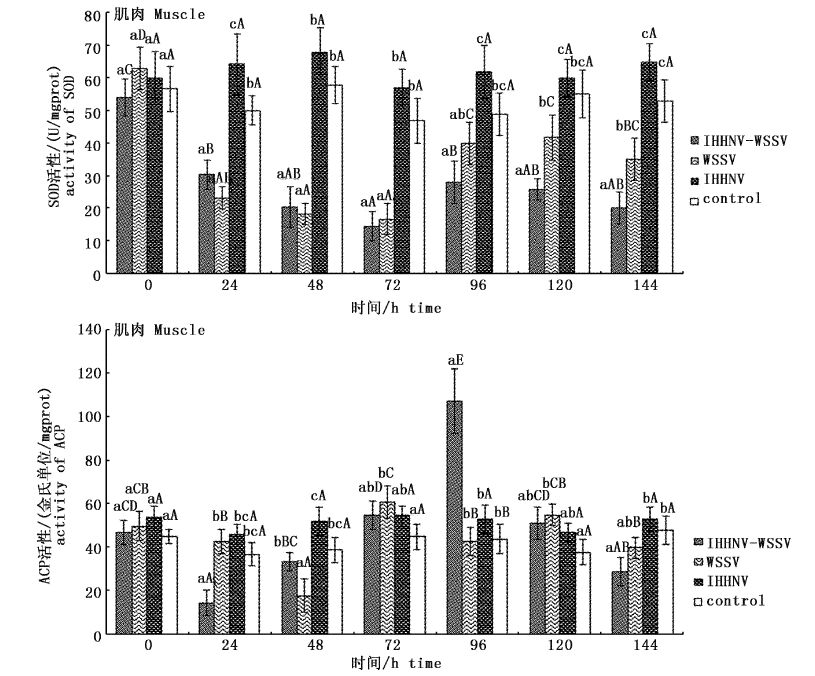
对肌肉SOD和ACP活性影响:如图4所示,WSSV感染后,WSSV组和IHHNV-WSSV组对虾肌肉中SOD活性也基本呈现先降后升再降的变化趋势。两组在攻毒后72 h内SOD活性持续下降,并在感染后很快就低于同期IHHNV组和control组(P<0.05)。随后,两组活性迅速上升并于感染后96 h同时到达峰值(P<0.05)。感染96 h后,WSSV组肌肉SOD活性下降缓慢,虽然始终低于同期对照组,但是一直高于IHHNV-WSSV共感染组(P<0.05);肌肉ACP的变化总体上与SOD类似,不同的是,WSSV组和IHHNV-WSSV组对虾肌肉ACP活性在攻毒后迅速降低,分别于感染后48 h和24 h到达最低值,随后,IHHNV-WSSV共感染组的ACP活性持续升高,并于感染后96 h到达峰值,远高于WSSV组和对照组,差异极显著。同样地,在随后的下降过程中,IHHNV-WSSV组的ACP活性迅速下降,很快低于同期WSSV组。同期对照组(IHHNV组和control组)对虾肝胰腺SOD和ACP虽然也出现小幅波动,但是差异均不显著(P>0.05)。
|
图4 WSSV感染后凡纳滨对虾肌肉中SOD和ACP的活性变化 Fig.4 Time-course of activities of SOD and ACP in the muscle of P. vannamei post-infection with WSSV |
检测结果表明,跟踪调查的两个淡水养殖场对虾都存在较高的WSSV和IHHNV共感染现象,共感染率平均为20.5%,养殖场2于9月暴发WSS时共感染率更是高达40%。近几年相关研究报道也证实,IHHNV-WSSV共感染的现象普遍存在:郁晓维等[20]的调查结果表明,浙江省养殖凡纳滨对虾中IHHNV和WSSV的共感染率高达46.7%~93.3%;国外的调查结果也显示[7],养殖凡纳滨对虾中检测到IHHNV和WSSV的共感染率可高达60%。可见,IHHNV-WSSV共感染的现象在养殖凡纳滨对虾中长期、持续存在,而且始终维持在较高的感染水平。虽然本研究中养殖场2在9月份对虾样品存在特殊性(采自WSS暴发池塘),但是2个养殖场的跟踪检测结果均显示,IHHNV-WSSV共感染率与同批次对虾的WSSV感染率成正相关。由于多点检测表明,上海养殖凡纳滨对虾的疾病以WSS为主,因此,探究目前流行的IHHNV和WSSV的共感染问题,对于WSSV的预防与控制有着重要的现实意义,据我们所知,目前还没有关于IHHNV和WSSV共感染的组织损伤及对虾免疫保护的相关研究。
综合2个养殖场5-9月的跟踪检测结果,我们发现,上海地区WSSV和IHHNV的平均感染率均较高,分别为42.6%和38.5%。但是纵观全年的跟踪结果,我们发现从虾苗投放到收获,WSSV的感染率随着管理、季节等变化而出现较大波动,尤其是在疾病暴发季节(7月),其感染率迅速大幅提高,而IHHNV的感染率走势较为温和,具体表现为在虾苗刚刚投放之时其感染率可能高于WSSV,而到疾病暴发之时却低于WSSV的现象。值得注意的是,疾病暴发季节的 “健康”凡纳滨对虾WSSV平均感染率高达40.74%(养殖场5和6),表明在WSS暴发季节,同地区“健康”凡纳滨对虾暴发WSS的风险远高于其他季节的对虾,需要养殖企业更为精心地管理与防控。另外,我们注意到,养殖场1在5月采集的对虾虽然没有处于疾病暴发季节,也未发现发病对虾,但是,其WSSV感染率高达44.4%,远高于未发病季节健康池对虾的WSSV检出率(如8月养殖场1的8.75%和5月养殖场2的18.2%)。跟踪发现,部分池塘于20d后暴发WSS。可见,“健康”对虾体内WSSV的高感染率预示了WSS暴发的潜在风险。此调查也说明病毒的跟踪检测对于WSS暴发预警的重要性。
3.2 IHHNV-WSSV共感染对淡水养殖凡纳滨对虾的致病性WSSV感染后,观察期内IHHNV-WSSV组凡纳滨对虾的累计死亡率始终略低于同期WSSV组,这与之前的相关研究报道一致。TANG等[21]在蓝对虾中发现,同时感染WSSV后,携带IHHNV的蓝对虾比未感染IHHNV的蓝对虾存活的时间更长。此后,研究人员在斑节对虾(P. monodon)和凡纳滨对虾中也发现过类似现象[22, 23],并推测可能是因为IHHNV在宿主细胞内竞争了WSSV的受体,从而延缓了WSSV复制速度的缘故[23]。我们的研究表明,尽管共感染在一定程度上减慢了对虾的死亡速度,但是,两者在感染一定时间后,组织细胞的病变数量和病变程度并没有显著差异;另一方面,由于IHHNV可导致凡纳滨对虾慢性矮小残缺综合征,感染虾生长缓慢,饲料回报率大幅降低,因此,综合而言,IHHNV-WSSV共感染的最终经济损失可能比单纯WSSV感染更大。
3.3 IHHNV-WSSV共感染对淡水养殖凡纳滨对虾SOD和ACP活性的影响免疫相关酶SOD和ACP在清除氧自由基、吞噬入侵病原和保护机体组织方面发挥着重要作用[12, 13, 14]。综合本研究SOD和ACP检测结果,我们发现,WSSV感染后,WSSV组和IHHNV-WSSV组对虾肝胰腺和肌肉中两种酶的活性都呈现降—升—降的变化趋势。无论IHHNV-WSSV组还是WSSV组,两种酶在观察期内活性高于control对照组的实际时长均不到72 h,更长时间是两组的酶活同时显著低于同期两个对照组(肌肉SOD活性始终低于对照组),可见,WSSV感染后激发机体的免疫力只是暂时的,更多时候表现为免疫抑制,这可能与WSSV强大的组织破坏能力密切相关,这或许也可以作为解释对虾感染WSSV后容易继发感染其他病原如气单胞菌等致病菌[24]的一个原因。
比较IHHNV-WSSV组和WSSV组的酶活变化趋势还可见,除了肌肉组织SOD外,IHHNV-WSSV组相对于WSSV组可以在一定程度上激发更早、更高一些的免疫应答,但是,短时间高峰过后,所有IHHNV-WSSV共感染组的SOD和ACP活性均出现快速下降,很快显著低于同期WSSV组并在低位维持到观察期结束。可见,虽然IHHNV-WSSV共感染可以更高、更快地激活机体的免疫保护,但是,随着感染时间的延长,IHHNV-WSSV共感染表现出比WSSV单感染更长时间的免疫抑制,这是否是由于双病毒感染导致组织损伤的叠加所致,值得继续探究。除此之外,还有一个现象值得注意,IHHNV组对虾肝胰腺和肌肉中两种酶的活性在感染过程中一直较为稳定,并始终高于同期control组。据我们多次实验观察,这种较高的活性可以维持到IHHNV感染后35 d左右。可见,在没有WSSV的参与下,单纯IHHNV感染对对虾表现为长期低水平的免疫激活。
综上分析,淡水养殖对虾WSSV和IHHNV的感染率很高,时刻威胁着上海地区养殖企业的经济效益。作为需要向OIE报告的重要对虾病毒,两者单独感染均可导致养殖企业比较严重的经济损失,而共感染还存在组织损伤叠加和更长时间的免疫保护低下等问题,因此,生产企业在防控WSSV感染的同时,尤其要严防IHHNV-WSSV的共感染现象。
| [1] | INOUYE K, MIWA S, OSEKO N, et al. Mass mortality of cultured kuruma shrimp Penaeus japonicus in Japan in 1993: electron microscopic evidence of the causative virus [J]. Fish Pathology, 1994, 29(2): 149-158. |
| [2] | 周俊芳, 杨先乐, 万夕和, 等. 不同靶点shRNA干扰对虾白斑综合征病毒增殖效果分析[J]. 华中农业大学学报, 2011, 30(1): 105-108. ZHOU J F, YANG X L, WAN X H, et al. Effect of the viral interference effects of shRNAs targeting different sites in white spot syndrome virus genome [J]. Journal of Huazhong Agricultural University, 2011, 30(1): 105-108. |
| [3] | 马晓燕, 李鹏, 严洁, 等. 对虾白斑综合症病毒的概述[J]. 南京师范大学报: 自然科学版, 2012, 35(4): 90-100. MA X Y, LI P, YAN J, et al. A review on shrimp white spot syndrome virus [J]. Journal of Nanjing Normal University: Natural Science Edition, 2012, 35(4): 90-100. |
| [4] | SÁNCHEZ-PAZ A. White spot syndrome virus: an overview on an emergent concern [J]. Veterinary Research, 2010, 41(6): 43. |
| [5] | LIGHTNER D V, REDMAN R M, BELL T A. Infectious hypodermal and hematopoietic necrosis, a newly recognized virus disease of penaeid shrimp [J]. Journal of Invertebrate Pathology, 1983, 42(1): 62-70. |
| [6] | BELL T A, LIGHTNER D V. IHHN virus: infectivity and pathogenicity studies in Penaeus stylirostris and Penaeus vannamei [J]. Aquaculture, 1984, 38(3): 185-194. |
| [7] | OTTA S K, ARULRAJ R, PRAVEENA P E, et al. Association of dual viral infection with mortality of Pacific white shrimp(Litopenaeus vannamei) in culture ponds in India [J]. Virus Disease, 2014, 25(1): 63-68. |
| [8] | CHEN Y B, ZHOU J F, WAN X H, et al. Establishment of a multiplex PCR and an investigation of co-infection rate of WSSV and IHHNV in Penaeid vannamei in northern of Jiangsu [J]. Journal of Animal and Veterinary Advances, 2012, 11(2): 181-185. |
| [9] | YEH S P, CHEN Y N, HSIEH S L, et al. Immune response of white shrimp, Litopenaeus vannamei, after a concurrent infection with white spot syndrome virus and infectious hypodermal and hematopoietic necrosis virus [J]. Fish&Shellfish Immunology, 2009, 26(4): 582-588. |
| [10] | TAN Y, XING Y, ZHANG H, et al. Molecular detection of three shrimp viruses and genetic variation of white spot syndrome virus in Hainan Province, China, in 2007 [J]. Journal of Fish Diseases, 2009, 32(9): 777-784. |
| [11] | YANG B, SONG X L, HUANG J, et al. A single-step multiplex PCR for simultaneous detection of white spot syndrome virus and infectious hypodermal and haematopoietic necrosis virus in penaeid shrimp [J]. Journal of Fish Diseases, 2006, 29(5): 301-305. |
| [12] | 林庆斌, 廖升荣, 熊亚红, 等. 超氧化物歧化酶(SOD)的研究和应用进展[J]. 化学世界, 2006, 47(6): 378-381. LIN Q B, LIAO S R, XIONG Y H, et al. Progress in the study and application of superoxide dismutases [J]. Chemical World, 2006, 47(6): 378-381. |
| [13] | 张明, 王雷, 郭振宇, 等. 脂多糖和弧菌对中国对虾血清磷酸酶、超氧化物歧化酶和血蓝蛋白的影响[J]. 海洋科学, 2004, 28(7): 22-25. ZHANG M, WANG L, GUO Z Y, et al. Effect of lipopolysaccharide and Vibrio anguillarum on the activities of phosphatase, superoxide dismutase and the content of hemocyanin in the serum of Fenneropenaeus chinensis [J]. Marine Science, 2004, 28(7): 22-25. |
| [14] | 刘晓云, 张志峰, 马洪明. 中国对虾血细胞酶细胞化学的初步研究[J]. 青岛海洋大学学报, 2002, 32(2): 259-265. LIU X Y, ZHANG Z F, MA H M. Study on enzyme cyto-chemistry of blood cells in Penaeus chinensis [J]. Journal of Ocean University of Qingdao, 2002, 32(2): 259-265. |
| [15] | RAI P, PRADEEP B, KARUNASAGAR I, et al. Detection of viruses in Penaeus monodon from India showing signs of slow growth syndrome [J]. Aquaculture, 2009, 289(3/4): 231-235. |
| [16] | TANG K F, NAVARRO S A, LIGHTNER D V. PCR assay for discriminating between infectious hypodermal and hematopoietic necrosis virus(IHHNV) and virus-related sequences in the genome of Penaeus monodon[J]. Diseases of Aquatic Organisms, 2007, 74(2): 165-170. |
| [17] | HOSSAIN M S, CHAKRABORTY A, JOSEPH B, et al. Detection of new hosts for white spot syndrome virus of shrimp using nested polymerase chain reaction [J]. Aquaculture, 2001, 198(1/2): 1-11. |
| [18] | TANG K F, POULOS B T, WANG J, et al. Geographic variations among infectious hypodermal and hematopoietic necrosis virus(IHHNV) isolates and characteristics of their infection [J]. Diseases of Aquatic Organisms, 2003, 53(2): 91-99. |
| [19] | 李志江. 考马斯亮蓝G250染色法测定啤酒中蛋白质含量[J]. 酿酒, 2008, 35(1): 70-72. LI Z J. Study on determination of protein content of beer by Coomassie Brilliant G-250 dye binding [J]. Liquor Making, 2008, 35(1): 70-72. |
| [20] | YU X W, WANG J P, ZHANG W, et al. Prevalence of Three shrimp viruses in Zhejiang Province in 2008 [J]. Virologica Sinica, 2011, 26(1): 67-71. |
| [21] | TANG K F J, DURAND S V, WHITE B L, et al. Induced resistance to white spot syndrome virus infection in Penaeus stylirostris through pre-infection with infectious hypodermal and hematopoietic necrosis virus-a preliminary study [J]. Aquaculture, 2003, 216(1/4): 19-29. |
| [22] | MOLTHATHONG S, JITRAKORN S, JOYJINDA Y, et al. Persistence of Penaeus stylirostris densovirus delays mortality caused by white spot syndrome virus infection in black tiger shrimp(Penaeus monodon) [J]. BMC Veterinary Research, 2013, 9(7): 33. |
| [23] | BONNICHON V, LIGHTNER D V, BONAMI J R. Viral interference between infectious hypodermal and hematopoietic necrosis virus and white spot syndrome virus in Litopenaeus vannamei [J]. Diseases of Aquatic Organisms, 2006, 72(2): 179-184. |
| [24] | 李继秋, 谭北平, 麦康森. 白斑综合征病毒与凡纳滨对虾肠道菌群区系之间关系的初步研究[J]. 上海水产大学学报, 2006, 15(1): 109-113. LI J Q, TAN B P, MAI K S. Study on the relationships between white spot syndrome virus outbreak in cultured shrimp(Penaeus vannamei) and the composition of aerobic heterotrophic bacterium communities in shrimp intestine [J]. Journal of Shanghai Fisheries University, 2006, 15(1):109-113. |
2. College of Fisheries and Life Science, Shanghai Ocean University, Shanghai 201306, China;
3. Shanghai Fengxian Fisheries Extension Station, Shanghai 201499, China
 2015, Vol. 24
2015, Vol. 24


