斑马鱼(Danio rerio)因其成年鱼个体小、易于饲养、发育快速、性成熟期短、繁殖力强、体外受精、胚胎在母体外发育并且透明等特点成为发育、遗传以及药物发现研究中常用的模式动物[1]。近年来,斑马鱼作为模式动物研究体内离子平衡稳态成为热点。目前研究主要集中在钠离子、钾离子等单价阳离子以及钙离子上[2, 3, 4, 5],但是对镁离子在斑马鱼这一模式系统中的研究却少有报道。
镁离子是真核细胞中第二丰富的阳离子,在许多细胞过程中都起着重要的作用。它可作为辅助因子用于需要ATP参与的所有酶促反应,也是许多需要激酶的反应体系的关键组成部分[6]。在调节神经肌肉兴奋性、肌肉收缩以及细胞通透性等方面镁离子也发挥着重要作用。此外,它还是钠、钾和钙离子通道和线粒体功能的调节因子[7, 8]。研究表明细胞周期蛋白M2(CNNM2)这一细胞周期蛋白家族的重要成员,通过调控上皮细胞镁离子运输以及肾脏的镁离子的重吸收等机制在体内镁离子的稳态上起着重要作用[9, 10, 11]。因此建立CNNM2基因敲除斑马鱼对于研究镁离子体内稳态与CNNM2的关系具有重要的意义。CRISPR/Cas9是最近发展起来的一种新型基因定向编辑技术,在人类细胞、小鼠、斑马鱼中成功实现了基因组定点修饰,并且具有较高的敲除效率[12, 13, 14]。在本研究中通过CRISPR/Cas9系统对斑马鱼的CNNM2基因进行敲除,从而获得能稳定遗传的CNNM2敲除个体,为CNMM2基因在镁离子调控中发挥的作用提供材料。
1 材料与方法 1.1 实验材料实验动物为Tubingen 品系斑马鱼,取自上海海洋大学适应生理学实验室,饲养在自动循环水养殖系统中,光暗周期比为14 h∶10 h(14L∶10D)。取健康、性成熟的斑马鱼,于饲养系统关灯前将雌雄按1∶2 的比例放入产卵缸内。次日给光后拿掉挡板,让其完成产卵与受精。
gRNA骨架载体pDR274由HWANG实验室馈赠;cas9表达载体pGH-T7-zCas9由北京大学张博老师惠赠;菌株E.coliDH5α购自北京全式金生物技术有限公司;T4 DNA 连接酶购自Promega公司;Premix Taq DNA Polymerase、DNA Ladder 1kb Marker均为TaKaRa公司产品;Bsa Ⅰ、Dra Ⅰ及Xba Ⅰ内切酶购自NEB公司;氨苄青霉素(ampicilin)及寡核苷酸(oligo);购自上海生工生物技术服务有限公司;琼脂糖购自普博生物技术有限公司;PCR产物纯化试剂盒购自天根生化(TIANGEN)科技有限公司;Gel Extraction kit和Plasmid Mini Kit购自Omega生物技术有限公司;DNA寡核苷酸退火缓冲液(Annealing Buffer for DNA Oligos)购自碧云天生物技术公司。
1.2 基因靶位点的设计CRISPR/Cas9 的剪切位点位于crRNA 互补序列下游邻近的PAM 区(Protospacer-Adjacent motif)的特征区域即NGG位点之前。本实验使用的sgRNA骨架载体由于需要预留T7启动子位置,所以就需符合5′-GG-N18-NGG-3′特征,这种特征的序列在每128 bp的随机DNA序列中就约重复出现一次。当然如果选择别的启动子进行gRNA的设计就可以相应地释放5′GG的要求[14]。
采用HWANG实验室开发的的ZIFIT Design Genome Editing Nucleases/CRISPR/Cas Nucleases网站(http://zifit.partners.org/ZiFiT/ChoiceMenu.aspx)进行基因打靶位点设计;根据JINEK 和CHYLINSKI等靶点设计原则进行筛选[15, 16](本实验采用限制性内切酶法检测突变,因此还要符合靶点上具有唯一的限制性内切酶的酶切位点);设计好的靶位点还应确认其在基因组中的唯一性:靶位点序列在NCBI网站进行blast,确认是斑马鱼基因中的单一位点。
1.3 gRNA表达载体的构建质粒pDR274通过Bsa Ⅰ进行酶切(37 ℃,4 h)。酶切产物经过琼脂糖凝胶电泳回收后加入T4 DNA连接酶和设计好的靶位点的一对oligos退火产物(通过Annealing buffer 95 ℃ 2 min,每8秒下降0.1 ℃,降至25 ℃得到),置于水浴锅中37 ℃连接过夜。连接产物转化至宿主大肠杆菌DH5α感受态细胞,涂布于具有卡那霉素抗性LB平板培养基上,37 ℃过夜培养,挑选单个克隆,经添加卡那霉素的LB液体培养基培养后进行PCR菌落鉴定和重组子快速鉴定。至少筛选5个阳性克隆,将其扩大培养后,抽提重组质粒送至上海生工生物技术有限公司进行测序。
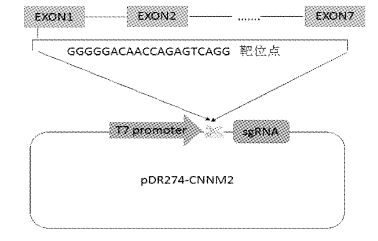
|
图1 gRNA构建示意图 Fig.1 Schematic diagram of sgRNA construction |
插入靶点的gRNA表达载体经过Dra Ⅰ酶切线性化后进行回收、纯化并溶于RNase Free的ddH2O中。参照T7 RiboMAXTMExpress Large Scale RNA Production System(Promega,p1300)使用说明书进行体外转录。Cas9质粒则经过Xba Ⅰ酶切线性化回收后为溶于无酶水作为模板,参照T7 Ultra Kit (Ambion,AM1345)使用说明书进行体外转录。二者体外转录产物均使用LiCl进行沉淀回收,1%琼脂糖电泳检测RNA的质量后保存于-80 ℃冰箱中。
1.5 gRNA和Cas9的体外转录插入靶点的gRNA表达载体经过Dra Ⅰ酶切线性化后进行回收、纯化并溶于RNase Free的ddH2O中。参照T7 RiboMAXTM Express Large Scale RNA Production System(Promega,p1300)使用说明书进行体外转录。Cas9质粒则经过Xba Ⅰ酶切线性化回收后为溶于无酶水作为模板,参照T7 Ultra Kit (Ambion,AM1345)使用说明书进行体外转录。二者体外转录产物均使用LiCl进行沉淀回收,1%琼脂糖电泳检测RNA的质量后保存于-80 ℃冰箱中。
1.6 靶位点活性检验体外转录好的sgRNA和Cas9 mRNA显微共注射至斑马鱼一细胞期胚胎中。每个胚胎sgRNA和Cas9的注射量分别约为30 pg和300 pg,对照组为注射等量的灭菌超纯水。显微注射后24~48 h之间在体式显微镜下挑选发育正常的胚胎去卵膜加入适量的50 mmol/L NaOH(每个胚胎10 μL左右);PCR 仪加热裂解胚胎,程序:95 ℃ 10 min,4 ℃ forever;取出后 Vortex振荡均匀;加入1/10体积1 mol/L Tris(pH 8.0)中和NaOH,混匀。至此粗提出胚胎基因组DNA。在CNNM2基因待敲除靶点上下游150 bp左右位置设计一对引物CNNM2-PCR-F和CNNM2-PCR-R(表1)。以上述基因组DNA为模板进行PCR反应,扩增产物大小为492 bp。用PCR产物纯化试剂盒(天根生化)进行纯化回收。取200 ng回收产物进行限制性内切酶酶切验证。由于本实验设计的靶位点在PCR产物中具有唯一的限制性酶切位点,所以通过酶切反应后如果产生突变那么PCR产物将不能被酶切完全。为进一步验证突变存在,以及突变的具体情况,我们将未能被酶切的片段回收进行TA克隆、测序进一步检测确定突变。
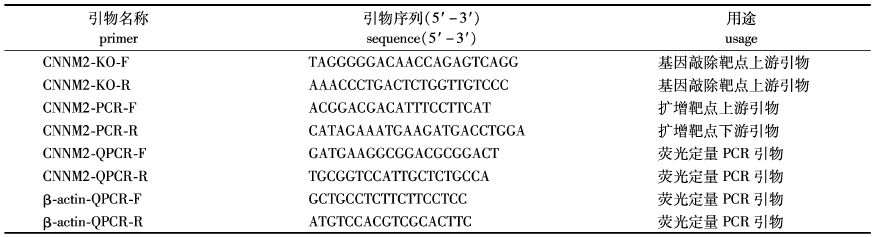
|
表1 引物列表 Tab. 1 Primer list |
提取F1杂合斑马鱼和野生(WT) 对照斑马鱼的脑、眼和心脏总RNA,利用逆转录试剂盒(TaKaRa) 逆转录成cDNA,利用引物CNNM2-QPCR-F和CNNM2-QPCR-R扩增目的基因,β-actin作为内参,确定CNNM2基因在两种组织中的表达情况,比较杂合子和野生对照斑马鱼的CNNM2基因的表达差异。
2 结果 2.1 gRNA靶位点的确定及表达载体的构建通过HWANG实验室的ZIFIT系统,搜索和确定gRNA的靶位点。将斑马鱼基因CNMM2基因的前2/3CDS序列输入CRISPR/Cas Nucleases Targeter系统中,可以获得一系列关于sgRNA识别的靶位点。根据上述位点筛选原则进行分析和优化,最终选择GGGGGACAACCAGAGTCAGG为CNMM2的sgRNA位点。对应的寡聚核苷酸链(oligo)分别为:CNMM2 Oligo1 TAGGGGGACAACCAGAGTCAGG;CNMM2 Oligo2 AAACCCTGACTCTGGTTGTCCC,靶位点具有Hin fI的限制性内切酶位点。
将设计的sgRNA位点合成的一对oligos进行退火,形成具有与经Bsa Ⅰ酶切后的骨架载体pDR274互补的overhang。通过酶切、连接的方式构建能特异性识别CNMM2对应序列的sgRNA。该载体均采用了菌落PCR法挑选阳性克隆以及PCR鉴定、酶切鉴定和DNA测序验证了每一个sgRNA的克隆情况,结果表明CNMM2 sgRNA构建成功。
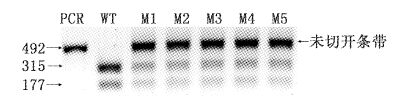
2.2 sgRNA活性检测及突变个体的筛选Cas9表达质粒和sgRNA表达载体,分别经Xba Ⅰ和Dra Ⅰ线性化,经酚氯仿抽提后,作为模板利用T7 RNA聚合酶体外转录合成Cas9 mRNA 和sgRNA。随后以约300pg Cas9 mRNA和30pg sgRNA剂量混合共注射到斑马鱼胚胎一细胞期的单细胞中。24~48 h后选择发育正常的胚胎,每5个为一组,共5组通过上述方法粗提基因组DNA。以此为模板我们对靶点DNA进行PCR扩增、纯化回收以及Hin fI酶进行酶切反应。图2结果显示5组平行反应与野生型相比具有未切开条带,说明具有敲除效用。并且通过image J软件计算未切开的PCR条带占所有条带的荧光亮度的百分比,得出结果表明平均突变效率为88%。随后我们对未切开条带进行回收TA克隆后挑选10个克隆进行测序,结果表明F0产生了不同程度的缺失、插入、移码等突变类型(图3)。
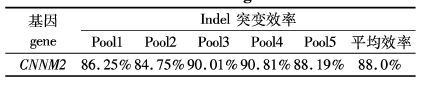
|
表2 显微注射CRISPR/Cas9后斑马鱼基因CNNM2突变效率 Tab. 2 Mutation frequencies induced by customized sgRNA:Cas9 nucleases at CNNM2 gene target sites in the zebrafish genome |
|
图2
CRISPR/Cas9 系统介导CNNM2的
基因修饰情况
Fig.2
CRISPR/Cas9 system mediated genetic
modifications in CNNM2
PCR为扩增包括靶点在内的一段DNA序列;WT是DNA 模板为野生对照基因组DNA经过Hin fI酶切后条带;M1-5是模版为显微注射CRISPR/Cas9后的基因组DNA经过Hin fI酶切后条带。 PCR target loci CNNM2 were amplified using genomic DNA templates from founders using primers CNNM2-PCR-F and CNNM2-PCR-R; WT and M1-5: Wild type and mutation PCR products were subjected to the HinfI cleavage assay to detect the modification in the target loci. |
|
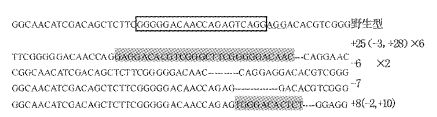
图3
F0 CNNM2位点的突变情况
Fig.3
Analysis of the founder of the target mutation
PAM基序表示为加下划线;黑框表示为靶点;灰色为插入片段表示;横线为缺失片段;插入(+),缺失(-)情况在每一行的右端显示。×N 表示此类型突变的个数。 The PAM sequence is underlined ; the targeting site are with frame; the insertion mutations are gray,the deletions are lined; insertions (+) ,deletions (-) are shown to the right of each allele. ×N indicates the number of this type mutation in 10 colonies. |
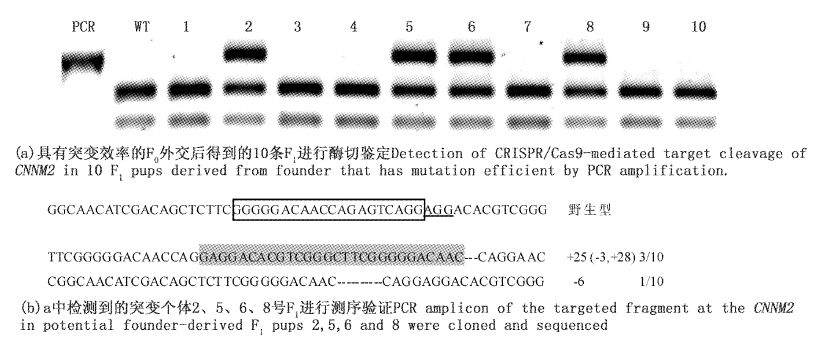
为进一步验证该技术造成的缺失是否可以稳定传代。先是检测F0外交得到的F1胚胎,筛选出生殖细胞中带有能稳定遗传变异类型的F0 成鱼。将这种F0 成鱼外交得到的后代(F1)养大后,随机挑选10条F1通过剪尾逐条检测靶位点序列,进行了PCR扩增、酶切鉴定及最后测序验证,结果显示4条斑马鱼获得了能稳定遗传的CNNM2突变(图4)。
|
图4
CNNM2位点的突变情况
Fig.4
Analysis of the transmission of the target mutation
PAM基序表示为下划线;黑框表示为靶点;灰色为插入片段表示;横线为缺失片段;插入(+),缺失(-)情况在每一行的右端显示。N/N为检测阳性数和总测序数。 The PAM sequence is underlined ; the targeting site are with frame; the insertion mutations are gray,the deletions are lined; insertions (+),deletions (-) are shown to the right of each allele. N/N indicates the number of this type mutation in 10 zebrafishes. |
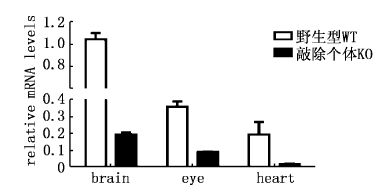
在建立了CNNM2基因敲除斑马鱼后,我们对产生的F1杂合子提取脑、眼和心脏总RNA后利用荧光定量PCR对所取组织的CNNM2表达情况进行了分析( 图5) ,结果表明CNNM2杂合子斑马鱼在所取组织中表达有明显地降低。
|
图5 Q-PCR分析CNNM2在F1杂合子 斑马鱼中的基因表达情况 Fig.5 Q-PCR analysis of CNNM2 gene expression in F1 heterozygous zebrafish |
CRISPR/Cas9系统相较于ZFNs[17]和TALENs[18- 19]两种人工核酸酶技术是一个天然存在的原核生物RNA干扰系统,其介导的基因组编辑是由crRNA指导的,对靶序列的识别是基于RNA与DNA的碱基配对过程来完成的,相比蛋白质对DNA序列的识别要精确更多[13, 15]。此外编码sgRNA的序列不超过100 bp,因此比构建TALENs和ZFNs更简单方便。较短的sgRNA序列也避免了超长、高度重复的TALENs编码载体带来的并发症。而且从实际应用的角度来说,CRISPRs比TALENs和ZFNs更容易操作,因为每一对TALENs都需要重新合成,而用于CRISPR的sgRNA只需要替换20个核苷酸就行。因此CRISPR/Cas9系统相较于TALENs和ZFNs具有更高的应用前景。
本研究在sgRNA靶点的筛选中,选择了位于CNNM2第一外显子区域的位置。因此在该靶点发生基因indel变异时更大限度地影响了这个基因的转录翻译从而达到沉默基因的作用。此外本研究靶点活性验证方式选择了限制性内切酶酶切法,这就要求靶点还需一个唯一的酶切位点。不同于直接测序法它不需要特别的仪器,只需经过PCR产物回收和酶切验证就能得到粗略的结果。而相较于错配酶切法而言,一般的限制性内切酶所需的成本更加低廉。本研究通过限制性酶切法验证敲除效率(图2),随后未切开条带的TA克隆和测序结果(图3)表明了CNNM2基因有4种突变类型。但是该方法也有一定的局限性,可能存在部分突变没有破坏限制性内切酶的酶切位点。因此仅仅通过回收未切开片段进行测序,确定突变情况不够完整,这就需要进一步地测序分析。
此外,在对CNNM2基因F1敲除杂合子的表型观察中未发现具有明显的形态发育异常,而ARJONA等[20]通过对CNNM2基因进行反义寡核苷酸(Morpholino,MO)敲除时会产生围心腔肿大等表型,这可能由于F1只是杂合子,部分CNNM2基因还发挥功效,因此需要通过自交筛选纯合子后进行更深入研究。总的来说本实验利用近年发展起来的基因组编辑技术CRISPR/Cas9系统对斑马鱼CNNM2基因进行敲除,效率达88%,建立了能稳定遗传的CNNM2敲除斑马鱼。CNNM2敲除斑马鱼的成功构建有利于下一步研究镁离子在斑马鱼离子代谢中的作用,为研究脊椎动物中CNNM2基因与镁离子体内调节之间的关系提供了研究材料,为进一步探讨镁离子的生理功能打下了坚实的基础。
| [1] | 贾顺姬,孟安明.中国斑马鱼研究发展历程及现状[J].遗传, 2012, 34(9):1082-1088.JIA S J, MENG A M. The development of zebrafish research in China[J]. Hereditas, 2012, 34(9):1082-1088. |
| [2] | LIAO B K, DENG A N, CHEN S C, et al. Expression and water calcium dependence of calcium transporter isoforms in zebrafish gill mitochondrion-rich cells[J]. BMC Genomics, 2007, 8:354. |
| [3] | TSENG D Y, CHOU M Y, TSENG Y C, et al. Effects of stanniocalcin 1 on calcium uptake in zebrafish (Danio rerio) embryo[J]. American Journal of Physiology Regulatory, Integrative and Comparative Physiology, 2009, 296(3):R549-R557. |
| [4] | VANOEVELEN J, JANSSENS A, HUITEMA L F A, et al. Trpv5/6 is vital for epithelial calcium uptake and bone formation[J]. The Faseb Journa, 2011, 25(9):3197-3207. |
| [5] | WANG Y F, TSENG Y C, YAN J J, et al. Role of SLC12A10.2, a Na-Cl cotransporter-like protein, in a Cl uptake mechanism in zebrafish (Danio rerio)[J]. American Journal of Physiology Regulatory, Integrative and Comparative Physiology, 2009, 296(5):R1650-R1660. |
| [6] | RYAZANOVA L V, DOROVKOV M V, ANSARI A, et al. Characterization of the protein kinase activity of TRPM7/ChaK1, a protein kinase fused to the transient receptor potential ion channel[J]. Journal of Biological Chemistry, 2004, 279(5):3708-3716. |
| [7] | HOENDEROP J G J, BINDELS R J M. Calciotropic and magnesiotropic TRP channels[J]. Physiology, 2008, 23(1):32-40. |
| [8] | KONRAD M, SCHLINGMANN K P, GUDERMANN T. Insights into the molecular nature of magnesium homeostasis[J]. American Journal of Physiology Renal Physiology, 2004, 286(4):599-605. |
| [9] | ARJONA F J, CHEN Y X, FLIK G, et al. Tissue-specific expression and in vivo regulation of zebrafish orthologues of mammalian genes related to symptomatic hypomagnesemia[J]. Pflügers Archiv:European Journal of Physiology, 2013, 465(10):1409-1421. |
| [10] | FERRÉ S, HOENDEROP J J, BINDELS R J. Role of the distal convoluted tubule in renal Mg2+ handling:molecular lessons from inherited hypomagnesemia[J]. Magnesium Research, 2011, 24(3):101-108. |
| [11] | KONRAD M, SCHLINGMANN K P. Inherited disorders of renal hypomagnesaemia[J]. Nephrology, Dialysis, Transplantation, 2014, 29(Suppl 4):63-71. |
| [12] | CONG L, RAN F A, COX D, et al. Multiplex genome engineering using CRISPR/Cas systems[J]. Science, 2013, 339(6121):819-823. |
| [13] | MALI P, YANG L H, ESVELT K M, et al. RNA-guided human genome engineering via Cas9[J]. Science, 2013, 339(6121):823-826. |
| [14] | HWANG W Y, FU Y F, REYON D, et al. Efficient genome editing in zebrafish using a CRISPR-Cas system[J]. Nature Biotechnology, 2013, 31(3):227-229. |
| [15] | JINEK M, CHYLINSKI K, FONFARA I, et al. A programmable dual-RNA-guided DNA endonuclease in adaptive bacterial immunity[J]. Science, 2012, 337(6096):816-821. |
| [16] | GASIUNAS G, BARRANGOU R, HORVATH P, et al. Cas9-crRNA ribonucleoprotein complex mediates specific DNA cleavage for adaptive immunity in bacteria[J]. Proceedings of the National Academy of Sciences of the United States of America, 2012, 109(39):2579-2586. |
| [17] | CADE L, REYON D, HWANG W Y, et al. Highly efficient generation of heritable zebrafish gene mutations using homo-and heterodimeric TALENs[J]. Nucleic Acids Research, 2012, 40(16):8001-8010. |
| [18] | ZU Y, TONG X J, WANG Z X, et al. TALEN-mediated precise genome modification by homologous recombination in zebrafish[J]. Nature Methods, 2013, 10(4):329-331. |
| [19] | SANDER J D, CADE L, KHAYTER C, et al. Targeted gene disruption in somatic zebrafish cells using engineered TALENs[J]. Nature Biotechnology, 2011, 29(8):697-698. |
| [20] | ARJONA F J, DE BAAIJ J H, SCHLINGMANN K P, et al. CNNM2 mutations cause impaired brain development and seizures in patients with hypomagnesemia[J]. PLoS Genetics, 2014, 10(4):e1004267. |
 2015, Vol. 24
2015, Vol. 24


