2. 中国水产科学研究院东海水产研究所, 上海 200090;
3. 上海海洋大学 上海高校知识服务平台水产动物遗传育种中心, 上海 201306
肌肉生长抑制素(Myostatin,MSTN)又称GDF-8(growth differentiation factor 8),是转化生长因子超家族的成员[1]。哺乳动物的MSTN基因主要在骨骼肌中表达,是肌肉生长的负向调节因子,一些养殖动物的双肌性状就是由于该基因的突变,导致MSTN蛋白无法正常抑制骨骼肌细胞的生长引起的[1, 2]。进一步的研究表明,MSTN基因敲除后的小鼠较正常小鼠体重增加30%,骨骼肌纤维数量明显增多,骨骼肌肉重量是正常小鼠的3倍以上[3],说明该基因对肌肉生长有抑制作用。因此,通过深入研究MSTN基因的生理功能及其调控机制,对改善养殖动物的生长性能具有一定应用前景[4]。
近年来,有关甲壳动物MSTN基因的研究日益增多,MSTN基因已经在多种甲壳动物中被克隆[5, 6, 7, 8],这些研究结果表明甲壳动物与脊椎动物MSTN蛋白结构域组成高度保守:都由N端的信号肽、前肽结构域和C端成熟肽结构域组成;前肽和成熟肽结构域之间具有保守的弗林蛋白裂解位点(RXXR)[5, 7, 8, 9, 10, 11, 12]。但是,甲壳动物和高等脊椎动物MSTN基因的组织分布差别较大,甲壳动物的MSTN基因在肌肉和非肌肉组织中都有广泛表达,而高等脊椎动物中的MSTN基因主要表达于肌肉组织中,这暗示MSTN在甲壳动物中并不是一种肌肉组织特异性蛋白,其生理功能可能并不局限于肌肉生长的调节[5, 6, 7, 8, 9, 10, 11, 12]。
甲壳动物的肌肉生长与蜕皮紧密联系,蜕皮前甲壳动物的肌肉需要经历一个可逆性的“萎缩”过程,这种肌肉的萎缩有利于甲壳动物从较小的旧壳,特别是大螯和附肢较小的关节部位中蜕出[13]。先前对陆地蟹(Gecarcinus lateralis)和斑节对虾(Penaeus monodon)的研究结果表明,甲壳动物MSTN的基因表达水平与其所处蜕皮阶段显著相关,但与预期不同的是,MSTN基因的表达水平与肌肉生长呈正相关,通常在刚刚蜕皮的A期表达水平最高,在蜕皮前的D期(肌肉萎缩期)表达水平最低[12],这暗示MSTN基因对于甲壳动物肌肉生长的调控作用可能与脊椎动物相反,主要正向调控肌肉生长。斑节对虾中MSTN的基因沉默实验也验证了这一推测:当通过dsRNA干扰使斑节对虾MSTN基因表达水平下降时,该虾的生长速度减慢[11]。
中华绒螯蟹(Eriocheir sinensis)是我国重要的经济蟹类,有关其生长蜕皮的分子机理研究较少[6, 14]。尽管其MSTN基因已经被克隆,推测其与中华绒螯蟹肌肉生长有关,但是尚不清楚中华绒螯蟹不同蜕皮阶段该基因的表达水平变化情况,这非常不利于中华绒螯蟹肌肉生长机制的研究。因此本研究根据GenBank登录的中华绒螯蟹MSTN(EsMSTN)基因序列(序列号:EU650662)设计特异性引物,通过荧光定量PCR技术研究了中华绒螯蟹MSTN基因在不同组织、不同蜕皮阶段的表达情况,旨在为进一步认识和深入研究中华绒螯蟹生长蜕壳过程中MSTN基因的功能提供基础资料。
1 材料与方法 1.1 实验材料实验用中华绒螯蟹幼蟹取自上海海洋大学崇明中华绒螯蟹养殖基地,平均体质量10 g左右,活体运到实验室后在室内水族箱(长×宽×高=75 cm×53 cm×45 cm)中暂养一周,箱底放置无毒PVC管作为隐蔽物,暂养期间每只水族箱放20只幼蟹,暂养期间每日下午17: 00按照蟹体质量的3%投喂对虾饲料。自然光照,水温控制在24~26 ℃,pH 7.0~9.0,溶解氧>5 mg/L,氨氮<0.5 mg/L,亚硝酸盐氮<0.15 mg/L。实验用蟹暂养一周后,挑选肢体健全,活力较好的个体用于实验,正式实验期间的养殖和投喂管理同暂养。参考康现江等[15]的方法,将中华绒螯蟹蜕皮周期划分为蜕皮期(E期)、蜕皮后期(AB期)、蜕皮间期(C期)和蜕皮前期(D期)4个蜕皮时期。每日检查每只蟹所处的蜕皮阶段,并采集处于特定蜕皮时期的中华绒螯蟹肌肉、表皮、胃、肠、肝胰腺、鳃、胸神经节和脑神经节的组织样品。每个蜕皮时期采集4只个体,所有样品液氮速冻后保存于-80 ℃冰箱待用。尽管D期可以进一步划分为D0、D1、D3-43个不同的亚期,但每个亚期的持续时间较短,且D2亚期仅通过形态学方法难以辨别,因此本研究中D期样品均采集自形态特征明显的D3-4亚期[16]。
1.2 实时荧光定量PCR(qRT-PCR)参照总RNA提取试剂盒(TaKaRa,Cat.D9108A)说明提取中华绒螯蟹各蜕皮时期组织样品总RNA,分别采用1%琼脂糖凝胶电泳和微量紫外分光光度计检测RNA完整度和纯度。提取的总RNA满足实验要求后,取100 ng作为模板,使用TaKaRa反转录试剂盒(Cat.D2639A)进行cDNA合成。根据中华绒螯蟹MSTN cDNA全长序列,采用Primer Premier 5.0软件设计定量PCR用特异性引物:EsMSTN F1/R1和EsMSTN F2/R2,同时以β-actin F/R为引物对内参基因β-actin进行扩增(表1)。
| 表1 实验用PCR引物及序列 Tab.1 Primers and their sequences used in this experiment |
参照TaKaRa定量PCR试剂盒(Cat.DRR420A)使用说明,将肌肉组织cDNA梯度稀释后作为模板进行标准曲线扩增。当实验结果满足无非特异性扩增,目标基因MSTN和内参基因β-actin的扩增效率为95%~105%,标准曲线R2>0.99时确定qRT-PCR的反应条件与体系,并最终确定EsMSTN F2/R2作为EsMSTN qRT-PCR实验用引物。反应体系为20 μL:上下游引物各0.4 μL(10 μmol/L),SYBR Premix Ex TaqTM (2×)10 μL,cDNA模板2 μL,ROX Reference DyeⅡ (50×)0.4 μL,RNase free H2O补足至20 μL。反应条件为:95 ℃预变性30 s;95 ℃变性3 s,60 ℃退火30 s,40个循环。
确定反应体系与条件后,首先以C期中华绒螯蟹肌肉、表皮、胃、肠、肝胰腺、鳃、胸神经节和脑神经节8种组织的cDNA样品为模板,研究EsMSTN在各个组织中的表达情况。根据EsMSTN在各组织中的表达分布情况,进一步对不同蜕皮阶段肌肉、胸神经节、肝胰腺、上皮、肠中EsMSTN的表达变化进行了研究。每个蜕皮时期重复4只个体,每只个体重复测定4个样品。
1.3 数据分析采用β-actin作为内参基因计算ΔCt,通过公式ΔΔCt=ΔCt样品-ΔCt对照计算ΔΔCt。2-ΔΔCt法计算EsMSTN-mRNA的相对表达水平[17],所得数据以平均值±标准差表示。采用SPSS 17.0软件对定量PCR数据进行ANOVA方差分析。分析前先采用Levene’s法对数据进行方差齐性检验,当不满足方差齐性时对数据进行反正弦或平方根处理,满足方差齐性后采用Duncan氏法进行多重比较,P<0.05时认为差异显著。
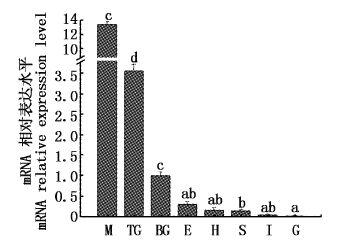
2 结果 2.1 EsMSTN在蜕皮间期不同组织中的表达情况qRT-PCR结果显示,在所有检测组织中,EsMSTN在蜕皮间期的肌肉组织中表达水平最高,肌肉中该基因的mRNA相对表达量远高于其他组织;胸神经节和脑神经节中的EsMSTN-mRNA表达水平仅次于肌肉;EsMSTN在上皮组织、肝胰腺和胃中也有少量表达;整体上,肠和鳃中的EsMSTN-mRNA表达水平极低(图1)。
|
图1
蜕皮间期中华绒螯蟹各组织中EsMSTN-mRNA的表达差异分析
Fig.1
Analysis of expression differences of EsMSTN-mRNA in various tissues at the intermolt period of E. sinensis
M.肌肉;TG.胸神经节;BG.脑神经节;E.表皮;H.肝胰腺;S.胃;I.肠道;G.鳃;柱形图上含有不同字母代表不同组织中的EsMSTN-mRNA表达量差异显著(P<0.05),图2同。 M.muscle;TG.thoracic ganglia;BG.Brain ganglia;E.Epithelium;H.Hepatopancreas;S.Stomach;I.Intestine;G.Gill. Bars with different letters mean significant differences (P<0.05) of EsMSTN-mRNA expression level in various tissues,the same as fig.2. |
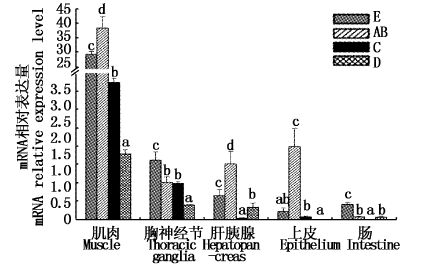
根据EsMSTN在蜕皮间期不同组织中的表达情况,选取肌肉、胸神经节、肝胰腺、肠和上皮5个主要组织,研究EsMSTN在中华绒螯蟹蜕皮过程中的表达变化情况。实验结果表明,EsMSTN-mRNA在5种组织中的表达水平均随着蜕皮阶段的变化而显著变化(P<0.05),但不同组织中的EsMSTN-mRNA变化趋势有所不同。肌肉中EsMSTN-mRNA最高相对表达量出现在AB期,此后显著下降,到D期表达水平最低;E期的EsMSTN-mRNA表达水平又显著上升,但仍显著低于AB期(P<0.05)。上皮组织中的EsMSTN-mRNA表达水平变化规律与肌肉类似。肝胰腺中EsMSTN mRNA表达水平变化规律与肌肉中略有不同,C期表达水平最低,D期次之。与上述3个组织中不同,胸神经节中EsMSTN-mRNA的相对表达量在E期最高,随后呈现逐渐递减趋势,AB期和C期EsMSTN-mRNA的表达水平显著低于E期,D期显著低于其他各期。肠中EsMSTN-mRNA的表达水平总体较低,最高表达水平出现在E期,C期表达量最低,AB和D期的EsMSTN-mRNA表达水平显著高于C期,但显著低于E期(图2)。
|
图2 不同蜕皮阶段中华绒螯蟹5种组织中的EsMSTN-mRNA表达差异分析 Fig.2 Analysis of expression differences of EsMSTN-mRNA in five tissues at the different molting stages of E. sinensis |
与高等脊椎动物中MSTN主要在骨骼肌中表达不同,MSTN在甲壳动物中具有广泛的组织分布,如:美洲螯虾(Homarus americanus)的肌肉、中肠、后肠、肝胰腺和胸神经节等11种组织中都有MSTN-mRNA表达,其中后肠和肌肉中表达水平最高,肝胰腺、胸神经节和中肠中也有较高表达水平[8];斑节对虾MSTN在肌肉、肝胰腺、眼柄、心脏、鳃和胃中都有表达,其中心脏中mRNA表达水平最高[11]。本研究结果显示,EsMSTN在蜕皮间期中华绒螯蟹的肌肉组织中优势表达,在神经组织(胸神经节和脑神经节)中也有较高的mRNA表达水平,其他组织中表达水平较低(图1),这与先前的研究结果基本一致[6]。值得注意的是,KIM等的研究表明EsMSTN-mRNA在中华绒螯蟹肠道中表达水平也相对较高,而本研究中该组织内的EsMSTN-mRNA相对表达水平很低,这很可能是由两个实验中采用的中华绒螯蟹所处的发育阶段和蜕皮阶段不同造成的。KIM等在研究中采用的是中华绒螯蟹成蟹,并且在实验样品采集时没有考虑蟹所处的蜕皮时期。本研究中检测EsMSTN组织分布的样品采用的是处于蜕皮间期(C期)的中华绒螯蟹幼蟹(体质量10 g左右),而同一甲壳动物在不同生长发育及蜕皮阶段,同一组织中的MSTN-mRNA表达水平可能有所不同[6, 8, 9]。这也有可能是造成不同甲壳动物MSTN组织分布存在差异的原因。
总体上,MSTN在甲壳动物非肌肉组织中的广泛表达可能与该基因的进化历程联系紧密。MSTN与GDF-11基因同属TGF-β超家族,共同组成MSTN/GDF11基因家族。该基因家族在脊椎动物进化过程中发生了两次基因复制:第一次发生在脊椎动物进化早期,MSTN与GDF11基因发生分化[18]。功能上,前者主要参与肌肉生长的负向调控,后者负责调节嗅觉上皮中的神经发生以及中轴骨骼的发育[19, 20];第二次基因复制发生在辐鳍鱼起源时,在鱼类中产生了多种MSTN基因,组织分布特异性更强[18, 21, 22]。无脊椎动物中,MSTN/GDF11由于没有经历基因的复制,始终只有一个基因型[23]。所以在组织分布上,甲壳动物MSTN兼有GDF11的特征,在胸神经节、脑神经节等非肌肉组织中也有广泛表达,这也暗示甲壳动物中MSTN的生理功能不局限于肌肉生长的调控。
在中华绒螯蟹不同蜕皮阶段,EsMSTN在5种检测组织中的mRNA相对表达量变化显著。其中,肌肉中EsMSTN-mRNA的总体表达水平最高,并且在E期以及AB期表达水平最高,D期最低。这与其他甲壳动物中的研究结果类似。如:凡纳滨对虾和斑节对虾肌肉组织中MSTN的mRNA表达水平在A期最高,B-C期显著下降[11, 12]。MSTN基因在蜕皮过程中的这种变化趋势与其对甲壳动物肌肉生长的调节作用密切相关,但调控方向可能与脊椎动物相反。脊椎动物中,MSTN是肌肉生长的负向调节因子,MSTN表达量的升高会导致肌肉量的降低和组织生长的速度减缓[1, 24]。而当陆地蟹的肌肉量在蜕皮前期减少78%时,其肌肉中MSTN-mRNA的表达水平逐渐降低[25];斑节对虾中MSTN的功能研究结果也表明,当对斑节对虾MSTN基因进行沉默,使其mRNA表达水平下降40%时,虾的生长速度减慢68%[11],这些结果都暗示MSTN正向调节甲壳动物的肌肉生长。因此,EsMSTN在蜕皮后的AB期表达水平最高,因为此时没有外骨骼的限制,动物肌肉组织正处于快速的生长阶段[26];而在蜕皮前期,为了方便身体从旧壳狭小的关节部位蜕出[13],甲壳动物的肌肉组织会经历一个不断萎缩的过程,对应地,EsMSTN的基因表达水平在此阶段较低。另外,肠道、上皮、肝胰腺和胸神经节中EsMSTN基因在E期或AB期显著较高的表达水平,暗示这些组织的细胞增殖和分化主要发生在这两个阶段,这与笔者之前的研究结果相一致[27],但组织间细胞增殖分化的时序可能存在一定差异。相对于其他非肌肉组织,蜕皮过程中EsMSTN在胸神经节中总体较高的表达水平表明EsMSTN可能兼有脊椎动物中GDF11的功能,参与神经发生的调节[20];而该组织中EsMSTN-mRNA在E期和AB期的高表达提示甲壳动物中MSTN类似于昆虫中的iMSTN/GDF11,正向调节神经的形成和发生[28, 29]。
| [1] | MCPHERRON A C, LEE S J. Double muscling in cattle due to mutations in the myostatin gene[J]. Proceedings of the National Academy of Science of the United States of America, 1997, 94(23): 12457-12461. |
| [2] | HADJIPAVLOU G, MATIKA O, CLOP A, et al. Two single nucleotide polymorphisms in the myostatin(GDF8) gene have significant association with muscle depth of commercial Charollais sheep[J]. Animal Genetics, 2008, 39(4): 346-353. |
| [3] | MCPHERRON A C, LAWLER A M, LEE S J. Regulation of skeletal muscle mass in mice by a new TGF-β superfamily member[J]. Nature, 1997, 387(6628): 83-90. |
| [4] | MEDEIROS E F, PHELPS M P, FUENTES F D, et al. Overexpression of follistatin in trout stimulates increased muscling[J]. American Journal of Physiology. Regulatory, Integrative and Comparative Physiology, 2009, 297(1): R235-R242. |
| [5] | KIM H W, MYKLES D L, GOETZ F W, et al. Characterization of a myostatin-like gene from the bay scallop, Argopecten irradians[J]. Biochimica et Biophysica Acta(BBA)-Gene Structure and Expression, 2004, 1679(2): 174-179. |
| [6] | KIM K S, JEON J M, KIM H W. A myostain-like gene expressed highly in the muscle tissue of Chinese mitten crab, Eriocheir sinensis[J]. Fisheries and Aquatic Sciences, 2009, 12(3): 185-193. |
| [7] | KIM K S, KIM Y J, JEON J M, et al. Molecular characterization of myostatin-like genes expressed highly in the muscle tissue from Morotoge shrimp, Pandalopsis japonica[J]. Aquaculture Research, 2010, 41(11): e862-e871. |
| [8] | MACLE K S, COVI J A, KIM H W, et al. Myostatin from the American lobster, Homarus americanus: Cloning and effects of molting on expression in skeletal muscles[J]. Comparative Biochemistry and Physiology Part A: Molecular & Integrative Physiology, 2010, 157(4): 328-337. |
| [9] | COVI J A, KIM H W, MYKLES D L. Expression of alternatively spliced transcripts for a myostatin-like protein in the blackback land crab, Gecarcinus lateralis[J]. Comparative Biochemistry and Physiology Part A: Molecular & Integrative Physiology, 2008, 150(4): 423-430. |
| [10] | LO P C H, FRASCH M. Sequence and expression of myoglianin, a novel Drosophila gene of the TGF-β superfamily[J]. Mechanisms of Development, 1999, 86(1/2): 171-175. |
| [11] | DE SANTIS C, WADE N M, Jerry D R, et al. Growing backwards: an inverted role for the shrimp ortholog of vertebrate myostatin and GDF11[J]. The Journal of Experimental Biology, 2011, 214(16): 2671-2677. |
| [12] | QIAN Z Y, MI X, WANG X Z, et al. cDNA cloning and expression analysis of myostatin/GDF11 in shrimp, Litopenaeus vannamei[J]. Comparative Biochemistry and Physiology Part A: Molecular & Integrative Physiology, 2013, 165(1): 30-39. |
| [13] | MYKLES D L. Crustacean muscle plasticity: Molecular mechanisms determining mass and contractile properties[J]. Comparative Biochemistry and Physiology Part B: Biochemistry and Molecular Biology, 1997, 117(3): 367-378. |
| [14] | 王瑶, 杨志刚, 郭子好, 等. 中华绒螯蟹RXR基因全长cDNA克隆及表达分析[J]. 水产学报, 2013, 37(12): 1761-1769. WANG Y, YANG Z G, GUO Z H, et al. The full length cDNA cloning and expression analysis of RXR from the Chinese mitten crab(Eriocheir sinensis)[J]. Journal of Fisheries of China, 2013, 37(12): 1761-1769. |
| [15] | 康现江, 田志环, 吴江立, 等. 中华绒螯蟹蜕皮周期及蜕皮过程中肝胰腺消化酶活性的变化[J]. 中国水产科学, 2012, 19(5): 806-812. KANG X J, TIAN Z H, WU J L, et al. Molt stages and changes in digestive enzyme activity in hepatopancreas during molt cycle of Chinese mitten crab, Eriocheir sinensis[J]. Journal of Fishery Sciences of China, 2012, 19(5): 806-812. |
| [16] | GUERAO G, ROTLLANT G, ANGER K. Characterization of larval moulting cycles in Maja brachydactyla(Brachyura, Majidae) reared in the laboratory[J]. Aquaculture, 2010, 32(1/2): 106-111. |
| [17] | LIVAK K J, SCHMITTGEN T D. Analysis of relative gene expression data using real-time quantitative PCR and the 2-ΔΔCT method[J]. Methods, 2001, 25(4): 402-408. |
| [18] | RODGERS B D, ROALSON E H, WEBER G M, et al. A proposed nomenclature consensus for the myostatin gene family[J]. American Journal of Physiology-Endocrinology and Metabolism, 2007, 292(2): E371-E372. |
| [19] | MCPHERRON A C, HUYNH T V, LEE S J. Redundancy of myostatin and growth/differentiation factor 11 function[J]. BMC Developmental Biology, 2009, 9: 24-24. |
| [20] | WU H H, IVKOVIC S, MURRAY R C, et al. Autoregulation of neurogenesis by GDF11[J]. Neuron, 2003, 37(2): 197-207. |
| [21] | GARIKIPATI D K, GAHR S A, RODGERS B D. Identification, characterization, and quantitative expression analysis of rainbow trout myostatin-1a and myostatin-1b genes[J]. Journal of Endocrinology, 2006, 190(3): 879-888. |
| [22] | GARIKIPATI D K, GAHA S A, ROALSON E H, et al. Characterization of rainbow trout myostatin-2 genes(rtMSTN-2a and-2b): Genomic organization, differential expression, and pseudogenization[J]. Endocrinology, 2007, 148(5): 2106-2115. |
| [23] | SAINA M, TECHNAU U. Characterization of myostatin/gdf8/11 in the Starlet Sea Anemone Nematostella vectensis[J]. Journal of Experimental Zoology Part B: Molecular and Developmental Evolution, 2009, 312B(7): 780-788. |
| [24] | LEE C Y, HU S Y, GONG H Y, et al. Suppression of myostatin with vector-based RNA interference causes a double-muscle effect in transgenic zebrafish[J]. Biochemical and Biophysical Research Communications, 2009, 387(4): 766-771. |
| [25] | COVI J A, BADER B D, CHANG E S, et al. Molt cycle regulation of protein synthesis in skeletal muscle of the blackback land crab, Gecarcinus lateralis, and the differential expression of a myostatin-like factor during atrophy induced by molting or unweighting[J]. The Journal of Experimental Biology, 2010, 213(1): 172-183. |
| [26] | MEDLER S, LILLEY T R, RIEHL J H, et al. Myofibrillar gene expression in differentiating lobster claw muscles[J]. Journal of Experimental Zoology Part A: Ecological Genetics and Physiology, 2007, 307(5): 281-295. |
| [27] | 王伟, 吴旭干, 楼宝, 等. 三疣梭子蟹(Portunus trituberculatus)RXR基因克隆及其在蜕皮过程中的表达分析[J]. 海洋与湖沼, 2014, 45(5): 1105-1114. WANG W, WU X G, LOU B, et al. Cloning of retinoid X receptor(RXR) and its expression analysis during molting in Portunus trituberculatus[J]. Oceanologia et Limnologia Sinica, 2014, 45(5): 1105-1114. |
| [28] | ABERLE H, HAGHGHI A P, FETTER R D, et al. Wishful thinking encodes a BMP type Ⅱ receptor that regulates synaptic growth in Drosophila[J]. Neuron, 2002, 33(4): 545-558. |
| [29] | LEE-HOEFLICHI S T, ZHAO X, MEHRA A, et al. The Drosophila type Ⅱ receptor, Wishful thinking, binds BMP and myoglianin to activate multiple TGF β family signaling pathways[J]. FEBS Letters, 2005, 579(21): 4615-4621. |
2. East China Sea Fisheries Research Institute, Chinese Academy of Fishery Sciences, Shanghai 200090, China;
3. Aquatic Animal Breeding Center of Shanghai University Knowledge Service Platform, Shanghai Ocean University, Shanghai 201306, China
 2015, Vol. 24
2015, Vol. 24


