2. 国家海洋局东海环境监测中心, 上海 200137;
3. 海洋赤潮灾害立体监测技术与应用国家海洋局重点实验室, 上海 200137
海洋中生物众多,蕴藏资源丰富,是人类赖以生存发展的重要物质基础,在人类社会的发展历史上有着非常重要的地位。如今,随着人类对地球资源开发的日益加剧和海上交通运输业的高速发展,海洋正承受着严重的环境污染损害,面临着严重的环境破坏威胁[1]。在众多的污染物之中,石油是近海的主要污染物。据统计显示,我国近年来每年排放进入大海的石油约有12×104 t[2],并且由于多种方面的原因,海洋石油污染正呈现日趋加剧的趋势[3]。21世纪作为海洋的世纪,海洋环境保护相关问题受到全球关注,如何有效地保护海洋环境,维持近海海域的生态平衡,已经成为各国制定其可持续发展战略非常重要的组成部分。研究石油对海洋浮游植物的影响,对研究海洋初级生产力状况、海洋生物多样性和海洋生态损害评估等具有非常重要的意义[4, 5]。
浮游植物作为海洋环境中的主要生物,其健康状态和海洋生态环境息息相关。在海洋食物链之中,浮游植物作为初级生产者,通过光合作用来制造有机物,是海洋食物链的第一营养阶层。浮游植物在海洋食物链中占有举足轻重的地位,对生态系统的物质循环与能量流动起着关键性作用。溢油污染严重影响浮游植物的生长、叶绿素等大分子的合成,破坏海洋生物链[7]。
目前关于石油类对浮游植物生长影响的研究已经较为广泛,基本上围绕着石油水溶解组分(water-accommodated fraction,WAF)的浓度变化展开研究,得出石油烃对浮游植物生长“低促高抑”的现象[7],即低浓度促进生长,高浓度抑制生长。在东海海域,各大油田开采均为轻质原油,鉴于其极易挥发的特性,与之前的研究结果可能会有细微差别。所以,本文采用轻质油水溶解成分进行实验,对东海原甲藻和赤潮异弯藻的生长情况进行研究,将在石油污染对浮游植物生长影响方面,填补轻质油领域的空白,为海洋石油污染的应急处置、损害赔偿和综合管理提供重要的技术。
1 材料与方法 1.1 实验材料 1.1.1 实验油种实验所用轻质原油采自东海平湖油气田。东海平湖油气田是我国在东海发现和开发的第一个中型油气田,位于东海陆架盆地西湖凹陷平湖断裂构造带中部,上海市的东南方向,距上海南汇嘴365 km,距舟山定海约260 km。油气田地理坐标为29°02′~29°08′N,124°54′~124°58′E。东海平湖油气田开发工程海上工程平湖综合平台于1998年建成,整体工程包括一座钻井生产平台、一条通往上海南汇约400 km的14″天然气管道和一条通往浙江岱山岛约300 km的10″原油管道,平湖综合平台目前拥有10口油井和10口气井。
1.1.2 实验藻种东海原甲藻(Prorocentrum donghaiense)和赤潮异弯藻(Heterosigma akashiwo) 取自上海海洋大学水域环境生态上海高校工程研究中心,用盐度为32的海水,加入f/2培养基,在实验室培养扩大后,取指数生长期的健康藻种。
1.2 实验方法 1.2.1 藻类培养微藻的培养采用f/2配方培养液,培养温度为(22±1) ℃,pH为7.8~7.9,明暗周期为12 h∶12 h,光源为白色日光灯,光照强度约为6 000 lx。在整个培养过程中,各操作步骤均进行灭菌处理,每日摇动培养器皿3~5次[1]。
1.2.2 轻质油水溶解组分制备首先将海水粗滤后经 0.45 μm 醋酸纤维滤膜二次过滤,将原油与过滤海水按照体积比 1∶9混合,置于磁力搅拌器上持续搅拌24 h,将混合液倒入分液漏斗中静置4 h,分离出下层的水相为实验母液,母液置于4 ℃冰箱保存。通过紫外分光光度法[31]测定,轻质油WAF母液浓度为11.72 mg/L[8]。
1.2.3 轻质油WAF胁迫实验在6个2 000 mL烧杯中,分别加入不同体积的轻质油WAF母液和过滤灭菌海水,总体积为1 000 mL。其中一只烧杯作为空白对照组,只加入过滤灭菌海水,轻质油WAF浓度为0,其余5组WAF的浓度分别为0.73、1.46、2.93、5.86和11.72 mg/L。加入指数生长期微藻藻液,使起始细胞密度为104 cell/cm3,于恒温培养箱培养,实验条件与微藻培养条件相同。此实验做3个平行,同时做一组空白平行,测轻质油WAF浓度变化。分别于0、 24、 48、 72和 96 h取2 mL 藻液,应用显微镜计数法测定细胞密度[1]。 对于上述实验,分别在10、16、20和28 ℃条件下进行。
微藻细胞计数采用血球计数板法[31]。
1.2.4 轻质油WAF浓度测定按照体积比配制不同轻质油WAF浓度梯度的海水培养液,分别于10、16、20和28℃下以空白平行组在0、24、48、72和96 h测轻质油WAF浓度变化。
1.2.5 96-EC50计算
当我们忽略实验样品的起始密度差别时,不同时间轻质油对东海原甲藻的生长抑制率P(%)由式(1)求得[17]:
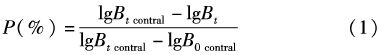
用96 h微藻的抑制率P(%)对轻质油WAF浓度作图,抑制率为50%时对应的浓度即为轻质油对微藻的96h-EC50。
1.3 数据处理本文运用SPSS 17.0统计软件进行数据处理与作图,微藻细胞数结果以3个平行组数据的平均值±标准差(Mean±SD)表示。
2 结果 2.1 轻质油WAF浓度变化鉴于东海海域石油开采及管道运输原油的特点,本实验采用轻质原油,轻质原油具有挥发性强的特点,制备成轻质油WAF水溶解组分后,测得的最高油浓度为11.72 mg/L。我们的实验中,将轻质油WAF浓度梯度分别设置为0.73、1.46、2.93、5.86和11.72 mg/L,并以不加油的实验海水作空白对照。
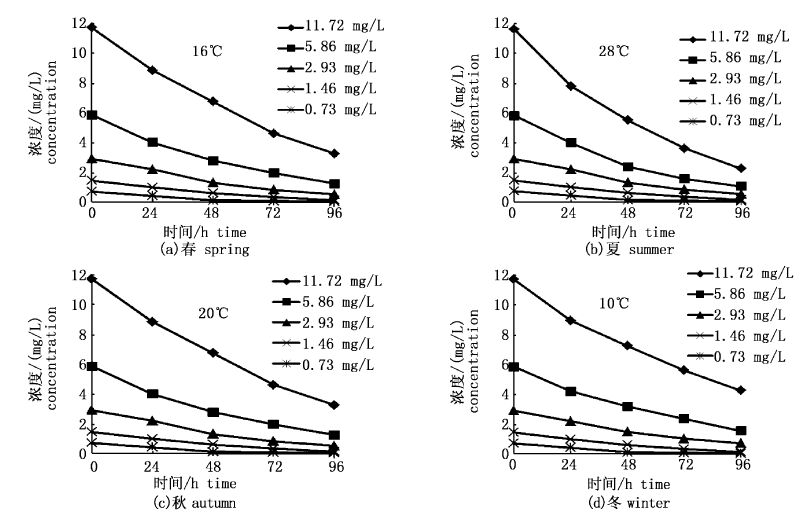
实验过程中,同时对轻质油WAF的浓度变化进行了周期性测定,结果如图1所示,随着实验的进行,实验海水中轻质油WAF浓度变化明显,尤其是5.86和11.72 mg/L两个浓度梯度,几乎呈直线下降趋势。同时,季节温度的变化也是影响轻质油浓度变化的关键因素,温度越高,轻质油挥发性越强,这在图1中也有一定的体现。
|
图1 各季不同轻质油WAF浓度随时间变化曲线 Fig.1 Curves of different light oil WAF concentration changes with time in all the seasons |
其实,与轻质油WAF相比,轻质原油本身的挥发性更强,根据实验结果显示,轻质原油的挥发最快的时间是在刚刚挥发开始的10 min内,10 min可以挥发75%左右,1 h可以挥发80%以上。经过8 d的挥发,油品基本上可以挥发90%以上。实验油质挥发性的因素,在以前的文献中是几乎未曾考虑过的。
图1表示不同实验温度实验海水在5个轻质油WAF浓度梯度下,油浓度随时间的变化曲线。从图中可以看到,随着时间变化,各组轻质油WAF的浓度都呈下降趋势,11.72和5.86 mg/L两组的下降趋势最为明显。同时,在不同实验温度下,轻质油WAF的浓度变化略微不同,比较之下发现温度越高下降越显著。
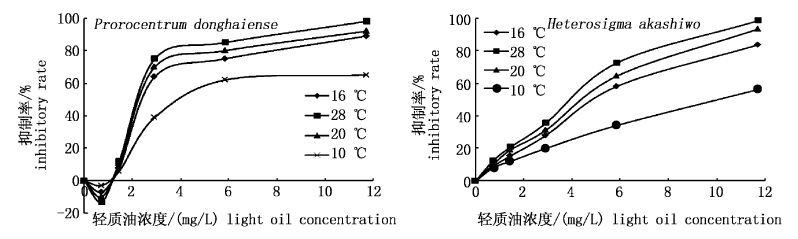
2.2 96h-EC50根据公式(1),用96 h东海原甲藻的抑制率P(%)对轻质油WAF浓度作图,抑制率为50%时对应的浓度即为轻质油对东海原甲藻的96 h-EC50,即96 h时的急性毒性参数。本实验结果如图2所示,经计算,10、16、20和28 ℃下的96 h-EC50分别为3.86、2.28、2. 21和2.03 mg/L。
|
图2 各季不同轻质油浓度对东海原甲藻和赤潮异弯藻的生长抑制率曲线 Fig.2 The percent inhibition curve of Prorocentrum donghaiense and Heterosigma akashiwo in light oil of different concentrations in all the seasons |
同样,用96 h赤潮异弯藻的抑制率P(%)对轻质油WAF浓度作图,赤潮异弯藻的96 h抑制率曲线如图2所示,经计算得轻质油对赤潮异弯藻的96 h-EC50在10、16、20和28 ℃下分别为9.72、4.30、4.79 和3.92 mg/L。
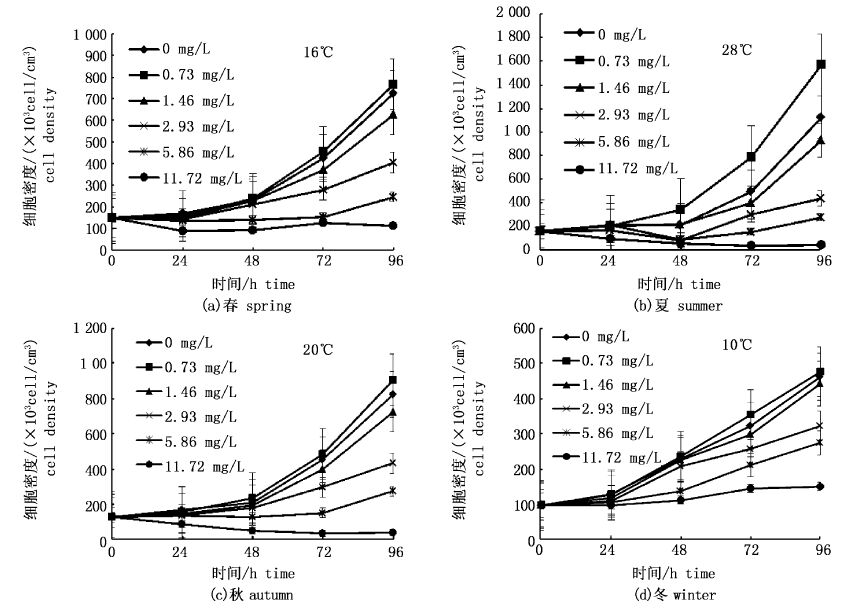
2.3 轻质油WAF对两种海洋微藻生长的影响表1为模拟东海海域四季海水参数。图3表示4种温度条件下,东海原甲藻在不同轻质油WAF浓度下的生长曲线。结果表明,当轻质油WAF浓度为0.73 mg/L时,东海原甲藻生长表现出一定的促进作用,相对空白对照组生长速率加快。随着轻质油WAF浓度的增大,东海原甲藻生长速率逐渐减缓,并表现出较明显的抑制作用,在轻质油WAF浓度为2.93 mg/L与5.86 mg/L时,表现出细胞密度先降低后增大的趋势,而轻质油WAF浓度11.72 mg/L时细胞生长处于高度抑制状态,基本不能再恢复增长。这种低促高抑的现象,与其他油质的实验结果[8, 9, 10, 11, 12, 13, 14, 15]相近。
| 表1 四季中浮游植物试验海水的参数 Tab.1 Parameters of phytoplankton experimental seawater in four seasons |
|
图3 各季不同轻质油WAF浓度下东海原甲藻生长曲线 Fig.3 Growth curve of Prorocentrum donghaiense with different doses of light oil water accommodated fraction in all the seasons |
从图3可知,东海原甲藻在不同实验温度的生长也存在着较大差异,温度是影响浮游植物生长和繁殖的重要环境因子之一。在适宜的温度范围内,当温度升高时,东海原甲藻生长速率加快,新陈代谢速率随之加快,促进了生物对毒物的吸收,使毒性增大。因此,随着温度的升高,轻质油WAF对东海原甲藻毒性作用增强,而温度较低时(10 ℃),即使轻质油WAF浓度为 11.72mg/L,东海原甲藻仍可保持一定的活性,恢复正常生长。
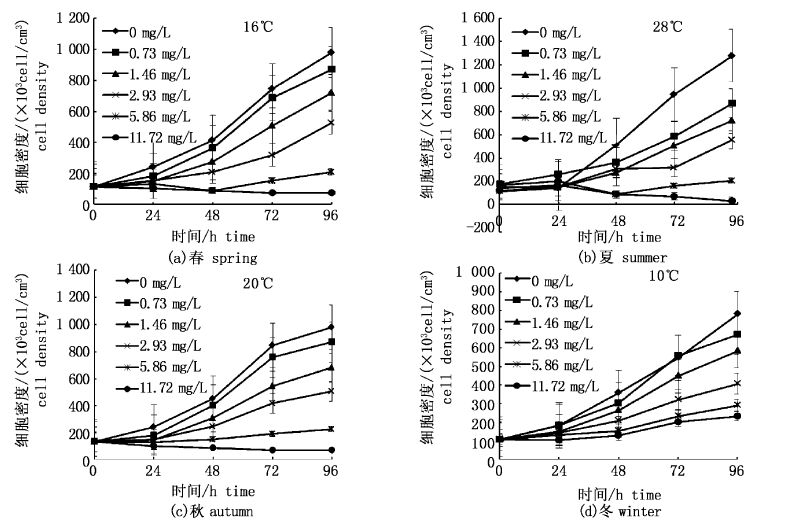
图4表示不同温度下,赤潮异弯藻在不同轻质油WAF浓度下的生长曲线。结果表明,轻质油对赤潮异弯藻的生长均表现出一定的抑制作用,随着轻质油WAF浓度的增大,赤潮异弯藻生长速率逐渐减缓,抑制作用增强,在轻质油WAF浓度为5.86 mg/L与11.72 mg/L时,细胞生长处于高度抑制状态,基本不能再恢复增长。这种抑制现象,与其他油质的实验结果[8, 9, 10, 11, 12, 13, 14, 15]相近。
|
图4 各季不同轻质油WAF浓度下赤潮异弯藻生长曲线 Fig.4 Growth curve of Heterosigma akashiwo with different doses of light oil water accommodated fraction in all the seasons |
从图4可知,赤潮异弯藻在不同温度下的生长也存在着较大差异,在适宜的温度范围内,当温度升高时,赤潮异弯藻生长速率加快,新陈代谢速率随之加快,促进了生物对毒物的吸收,使毒性增大。因此,随着温度的升高,轻质油WAF对赤潮异弯藻毒性作用增强,同样温度较低时(10 ℃),即使轻质油WAF浓度为11.72 mg/L,东海原甲藻仍可保持一定的活性,恢复正常生长。
3 讨论 3.1 轻质油浓度对浮游植物生长的影响轻质油浓度对浮游植物生长有一定的抑制作用,浓度越高抑制作用越大。本实验所得结果与前人研究结论基本相同[21, 22, 23, 24],只是所用材料轻质油挥发性强,这与余氯的研究有些相似[26, 27],前面溢油相关的文章没有考虑过这一因素。付怀洲[8]用柴油WAF(1∶9)做实验,研究了其对赤潮异弯藻的毒性,发现在柴油WAF处于低浓度(0.81 mg/L)时就有比较明显的抑制作用,而随着浓度的增大抑制作用变大。CHAO等[9]研究了两种燃料油WAF对中肋骨条藻、小球藻的生长抑制率问题,发现当油的浓度达到一定值时都能抑制两种藻的生长。王向艺[13]的实验显示,原油WAF对藻类的生长表现为低浓度时的促进作用和高浓度时的抑制作用,出现促进作用的原因可能是原油中的某些成分提供了藻类生长所需的原料。李克强等[6]研究显示,在现场和实验室条件下,No.0 柴油水溶组分在低浓度时对浮游植物生长表现出明显的促进作用,最大生长促进率分别约为180% 和120%,然而,No.0 柴油水溶组分在高浓度条件下,石油烃对浮游植物生长效应影响不甚显著,甚至表现出明显的抑制作用。结合以上研究结果,与本文实验结果对照,结果基本相同。
3.2 温度对浮游植物耐受性的影响不同季节的水温也是导致浮游植物耐受能力差异的重要原因之一。实验结果显示,不同的季节水温条件下,两种海洋微藻生长情况差异明显,温度越高海洋微藻耐受性越差。我们知道,温度是影响浮游植物生长与繁殖的重要环境因子之一。在适宜的温度范围内,当温度升高时,浮游植物新陈代谢速率随之加快,这促进了其对毒性物质的吸收,导致毒性增大。因此,冬季东海原甲藻在轻质油WAF浓度为3.86 mg/L时即达到半抑制生长,赤潮异弯藻在轻质油WAF浓度为9.72 mg/L达到这一状态。但是在夏季,两种海洋微藻达到半抑制生长状态的轻质油WAF浓度分别为2.03 mg/L和3.92 mg/L。这一结果与黄逸君等[18]的实验结论相符,其实验指出,中肋骨条藻在冬季,WAF浓度为9.94 mg/L时,14 d内可恢复生长,但是在夏季,相同WAF浓度下,中肋骨条藻的生长却被完全抑制,无法恢复生长。GONZLEZ等[20]发现,在同一WAF浓度污染下,聚球藻属(Synechococcus)和原绿球藻属(Prochlorococcus)的生长在秋季较高水温的影响下受到显著抑制,然而在冬季低温时对其生长的影响不大。
3.3 不同浮游植物对轻质油的耐受性海洋微藻种类不同,轻质油WAF对它的抑制作用也存在较大差异。本实验中选用的两种海洋微藻为东海原甲藻和赤潮异弯藻,结果显示赤潮异弯藻的耐受性更高,夏季东海原甲藻的96 h-EC50为2.03 mg/L,而赤潮异弯藻则为3.92 mg/L,冬季赤潮异弯藻96 h-EC50更是高达9.72 mg/L。张聿柏[1]的实验中也证明了这一点,石油烃对青岛大扁藻、球等鞭金藻、小东海原甲藻3种海洋微藻的急性毒性 96 h-EC50 分别为13.84 mg/L、18.83 mg/L和6.73 mg/L。黄逸君等[18]的实验也显示,不同种类海洋微藻在石油烃胁迫下,敏感性存在较大差异。王悠等[19]研究了多环芳烃的一种——蒽后发现,球等鞭金藻8701在蒽浓度为1.5 μg/L,胁迫48 h时的刺激作用最为显著;中肋骨条藻在蒽浓度为3 μg/L,胁迫24 h时的刺激作用最为显著,且两者均与对照组之间存在显著性差异。马帅[28]的研究显示,小新月菱形藻对原油WAF胁迫更加敏感。
| [1] | 张聿柏. 石油烃对海洋微藻的毒性效应及其机理研究[D]. 青岛:中国海洋大学, 2013.CHEN J B. Toxic Effects and Mechanisms of Petroleum Hydrocarbon on Marine Microalgae [D].Qingdao: Ocean University of China, 2013. |
| [2] | 陈建秋. 中国近海石油污染现状、影响和防治[J]. 节能与环保, 2002(3):15-17.CHEN J Q. The present situation, influence and control of oil pollution in China offshore [J]. Energy Conservation and Environment Protection, 2002(3):15-17. |
| [3] | 郭志平. 我国近海面临的石油污染及其防治[J]. 浙江海洋学院学报:自然科学版, 2004, 23(3):269-272.GUO Z P. The prevention and control of oil pollution off Chinese coastal waters [J]. Journal of Zhejiang Ocean University:Natural Science, 2004, 23(3):269-272. |
| [4] | 桂客. 海上溢油污染的危害及防治措施[J]. 环境保护与循环经济, 2011(11):56-58.GUI K. The harm and prevention measures of oil spill pollution [J]. Environmental Protection and Circular Economy, 2011(11):56-58. |
| [5] | 宋飞彪, 王伟洪, 张杰, 等. 石油烃污染对海洋浮游植物的影响[J]. 环境科学与管理, 2013, 38(3):84-87.SONG F B, WANG W H, ZHANG J, et al. Influence of Petroleum Hydrocarbon Pollution on Marine Phytoplankton [J]. Environmental Science and Management, 2013, 38(3):84-87. |
| [6] | 李克强, 王修林, 祝陈坚, 等. No.0柴油水溶组分海洋浮游植物生态效应研究[J]. 环境科学, 2007, 28(2):304-308.LI K Q, WANG X L, ZHU C J, et al. Ecological Effect of No10 Diesel Water Accommodated Fraction on Marine Algae [J]. Environmental Science, 2007, 28(2):304-308. |
| [7] | 王君丽, 刘春光, 冯剑丰, 等. 石油烃对海洋浮游植物生长的影响研究进展[J]. 环境污染与防治, 2011, 4(4):81-86.WANG J L, LIU C G, FENG J F, et al. Literature review of the effects of petroleum hydrocarbons on marine phytoplankton [J]. Environmental pollution and control, 2011, 4(4):81-86. |
| [8] | 付怀洲. 原油及O-#柴油对海洋微藻的急性毒性及遗传毒性研究[D]. 青岛:中国海洋大学, 2012.FU H Z. Acute toxicity and genetic toxicity of crude oil and No.0 diesel oil on marine microalgae [D]. Qingdao:Ocean University of China, 2012. |
| [9] | CHAO M, SHEN X Q, LUN F X, et al. Toxicity of fuel oil water accommodated fractions on two marine microalgae, S.costatum and chlorela spp [J]. Bulletin of Environmental Contamination and Toxicology, 2012, 88:712-716. |
| [10] | DEASI S R, VERLECAR X N, ANSARI Z A, et al.Evaluation of genotoxic responses of Chaetoceros tenuissimus and S.costatum to water accommodated fraction of petroleum hydrocarbons as biomarker of exposure [J]. Water Research, 2010, 44 (7):2235-2244. |
| [11] | LEITE M B N L, ARAUJO M M S D, NASCIMENTO I A, et al. Toxicity of water soluble fractions of biodiesel fuels derived from castor oil, palm oil, and waste cooking oil [J]. Environmental Toxicology and Chemistry, 2011, 30 (4):893-897. |
| [12] | LEE H J, SHIM W J, LEE J H, et al. Temporal and geographical trends in the genotoxic effects of marine sediments after accidental oil spill on the blood cells of striped beakperch (Oplegnathus fasciatus) [J]. Marine Pollution Bulletin, 2011, 62(10):2264-2268. |
| [13] | 王向艺.原油和消油剂对三种藻的急性毒性效应[D]. 大连:大连海事大学, 2012.WANG X Y. Acute Toxicity Effects of Crude Oil and Dispersant to Three Kinds of Algae [D]. Dalian: Dalian Maritime University, 2012 . |
| [14] | 刘娜. 油污染对小球藻与卤虫的毒性效应研究[D]. 大连:大连海事大学, 2006.LIU N. Research on Acute Toxicity of Spilling oils to Chlorella spp. And Artemia [D]. Dalian:Dalian Maritime University, 2006. |
| [15] | 姚念娣. 消油剂处理燃料油对两种海洋生物的毒性效应影响研究[D]. 大连:大连海事大学, 2012.YAO N D. Research on toxicity of fuel oil processed by the dispersant to two marine organisms [D]. Dalian:Dalian Maritime University, 2012. |
| [16] | 张蕾, 王修林, 韩秀荣, 等. 石油烃污染物对海洋浮游植物生长的影响——实验与模型[J]. 青岛海洋大学学报:自然科学版, 2002, 32(5):804-810.ZHANG L, WANG X L, HAN X R, et al. Effects of Petroleum Hydrocarbon on the Growth of Marine Algae: Experiment Versus Model [J]. Journal of Qingdao Maritime University:Natural Science, 2002, 32(5): 804-810. |
| [17] | 江 玉,吴志宏,韩秀荣, 等. 多环芳烃对海洋浮游植物的生物毒性研究[J]. 海洋科学, 2002, 26(1):46-50.JIANG Y, WU Z H, HAN X R, et al. Toxiticy of polycyclic aromatic hydrocarbons(PAHs) to marine algae [J]. Marine Sciences, 2002, 26(1):46-50. |
| [18] | 黄逸君, 陈全震, 曾江宁, 等. 原油和消油剂对海洋桡足类的急性毒性效应[J]. 应用与环境生物学报, 2010, 16(4):566-571.HUANG Y J, CHEN Q Z, ZENG J N, et al. Acute Toxicity of Crude Oil and Dispersant to Marine Copepods [J]. Chinese Journal of Applied & Environmental Biology, 2010, 16(4):566-571. |
| [19] | 王悠, 唐学玺, 李永祺, 等. 低浓度蒽对两种海洋微藻生长的兴奋效应[J]. 应用生态学报, 2002, 13(3):343-346.WANG Y, TANG X X, LI Y Q, et al. Stimulation effect of anthracene on marine microalgae growth [J]. Chinese Journal of Applied Ecology, 2002, 13(3):343-346. |
| [20] | GONZALEZ J, FIGUEIRAS F G, ARANGUREN-GASSIS M, et al. Effect of a simulated oil spill on natural assemblages of marine phytoplankton. Estuarine [J], Coastal and Shelf Science, 2009, 3(83):265-276. |
| [21] | 谢永红, 苏荣国, 张丽笑, 等. 三丁基锡对中国近海常见海洋微藻的毒性效应[J], 生态环境学报, 2011, 20(6/7):1075-1080.XIE Y H, SU R G, ZHANG L X, et al. The toxic effects of chloride tributyltin on the predomina [J]. Ecology and Environment, 2011, 20(6/7):1075-1080. |
| [22] | 何艺, 陈欢, 杨剑, 等. 荧蒽对披针舟形藻生长及叶绿素荧光特性的影响[J]. 环境科学与技术, 2011, 34(4):10-13.HE Y, CHEN H, YANG J, et al. Effects of Fluoranthene on Growth and Chlorophyll Fluorescence Characteristics of Navicula lanceolata[J]. Environmental Science and Technology, 2011, 34(4):10-13. |
| [23] | PéR F B. Fuel toxicity on Isochrysis galbana and a coastal phytoplankton assemblage: Growth rate vs. variable fluorescence [J]. Ecotoxicology and Environmental Safety, 2010, 73(3):254-261. |
| [24] | 于腾. 多溴联苯醚对2种海洋饵料微藻的急性毒性效应研究[D]. 青岛:中国海洋大学, 2011.YU Teng. Acute Toxic Effects and Mechanisms of PBDEs on Two Species of Marine Bait-microalgae[D]. Qingdao:Ocean University of China, 2011. |
| [25] | CARRERA-MARTINEZ D, MATEOS-SANZ A, LOPEZ-RODAS V, et al. Adaptation of microalgae to a gradient of continuous petroleum contamination [J]. Aquatic Toxicology, 2011, 101:342-350. |
| [26] | 江志兵, 曾江宁, 陈全震, 等. 不同季节升温条件下余氯对桡足类的毒性[J]. 水生生物学报, 2009, 33(5):896-904.JIANG Z B, ZENG J N, CHEN Q Z, et al. Toxiticy of Residual Chlorine on Copepods Under Temperature Increase In Different Seasons [J]. Acta Hydrobiol Ogica Sinica, 2009, 33(5):896-904. |
| [27] | 毕亚梅. 余氯对浮游生物毒理效应及损失量初步评估[D]. 上海:上海海洋大学, 2011.BI Y M. Preliminary assessment on resources loss and biological toxicological effects of residual chlorine to Plankton [D]. Shanghai :Shanghai Ocean University, 2011. |
| [28] | 马帅. 原油和4种溢油分散剂对青岛大扁藻和小新月菱形藻毒性效应的研究[D]. 青岛:中国海洋大学, 2013.MA S. Toxicity of crude oil and four kinds of dispersants to P.helgolandica and N.closterium [D].Qingdao: Ocean University of China, 2013. |
| [29] | ELSHEEKHM M, ELNAGGARA H, OSMANME H,et al. Comparative studies on the greenalgae Chlorella homosphaera and Chlorella vulgariswish respect to oil pollution the river Nile[ J].Water, Air, and Soil Pollution, 2000, 124(1/2):187-204. |
| [30] | APRAIZ I, CAJARAVILLE M P, CRISTOBAL S. Peroxisomal proteomics: biomonitoring in mussels after the Prestige,s oil spill.Marine Pollution Bulletin, 2009, 58(12):1815-1826. |
| [31] | 中华人民共和国国家质量监督检验检疫总局,中国国家标准化管理委员会. GB/T12763.6-2007,海洋调查规范第6部分:海洋生物调查[S]. 北京:中国标准出版社,2007.The People's Republic of China General Administration of Quality Supervision, the Standardization Administration of China. GB/T12763-2007,The People's Republic of China national standard: Marine survey Part 6: Marine Biological Survey[S]. Beijing: China Standard Publishing House, 2007. |
2. East China Sea Environmental Monitoring Center, SOA, Shanghai 200137, China;
3. Key Laboratory of Integrated Monitoring and Applied Technology for Marine Harmful Algal Blooms, SOA, Shanghai 200137, China
 2015, Vol. 24
2015, Vol. 24


